Serviços Personalizados
Journal
Artigo
Links relacionados
Compartilhar
Revista Médica del Uruguay
versão On-line ISSN 1688-0390
Rev. Méd. Urug. vol.30 no.1 Montevideo mar. 2014
Trasplante alogénico haploidéntico de progenitores hematopoyéticos en pediatría en Uruguay
Dres. Gustavo Dufort*, Luis A. Castillo†, Silvia Pisano‡, Mariela Castiglioni§, Carolina Pagés§, Elizabeth Simón§, Silvana Zuccolo§, Andrea Incoronato§, Rodrigo Barcelona§, Magdalena Schelotto§, Fabiana Morosini§, María Ferrando§, Clara Peña¶, Anaulina Silveira**, Adriana Tiscornia‡, Rossana Mezzano‡, Felipe Lemos‡, Luján Guerrero††, Valentina Ferreira††, Hugo Giordano‡‡, Beatriz Boggia§§, Aldo Quarnetti¶¶, Agustín Dabezies*
* Coordinador del Centro Hemato-Oncológico Pediátrico. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
† Director del Centro Hemato-Oncológico Pediátrico. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
‡ Departamento de Hemoterapia y Medicina Transfusional. Centro Hospitalario Pereira Rossell. ASSE. Montevideo, Uruguay.
§ Centro Hemato-Oncológico Pediátrico. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
¶ Nurse Jefe. Centro Hemato-Oncológico Pediátrico. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
** Analista de datos. Centro Hemato-Oncológico Pediátrico. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
†† Departamento de Radioterapia. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
‡‡ Jefe del Laboratorio de Citometría de Flujo. Asociación Española. Montevideo, Uruguay.
§§ Jefe del Departamento de Hemoterapia y Medicina Transfusional. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.
¶¶ Jefe del Departamento de Radioterapia. Centro Hospitalario Pereira Rossell. Montevideo, Uruguay.Correspondencia: Dr. Gustavo Dufort, Centro Hemato-Oncológico Pediátrico, Centro Hospitalario Pereira Rossell, Bvar. Artigas 1556, Montevideo. Uruguay.
Correo electrónico: gdufort@chasque.net
Conflictos de intereses: los autores declaran no tener conflictos de intereses.
Recibido: 26/8/13 Aceptado: 10/2/14
Palabras clave: TRASPLANTE HOMÓLOGO
HAPLOIDÍA
CÉLULAS MADRE HEMATOPOYÉTICAS
Keywords:
TRANSPLANTATION, HOMOLOGOUS
HAPLOIDE
HEMATOPOIETIC STEM CELLS
Resumen
Introducción: el trasplante alogénico de progenitores hematopoyéticos (TPH) es actualmente la única opción de tratamiento curativo disponible para un número de neoplasias hematológicas de alto riesgo, así como para algunas enfermedades no malignas hereditarias o adquiridas. El TPH haploidéntico (HI) es una opción válida para pacientes que no tienen un hermano HLA-idéntico. Objetivo: describir los resultados obtenidos con TPH HI en pediatría. Material y método: en el año 2005 se inició en el Centro Hemato-Oncológico Pediátrico del Centro Hospitalario Pereira Rossell un programa de TPH HI para aquellos pacientes sin donante relacionado HLA-idéntico. Resultados: se trasplantaron 32 pacientes, 24 con neoplasias hematológicas y 8 con enfermedades no malignas. Se utilizaron dos estrategias de prevención de la enfermedad injerto contra huésped (EICH), depleción de linfocitos T (DLT) in vitro (28 pacientes) y DLT alorreactivos in vivo con altas dosis de ciclofosfamida postrasplante (4 pacientes). Veintisiete pacientes (84%) tuvieron un implante con quimerismo total del donante. La incidencia de EICH agudo y crónico fue de 26,9% y 11,8%, respectivamente. La muerte no relacionada a recaída al año del trasplante fue de 21,9%. Con una mediana de seguimiento de 32 meses, la sobrevida global a dos años fue de 52,4%. Conclusiones: el TPH HI ha demostrado ser una opción factible en nuestro medio para aquellos pacientes sin donante HLA-idéntico. Los resultados son comparables a los obtenidos con otros donantes alternativos y con costos más accesibles. Uruguay está hoy día mejor posicionado para ofrecer un TPH a los pacientes que así lo requieran. Introducción
El trasplante de progenitores hematopoyéticos (TPH) consolidó su aplicación clínica ya hace más de 40 años(1), y se ha convertido en un procedimiento de uso común en un número creciente de enfermedades malignas y no malignas, habiéndose difundido prácticamente en todo el mundo(2). El primer TPH alogénico exitoso se realizó en 1968 en un niño que padecía una inmunodeficiencia combinada severa y en el que se utilizó como donante a una hermana sana(3). Desde entonces este procedimiento ha conocido un desarrollo espectacular. Uno de los avances verdaderamente revolucionarios del TPH es el uso cada vez más exitoso de donantes alternativos. Un hermano HLA-idéntico es considerado el gold standard como donante de progenitores hematopoyéticos. Sin embargo, solo 25% a 30% de los niños en los que un TPH está indicado, tienen la opción ideal de un hermano HLA-idéntico. Cuando no se dispone de un hermano compatible, y la enfermedad acarrea un pronóstico suficientemente malo, el orden de selección de un donante alternativo para la mayoría de las instituciones y estudios de grupos cooperativos es primero un donante no relacionado (DNR) fenotípicamente idéntico(4,5), o una unidad de sangre de cordón umbilical (SCU)(6), seguido por un donante familiar parcialmente compatible o haploidéntico (HI)(7). Sin embargo, este orden de preferencia no ha sido validado científicamente, y la respuesta de cuál es el mejor donante alternativo en ausencia de un hermano HLA-idéntico es materia de debate(8-11). El TPH HI ha encontrado un lugar en el tratamiento de neoplasias hematológicas de alto riesgo en pacientes de todas las edades y también en el tratamiento de algunas enfermedades no malignas en niños. La principal ventaja del TPH HI es la disponibilidad universal, rápida y cercana de los donantes. Ellos están muy motivados para donar a un familiar y pueden volver a donar en caso de rechazo, o donar linfocitos en caso de pérdida de quimerismo o recaída postrasplante. La mayor desventaja del TPH HI es la intensa alorreactividad bidireccional contra las moléculas HLA alogénicas que históricamente se ha asociado a una alta incidencia de rechazo y de enfermedad injerto contra huésped (EICH)(12).
En Uruguay, el primer TPH alogénico en un paciente pediátrico se realizó en 1997, en un niño con leucemia aguda mieloblástica(13). El número total de TPH realizados hasta fines del 2012 fue de 250. Uruguay es un país con una población de 3,3 millones de habitantes y 130 nuevos casos de cáncer en niños son diagnosticados anualmente(14). Se estima que cada año, 10 a 12 pacientes serán candidatos a un TPH alogénico, de los cuales solo un tercio tendrá un hermano HLA compatible. Esto significa que siete u ocho pacientes por año necesitarán un TPH de un donante alternativo. La mayoría de estos pacientes tendrán una enfermedad de alto riesgo –como una leucemia aguda– que requerirá un trasplante urgente. En este escenario, dos aspectos importantes fueron considerados: en primer lugar, que un centro con un pequeño número de trasplantes al año debe concentrar los esfuerzos en realizar trasplantes de un solo tipo de donantes alternativos y de esa manera desarrollar y adquirir experiencia en un área en particular; en segundo lugar, nuestra escasa experiencia previa coincide con lo que la literatura señala como la principal desventaja de los TPH de DNR, la cantidad de tiempo requerido desde la decisión de realizar una búsqueda de un DNR y la adquisición de los PH para realizar el trasplante es, en la mayoría de los casos, excesivamente largo para pacientes que necesitan un trasplante urgente(15,16). Por otro lado, ambos, el TPH de SCU y el TPH HI, tienen méritos y limitaciones, pero todavía nunca han sido comparados en un estudio randomizado en pediatría.
En el año 2005, con la cobertura del Fondo Nacional de Recursos (FNR) se inició en el Centro Hemato-Oncológico Pediátrico (CHOP) del Centro Hospitalario Pereira Rossell (CHPR) el programa de TPH HI para aquellos pacientes sin donante relacionado HLA-idéntico con enfermedades hematológicas malignas y no malignas con indicación de TPH. El objetivo del programa se resume en que cada niño o adolescente con indicación de TPH tenga acceso al tratamiento en el momento que sea necesario y sin limitaciones económicas.
Analizaremos nuestra experiencia en TPH HI en enfermedades hematológicas malignas y no malignas utilizando dos estrategias diferentes de prevención de la EICH: depleción de linfocitos T (DLT) in vitro usando el anticuerpo monoclonal OKT3, y depleción selectiva de linfocitos T alorreactivos in vivo con altas dosis de ciclofosfamida postrasplante (Cy/PT).
Material y método
Criterios de inclusión
Fueron elegidos pacientes sin donante familiar HLA-idéntico con neoplasias hematológicas de alto riesgo potencialmente curables con TPH alogénico, o con enfermedades hematológicas no malignas en las cuales el trasplante fuera considerado la mejor opción terapéutica. Cada situación particular fue analizada y autorizada por el FNR de acuerdo con las normativas de cobertura(17). Un consentimiento informado fue obtenido de los padres, como es requerido de acuerdo con la Declaración de Helsinki. Tipificación HLA
Pacientes y donantes fueron tipificados para loci HLA-A, HLA-B, HLA-C, HLA-DR, y HLA-DQ por microlinfocitotoxicidad o por métodos moleculares de resolución intermedia (amplificación por PCR e hibridación de oligonucleótidos). Selección del donante
Los donantes fueron familiares de primer grado (padres o hermanos) que compartieran al menos un haplotipo con el receptor. Inicialmente la selección fue realizada en forma aleatoria hasta el 2008, cuando un análisis retrospectivo encontró que los pacientes trasplantados de su madre tuvieron una mejor evolución comparado con los que recibieron injertos paternos(18). A partir de esta publicación se priorizó a la madre como donante. Movilización de progenitores hematopoyéticos
Todos los pacientes recibieron PH de sangre periférica (PHSP) del donante movilizados mediante la administración s/c de G-CSF dos veces por día (10 mcg/kg/día) durante cinco días. La recolección de PH fue realizada en el quinto día mediante leucoféresis de grandes volúmenes utilizando un separador celular COBE Spectra 7.0 Apheresis System (CaridianBCT Inc, Lakewood, CO, USA). Fueron procesadas un total de cuatro volemias a un flujo de 80-95 mL/min. Citometría de flujo
El análisis del producto de leucaféresis inicial y del producto final deplecionado de linfocitos T fue realizado por citometría de flujo (CyAn ADP Beckman Coulter Inc., Brea, CA, USA). Las células CD3+ se analizaron utilizando anticuerpos marcados con fluorocromos sensibles (Beckman Coulter Inc., Brea, CA, USA). El conteo de células CD34+ se realizó siguiendo los protocolos habituales (ISAGHE)(19). Depleción de linfocitos T
La DLT fue realizada por selección negativa de células CD3+ de una parte del producto de leucaféresis y por selección positiva de células CD34+ de otra, utilizando el dispositivo CliniMACS (Miltenyi Biotec, Bergish-Gladbach, Alemania). Las células mononucleares de sangre periférica (CMSP) del donante fueron procesadas inmediatamente o almacenadas a 4 °C durante la noche. Para remover el exceso de plaquetas, las CMSP fueron lavadas con buffer PBS CliniMACS (fosfato salino tamponado suplementado con 1 mM EDTA y 0,5% de albúmina humana). Para la DLT por selección negativa, las CMSP fueron incubadas con IGIV durante 5 minutos para bloquear uniones no específicas, luego incubadas 30 minutos con anticuerpos anti CD3 (OKT3) directamente conjugados a microperlas magnéticas (reactivo CD3, Miltenyi, Biotec, Bergisch Gladbach, Alemania) a temperatura ambiente con agitación continua, lavadas dos veces con buffer CliniMACS, y resuspendidads en 150 o 300 ml de buffer(20). La cantidad de anticuerpo usada fue calculada de acuerdo a las instrucciones del fabricante. Finalmente, el producto fue procesado en el dispositivo CliniMACS Plus (Miltenyi Biotec) utilizando un set TSLS y el programa CliniMACS 2.1. La selección positiva de células CD34+ se realizó siguiendo el protocolo habitual(21). Nuestro objetivo fue infundir = 10 x 106 CD34+ y 1,0 x 105 CD3+ por kilogramo de peso del paciente. Régimen de condicionamiento e infusión de PH
Los pacientes con neoplasias hematológicas sometidos a TPH HI con DLT in vitro recibieron un régimen de condicionamiento de intensidad reducida (CIR) con fludarabina 30 mg/m2 días -9 a -5, thiotepa 5 mg/kg c/12 h día -4 y una dosis diaria de melfalán (70 mg/m2) los días -3 y -2. Para prevenir el rechazo se utilizó OKT3 (Cimab, La Habana, Cuba) in vivo (0,1 mg/kg, máximo 5 mg) desde el día +1 al +15 hasta setiembre de 2008 (primeros nueve pacientes), después de lo cual el OKT3 fue sustituido por globulina antitimocítica de conejo (GAT) 1,5 mg/kg los días -9 a -6 en conjunción con irradiación nodal total (INT) con 7 Gy en dos fracciones el día -1. El régimen preparativo de los pacientes con anemia de Fanconi (AF) consistió en fludarabina 150 mg/m2, ciclofosfamida (Cy) 40 mg/kg, GAT e INT con 3 Gy. Los pacientes con osteopetrosis maligna (OPM) se acondicionaron con fludarabina 160 mg/m2, busulfán i/v 16 mg/kg, thiotepa 15 mg/kg y GAT 13 mg/kg de acuerdo a las guías de consenso de la Sociedad Europea de Inmunodeficiencias (ESID) y el Grupo de Trabajo Europeo de Trasplante de Médula Ósea (EBMT WP) en errores congénitos(22). Todos los pacientes que recibieron PH con DLT recibieron como prevención del síndrome linfoproliferativo postrasplante (SLPT) rituximab 375 mg/m2 el día -1. Los pacientes que recibieron TPH HI sin DLT fueron condicionados con un CIR en base a fludarabina 30 mg/m2 los días -6 a -2 , Cy 14,5 mg/kg los días -6 y -5, e irradiación corporal total (ICT) con 4 Gy en dos fracciones el día -1. El día 0 los pacientes recibieron PHSP del donante, un grupo luego de la DLT, y el otro sin manipulación previa. Profilaxis de la EICH
En los pacientes que recibieron TPH HI con DLT in vitro la inmunosupresión postrasplante se realizó con ciclosporina A (CSA) 1,5 mg/kg i/v c/12 h desde el día -1. La CSA fue administrada v/o cuando fue posible, y suspendida progresivamente a partir del día +30 en ausencia de EICH. Los pacientes trasplantados con PH sin DLT recibieron Cy 50 mg/kg los días +3 y +4, y a partir del día +5 CSA i/v 1,5 mg/kg c/12 h y micofenolato de mofetilo (MMF) v/o 45 mg/kg/d divididos en tres dosis. En ausencia de EICH, el MMF se suspendió el día +35 y la CSA el día +90. Tratamiento de soporte
Cada paciente fue aislado en una habitación equipada con filtro de aire de alta eficiencia y flujo de aire laminar, y recibió profilaxis antifúngica (fluconazol), antiviral (aciclovir), anti Pneumocystis jirovecii (cotrimoxazol) e infusiones regulares de inmunoglobulina intravenosa polivalente hasta que hubiera evidencia de reconstitución inmune. El CMV fue monitorizado semanalmente por PCR cuantitativo a partir del día +1, y de detectarse reactivación viral (>200 copias/mL) se inició tratamiento anticipado con ganciclovir i/v 5 mg/kg c/12 h. También semanalmente se realizó dosificación de antígeno galactomanano en sangre y detección de adenovirus en materias fecales. Se administró G-CSF i/v 10 mcg/kg/día a partir del día +5 continuando hasta el implante de los neutrófilos. Todos los hemoderivados fueron desleucotizados e irradiados previo a su administración. Quimerismo
El quimerismo se evaluó a partir de sangre periférica entera de los receptores, usando polimorfismos del ácido desoxirribonucleico (ADN) basado en la amplificación por PCR de 15 loci de STR, dos veces al mes, desde el día +14 al día +100, y posteriormente con menor frecuencia en los pacientes con quimerismo completo del donante. Los niveles de quimerismo fueron definidos como: quimerismo completo del donante, > 95% células del donante; quimerismo mixto, 10%-95%, y no quimerismo, < 5%. Reconstitución inmune
La reconstitución de CD3+, CD4+, CD8+, CD19+ y CD16+ fue monitorizada por citometría de flujo aproximadamente los días 30, 60, 90, 180, 270 y al año. Infusión de linfocitos T del donante
Algunos pacientes recibieron infusión de linfocitos T (ILT) en caso de quimerismo mixto o recaída de la enfermedad subyacente, o ambos. Se obtuvo sangre total fresca del donante y se administró una dosis ajustada a un contenido de células CD3+ de 2,5 a 5,0 x 104/kg. El procedimiento se reiteró las veces que se consideró necesario. Definiciones
Implante fue definido para los neutrófilos como el primer día en el cual el recuento absoluto de neutrófilos (RAN) fue consistentemente mayor de 500/μL con evidencia de hematopoyesis del donante. El implante de plaquetas fue definido como el primer día de un recuento mayor de 20.000/μL sin transfusión de plaquetas durante los siete días previos. Rechazo primario fue definido como el fracaso de alcanzar un RAN mayor de 500/μL al día +30 del trasplante, y rechazo secundario la pérdida sostenida del injerto (RAN menor de 500/μL) por cinco días después de un implante inicial. La EICH aguda y crónica fue diagnosticada y clasificada como ha sido descrito(23). Análisis estadístico
Las probabilidades de sobrevida libre de eventos (SLE) y sobrevida global (SG) fueron estimadas usando el método Kaplan-Maier(24). La SG fue definida como el número de días desde el trasplante a la muerte por cualquier causa. Evento fue definido como muerte, recaída o rechazo. Mortalidad no relacionada a recaída (MNR) incluyó solo a pacientes que murieron sin que precediera recaída de la enfermedad. La fecha del último seguimiento para todos los pacientes sobrevivientes fue el 31 de enero de 2013.
Resultados
Pacientes
Un total de 32 pacientes con una mediana de edad de 7 años (rango, 0,3 - 17 años) fueron tratados entre abril de 2005 y diciembre de 2012. Las características de los pacientes se describen en la tabla 1. Veinticuatro pacientes tenían neoplasias hematológicas de alto riesgo y ocho pacientes enfermedades no malignas. Al momento del trasplante los pacientes con leucemia aguda mieloblástica (LAM) y leucemia aguda linfoblástica (LAL) estaban en remisión completa (RC). Donantes y características del injerto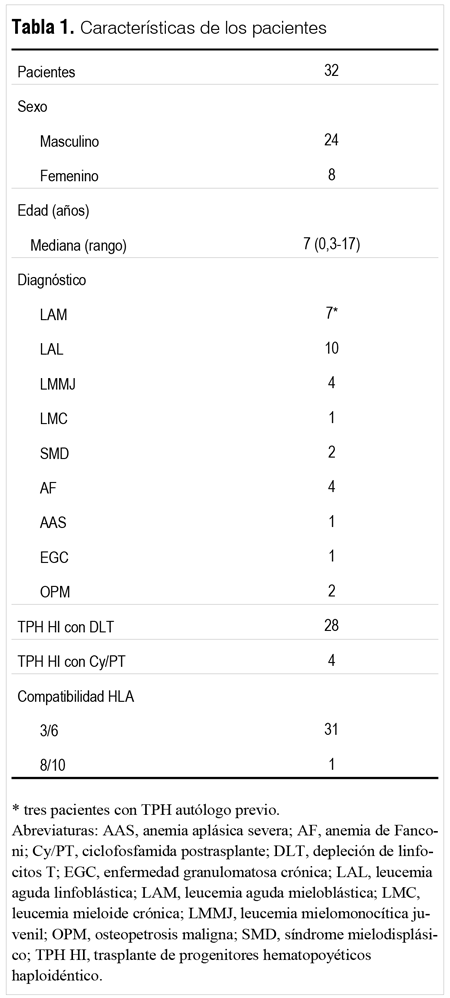
La madre fue donante en 17 casos, el padre en 13 casos, y en dos casos fueron hermano y hermana, respectivamente. Veintiocho pacientes recibieron PHSP con DLT in vitro. La mediana de DLT fue de 3,5 log (rango, 1,44 - 4,5) y la mediana de células CD34+ y CD3+ infundidas fue de 14,96 x 106/kg (rango, 1,01 - 46,4) y 1,8 x 105/kg (rango, 0,86 - 5,0), respectivamente. Cuatro pacientes recibieron PHSP sin previa manipulación con una mediana de células CD34+ de 17,8 x 106/kg (rango, 6,38 - 19,69) y CD3+ de 2,50 x 108/kg (rango, 1,58 - 9,42), respectivamente. Las características de los donantes y del injerto se muestran en la tabla 2.
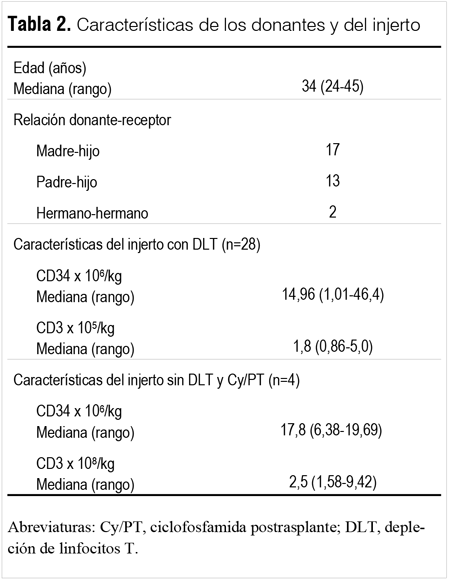
Implante
De los 32 pacientes, 27 (84%) tuvieron un implante con quimerismo total del donante. La mediana de tiempo requerido para alcanzar un RAN > 500/μL fue de 11 días (rango, 9 - 17), mientras que para mantener un recuento plaquetario > 20.000/μL sin transfusión fue de 16 días (rango, 11 - 28) (tabla 3). En cuatro pacientes falló el implante primario, dos pacientes con leucemia mielomonocítica juvenil (LMMJ) que posteriormente tuvieron una recuperación hematológica autóloga, y dos pacientes con síndrome mielodisplásico (SMD) y OPM, respectivamente, que fallecieron antes del día +100. El quinto paciente (OPM) falleció sin evidencia de implante antes del día +30 del trasplante a consecuencia de una hemorragia intracraneana. Uno de los pacientes con LMMJ recibió un segundo TPH HI, lográndose un implante con quimerismo mixto, pero en la evolución fallece de una rápida progresión de su enfermedad; el restante continúa en remisión de su enfermedad. Dos pacientes, uno con leucemia mieloide crónica (LMC) y otro con LAM presentaron un rechazo secundario el día +78 y +28, respectivamente. El paciente con LMC recibió un segundo TPH HI exitoso de su otro padre utilizando un régimen preparativo con fludarabina 30 mg/m2 los días -6 a -2, Cy 60 mg/kg el día -6, y OKT3 para prevenir el rechazo. El paciente con LAM falleció el día +60 de una falla cardíaca probablemente secundaria a antraciclínicos. Los 32 pacientes requirieron soporte transfusional. La mediana de transfusiones de plaquetas fue de 6 (rango, 1 - 25), y de glóbulos rojos de 2 (rango, 0 - 12). Toxicidad, infecciones, EICH y MNR
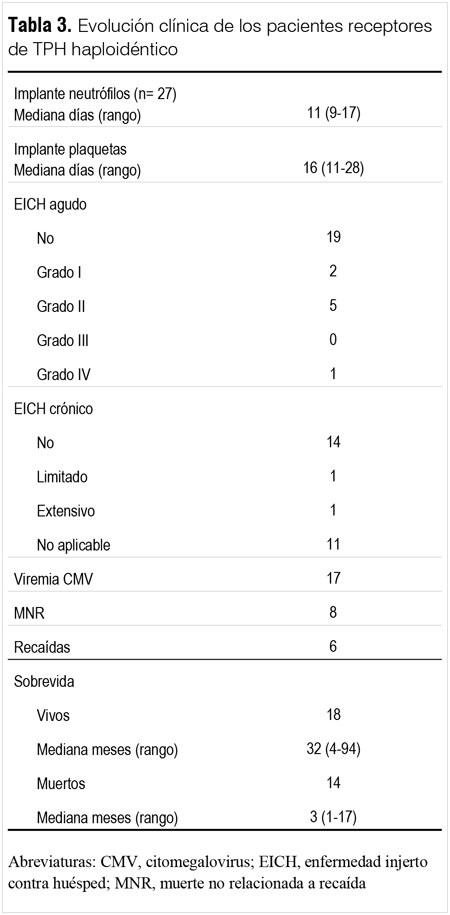
Los regímenes de condicionamiento usados fueron bien tolerados, siendo la toxicidad gastrointestinal la más común. La mayoría de los pacientes tuvieron náuseas, vómitos y diarrea. Mucositis grado II y III fue observada en 28 de los 32 pacientes, 25 de los cuales recibieron nutrición parenteral por una media de 10 días (rango, 8 - 16). Hubo un caso de toxicidad gastrointestinal fatal con las características histológicas de una enteritis rádica en el paciente con anemia aplásica severa (AAS). Un paciente con AF presentó un síndrome de encefalopatía posterior reversible (PRES) el día +31 postrasplante. No se observó toxicidad significativa en los pacientes que previamente habían recibido un TPH autólogo.
Un total de 17 de 27 pacientes evaluables (63%) presentaron reactivación del CMV (> 200 copias/μL) en una o más oportunidades. A pesar de recibir tratamiento anticipado con ganciclovir i/v, tres pacientes desarrollaron la enfermedad. Dos pacientes, con EICH aguda y crónica, respectivamente, desarrollaron una neumonitis intersticial por CMV, causa por la cual fallecieron, y el tercer paciente una retinitis severa. No hubo infecciones bacterianas clínicamente significativas. Hubo solo un caso de infección micótica invasiva en un paciente con SMD y fallo de implante, que desarrolló una aspergilosis senoorbitaria fatal en el curso de una neutropenia prolongada.
La incidencia acumulativa de EICH agudo grados II-IV fue de 26,9% con un caso grado IV de curso fatal (figura 2A). Dos pacientes presentaron EICH crónico (incidencia acumulativa 11,8%), una forma extensiva y una limitada (figura 2B). Los cuatro pacientes que recibieron TPH HI con Cy/PT presentaron EICH agudo grado II, y solo uno de ellos EICH crónico limitado hasta el momento.
La incidencia acumulativa de MNR al año del trasplante fue de 21,9% (figura 3A). En la tabla 4 se muestran las causas de MNR y el tiempo de muerte después del TPH.

Reconstitución inmune
La reconstitución inmune fue estudiada en 15 pacientes que recibieron TPH HI con DLT. Los resultados se representan en la figura 1. Todos los pacientes experimentaron un profundo deterioro de la función inmune, principalmente durante los primeros tres meses. Los valores absolutos de CD4+ muestran un aumento a partir de los tres a seis meses postrasplante, alcanzando valores normales recién a los 12 meses. La mediana de linfocitos T supresores CD8+ está descendida en los primeros tres meses, pero posteriormente se mantiene en rango normal. Los linfocitos B CD19+ alcanzan niveles normales a los seis meses, mientras que el recuento absoluto de las células NK se mantiene siempre dentro de valores normales. Infusión de linfocitos del donante
Cinco pacientes recibieron ILT del donante (una a tres veces) por recaída (n=2) o por quimerismo mixto (n=3). Los dos pacientes en recaída fallecieron por progresión de la enfermedad, y de los pacientes con quimerismo mixto, uno tuvo un rechazo y los otros dos mantuvieron quimerismos mixtos estables. Recaídas, SLE y SG
Ocho pacientes tuvieron una MNR y seis pacientes recayeron de su enfermedad y fallecieron (tabla 4). La incidencia acumulativa de recaída al año fue de 29,4% (figura 3B). Dieciocho pacientes sobreviven con una mediana de seguimiento de 32 meses (rango, 4 - 94). La SG y SLE estimada a dos años por Kaplan-Maier fue de 52,4% ± 9,5% y de 53,1% ± 9,4%, respectivamente, para toda la serie (figura 4A y figura 4B). Para los pacientes con neoplasias hematológicas la SG y SLE estimada a dos años fue de 48,5% ± 11,3% (figura 5A). Para los pacientes con enfermedades no malignas, la SG estimada fue de 62,5% ± 17,1% (figura 5B), y si analizamos solo los pacientes con AF, la sobrevida fue de 100%.

Discusión
Uruguay es un país con una población pequeña en un territorio pequeño, lo que es adecuado para concentrar esfuerzos y recursos. El cáncer en pediatría es una enfermedad rara y por lo tanto requiere de la centralización de los pacientes para obtener los mejores resultados(25). El TPH alogénico es un procedimiento terapéutico de alto costo y complejidad que es requerido por una minoría de pacientes, para los cuales generalmente es la única posibilidad curativa. La mayoría de este pequeño grupo de pacientes no tendrá un hermano HLA-idéntico y por ende su única opción será un donante alternativo.
En la década pasada hubo un creciente interés en el uso del TPH HI debido a la rápida y casi universal disponibilidad de los donantes, lo cual es un problema crítico en pacientes con neoplasias hematológicas en etapa avanzada. El entusiasmo por este procedimiento ha sido motivado por los significativos avances en este campo y las mejoras en los tratamientos de soporte, lo que ha permitido trasplantar pacientes sorteando las barreras del sistema HLA en forma más segura, a la vez que mitigar los históricos problemas del fallo de implante y de la EICH(26). Nuestro aporte suma a la creciente literatura que apoya el TPH HI como una alternativa viable para aquellos pacientes sin un acceso rápido a un donante HLA compatible(27).
Los primeros intentos de TPH HI utilizando médula ósea (MO) no manipulada estuvieron asociados con efectos secundarios severos y la mayoría de las veces letales(12). Desde entonces, diferentes estrategias de manipulación del injerto in vitro han sido introducidas en el TPH HI para deplecionar los linfocitos T y de esa forma prevenir la EICH, incluyendo selección de células CD34+(28), depleción de células CD3+(29), depleción de células CD3+/CD19+(30), y, más recientemente, depleción de linfocitos TcRαβ(31). Además, se han desarrollado otras estrategias de trasplante utilizando MO o PHSP sin DLT con intensa profilaxis para la EICH(32), o con DLT in vivo usando GAT o anticuerpos monoclonales (alemtuzumab)(33). Otra estrategia ha sido la depleción in vivo de linfocitos T alorreactivos usando altas dosis de Cy postrasplante, y de esa forma inducir tolerancia inmunológica(34).
En esta publicación describimos 32 pacientes con enfermedades hematológicas malignas y no malignas que recibieron dos modalidades diferentes de TPH HI: TPH HI con DLT in vitro, la mayoría de los pacientes, y TPH HI con depleción de linfocitos T alorreactivos in vivo (Cy/PT), estrategia de reciente aplicación en nuestra experiencia.
Veintisiete pacientes (84%) tuvieron un implante mantenido con hematopoyesis del donante. Aquellos que presentaron un rechazo primario eran portadores de patologías en las que el riesgo de rechazo podía ser previsible, como ser un paciente con OPM que ya tenía diez meses de vida al momento del trasplante, o el paciente con un SMD secundario a una AAS que previamente había recibido múltiples transfusiones. Los cuatro rechazos fueron en pacientes que recibieron PH con DLT, y la incidencia es comparable con otras experiencias(7,35).
La incidencia acumulativa de EICH agudo (II-IV) y crónico fue de 26,9% y 11,8%, respectivamente, lo que es similar, o incluso levemente menor a lo esperado en otras modalidades de TPH de donantes alternativos. La MNR al año del trasplante fue de 21,9%. Series similares y otras con diferentes donantes alternativos tienen MNR en rangos de 10% a 30%(36-39). La mayoría de las series, al igual que la nuestra, incluyen pacientes con enfermedades en etapas avanzadas y con tratamientos previos intensos. En nuestra serie las causas de MNR fueron heterogéneas, pero dos pacientes fallecieron a causa de infección por CMV. La incidencia de reactivación del CMV en trasplantes con DLT es muy alta y está directamente relacionada a la inmunodeficiencia celular intrínseca al TPH deplecionado de linfocitos T(40). Para asegurar la detección temprana de infección por CMV, su vigilancia intensiva debe ser considerada como un componente esencial del manejo del TPH HI(41).
Una ventaja de gran impacto en nuestra serie fue la corta duración de la neutropenia. De hecho, no hubo infecciones bacterianas clínicamente significativas y solo un caso de infección micótica invasiva. Ningún paciente presentó un SLPT, lo que confirma que el rituximab ofrece una profilaxis efectiva.
La SG estimada a los dos años fue de 48,5% para los pacientes con neoplasias hematológicas y de 62,5% para aquellos con enfermedades no malignas. Estos resultados demuestran que el TPH HI con DLT y con Cy/PT luego de un CIR, se asocia con un alto porcentaje de implante, tasas tolerables de EICH y MNR, y una SG a largo plazo comparable a la obtenida con otro tipo de donantes alternativos.
Nuestra experiencia con DLT in vivo utilizando la selección negativa de células CD3+ ha sido satisfactoria, no sin haber pasado por una curva de aprendizaje para lograr logaritmos adecuados de depleción(27). La mayoría de nuestros pacientes también recibieron PH CD34+ obtenidos por selección positiva con el objetivo de asegurar una “megadosis de CD34” como instrumento para sortear la barrera del sistema HLA(42). Demostramos la factibilidad en nuestro medio de un procedimiento que requiere alta tecnología y un equipo profesional entrenado(27). Sin embargo, la reconstitución inmune lenta, que es común a todas las estrategias de TPH, es más pronunciada después de este tipo de trasplantes, lo que expone al paciente a complicaciones infecciosas y por lo tanto obliga a una monitorización clínica y paraclínica estricta y prolongada, determinando un aumento de los costos, ya elevados en este tipo de trasplantes(43). El TPH HI utilizando Cy/PT es un procedimiento que ha tenido un importante desarrollo en los últimos años en centros de excelencia(44-46). En nuestra experiencia es un procedimiento que ha sido muy atractivo, ya que tiene todas las ventajas del TPH HI pero no requiere de la costosa tecnología de la DLT in vitro. Además, los resultados han sido alentadores respecto a una menor incidencia de infecciones y una más rápida recuperación inmunológica(47,48). Nuestra experiencia con esta modalidad de TPH HI es por el momento limitada, aunque todos los pacientes han implantado, no hubo toxicidades ni infecciones significativas, no hubo MNR, los cuatro pacientes presentaron EICH agudo de grado leve, y un solo paciente desarrolló EICH crónico limitado. El TPH HI con Cy/PT no requiere tecnología costosa y tiene resultados comparables, lo que lo transforma en una alternativa viable y atractiva para nuestro medio.
En suma, nuestra experiencia en pediatría demuestra que estamos favorablemente posicionados para ofrecer un TPH a los pacientes que así lo requieran, ya sea para el tratamiento de una neoplasia hematológica de alto riesgo, o una enfermedad hematológica no maligna que ponga en peligro la vida, con resultados comparables a los publicados internacionalmente. Finalmente, con la utilización de esta técnica de TPH hemos conseguido cumplir con el objetivo trazado: todos los niños y adolescentes que necesitaron un trasplante accedieron al procedimiento en tiempo e independientemente de sus recursos económicos. Agradecimientos
Muy especialmente a las nurses, nutricionistas, auxiliares de enfermería y equipo psicosocial del CHOP; técnicos en hemoterapia y técnicos en radioterapia del CHPR; a todos ellos por su disposición y dedicación desinteresada en la atención de los pacientes. Agradecemos al Laboratorio de Histocompatibilidad e Inmunogenética del Instituto Nacional de Donación y Trasplante por su contribución. Abstract
Introduction: allogenic hematopoietic stem cell transplantation (HSCT) is the only currently available curative treatment for a number of high-risk hematologic malignancies and for a range of inherited and acquired non-malignant diseases. Haploidentical (HI) HSCT is a valid option for patients who lack an HLA-identical brother.
Objective: to describe the results obtained with HI HSCT in pediatrics.
Method: in 2005 an HI HSCT program was started at the Pediatric Hemato-Oncological Department of the Centro Hospitalario Pereira Rossell, for patients who lack an HLA-matched related donor.
Results: Thirty two patients were transplanted, 24 of them with hematological malignancies and 8 with non-malignant diseases. Two strategies were used to prevent the Graft-Versus-Host-Disease (GVHD), in- vitro T-cell depletion (28 patients) and in-vivo depletion of aloreactives T-cells with high-dose post-transplantation cyclophosphamide (4 patients). Successful engraftment occurred in 27 patients (84%), with full-donor chimerism. Incidence of acute and chronic GVHD was 26.9% and 11.8% respectively. One year non-relapsed mortality was 21.9%. With a median follow-up of 32 months, the overall survival was 52.4%.
Conclusions: HI HSCT has proved to be a feasible option in our country for those patients without an HLA-identical donor. The results obtained are comparable to those obtained with other alternative donors and costs are more reasonable. Today, Uruguay is in a better position to offer a HSCT to patients who need it. Resumo
Introdução: o transplante alogênico de células-tronco hematopoiéticas (TCH) atualmente é a única opção terapêutica curativa disponível para várias neoplasias hematológicas de alto risco, e também para algumas patologias não malignas hereditárias ou adquiridas. O TCH haploidêntico (HI) é uma opção válida para pacientes que não tem irmão HLA-id.
Objetivo: descrever os resultados obtidos com TCH HI em Pediatria.
Material e método: em 2005 no Centro Hemato-Oncológico Pediátrico do Centro Hospitalario Pereira Rossell começou um programa de TCH HI para pacientes sem doador relacionado HLA-idêntico.
Resultados: foram transplantados 32 pacientes, 24 com neoplasias hematológicas e 8 com patologias não malignas. Foram utilizadas duas estratégias para a prevenção da doença enxerto versus hospedeiro (DEVH): depleção de linfócitos T (DLT) in vitro (28 pacientes) e DLT alorreativos in vivo com altas doses de ciclofosfamida pós-transplante (4 pacientes). Vinte e sete pacientes (84%) tiveram um implante com quimerismo total do doador. A incidência de DEVH aguda e crônica foi de 26,9% e 11,8% respectivamente. A porcentagem de óbito não relacionado à recaída um ano depois do transplante foi de 21,9%. A sobrevida global aos dois anos do transplante foi de 52,4% com uma mediana de seguimento de 32 meses.
Conclusões: o TCH HI mostrou ser uma opção viável no nosso meio para pacientes sem doador HLA-idêntico. Os resultados são comparáveis aos obtidos com outros doadores alternativos com custos más acessíveis. Atualmente o Uruguai tem melhores condições para oferecer TCH aos pacientes que o necessitem. Bibliografía
1. Thomas ED, Buckner CD, Banaji M, Clift RA, Fefer A, Flournov N et al. One hundred patients with acute leukemia treated by chemotherapy, total body irradiation, and allogeneic marrow transplantation. Blood 1977; 49(4):511-33.
2. Ljungman P, Bregni M, Brune M, Cornelissen J, de Witte T, Dini G et al. Allogeneic and autologous transplantation for haematological diseases, solid tumour and immune disorders: Current practice in Europe 2009. Bone Marrow Transplant 2010; 45(2) :219-34 .
3. Gatti RA, Meuwissen HJ, Allen HD, Hong R, Good RA. Immunological reconstitution of sex-linked lymphopenic immunological deficiency. Lancet 1968; 2(7583):1366-9 .
4. Eapen M, Rubinstein P, Zhang MJ, Camitta BM, Stevens C, Cairo MS et al. Comparable long-term survival after unrelated and HLA matched sibling donor hematopoietic stem cell transplantations for acute leukemia in children younger than 18 months. J Clin Oncol 2006; 24(1):145-51 .
5. Dahlke J, Kroger N, Zabelina T, Ayuk F, Fehse N, Wolschke C et al. Comparable results in patients with acute lymphoblastic leukemia after related and unrelated stem cell transplantation. Bone Marrow Transplant 2006; 37(2): 155-63.
6. Eapen M, Rubinstein P, Zhang MJ, Stevens C, Kurtzberg J, Scaradavou A et al. Outcomes of transplantation of unrelated donor umbilical cord blood and bone marrow in children with acute leukemia: a comparison study. Lancet 2007; 369(9577):1947-54.
7. Klingebiel T, Cornish J, Labopin M, Locatelli F, Darbyshire P, Handgretinger R et al. Results and factors influencing outcome after fully haploidentical hematopoietic stem cell transplantation in children with very high-risk acute lymphoblastic leukemia: impact of center size. An analysis on behalf of the Acute Leukemia and Pediatric Disease Working Parties of the European Blood and Marrow Transplant group. Blood 2010; 115(17):3437-46.
8. Hough R, Cooper N, Veys P. Allogeneic haemopoietic stem cell transplantation in children: what alternative donor should we choose when no matched sibling is available? Br J Haematol 2009; 147(5):593-613.
9. Rocha V, Locatelli F. Searching for alternative hematopoietic stem cell donors for pediatric patients. Bone Marrow Transplant 2008; 41(2):207-14.
10. Ballen KK, Koreth J, Chen YB, Dey BR, Spitzer TR. Selection of optimal alternative graft source: mismatched unrelated donor, umbilical cord blood, or haploidentical transplant. Blood 2012; 119(9):1972-80.
11. Zuckerman T, Rowe JM. Alternative donor transplantation in acute myeloid leukemia: which source and when? Curr Opin Hematol 2007; 14(2):152-61.
12. Powles RL, Morgenstern GR, Kay HE, McElwain TJ, Clink HM, Dady PJ et al. Mismatched family donors for bone-marrow transplantation as treatment for acute leukemia. Lancet 1983; 1(8325):612-5.
13. Dufort y Alvarez G, Castiglioni M, Pagés C, Dabezies A, Decaro J, Castillo L. Trasplante de progenitores hematopoyéticos en pediatría: 10 años de experiencia. Arch Pediatr Urug 2008; 79(3):201-9.
14. Castillo LA, Fluchel M, Dabezies A, Pieri D, Brockhorst N, Barr R. Childhood cancer in Uruguay: 1992-1994. Incidence and mortality. Med Pediatr Oncol 2001; 37(4):400-4.
15. Barker J, Krepski, TP, DeFor TE, Davies SM, Wagner JE, Weisdorf DJ. Searching for unrelated donor hematopoietic stem cells: availability and speed of umbilical cord blood versus bone marrow. Biol Blood Marrow Transplant 2002; 8(5):257-60.
16. Grewal SS, Barker JN, Davies SM, Wagner JE. Unrelated donor hematopoietic cell transplantation: marrow or umbilical cord blood? Blood 2003; 101(11):4233-44.
17. Fondo Nacional de Recursos. Trasplante de Médula Ósea o Trasplante de Progenitores Hematopoyéticos: normativa de cobertura del Fondo Nacional de Recursos. Montevideo: FNR, 2006.Disponible en: http://www.fnr.gub.uy /sites/default/files/normativas/tecnicas/n_tmo_0.pdf [Consulta: 12 dic. 2012].
18. Stern M, Ruggeri L, Mancusi A, Bernardo ME, de Angelis C, Bucher C et al. Survival after T cell-depleted haploidentical stem cell transplantation is improved using the mother as donor. Blood 2008; 112(7):2990-5.
19. Leuner S, Arland M, Kahl C, Jentsch-Ullrich K, Franke A, Hoffkes HG. Enumeration of CD34-positive hematopoietic progenitor cells by flow cytometry: comparison of a volumetric assay and the ISHAGE gating strategy. Bone Marrow Transplant 1998; 22(7):699-70.
20. Dykes JH, Toporski J, Juliusson G, Békássy AN, Lenhoff S, Lindmark A et al. Rapid and effective CD3 T-cell depletion with a magnetic cell sorting program to produce peripheral blood progenitor cell products for haploidentical transplantation in children and adults. Transfusion 2007; 47:2134-42.
21. Schumm M, Lang P, Taylor G, Kuci S, Klingebiel T, Buhring HJ et al. Isolation of highly purified autologous and allogeneic peripheral CD34+ cells using the CliniMACS device. J Hematother 1999; 8:209-18.
22. European Society for Blood and Marrow Transplantation. Osteopetrosis: consensus guidelines for diagnosis, therapy and follow up. Disponible en: htpp: //www.ebmt.org/Contents/About-EBMT/Who-We-Are/Workingparties/Documents/00_OP_ Guidelines_02122011.pdf [Consulta: 12 dic 2012]
23. Sullivan KM. Graft-versus-host-disease. In: Blume KG, Forman SJ, Appelbaum FR, editors. Thomas’ Hematopoietic Cell Transplantation. Blackwell Science Ltd., 2004:635-64
24. Kaplan E, Meier P. Nonparametric estimation from incomplete observations. Journal of the American Statistical Association 1958; 84:360-72 .
25. Murphy SB. The national impact of clinical cooperative group trials for pediatric cancer. Med Pediatr Oncol 1995.
26. Handgretinger R, Chen X, Pfeiffer M, Mueller I, Feuchtinger T, Hale GA et al. Feasability and outcome of reduced intensity conditioning in haploidentical transplantation. Ann NY Acad Sci 2007; 1106:279-89.
27. Dufort G, Pisano S, Incoronato A, Castiglioni M, Pages C, Simon E et al. Feasibility and outcome of haploidentical SCT in pediatric high-risk hematologic malignancies and Fanconi anemia in Uruguay. Bone Marrow Transplant 2012; 47(5):663-8.
28. Handgretinger R., Klingebiel T, Lang P, Schumm M, Neu S, Geiselhart A et al. Megadose transplantation of purified peripheral blood CD34(+) progenitor cells from HLA-mismatched parental donors in children. Bone Marrow Transplant 2001; 27:777-83.
29. Gordon PR, Leimig T, Mueller I, Babarin-Dorner A, Holladay MA, Houston J et al. A large-scale method for T cell depletion: towards graft engineering of mobilized peripheral blood stem cells. Bone Marrow Transplant 2002; 30:69-74.
30. Barfield RC, Otto M, Houston J, Holladay MA, Geiger T, Martin J et al. A one-step large-scale method for T- and B-cell depletion of mobilized PBSC for allogeneic transplantation. Cytotherapy 2004; 6:1-6.
31. Handgretinger R. Negative depletion of CD3+ and TcR;+ T cells. Curr Opin Hematol 2012; 19:434-9.
32. Huang, X.J. & Y.J. Chang. Unmanipulated HLAmismatched/haploidentical blood and marrow hematopoietic stem cell transplantation. Biol. BloodMarrow Transplant 2011; 17:197-204.
33. Rizzieri DA, Koh LP, Long GD, Gasparetto C, Sullivan KM, Horwitz M et al. Partially matched, nonmyeloablative allogeneic transplantation: clinical outcomes and immune reconstitution. J. Clin Oncol 2007; 25:690-7.
34. Luznik L, Bolanos-Meade J, Zahurak M, Chen AR, Smith BD, Brodsky R et al. High-dose cyclophosphamide as single-agent, short-course prophylaxis of graft-versus-host disease. Blood 2010; 115:3224-30.
35. Bader P, Soerensen J, Koehl U, Kreyenberg H, Jarisch A, Weber G et al. Excellent engraftment and rapid immune recovery in haplo-identical stem cell transplantation using CD3/CD19 depleted peripheral stem cell grafts after reduced intensity conditioning. Bone Marrow Transplant 2008; 14(2):27.
36. Hale GA, Kasow KA, Madden R, et al. Mismatched family member donor transplantation for patients with refractory hematologic malignancies: longterm followup of a prospective clinical trial [abstract]. Blood (ASH Annual Meeting Abstracts) 2006; 108: abstr 3137
37. Hale GA, Kasow KA, Gan K, et al. Haploidentical stem cell transplantation with CD3 depleted mobilized peripheral blood stem cell grafts for children with hematologic malignancies [abstract]. Blood (ASH Annual Meeting Abstracts) 2005; 106: abstr 2910.
38. Tuve S, Gayoso J, Scheid C, Radke J, Kiani A, Serrano D et al. Haploidentical bone marrow transplantation with postgrafting cyclophosphamide: multicenter experience with an alternative salvage strategy. Leukemia 2011; 25:880-3.
39. Leung W, Campana D, Yang J, Pei D, Coustan-Smith E, Gan K et al. High success rate of hematopoietic cell transplantation regardless of donor source in children with very high-risk leukemia. Blood 2011; 118(2):223-30.
40. Ball LM, Lankester AC, Bredius RGM, Fibbe WE, van Tol MJD, Egeler RM. Graft dysfunction and delayed immune reconstitution following haploidentical peripheral blood hematopoietic stem cell transplantation. Bone Marrow Transplant 2005; 35:S35-8.
41. Paris C, Kopp K, King A, Santolaya ME, Zepeda AJ, Palma J. Cytomegalovirus infection in children undergoing hematopoietic stem cell transplantation in Chile. Pediatr Blood Cancer 2009; 53:453-8.
42. Reisner Y, Martelli MF. Tolerance induction by ‘megadose’ transplants of CD34+ stem cells: a new option for leukemia patients without an HLA-matched donor. Curr Opin Immunol 2000; 12:536-41.
43. Seggewiss, R. & H. Einsele. Immune reconstitution after allogeneic transplantation and expanding options for immunomodulation: an update. Blood 2010; 115:3861-8.
44. Luznik L, Jalla S, Engstrom LW, Iannone R, Fuchs EJ. Durable engraftment of major histocompatibility complex-incompatible cells after nonmyeloablative conditioning with fludarabine, lowdose total body irradiation, and posttransplantation cyclophosphamide. Blood 2001; 98: 3456-64.
45. O’Donnell PV, Luznik L, Jones RJ, Vogelsang GB, Leffell MS, Phelps M et al. Nonmyeloablative bone marrow transplantation from partially HLA-mismatched related donors using posttransplantation cyclophosphamide. Biol Blood Marrow Transplant 2002; 8:377-86.
46. Luznik L, O’Donnell PV, Symons HJ, Chen AR, Leffell MS, Zahurak M et al. HLA-haploidentical bone marrow transplantation for hematologicmalignancies using nonmyeloablative conditioning and high-dose posttransplantation cyclophosphamide. Biol Blood Marrow Transplant 2008; 14:641-50.
47. Munchel A, Kesserwan C, Symons HJ, Luznik L, Kasamon YL, Jones RJ et al. Nonmyeloablative,HLA-haploidentical bone marrow transplantation with high dose, post-transplantation cyclophosphamide. Pediatr Rep 2011; 3(Suppl 2):e15.
48. Dominietto A, Raiola AM, Bruno B, et al. Rapid Immune Reconstitution Following Unmanipulated Haploidentical BMT with Post-Transplant High Dose Cyclophosphamide. Blood 2011(ASH Annual Meeting Abstracts); 118: Abstract 3050.














