Serviços Personalizados
Journal
Artigo
Links relacionados
Compartilhar
Revista Médica del Uruguay
versão On-line ISSN 1688-0390
Rev. Méd. Urug. vol.20 no.2 Montevideo ago. 2004
La terapia hormonal en la posmenopausia y las promesas incumplidas
Dres. Francisco Cóppola*, José Nader†, Rafael Aguirre‡
Unidad de Climaterio del Hospital de la Mujer. Centro Hospitalario Pereira Rossell.
Facultad de Medicina. Universidad de la República. Montevideo, Uruguay.
Resumen
El uso de la hormonoterapia de reemplazo en la posmenopausia fue una práctica extendida a lo largo del último cuarto de siglo. Su prescripción se basaba en los beneficios a nivel cardiovascular, óseo y sobre la función cognitiva, que justificaban el mayor riesgo de cáncer de mama de la misma. Sin embargo, el desarrollo en los últimos años de estudios clínicos aleatorizados para evaluar los reales beneficios de la hormonoterapia han dado por tierra con las promesas de prevención cardiovascular y de la función cognitiva que se le atribuía a esta terapia, confirmando además el mayor riesgo de cáncer mamario. Esto llevó a la inversión de la relación riesgo-beneficio de su uso prolongado en la mayoría de las pacientes y a una drástica reducción de su prescripción y comercialización en todo el mundo. El presente artículo busca revisar las razones de estos cambios, divulgar sus repercusiones y reflexionar sobre las lecciones a aprender antes de instaurar una nueva intervención farmacológica.
Palabras clave: TERAPIA DE REEMPLAZO HORMONAL.
POSMENOPAUSIA.
* Prof. Adj. Clínica Ginecotocológica "C". Coordinador de la Unidad de Climaterio del Hospital Pereira Rossell. Centro Hospitalario Pereira Rossell. Ex Asistente de Cátedra de Endocrinología. Facultad de Medicina. Universidad de la República. Montevideo. Uruguay.
† Ex Asistente de Clínica Ginecotocológica "C". Docente Honorario Clínica Ginecotocológica "C". Coordinador de la Unidad de Climaterio del Hospital Pereira Rossell. Centro Hospitalario Pereira Rossell. Facultad de Medicina. Universidad de la República. Montevideo. Uruguay.
‡ Ex Asistente de Clínica Ginecotocológica "C". Docente Honorario Clínica Ginecotocológica "C". Centro Hospitalario Pereira Rossell. Facultad de Medicina. Universidad de la República. Montevideo. Uruguay.
Correspondencia: Dr. Rafael Aguirre
Santiago Gadea 3056 Ap. 601. CP 11600. Montevideo, Uruguay.
E-mail: climater@mednet.org.uy
Recibido: 3/10/03.
Aceptado luego de modificaciones: 16/3/04.
Este trabajo fue publicado en la Revista Brasilera de Clínica y Terapéutica 2003. Se reedita con modificaciones y autorización del editor de dicha publicación.
Uso extensivo y generalizado de la terapia hormonal
La terapia de reemplazo hormonal (TRH) en la posmenopausia ha sido una práctica común en la mayoría de los países occidentales a lo largo de las décadas de 1980 y 1990. Con ello se buscaba evitar las complicaciones que aparecían como propias de la deficiencia hormonal, esto es, las complicaciones vasculares, el deterioro cognitivo y la osteoporosis. La observación clínica y epidemiológica de un aumento del riesgo cardiovascular inmediatamente luego de la menopausia, igualando dicho riesgo al del hombre, llevó a la rápida conclusión de que las hormonas ováricas jugaban un papel como factor protector cardiovascular. La lógica indicaba que si se sustituía la función endócrina ovárica, mediante el aporte exógeno de hormonas, la protección se prolongaría en el tiempo y evitaría muertes de origen cardiovascular(1).
Durante muchos años los estudios de puntos intermedios (vasodilatación arterial, cambios en el perfil lipídico y del estrés oxidativo, etcétera) reforzaron la suposición de que los estrógenos, por diversos mecanismos, protegían a la mujer de presentar complicaciones de origen cardiovascular. Los estudios observacionales que comparan la existencia de complicaciones cardiovasculares entre las usuarias de TRH y las no usuarias, mostraban enormes diferencias a favor de las primeras.
Con estos datos, y apoyados con gran impulso por la industria farmacéutica, muchos profesionales comenzaron a recomendar el uso extensivo, generalizado y prolongado de la terapia hormonal en la posmenopausia, con la finalidad de prevenir enfermedades crónicas fundamentalmente cardiovasculares.
No obstante, no todos se aferraron a esta idea predominante y un grupo de investigadores consideró que los datos científicos eran insuficientes para recomendar una terapia con fines preventivos en la población sana. Se requerían estudios randomizados para evaluar el riesgo-beneficio de la terapia prolongada, y dichos estudios comenzaron a diseñarse al inicio de los años 1990. En 1991, la doctora E. Barret-Connor fue una de las primeras investigadoras en alertar que las conclusiones sobre el beneficio de la TRH sobre la salud eran sacadas de estudios con graves errores metodológicos. Estos estudios observacionales generalmente comparaban poblaciones muy diferentes (usuarios con no usuarios de servicios de salud, por ejemplo), por lo que se necesitaban estudios randomizados en donde las diferencias poblacionales fueran neutralizadas por el azar, de forma de establecer exactamente el valor de la terapéutica(2). Incluso previamente se demostró que el solo hecho de adherirse a las indicaciones médicas era un fuerte marcador de bajo riesgo coronario, aun utilizando placebo(3).
Con la finalidad de resolver esta cuestión fueron diseñados diferentes estudios randomizados, algunos muy importantes, como el WHI, promovido por el Instituto Nacional de Salud de los Estados Unidos de Norteamérica (NIH. http://www.nhlbi.nih.gov/whi/ )
La publicación de los resultados de estos estudios clínicos aleatorizados marcó un punto de quiebre en las expectativas sobre el efecto de la TRH en la salud de la mujer. En términos generales, los estudios randomizados se mostraron inconsistentes con los estudios observacionales en relación a la protección cardiovascular y de la enfermedad de Alzheimer que se le asignaba a la TRH. Por otro lado, reafirmaron las observaciones que asocian la terapia hormonal con un aumento del riesgo de cáncer mamario, tromboembolismo y enfermedad hepatobiliar, y una acción protectora sobre el desarrollo de fracturas osteoporóticas y cáncer de colon.
Falta de protección cardiovascular - aumento del riesgo
Como se mencionó, los estudios observacionales señalaban la existencia de una protección cardiovascular, que superaba 50% en las pacientes que recibían TRH. El primer llamado de atención, en contradicción con este concepto, fue la publicación del estudio HERS (Heart and Estrogen/Progestin Replacement Study), randomizado, controlado, doble ciego, diseñado para prevención secundaria, (pacientes portadoras de enfermedad cardiovascular). El mismo involucró 2.763 pacientes, un seguimiento a cuatro años y el uso de terapia hormonal combinada (estrógenos y progesterona). Los resultados mostraron que no sólo no hay beneficios, sino que existe un incremento de 50% en el riesgo de eventos adversos cardiovasculares en el primer año de uso de la TRH(4).
Como en este estudio el riesgo tiende a disminuir con el tiempo de uso de la terapia, se supuso que el seguimiento más prolongado de estas pacientes (estudio HERS II, seguimiento por 6,8 años) iba a neutralizar este aumento del riesgo o posiblemente mostrar un efecto protector final a lo largo del período. Sin embargo, la reciente culminación de este estudio desmiente esta hipótesis manteniéndose el mayor riesgo cardiovascular con la TRH(5).
Con esta nueva evidencia sobre los beneficios y riesgos cardiovasculares de la TRH, la American Heart Association revisó las recomendaciones sobre TRH y desaconsejó su uso para la protección cardiovascular(6). Posteriormente otras investigaciones clínicas randomizadas (WEST, WELL-HART, ERA ) reafirmaron que, tanto al valorar los puntos finales (muerte cardiovascular o infarto agudo de miocardio [IAM]), como los puntos intermedios (diámetro de arteria coronaria), ni las combinaciones estrógeno-progestacionales ni los estrógenos solos son útiles para la prevención cardiovascular secundaria(7-9).
Quedaba así entonces sólo por resolver la utilidad de la TRH en la prevención cardiovascular primaria.
En el año 2002 la publicación de los resultados que llevaron a la interrupción prematura de la rama de estrógeno-progesterona del WHI (más de 16 mil pacientes, con útero, a 5,2 años), señaló para esta formulación de TRH, que las conclusiones sobre la protección cardiovascular primaria son similares a las encontradas en prevención secundaria (falta de protección, aumento del riesgo)(10). La posibilidad de que los estrógenos solos (en pacientes histerectomizadas, rama del WHI que aún continúa) tenga algún papel en prevención primaria, debe considerarse en investigación y esperamos los resultados que se publicarán en 2005.
Un reciente estudio menor (EPAT), diseñado para conocer el papel de los estrógenos solos en la disfunción endotelial, parece demostrar un enlentecimiento en la progresión de aterosclerosis inicial en pacientes que reciben estradiol sin progesterona. Sin embargo, es prudente esperar la finalización de estudios mayores con valoración de los puntos finales (IAM, muerte cardiovascular)(11).
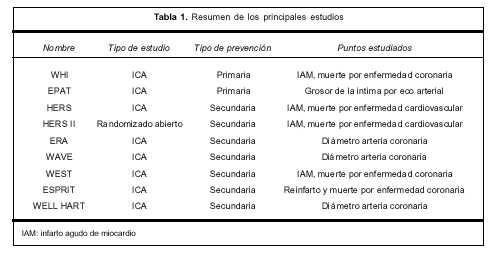
En la tabla 1 se muestran los principales estudios al respecto de protección cardiovascular de la TRH y los puntos estudiados.
Aumento del riesgo de cáncer de mama
Desde el inicio del uso de la TRH varias líneas de evidencia sugerían que la TRH incrementaba el riesgo de cáncer de mama. Los estrógenos promueven el crecimiento de tumores en animales e incrementa la proliferación de células cancerosas humanas in vitro(12-14). El riesgo epidemiológico vinculando la exposición prolongada a estrógenos (menarca precoz, menopausia tardía, obesidad), así como la asociación de niveles sanguíneos elevados de estrógenos y testosterona con cáncer de mama, sugerían desde un inicio esta relación de riesgo. Muchos clínicos justificaban el uso de TRH en el hecho que el cáncer de mama, en las usuarias de TRH, es de diagnóstico precoz y menor mortalidad que en la población general. Sin embargo, este hecho era también explicable por el mejor control al que es sometida la población usuaria de TRH. Además se refería que el mayor riesgo de cáncer de mama se justificaba al existir un menor riesgo cardiovascular y de fracturas osteoporóticas.
En 1997 se publicó un metaanálisis que reunió 55 estudios epidemiológicos sobre la relación de la TRH y el cáncer de mama. El mismo reafirmaba la vinculación de la TRH en la génesis del cáncer y fue hasta la publicación del WHI la mejor evidencia a tener en cuenta(15).
Con la interrupción del WHI en la rama estrógeno-progestágeno no se modificó el concepto general de los estudios observacionales previos, la TRH se asoció a mayor riesgo de cáncer de mama. Existe un aumento significativo en el riesgo y este está en relación directa al tiempo de exposición a las hormonas(10). Una reciente publicación definitiva y más detallada del WHI sobre la relación de la TRH y el cáncer de mama aclara mejor estos conceptos(16). En la misma queda claro que el mayor riesgo de cáncer de mama, asociado al uso de terapia hormonal estrógeno-progestacional, es significativamente mayor al del grupo placebo ya en el tercer año de tratamiento y no difiere de este en cuanto al tipo histológico ni a la presencia de receptores. La diferencia está marcada por la mayor evolutividad y estadio en los cánceres que se vinculan al uso de tratamiento hormonal.
Ahora se sabe que los cánceres asociados al tratamiento con estro-progestágenos son de peor pronóstico, modificando sustancialmente lo que se pensaba hasta el momento. Se aclaró, además, que el aumento de la densidad mamaria que provoca la terapia hormonal aparece precozmente y es capaz de retardar el diagnóstico.
En este punto queda por analizar lo que ocurre con los estrógenos sin oposición (rama del WHI no finalizada), así como con otras formulaciones, vías, además de la terapia con tibolona.
Un reciente estudio realizado en el Reino Unido, de carácter observacional pero de gran peso estadístico por el volumen de población estudiada (un millón de pacientes), parece aclarar que la combinación de estrógeno con progesterona, cualquiera sea la vía o la formulación, se relaciona directamente con el desarrollo de cáncer de mama a partir del primer año de uso(17). Los estrógenos solos y la tibolona también son capaces de aumentar el riesgo de cáncer de mama aunque en forma más débil. En las pacientes que recibieron TRH en el pasado, si transcurrió un período de más de cinco años sin usarla, normalizan el riesgo.
En suma, tanto los estudios observacionales como los randomizados son concordantes y apuntan en la misma dirección: la asociación de terapia hormonal y cáncer de mama es evidente. A juzgar por el breve lapso en que aparece esta vinculación (entre uno y tres años), es biológicamente más probable que se deba al estímulo de un cáncer preexistente acompañado o no del eventual retardo del diagnóstico debido al aumento en la densidad mamaria(16).
Función cognitiva
En el caso de la función cognitiva, los estudios observacionales también sugerían beneficios y protección contra la demencia(18). Sin embargo, en el metaanálisis realizado por Hogervorst se observó que estos hallazgos no eran constantes(19,20). Por otro lado, los estudios aleatorizados y controlados nunca confirmaron estos beneficios(21,22).
El estudio WHIMS (The Womens Health Initiative Memory Study), incluido dentro de la rama suspendida estrógeno-progestacional del WHI, se diseñó para resolver este problema. Una vez más, al igual que en lo cardiovascular, los resultados fueron diametralmente contrarios a lo señalado por los estudios observacionales. Se comprobó un significativo aumento del riesgo de deterioro cognitivo en las pacientes sometidas a tratamiento en relación al placebo(23).
Las inconsistencias
Como el principal justificativo para administrar TRH, y exponer a las pacientes a los riesgos secundarios a la misma, era la supuesta protección cardiovascular, los nuevos conocimientos provocan un profundo cambio en el concepto de uso a largo plazo de la terapia hormonal. De ahora en más, queda claro que la terapéutica sólo es útil para cohibir la sintomatología climatérica y para la prevención de la osteoporosis, siendo el balance riesgo-beneficio de resultado desfavorable para el uso prolongado (necesario para la prevención ósea). Además, la existencia de terapéuticas alternativas para la prevención de la osteoporosis pone, aun más, en tela de juicio la conveniencia de la TRH.
Ahora bien ¿cómo se explican las inconsistencias entre los estudios randomizados y los observacionales en relación a la terapia de reemplazo hormonal? ¿Por qué las inconsistencias se ven en el área cardiovascular y de la función cognitiva y no en los demás aspectos? Un artículo de interés fue recientemente publicado, en el mismo se plantea que dichas inconsistencias tienen diferentes motivos(24).
A destacar:
1) Diferencias metodológicas
a. El sesgo del "usuario saludable". En los estudios observacionales, las mujeres que optan por tomar hormonas son generalmente más saludables (mayor preocupación, cuidados de salud, consulta médica) que las mujeres que optan por no tomarlas, y este desequilibrio podría llevar a que se sobrestime el efecto proteccionista y se infravalore los riesgos asociados con la terapia hormonal. Se le atribuirían beneficios a la terapia hormonal que en realidad dependen de mejores hábitos de salud.
b. Sesgo de mayor "compliance". Las mujeres que adhieren a la terapia hormonal tienden a adherir a otro tipo de terapia que lleva a una mejor protección cardiovascular. Ya se demostró que las personas que obedecen en el uso de placebo (mejor adherencia) tienen sustancialmente más bajo riesgo de enfermedades cardiovasculares que aquellas que no obedecen el uso (baja adherencia) tanto de placebo como de la medicación activa(25). La complacencia hacia un tipo de terapia se asocia con la complacencia hacia otras (antihipertensivos, hipolipemiantes, etcétera) y es un marcador del seguimiento de hábitos de vida más saludables.
2) Diferencias biológicas
a. Diferentes regímenes hormonales: los resultados de estudios para un tipo de terapia o un tipo de formulación puede ser que no se apliquen a otras, por lo que son necesarias investigaciones específicas para cada formulación.
b. Características de la población: variaciones en el nivel de estrógenos endógenos, tiempo desde la menopausia, nivel de aterosclerosis al inicio. Los estudios pueden ser concluyentes en términos generales pero de escasa potencia para aplicarlos en subgrupos específicos (hipertensos obesos o delgados, etcétera). Por otra parte, es posible que las inconsistencias entre los estudios observacionales y aleatorizados se exprese en la función cardiovascular y cognitiva como consecuencia de que ambos aspectos son más dependientes que otros de los hábitos de vida saludables.
3) Sesgo de publicación
Los sesgos en la publicación de los resultados positivos y la subnotificación de los negativos constituyen la tercera amenaza para la distorsión en los datos clínicos(26). Un estudio sobre los centros de investigación universitarios e industriales de Estados Unidos mostró que 35% de los acuerdos firmados permitía al patrocinador suprimir información en la publicación, 53% permitía el retraso en la publicación y 30% autorizaba ambas prácticas(27).
Repercusión
– La aceptación del nuevo enfoque fue rápida a nivel de las instituciones científicas y más lenta a nivel de los médicos.
– El Colegio Americano de Ginecología y Obstetricia rápidamente, a un mes de la publicación del WHI, recomendó usar terapia hormonal en la menopausia solamente para el tratamiento sintomático, el menor tiempo y la menor dosis posibles advirtiendo la necesidad de informar a las pacientes de los riesgos. www.acog.org
– La Sociedad Americana de Menopausia (NAMS), en un reporte aconseja los mismos criterios y aclara que si bien el tratamiento puede ser efectivo para la osteoporosis, como con este fin el tratamiento debe ser prolongado, es conveniente, ya que se dispone, la utilización de otras estrategias de tratamiento(28).
– Se suspendió un estudio similar al WHI que estaba en curso con más de 5.000 pacientes reclutadas en Inglaterra (WISDOM)(29).
– La Food and Drug Administration (FDA) ajustó sus indicaciones de acuerdo a los mismos criterios, aprobando además las dosis bajas. www.fda.gov
– Se desaconsejó claramente el uso de terapia hormonal con la finalidad de prevenir la enfermedad de Alzheimer. www.nia.nih.gov
– Esto fue acompañado de una abrupta caída de la prescripción y facturación de la TRH(30).
Lecciones
Los estudios observacionales en modelos animales y la investigación básica tienen un tremendo valor para la generación de hipótesis, pero no deben usarse para justificar las intervenciones farmacológicas, fundamentalmente cuando se trata de población sana.
Una segunda lección es determinar el exacto valor de los puntos intermedios. Si podemos entender cómo un fármaco que baja el LDL colesterol, aumenta el HDL y mejora otros factores de riesgo como la función endotelial y no es capaz de producir un beneficio cardiovascular sino que incluso puede aumentarlo, podremos comprender aspectos biológicos aún no conocidos de la patogénesis de la aterosclerosis.
Nota de autores (marzo de 2004)
La presente revisión se refiere a los resultados de la terapia de reemplazo a la fecha de su presentación a la Revista Médica del Uruguay. Una vez aprobada su publicación en la misma, el NIH (National Institute of Health of USA), con fecha 2 de marzo de 2004, en un comunicado oficial anuncia la interrupción de la segunda rama del estudio WHI (estrógenos solos) luego de siete años de seguimiento y 11.000 pacientes. Dicha rama estaba diseñada para finalizar en 2005, sin embargo sus resultados preliminares justificaron la interrupción ya que no se comprobaron cambios en el riesgo cardiovascular (motivo que justificaba el estudio) comprobándose un aumento del riesgo de accidentes vasculares encefálicos. Esto justifica mantener las recomendaciones de uso de la TRH al tratamiento de los bochornos moderados o severos, utilizando la menor dosis posible durante el menor tiempo posible, y a la prevención de la osteoporosis, siempre que no sea posible otro enfoque terapéutico y la relación riesgo-beneficio sea adecuada.
Summary
Hormone replacement therapy in menopause has been extensively used in the last 25 years of 20th Century. Prescription was based on the benefits showed at the cardiovascular and skeletal levels as well as at different cognitive functions that justified the higher breast cancer risk seen during menopause. However, the last randomized clinical studies to assess actual benefits of hormone therapy had cut out promises about cardiovascular prevention and cognitive functions, confirming the higher risk of breast cancer. Relation risk-benefit was inverted and prescriptions and mercantilization all over the world decreased. The paper analiyses these changes, promotes results and criticizes pharmacological interventions.
Résumé
L’emploi de l’hormonothérapie de substitution dans la post-ménopause a été une pratique très étendue au long des 25 dernières années. Sa prescription était basée sur les bénéfices cardiovasculaires, osseux et de la cognition, ce qui justifiait le risque de cancer de sein. Cependant, le développement pendant les dernières années des études cliniques faites pour évaluer les vrais bénéfices de l’hormonothérapie a fait que les promesses de prévention cardiovasculaire et de la fonction cognitive attribuées à cette thérapie s’effondrent, tout en prouvant l’accroissement de l’incidence du cancer de sein. Cela a mené à l’inversion du rapport risque-bénéfice de son emploi prolongé chez la plupart des patientes et à une réduction drastique de sa prescription et vente dans le monde entier. Cet article vise à faire une révision des raisons de ces changements et de réfléchir sur les leçons à apprendre avant d’instaurer une nouvelle intervention pharmacologique.
Bibliografía
1. Grodstein F, Stampfer M. The epidemiology of coronary heart disease and estrogen replacement in posmenopausal women. Prog Cardiovasc Dis 1995; 38(3): 199-210.
2. Barret-Connor E. Postmenopausal estrogen and prevention bias. Ann Inter Med 1991; 115(6): 455-6.
3. Influence of adherence to treatment and response of cholesterol on mortality in the coronary drug project. N Engl J Med 1980; 303(18): 1038-41.
4. Hulley S, Grady D, Bush T, Furberg C, Herrington D, Riggs B, et al. Randomized trial of estrogen plus progestin for secondary prevention of coronary heart disease in postmenopausal women. JAMA 1998; 280(7): 605-13.
5. Grady D, Herrington D, Bittner V, Blumenthal R, Davison M, Hlatky M, et al. Cardiovascular disease outcomes during 6.8 years of hormone therapy: heart and Estrogen/progestin Replacement Study follow-up (HERS II). JAMA. 2002 Jul 3;288(1):49-57. Erratum in: JAMA 2002 Sep 4;288(9):1064.
6. Mosca L, Collins P, Herrington DM, Mendelsohn ME, Pasternak RC, Robertson RM, et al. Hormone replacement therapy and cardiovascular disease: a statement for healthcare professionals from the American Heart Association. Circulation 2001; 104(4): 499-503.
7. Viscoli CM, Brass LM, Kernan WN, Sarrel PM, Suissa S, Horwitz RI. A clinical trial of estrogen-replacement therapy after ischemic stroke. N Engl J Med 2001; 345(17): 1243-9.
8. Hodis HM, Mack WJ, Azen SP, Lobo RA, Shoupe D, Mahrer PR, et al. Hormone therapy and the progression of coronary-artery atherosclerosis in postmenopausal women. N Engl J Med 2003; 349(6): 535-45.
9. Herrington DM, Reboussin DM, Brosnihan KB, Sharp PC, Shumaker SA, Snyder TE, et al. Effects of estrogen replacement on the progression of coronary-artery atherosclerosis. N Engl J Med 2000; 343(8): 522-9.
10. Rossouw JE, Anderson GL, Prentice RL, LaCroix AZ, Kooperberg C, Writing Group for the Woman Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal woman: principal results From the Women’s Health Initiative randomized controlled trial. Jama 2002; 288(3): 321-33.
11. Hodis HN, Mack WJ, Lobo RA, Shoupe D, Sevanian A, Mahrer PR, et al. Estrogen in the prevention of atherosclerosis. Ann Inter Med 2001; 135(11): 939-53.
12. International Agency for Research on Cancer. Sex hormones (II). In: IARC Monographs on the Evaluation of the Carcinogenic Risk of Chemicals to Humans. Lyon: IARC, 1979: v.21
13. Clemons M, Goss P. Estrogen and the risk of breast cancer. N Engl J Med 2001; 344(4): 276-85.
14. Fuchs-Young R, Glasebrook AL, Short LL, Draper MW, Rippy MK, Cole HW, et al. Raloxifene is a tissue-selective agonist/antagonist that functions through the estrogen receptor. Ann N Y Acad Sci 1995; (761): 355-60.
15. Breast cancer and hormone replacement therapy: collaborative reanalysis of data from 51 epidemiological studies of 52,705 women with breast cancer and 108,411 women without breast cancer. Collaborative Group on Hormonal Factors in Breast Cancer. Lancet. 1997 Oct 11;350(9084):1047-59. Erratum in: Lancet 1997 Nov 15;350(9089):1484.
16. Chlebowski RT, Susan LH, Langer RD, Stefanick ML, Gass M, Lane D, et al. Influence of estrogen plus progestin on breast cancer and mammography in healthy postmenopausal women: the Women’s Health Initiative Randomized Trial. JAMA 2003; 289(24): 3243-53.
17. Beral V, Million Women Study Collaborators. Breast cancer and hormone-replacement therapy in the Million Women Study. Lancet 2003; 362(9382): 419-27.
18. Carlson MC, Zandi PP, Plassman BL, Tschanz JT, Welsh-Bohmer KA, Steffens DC, et al. Hormone replacement therapy and reduced cognitive decline in older women: the Cache County Study. Neurology 2001; 57(12): 2210-6.
19. Hogervorst E, Williams J, Budge M, Riedel W, Jolles J. The nature of the effect of female gonadal hormone replacement therapy on cognitive function in post-menopausal women: a meta-analysis. Neuroscience 2000; 101(3): 485-512.
20. Yaffe K, Sawaya G, Lieberburg I, Grady D. Estrogen therapy in postmenopausal women: effects on cognitive function and dementia. JAMA 1998; 279(9): 688-95.
21. Henderson VW, Paganini-Hill A, Miller BL, Elble RJ, Reyes PF, Shoupe D, et al. Estrogen for Alzheimer’s disease in women: randomized, double-blind, placebo-controlled trial. Neurology 2000; 54(2): 295-301.
22. Mulnard RA, Cotman CW, Kawas C, Van Dick CH, Sano M, Doody R, et al. Estrogen replacement therapy for treatment of mild to moderate Alzheimer disease: a randomized controlled trial. JAMA 2000; 283(8): 1007-15.
23. Rapp SR, Espeland MA, Shumaker SA, Henderson VW, Brunner RL, Manson JE, et al. Effect of estrogen plus progestin on global cognitive function in postmenopausal women: the Women’s Health Initiative Memory Study: a randomized controlled trial. JAMA 2003; 289(20): 2663-72.
24. Grodstein F, Clarkson TB, Manson JE. Understanding the divergent data on postmenopausal hormone therapy. N Engl J Med 2003; 348(7): 645-50.
25. Petitti DB. Coronary heart disease and estrogen replacement therapy: can compliance bias explain the results of observational studies? Ann Epidemiol 1994; 4(2): 115-8.
26. Chalmers I. Underreporting research in scientific misconduct. JAMA 1990; 263(10): 1405-8.
27. Cohen W, Florida R, Goe WR. University-industry research centers in the United States. Pittsburgh: Carnegie-Mellon University, 1994
28. North American Menopause Society. Amended report from the NAMS Advisory Panel on Postmenopausal Hormone Therapy. Menopause 2003; 10(1): 6-12.
29. White C. Second long term HRT trial stopped early. BMJ 2002; 325(7371): 987.
30. Austin PC, Mamdani MM, Tu K, Jaakkimainen L. Prescriptions for estrogen replacement therapy in Ontario before and after publication of the Women’s Health Initiative Study. JAMA 2003; 289(24): 3241-2.