Serviços Personalizados
Journal
Artigo
Links relacionados
Compartilhar
Revista Uruguaya de Cardiología
versão On-line ISSN 1688-0420
Rev.Urug.Cardiol. vol.30 no.2 Montevideo ago. 2015
Artículo original
Tratamiento de la reestenosis coronaria: experiencia con balón liberador de paclitaxel
Dres. Pedro Trujillo, Gustavo Vignolo, Ignacio Batista, Rafael Mila,
Sebastián Albistur, Ariel Durán, Ricardo Lluberas
Centro Cardiovascular Universitario. Departamento de Cardiología. Hospital de Clínicas.UDELAR. Montevideo, Uruguay.
Correo electrónico: petruji67@gmail.com
Recibido marzo 9, 2015; aceptado junio 2, 2015.
Resumen
Objetivo: comunicar la experiencia preliminar acerca de la evaluación clínica e invasiva del tratamiento de la reestenosis intrastent convencional con el uso de balón liberador de paclitaxel.
Método: se realiza un análisis de tres momentos evolutivos denominados "previo", "índice" y "control" de una serie de casos de reestenosis intrastent (RIS) tratados con balón liberador de paclitaxel (BLP). El evento previo es la situación clínica que motivó el implante de stent convencional (SC) inicial, acerca del cual se hace un análisis clínico-angiográfico retrospectivo. El evento índice, que corresponde a la captación del paciente, es la evolución reestenotica del SC inicial e incluyó un análisis clínico, un estudio angiográfico y la angioplastia con BLP. El evento control incluye el análisis clínico, angiográfico y ultrasonografico al año de seguimiento. Las variables pesquisadas fueron: características basales de la población, presentación clínica, arterias coronarias y sectores involucrados, tipo de RIS, diámetro luminal mínimo (DLM) y área luminal mínima (ALM) por angiografía y adicionalmente por ultrasonografía en el seguimiento.
Resultados: se incluyeron ocho pacientes. La edad promedio fue de 57 años. Los cuadros clínicos que determinaron la angioplastia coronaria inicial fueron: cuatro síndromes coronarios agudos con sobreelevación persistente del segmento ST, dos infartos agudos de miocardio de tipo no Q y dos anginas inestables (AI). Los cuadros clínicos en el momento del diagnóstico de RIS y en los cuales se aplicó BLP fueron: tres AI, cuatro IAM no Q y un paciente asintomático con isquemia demostrada por estudio funcional. Las arterias y el sector involucrados fueron: dos arterias descendentes anteriores (ADA) proximal, tres ADA media, una arteria circunfleja media y dos arterias coronarias derechas media. Siete pacientes presentaban RIS difusa y uno focal. En el seguimiento clínico posterior a la aplicación de BLP a los seis, nueve y doce meses se observó una muerte no cardiovascular y una pérdida de seguimiento, el resto estaban asintomáticos. En la angiografía de control al año se comprobó RIS binaria en un solo caso. El análisis por imágenes determinó que en promedio el DLM y el ALM aumentaran dos veces y cuatro veces y media respectivamente entre los eventos “índice” y “control”. La pérdida tardía de DLM o late loss promedio entre el tratamiento con BLP y el control final fue de 0,47 mm. No se comprobó ninguna complicación vinculada al uso de BLP.
Conclusión: la utilización de BLP en el tratamiento de la RIS de SC determinó una ganancia de DLM y ALM mantenida al año de seguimiento, no registrándose complicaciones atribuibles al procedimiento.
Palabras clave:
REESTENOSIS CORONARIA
ESTUDIO OBSERVACIONAL
INFORMES DE CASOS
Summary
Objective: clinical, angiographic and intracoronary ultrasound analysis of a series of cases of conventional in-stent restenosis (ISR) treated with paclitaxel eluting balloon (PEB) with 12 months follow up.
Method: an analysis of three evolutionary stages called “previous”, “index” and “control” of a series of cases of stent restenosis (ISR) treated with paclitaxel eluting balloon (PEB) is performed. The previous event is the clinical situation which led to the initial bare-metal stent (BMS) implant, on which a retrospective clinical and angiographic analysis is done. The index event, which corresponds to the acquisition of the patient, is the restenotic evolution of the initial BMS and included a clinical analysis, angiography and angioplasty with PEB. The event control includes the clinical, angiographic and ultrasonographic analysis at one year. The researched variables were baseline characteristics of the population, clinical presentation, coronary arteries and sectors involved, the type of ISR, the minimum luminal diameter (MLD) and minimal lumen area (MLA) by angiography and additionally by ultrasonography.
Results: 8 patients were included. The mean age was 57 years old. Clinical conditions that led to the initial angioplasty were: 4 acute coronary syndromes with persistent ST-segment elevation, 2 non Q wave acute myocardial infarctions and 2 unstable anginas (UA). The clinical presentations at the time of ISR diagnosis, in which PEB was applied were: 3 UA, 4 non Q wave acute myocardial infarctions and 1 asymptomatic patient with ischemia demonstrated by functional studies. Arteries involved were: 2 proximal anterior descending arteries, 3 mid anterior descending arteries, 1 mid circumflex artery and 2 mid right coronary arteries. 7 patients had diffuse ISR and 1 focal ISR. Clinical follow-up at 6,9 and 12 months after PEB angioplasty observed one not cardiovascular death and one lost at follow-up, the remainings patients were asymptomatics. Angiographic follow up showed ISR in 1 case. The image analysis determined that on average the MLD and MLA increase twice and four and a half times respectively between events “index” and “control”. Average late loss (final reduction in DLM) was 0,47 mm. No complications related to the use of PEB occurred.
Conclusion: the use of PEB in the treatment of ISR BMS resulted in a gain of DLM and ALM maintained at one year, recording no complications attributable to the procedure.
Key words:
CORONARY RESTENOSIS
OBSERVATIONAL STUDY
CASE REPORTS
Introducción
La reestenosis intrastent (RIS) se define como un estrechamiento de la luz de una arteria coronaria tratada previamente con angioplastia y colocación de stent. En su base patogénica se incluyen mecanismos como el retroceso elástico y la proliferación celular, predominando este último mecanismo. De acuerdo a diferentes series, su incidencia aproximada es de 40% para la angioplastia con balón, de 20% para stents convencionales (SC) y de 8% cuando se utilizan stents liberadores de fármacos (SLF) (1-4). El tratamiento de esta “segunda enfermedad” representa un desafío tanto clínico como técnico y se han evaluado diferentes modalidades terapéuticas. Las más destacadas son: una nueva dilatación con balón, braquiterapia local, implante de un nuevo stent (SC o SLF) y la angioplastia con balón liberador de paclitaxel (BLP). Esta última consiste en la dilatación de la zona estenótica con un balón especializado, cuya característica distintiva es la capacidad de lograr una rápida liberación de droga antiproliferativa (paclitaxel) en la pared vascular. Las tasas muy elevadas de recurrencia de reestenosis para el tratamiento con balón e implante de un nuevo stent convencional, así como las complicaciones vinculadas a la braquiterapia, hacen que estas opciones sean poco atractivas. Por esto, la posibilidad de aplicación de BLP o implante de SLF subsisten como las principales herramientas terapéuticas.
Los SLF se utilizan ampliamente en el tratamiento de los pacientes con RIS. Sin embargo, se plantea que el éxito de su utilización se debe predominantemente a la acción del fármaco antiproliferativo que inhibe el proceso patogénico de base, siendo menos relevante el efecto de soporte, salvo en casos especiales. Las ventajas teóricas del uso de BLP sobre SLF incluyen: el no agregado de metal a la pared arterial (cuerpo extraño), la independencia del uso de polímeros que podrían inducir reestenosis y una liberación más homogénea del fármaco antiproliferativo (superficie continua del balón versus discontinua del stent). Existe evidencia proveniente de estudios randomizados que avalan la utilización de BLP en el tratamiento de la RIS (5), sin embargo, en nuestro medio la experiencia es muy limitada y solo existen reportes con seguimiento clínico (6). El presente estudio piloto tiene como objetivo comunicar nuestra experiencia sobre la evaluación clínica e invasiva (angiográfica y ultrasonográfica) del tratamiento de la RIS con BLP.
Se analizan todos los casos tratados con BLP entre agosto del 2012 y julio del 2013. Se consideraron como criterios de inclusión: edad mayor de 18 años, presentar RIS por SC y dar consentimiento informado para el tratamiento con BLP y para el seguimiento angiográfico y ultrasonográfico a los 12 meses. El comité de Ética del Hospital de Clínicas evaluó y aprobó este protocolo de estudio. Fueron criterios de exclusión: enfermedad grave sistémica asociada (incluyendo insuficiencia renal o insuficiencia hepática severas), enfermedad que afecte la expectativa de vida a un año y necesidad de implante de un nuevo stent para el tratamiento de la RIS.
El estudio incluyó el análisis de tres eventos clínico-angiográficos denominados: índice, previo y control. En la figura 1 se muestra el esquema general del estudio.
El evento previo es la situación clínica que motivó el implante de SC inicial, acerca del cual se hace un análisis clínico-angiográfico retrospectivo. Se registraron los datos clínicos, angiográficos generales y del stent colocado, específicamente diámetro y longitud.
El evento índice, que corresponde a la captación del paciente, es la evolución reestenotica del SC inicial e incluyó un análisis clínico, un estudio angiográfico y la aplicación del BLP.
Desde el punto de vista clínico se registraron las características basales de la población estudiada y se clasificó la presentación clínica en síndrome coronario agudo con sobreelevación persistente del segmento ST, IAM noQ, angina inestable (AI) o asintomático con isquemia demostrada por estudio funcional.
Se utilizó un equipo angiográfico Artis Zee floor (SIEMENS, Munich-Germany) con un sistema angiográfico modular AXIOM Artis, digital, monoplano, equipado con un tecnología de detector plano. Este equipamiento cuenta con un software de cuantificación coronaria 2D validado que se denomina Scientific QCA Analysis que permite realizar una angiografía cuantitativa (AC). La AC con algoritmos para detección automática de bordes y video-densitometría permitió la evaluación de las dimensiones luminales del segmento arterial afectado con un alto grado de exactitud (8).
Los datos por AC incluyeron: diámetro luminar mínimo (DLM), diámetro de referencia de la arteria y área luminal mínima (ALM).
Se definió RIS en forma binaria (sí/no) de acuerdo a la existencia de un estrechamiento de la luz arterial mayor o igual al 50% a nivel del segmento tratado previamente, es decir el largo del stent y 5 mm proximal y distal al mismo. Se clasificó la RIS de acuerdo a la clasificación de Merhan (7), definiéndose como focal si el estrechamiento es menor a 10 mm de longitud, pudiendo ser de borde o no de acuerdo a la ubicación de la misma, difusa si es mayor de 10 mm, proliferativa si excede el o los bordes del stent y oclusiva si el estrechamiento es del 100% con flujo TIMI 0.
El evento índice incluyó además la angioplastia con BLP. Se aplicó un protocolo específico para este procedimiento, que incluyó el cruce de la zona de RIS con una guía de angioplastia, predilatación prolongada y repetida con balón convencional alcanzando igual diámetro que el BLP que se ha decidido aplicar posteriormente y aplicación del BLP, manteniéndolo insuflado durante 30-60 segundos para lograr la liberación del fármaco. El sector tratado con BLP debe exceder en longitud a la RIS. La relación objetivo de diámetros entre el stent previo y el BLP debe ser de 1:1 si el stent previo estaba correctamente expandido.
Se pesquisaron complicaciones angiográficas vinculadas a la angioplastia con BLP: disección, trombosis, retroceso elástico y necesidad de implante de un nuevo stent.
En el evento control se realizó un seguimiento clínico presencial a las 48 horas, 3, 6, 9 y 12 meses. Se consideraron como eventos cardiovasculares adversos mayores: angina estable, angina inestable, infarto agudo de miocardio no fatal, muerte cardiovascular, necesidad de una nueva revascularización de la lesión o del vaso tratado. Se realizó un estudio angiográfico con evaluación visual, cuantitativa y ultrasonográfica (IVUS) de la zona tratada con BLP a los 12 meses de seguimiento.
Las contraindicaciones para la realización del IVUS fueron: imagen de gran trombo en la arteria a evaluar, gran tortuosidad o calcificación que impidieran el avance de la sonda y reestenosis oclusiva (oclusión de 100%, TIMI 0). Los datos obtenidos por IVUS fueron el DLM y el ALM. Se utilizó el software del equipo iLab Ultrasound Imaging System para establecer las medidas mencionadas.
Resultados
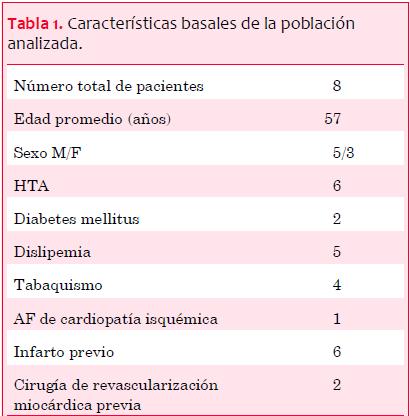
Se analizaron ocho pacientes con RIS, edad promedio de 57 años, tratados con angioplastia con BLP. Las características basales y los factores de riesgo cardiovascular de la población se detallan en la tabla 1.
La presentación clínica y las características angiográficas del evento previo se presentan en la tabla 2. La presentación en este evento correspondió en la mitad de los casos a síndrome coronario agudo con elevación del segmento ST (SCAcST) y en la otra mitad a síndromes coronarios agudos sin sobreelevación del ST (SCAsST). En el procedimiento inicial de angioplastia coronaria, en todos los casos se utilizó SC de diámetros entre 2,5 y 3,5 mm y longitudes entre 12 y 30 mm. El promedio de diámetro y longitud de los stents implantados fue de 2,9 y 20 mm respectivamente. Los segmentos tratados correspondieron en cinco casos a la arteria descendente anterior, dos casos a la arteria coronaria derecha y uno a la arteria circunfleja.
La forma de presentación en el evento Índice correspondió en 7 de 8 casos a SCAsST, con AI en 4 casos e IAM no Q en 3. Un paciente se presentó asintomático con isquemia demostrada por estudio funcional. La RIS comprobada fue difusa en 7 de 8 casos y focal en 1, no habiéndose comprobado RIS proliferativa ni oclusiva en ningún caso. El análisis por IC-stent no identificó ninguna fractura de stent. El tratamiento con BLP implicó el uso de dispositivos con diámetro entre 2,5 y 3,5 mm y longitudes entre 15 y 25 mm. En todos los casos el procedimiento fue considerado exitoso por el operador actuante. No se comprobó ninguna complicación asociada al uso de BLP (tabla 3).
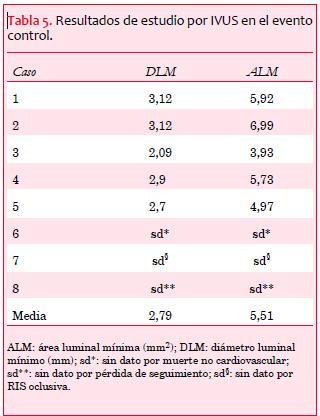
En el evento control y desde el punto de vista clínico, 6 de 8 pacientes se presentaron asintomáticos, no contando con datos de un paciente por pérdida de seguimiento y por una muerte no CV. Desde el punto de vista angiográfico, se comprobó un caso de nueva RIS, de tipo oclusivo, que requirió una nueva revascularización mediante angioplastia con implante de SLF. No se comprobaron alteraciones estructurales de los stents (tabla 4).
La evolución del ALM (figura 4) fue similar a la del DLM, con una ganancia asociada a la angioplastia con BLP que se mantuvo en el evento control. En un caso (caso 2) se observó aumento del ALM en el evento control, aunque sin aumento del DLM, lo cual es atribuible a irregularidad de la luz arterial o a error del método.
Discusión
La angioplastia coronaria con stents constituye una importante herramienta en el tratamiento de la cardiopatía isquémica; sin embargo, esta técnica implica riesgo de complicaciones evolutivas como trombosis intrastent, RIS y neoateromatosis. La RIS de los SC se mantiene como un problema clínico relevante y la decisión de tratarla con un SLF o con la aplicación de un BLP es controvertida. Múltiples estudios han demostrado la eficacia del BLP en diferentes escenarios clínicos (arterias de fino calibre, oclusiones crónicas totales, bifurcaciones y RIS) (13-17). En el tratamiento de la RIS el BLP ha sido comparado con SLF de primera y segunda generación con excelentes resultados clínicos-angiográficos y con tasas de reestenosis de un solo dígito(5,18,19). En el mismo sentido, su utilización tiene una recomendación IA en la guía de revascularización miocárdica de la Sociedad Europea de Cardiología más reciente, siendo su uso particularmente atractivo cuando existe más de una capa de stents en el segmento a tratar(20).
En nuestro medio el tratamiento de la RIS es exclusivo del implante de SLF y solo existen reportes con bajo número de pacientes con aplicación de BLP. El presente trabajo, comunica el análisis de una serie de pacientes con RIS tratados con BLP (Pantera Lux) con seguimiento clínico, angiográfico y ultrasonográfico.
La población incluida en esta serie, evidencia en el evento previo un riesgo clínico y angiográfico elevado de RIS, dado que la presentación clínica fue en todos los casos un síndrome coronario agudo y se trataron arterias coronarias de fino calibre con lesiones segmentarias.
En este grupo la angioplastia protocolizada con BLP fue utilizada también en un escenario de riesgo elevado de nueva RIS. Es así que en 7 de 8 casos la RIS inicial fue difusa (>10 mm) y la presentación clínica fue nuevamente la de un síndrome coronario agudo, a pesar de lo cual la angioplastia logró una ganancia luminal adecuada y en ningún caso se asoció a disección o trombosis coronaria.
El caso que evolucionó a una nueva RIS, en esta instancia oclusiva, correspondió a un paciente diabético, con una arteria tratada fina (2,5 mm de diámetro) en el que se logró la menor ganancia luminal en la angioplastia con BLP, evaluada tanto por DLM como por ALM. Probablemente este caso debió haber sido tratado inicialmente con SLF. Sin embargo, nuestro análisis imagenológico no identificó una alteración estructural que justificara este planteo.
Los resultados obtenidos en nuestra serie están en concordancia con los resultados presentados sobre eficacia y seguridad del uso de BLP en el tratamiento de la RIS. Esto abona la idea de que en el tratamiento de la RIS, una vez excluidas algunas condiciones particulares que exigen un nuevo soporte vascular metálico, el tratamiento con BLP con paclitaxel es una opción válida.
Limitaciones
Se trata de una serie con un bajo número de casos. Se realizó IVUS solo en el evento control.
Conclusiones
La utilización de BLP en el tratamiento de la RIS determinó una ganancia de DLM y ALM mantenidas al año de seguimiento, no registrándose complicaciones atribuibles al procedimiento.
Financiación del estudio
Los BLP fueron donados al Centro Cardiovascular Universitario por la compañía Biotronik. Esta no intervino en ninguna de las etapas del estudio.
Bibliografía
1. Fischman DL,
2. Serruys PW, de Jaegere P, Kiemeneij F, Macaya C, Rutsch W, Heyndrickx G, et al. A comparison of balloon expandable stent implantation with balloon angioplasty in patients with coronary artery disease: Benestent Study Group. N Engl J Med 1994; 331(8):489–95.
3. Moses JW, Leon MB, Popma JJ, Fitzgerald PJ, Holmes DR, O’Shaughnessy C, et al. Sirolimus-eluting stents versus standard stents in patients with stenosis in a native coronary artery. N Engl J Med 2003; 349(14): 1315-23.
4. Stone GW, Ellis SG, Cox DA, Hermiller J, O’Shaughnessy C, Mann JT, et al. A polymer based, paclitaxel-eluting stent in patients with coronary artery disease. N Engl J Med 2004;350(3): 221-31.
5. Unverdorben M, Vallbracht C, Cremers B, Heuer H, Hengstenberg C, Maikowski C, et al. Paclitaxel coated balloon catheter versus paclitaxel coated stent for the treatment of coronary instent restenosis. Circulation 2009;119(23):2986-94.
6. Jubany L, Korytnicki D, Artucio C, Tuzman A, Irigoin J, Pouso M, et al. Resultado angiográfico inicial y evolución clínico-centellográfica a seis meses de la ATC con balón liberador de Paclitaxel en reestenosis severa intrastent [Resumen]. Rev Urug Cardiol 2012;27 Supl 1:S45-6.
7. Mehran R, Dangas R,
8. Chrysafios G, Serruys P. Contemporary angiographic analysis of coronary stenosis. En: Escaned J, Serruys P, editores. Coronary stenosis imaging, structure and physiology.
9. Bismuth V, Vaillant R, Funck F, Guillard N, Najman L. A comprehensive study of stent visualization enhancement in X-ray images by image processing means. Med Image Anal 2011; 15(4):565-76. doi: 10.1016/j.media.2011.03.002.
10. Sianos G, Hofma S, Ligthart JM, Saia F, Hoye A, Lemos PA, et al. Stent fracture and restenosis in the drug eluting stent era. Catheter Cardiovasc Interv 2004;61(1):111-6.
11. Kim MS, Eng MH,
13. Scheller B, Hehrlein C, Bocksch W, Rutsch W, Haghi D, Dietz U, et al. Treatment of coronary in-stent restenosis with a paclitaxel coated balloon catheter. N Engl J Med 2006;355(20):2113-24.
14. Scheller B, Hehrlein C, Bocksch W, Rutsch W, Haghi D, Dietz U, et al. Two year follow up after treatment of coronary instent restenosis with a paclitaxel coated balloon catheter. Clin Res Cardiol 2008;97(10):773-81.
15. Unverdorben M, Kleber FX, Heuer H, Figulla HR, Vallbracht C, Leschke M, et al. Treatment of small coronary arteries with a paclitaxel coated balloon catheter. Clin Res Cardiol 2010; 99(3):165-74.
16. Pöss J, Jacobshagen C, Ukena C, Böhm M. Hot lines and clinical trial updates presented at the German Cardiac Society Meeting 2010: FAIRHF, CIPAMI, LIPSIANSTEMI, Hand held BNP, PEPCAD III, remote ischaemic conditioning, CERTIFY, PreSCDII, German Myocardial Infarction Registry, DiaRegis. Clin Res Cardiol. 2010;99(7): 411-7
17. Windecker S, Kolh P, Alfonso F, Collet JP, Cremer J, Falk V, et al. 2014 ESC/EACTS Guidelines on myocardial revascularization: The Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS)Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2014;35(37): 2541- 619.
18. Mathey DG, Boxberger M, Bonaventura K, Kleber FX. Treatment of bifurcation lesions with a drug eluting balloon: the PEPCAD V (Paclitaxel Eluting PTCA Balloon in Coronary Artery Disease) trial. EuroIntervention. 2011;7:K615.
19. Alfonso F, Perez-Vizcayno MJ, Cárdenas A, García Del Blanco B, Seidelberger B, Iñiguez A, et al. A randomized comparison of drug-eluting balloon versus everolimus-eluting stent in patients with bare-metal stent In-stent restenosis: the RIBS V clinical trial. J Am Coll Cardiol 2014; 63(14): 1378-86.
20. Hehrlein C, Dietz U, Kubica J, Jorgensen E, Hoffmann E, Naber C, et al. Twelve-month results of a paclitaxel releasing balloon in patients presenting with in-stent restenosis first-in-man (PEPPER) trial. Cardiovasc Revasc Med 2012; 13(5):260-4.