Dres. Robinson Rodríguez*, Karina Lombardo†, Gloria Roldán†, Jaime Silvera‡, Roberto Lagomarsino‡
Unidad de Neuro-Oncología. Departamento de Oncología. Hospital de Clínicas. Facultad de Medicina. Universidad de la República. Montevideo, Uruguay.
Resumen
Introducción: el glioblastoma multiforme (GBM) representa la forma más agresiva de los gliomas. La sobrevida a cinco años con el tratamiento quirúrgico exclusivo es nula. El agregado radioterapia (RT) y quimioterapia (QT) prolongan la sobrevida. Objetivo: evaluar el impacto del tratamiento en la sobrevida de pacientes portadores de GBM. Pacientes y métodos: se incluyeron los pacientes con diagnóstico histológico de GBM asistidos en la Unidad de Neuro-Oncología del Hospital de Cínicas, de 1980 a 2000. Se recabaron datos patronímicos, clínicos, paraclínicos y evolutivos de las historias clínicas. Se calculó la sobrevida mediante el método de Kaplan Meier y Mantel Cox. Resultados: se estudiaron 65 pacientes con una edad mediana de 58 años (rango: 6-79). Recibieron cirugía 100% (completa en 22 pacientes, subtotal en 9, parcial en 32 y biopsia en 2). El 92% recibió RT posoperatoria y 25% QT. La mediana de sobrevida fue de 46,6 semanas y la sobrevida global al año fue de 28%. La probabilidad de sobrevida al año fue 0 en los pacientes que recibieron cirugía exclusiva; 0,23 en los que se agregó RT, y 0,62 en los tratados con QT (p=0,0001). El análisis multivariable identificó como variables independientes: el tratamiento multimodal incluyendo quimioterapia (p=0,003) y buen estado neurológico posoperatorio (p=0,007). Conclusiones: la mediana de sobrevida de esta serie fue similar a lo descrito en la literatura, existiendo una sobrevida mayor en los pacientes con buen estado neurológico tratados con cirugía seguida de RT y QT.
Palabras clave: GLIOBLASTOMA - terapia ANÁLISIS DE SUPERVIVENCIA
Keywords: GLIOBLASTOMA - therapy SURVIVAL ANALYSIS
* Colaborador honorario del Servicio de Oncología Clínica. Coordinador de la Unidad de Neuro-Oncología Departamento de Oncología. Hospital de Clínicas. Facultad de Medicina, Universidad de la República. Uruguay.† Ex Residentes de Oncología Médica. Facultad de Medicina, Universidad de la República. Uruguay.‡ Oncólogo. Uruguay.
Correspondencia: Dr. Robinson Rodríguez. Departamento de Oncología. Hospital de Clínicas. Avda. Italia s/n, planta baja. Montevideo, Uruguay. Correo electrónico: rrodri@hc.edu.uy. Recibido:8/6/12 Aceptado:26/10/12. Conflicto de interés: los autores del presente artículo declaran que no existen conflictos de interés.
Introducción
]]> Los tumores malignos del sistema nervioso central (SNC) han sido históricamente considerados muy agresivos y de mala evolución, despertando poco interés en su estudio, así como pesimismo en el paciente, la familia y el equipo asistencial. Representan el 2% de todos los tumores malignos en el adulto. En Estados Unidos la incidencia es de 6/100.000 individuos(1). Esto refleja un dramático aumento en la incidencia de tumores primarios encefálicos, en particular en los pacientes añosos en las últimas décadas.En Uruguay y de acuerdo a los registros de la Comisión Honoraria de Lucha contra el Cáncer, la incidencia es de 5,68 casos para hombres y de 4,25 para las mujeres(2).
La incidencia de tumores primitivos encefálicos es variable, dependiendo fundamentalmente del intervalo etario considerado. Se trata de los tumores sólidos más frecuentes en niños, constituyendo la segunda causa de muerte por cáncer en menores de 15 años, y la tercera entre los 15 y 34 años; sin embargo, la mayoría de los tumores intracraneales ocurren en mayores de 45 años.
Los gliomas son los tumores más frecuentes del SNC, constituyendo entre 50% a 70% de los tumores primarios del SNC. Dentro de los mismos los astrocitomas son los más frecuentes; en un extremo se encuentra el astrocitoma pilocítico (glioma grado 1) y el astrocitoma grado 2, ambos gliomas de bajo grado, y en el otro extremo los gliomas agresivos, astrocitoma anaplásico (glioma grado 3) y el glioblastoma multiforme (GBM) o glioblastoma (glioma grado 4). Este último puede ser un tumor de novo o la evolución de otros gliomas de menor grado, con un comportamiento muy agresivo(3,4).
En conjunto, el astrocitoma anaplásico y el GBM representan más de la mitad de todos los tumores astrocitarios, siendo estos últimos los tumores intracraneales primarios más frecuentes, 15% a 20% de todos los tumores intracraneales y 50% de todos los gliomas(5,6).
El GBM predomina en la quinta y sexta décadas de la vida y es raro su aparición en pacientes jóvenes, menores de 30 años, con alta frecuencia en hombres (3:2)(6). La incidencia de todos los gliomas se incrementa con la edad, pero este incremento es aun mayor para los GBM, lo que indicaría, según algunos autores, un diferente mecanismo de carcinogénesis(7).
Las modalidades imagenológicas empleadas para el estudio de los tumores encefálicos son la resonancia magnética (RM) y la tomografía computada (TC), las cuales pueden definir la extensión de la neoplasia, así como el edema peritumoral y el efecto de masa típicamente asociados en los GBM. La RM permite mejor delimitación, y diferencia de hemorragia intratumoral, por lo que se considera más sensible y específica que la TC, por lo cual ha sustituido a esta(8,9).
El glioblastoma es el tumor primario más frecuente del adulto, en general rápidamente fatal, con una mediana de sobrevida de 9 a 12 meses(6).
En el grupo de pacientes mayores de 60 años, la mediana de sobrevida es de 35 semanas(10). Se han asociado con un pronóstico más favorable, la edad más temprana al momento del diagnóstico, un mejor nivel de funcionamiento neurológico y la resección amplia(5). Clásicamente se menciona que la performance estatus preoperatoria es un importante factor pronóstico, así como el volumen tumoral resecado(11,12).
El objetivo de este trabajo es evaluar las características clínicas, tratamiento y sobrevida de los pacientes portadores de GBM de hemisferios cerebrales tratados en la Unidad de Neuro-Oncología del Departamento de Oncología del Hospital Clínicas de la Facultad de Medicina, Montevideo, Uruguay.
]]> Revisión de la literaturaCirugía
La cirugía citorreductora, aunque no es curativa, sigue desempeñando un papel importante, ya que permite confirmar el diagnóstico histológico definitivo, aliviar en forma inmediata los efectos del ascenso de la presión intracraneana y de la compresión neurológica focal. Por lo tanto, en la mayoría de los pacientes debe contemplarse algún grado de cirugía citorreductora siempre que pueda llevarse a cabo sin alto riesgo de deteriorar la función neurológica. En el caso de las lesiones situadas en zonas elocuentes o inaccesibles (cerebrales profundas o tronco cerebral), la biopsia estereotáxica permite establecer el diagnóstico(5).
Aunque existe una correlación positiva entre la supervivencia y la magnitud de la extirpación tumoral, su naturaleza infiltrante hace que todos recidiven. La mediana de sobrevida solo con cirugía es de cuatro meses.
Radioterapia
Hasta hace pocos años, la radioterapia (RT) era el único tratamiento estándar luego de la cirugía, mejorando la sobrevida, pero menos de 15% de los pacientes están vivos a dos años y la supervivencia a largo plazo es rara(5). Bouchard y Pierce reportaron en 1960 que los pacientes que recibieron RT craneal posoperatoria tuvieron mayor sobrevida que aquellos que no la recibieron. Esta observación fue confirmada por the Brain Tumor Study Group (BTSG) en el ensayo randomizado 69-01, reportando una mediana de sobrevida en este estudio de 36 versus 14 semanas (p=0,001) a favor del grupo que recibió RT. Subsecuentes ensayos del Scandinavian Glioblastoma Study Group y del BTSG han demostrado la ventaja de la administración de RT luego de la cirugía(13). El primer análisis con vistas a establecer la dosis de RT necesaria para obtener un beneficio en la sobrevida fue publicado por Walker y colaboradores, quienes concluyeron que existe una clara respuesta con dosis totales de 50 a 60 Gy. Otro estudio randomizado conducido por el Eastern Cooperative Oncology Group (ECOG) no pudo demostrar un beneficio de administrar dosis superiores (60 - 70 Gy). La dosis estándar de RT, por lo tanto, es de 60 Gy en fraccionamiento de 1,8 a 2,0 Gy diarios (13,14). La RT se administra en el período posoperatorio entre tres y cuatro semanas luego de la cirugía, con una adecuada cicatrización de la herida operatoria(15). Los regímenes de hiperfraccionamiento están siendo investigados(13,16). La RT hiperfraccionada permite alcanzar mayor dosis que la RT estándar en tratamientos diarios múltiples(13). Altas dosis, mayores a 70 Gy o hiperfraccionamiento (mayor de 80 Gy), no han mostrado incrementos en la sobrevida.
Mejoras en los estudios imagenológicos, particularmente con el desarrollo de la TC y la RM, han redefinido la planificación del tratamiento de RT y el blanco de acción para los pacientes portadores de gliomas. Para los pacientes con gliomas unifocales, el volumen inicial debe abarcar 2 a 3 cm del margen tumoral (con o sin edema peritumoral) definido por TC o RM, dado que luego del tratamiento inicial los tumores recurren entre 1 a 2 cm del tumor original(17).
La radiocirugía y la RT estereotáxica fraccionada son un campo de activa investigación, y si bien no forman parte del tratamiento de primera línea del glioblastoma, en casos seleccionados pueden ser empleadas en el retratamiento de estos pacientes(18).
Quimioterapia
La quimioterapia (QT) usada como adyuvante o en la recaída de los gliomas agresivos y en particular en el glioblastoma ha tenido un rol marginal, siendo las más empleadas las nitrosureas, como la carmustina (BCNU), lomustina (CCNU), nimustina (ACNU) y la procarbazida, hasta el advenimiento de la temozolomida, que luego de resultados alentadores en la recaída pasó a ser el tratamiento de primera línea en forma concurrente con la RT y adyuvante por seis meses, luego del trabajo de Stupp y colaboradores publicado en el año 2005(19-36).
]]> Walker y colaboradores, en un ensayo cooperativo, evaluaron el tratamiento de los gliomas anaplásicos con BCNU (80 mg/m2 día por tres días cada seis a ocho semanas) y/o RT posoperatoria (5.000 a 6.000 cGys), demostrando que estos tratamientos mejoraban la sobrevida comparados con el mejor cuidado convencional(19). Los mismos autores, en un estudio randomizado de cirugía seguida de RT con y sin nitrosourea adyuvante, no encontraron aumento de la sobrevida con el agregado de la QT(20).Uno de los principales problemas para demostrar el beneficio de la QT en adyuvancia es que la mayoría de los estudios en forma individual no cuentan con el número suficiente de pacientes(20,21). En 1993, Fine demuestra, por medio de un metaanálisis, la ventaja del agregado de QT a la RT posoperatoria con un aumento de la sobrevida a dos años de 16,4% a 25% en pacientes con astrocitoma anaplásico y GBM(22).
Hildebrand y colaboradores, en un estudio randomizado de astrocitomas anaplásicos, compararon el agregado de dibromodulcitol y carmustina a la RT, encontrando un beneficio en la mediana de sobrevida y progresión lesional en el brazo que recibió QT(23). Sin embargo, más recientemente un estudio randomizado que comparó el agregado de poliquimioterapia tipo PCV (procarbazida, lomustina y vincristina) en pacientes con astrocitoma anaplásico y GBM, no encontraron beneficio en la sobrevida en comparación con el brazo que solo recibió RT(24). En el 2002, Stewart publica un nuevo meta-análisis, basado en 12 ensayos clínicos, que muestra un aumento de la sobrevida a dos años en pacientes que recibieron QT adyuvante, del 31% a 37% en astrocitoma anaplásico y de 9% a 13% en GBM(25).
En nuestro medio, en un estudio randomizado de cirugía seguida de RT con y sin QT con tenipósido en gliomas astrocitarios malignos, si bien hubo un aumento de la mediana de sobrevida con el agregado de QT, la misma no alcanzó significación estadística(26).
En el tratamiento adyuvante de los gliomas agresivos no hay evidencia de que la combinación de QT sea superior a la monoquimioterapia(27), siendo mayor el impacto en la sobrevida en niños y adultos jóvenes en comparación con pacientes añosos, en los cuales produce un beneficio menor (más de 60 años)(10).
La temozolomida, un alquilante de última generación, de uso por vía oral, fue empleada en la recaída de los gliomas agresivos y fueron publicados por lo menos cuatro ensayos clínicos no randomizados y uno randomizado, con resultados alentadores por las respuestas objetivas, prolongación de la sobrevida libre de progresión, pero sin un claro aumento de la sobrevida global(28-34).
Un estudio piloto de fase II valoró la tolerancia y eficacia de temozolomida concurrente con RT radical con un fraccionamiento habitual y luego adyuvancia mensual durante seis meses en glioblastoma con buena tolerancia y una tasa de sobrevida de 31% a dos años(35).
En el año 2005, Stupp y colaboradores publicaron el ensayo clínico randomizado, multicéntrico, fase III, que comparó cirugía seguida de RT y cirugía seguida de RT con temozolomida concurrente y adyuvante durante seis meses como primera línea de tratamiento.
Fueron randomizados 573 pacientes con una mediana de edad de 56 años y con un seguimiento mediano de 28 meses, la mediana de sobrevida fue de 14,6 meses para el brazo de RT y temozolomida contra 12,1 meses para el brazo de RT.
La tasa ajustada mostró una reducción de la mortalidad de 37% en el brazo que incluyó QT, 0,63 (p < 0,001).
]]> La tasa de sobrevida a dos años fue de 26,5% para la asociación contra 10,4 % para el brazo de RT exclusiva.En resumen, la temozolomida en combinación con la RT como primera línea de tratamiento para el glioblastoma prolonga la sobrevida y se convirtió en el tratamiento estándar(36).
En el año 2009, Stupp y colaboradores comunican los resultados de dicho estudio luego de un seguimiento de cinco años(37).
La sobrevida global fue de 27,2% a dos años, 16% a tres años, 12,1% a cuatro años y 9,8% a cinco años para el brazo de RT y temozolomida, mientras que fue de 10,9%, 4,4%, 3% y 1,9% para RT exclusiva, respectivamente.
El beneficio del tratamiento combinado fue para todos los subgrupos de riesgo, incluyendo a los pacientes entre 60 y 70 años de edad.
La metilación del promotor de la MGMT (metil guanina metil transferasa) fue el predictor más importante del beneficio del tratamiento con temozolomida.
Pacientes y métodos
En este estudio retrospectivo fueron incluidos los pacientes que consultaron en la Unidad de Neuro-Oncología del Departamento de Oncología del Hospital de Clínicas de la Facultad de Medicina de Montevideo, Uruguay, con diagnóstico histológico de glioblastoma de hemisferios cerebrales, en el período comprendido entre enero de 1980 a diciembre de 2000.
Se revisaron las historias clínicas del Departamento de Oncología, y cuando lo requirió, se consultó la historia central recabando los siguientes datos: edad, sexo, síntomas al inicio del cuadro y duración, localización tumoral, paraclínica realizada, tratamiento instituido. Se incluyeron detalles de la cirugía y el estado neurológico posterior a la misma, así como de la radioterapia dosis y tiempo de la misma, y si recibió quimioterapia, fármacos y series realizadas. Se determinó también tiempo de seguimiento. En aquellos pacientes en que teníamos una pérdida de seguimiento, se trató de ubicarlos por vía telefónica a su domicilio o a través del documento de identidad, verificar la fecha de fallecimiento en el Registro de la Comisión Honoraria de Lucha contra el Cáncer.
Por el tipo de cirugía realizada se catalogó como completa cuando el cirujano logró la exéresis tumoral macroscópicamente completa; subtotal cuando persistió un pequeño remanente (menor a 10% del volumen inicial), parcial cuando la exéresis comprendió entre 50% y 90% del tumor, y biopsia cuando solo se pudo obtener una muestra para diagnóstico.
]]> Según el estado neurológico posoperatorio se catalogó como bueno cuando el paciente no presentaba déficit neurológico, regular cuando tenía algún signo deficitario, pero que le permitía realizar sus actividades cotidianas, y malo cuando la secuela le impedía realizar su actividad cotidiana sin ayuda.Se consideró como paciente tratado con RT aquel que completó al menos 40 Gy, así como con respecto a la QT los que recibieron tres series o más.
Se calculó el tiempo de sobrevida en base al intervalo entre la cirugía y la fecha de fallecimiento o del último control. Los datos de sobrevida global y estratificada fueron representados gráficamente según método de Kaplan-Meier, ofreciendo al final de los intervalos las probabilidades de sobrevida con intervalos de confianza de 95% (IC 95%). Las curvas fueron comparadas a través de la prueba de Mantel Cox con alfa = 0,05 en todos los estratos considerados.
En el modelo multivariable se incluyeron: edad (como variable continua), sexo, tratamiento (cirugía, radioterapia y quimioterapia versus cirugía y radioterapia), estado neurológico (bueno versus malo/regular).
El proceso de datos se realizó a través de Epi.Info 6,04b, Prophet (INH) y SPSS V8,01 para Windows.
Resultados
Se incluyeron 65 pacientes cuyas características se muestran en la tabla 1 a-b. La edad mediana de presentación fue de 58 años con un rango de 6 meses a 79 años (figura 1). La distribución por sexo fue de 32 hombres y 33 mujeres, respectivamente. En cuanto a la topografía tumoral, en 33 pacientes se localizó en hemisferio derecho, en 31 en izquierdo y en uno fue bilateral (tabla 2).
La duración de los síntomas previos al diagnóstico osciló entre dos días y un año, con una media de 55 días y una mediana de 60 días (en un paciente no contamos con el dato). En la presentación clínica se destaca el déficit motor en 58% de los pacientes, hipertensión endocraneana en 47%, trastornos del lenguaje (24%), crisis convulsivas (23%), síndrome frontal (16%), cefalea (13%), trastornos visuales (9%), trastornos del carácter (6%) y déficit sensitivo (4%) (tabla 3).

Previo a la cirugía los pacientes fueron estudiados con TC de cráneo.
]]> Todos los pacientes de la casuística fueron abordados quirúrgicamente con diferente grado de agresividad. La exéresis fue completa en 22 pacientes, subtotal en 9, parcial en 32 y biopsia en 2 pacientes (tabla 4).
El estado neurológico posoperatorio fue bueno en 36 pacientes (55%), regular en 22 (34%) y malo en 7 pacientes (11 %).
Recibieron RT posoperatoria 60 pacientes (92%), y con el agregado de QT, 30 pacientes (46%), pero solo 16 recibieron tres o más ciclos (25%).
Los fármacos usados en primera línea fueron procarbazida a dosis habitual por vía oral, de 14 días de tratamiento y una semana de descanso, mientras que el tenipósido por vía intravenosa a la dosis de 50 mg por día durante cinco días mensual.
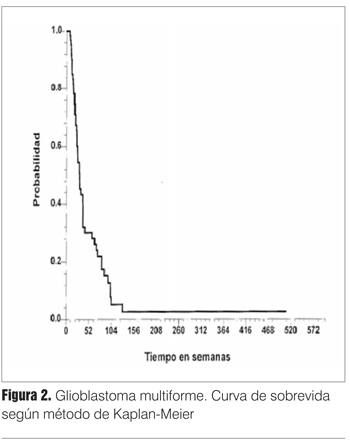
La mediana de sobrevida de la serie fue de 46,6 semanas, y la sobrevida al año de 28%, con un seguimiento entre 5 y 508 semanas (figura 2).
Factores pronósticos-análisis univariable
Edad y sexo
En los pacientes menores de 60 años (22 pacientes) la mediana de sobrevida fue de 30,5 semanas y la sobrevida al año fue de 32%. En los pacientes de 60 años o más, la mediana de sobrevida fue de 21 semanas y la sobrevida al año fue de 27%. La diferencia de sobrevida estuvo en el límite de la significación estadística (p?0,06).
]]> La mediana de sobrevida fue de 30 semanas para las mujeres y de 22 semanas para los hombres, con sobrevidas al año de 22% y 38%, respectivamente (p?0, 95).Estado neurológico
Según estado neurológico, la sobrevida mediana fue: bueno 32,5 semanas, regular 20,5 semanas y malo 21 semanas. La sobrevida al año fue de 48%, 12% y 0%, respectivamente (p?0,009).
Tratamiento
Los pacientes tratados con cirugía exclusiva tuvieron una mediana de sobrevida de 20,2 semanas. En los que recibieron cirugía más radioterapia la mediana fue de 20,5 semanas. En los que se agregó a la cirugía y radioterapia, quimioterapia, la mediana de sobrevida fue de 69,5 semanas. La sobrevida al año, según cirugía, cirugía más RT, cirugía más RT más QT fue de: 0%, 23% y 62%, respectivamente.
Estos resultados tuvieron significación estadística a favor del grupo que recibió quimioterapia (p?0,0001).
Cuando fueron comparados los grupos que recibieron QT o no recibieron, se vio que la mediana de sobrevida fue de 69,5 semanas versus 20 semanas, con una sobrevida al año de 62% y 3%, respectivamente (p? 0,001).
La mediana de sobrevida en los pacientes en que se efectuó cirugía parcial fue de 22,5 semanas. Los que recibieron cirugía total y subtotal tuvieron una mediana de 31 semanas, siendo la sobrevida al año de 24%, y 39%, respectivamente (p?0,12).
La radioterapia fue efectuada a través de un equipo de Cobalto 60. Los pacientes que recibieron tratamiento holocraneal (HC) tuvieron una mediana de sobrevida de 21 semanas y los que fueron irradiados con campos reducidos (CPO), de 34 semanas. La sobrevida al año fue de 14% y 49%, respectivamente (p?0,001).
Factores pronósticos-análisis multivariable
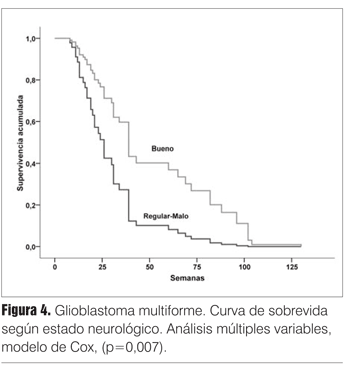
]]> En el análisis multivariable la inclusión de quimioterapia en el tratamiento posoperatorio y el buen estado neurológico posoperatorio se identificaron como factores pronósticos independientes asociados con una prolongación estadística de la sobrevida global (p=0,003 y p=0,007, respectivamente) (figuras 3 y 4).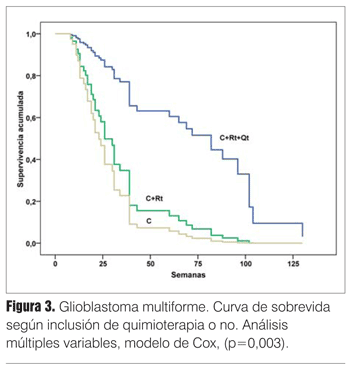
Tratamiento de la recidiva
Solo seis pacientes de la serie recibieron tratamiento oncoespecífico en el momento de la recidiva o progresión lesional, correspondiendo a cuatro hombres y dos mujeres.
En dos casos se realizó exéresis quirúrgica y todos recibieron quimioterapia, siendo los citostáticos empleados procarbazida en uno, carmustina en dos, tenipósido en dos y procarbazida, seguido de tenipósido, en uno.
La sobrevida adicional osciló entre 1 y 12 meses.
Los dos pacientes que fueron tratados con cirugía y quimioterapia tuvieron una sobrevida adicional de 11 y 12 meses, respectivamente.
El caso tratado con quimioterapia secuencial presentó una sobrevida adicional de nueve meses.
]]> DiscusiónEl tratamiento del GBM ha evolucionado en los últimos años. Sabiendo que la cirugía sola no es curativa, se ha intentado mediante la integración de otras modalidades, como RT y QT, prolongar el tiempo de sobrevida. El principal objetivo de la exéresis, lo más completa posible, es la confirmación diagnóstica y la reducción de la masa tumoral, la cual es dificultosa por su naturaleza infiltrante y su rápido crecimiento(1).
El grado de resección tiene importancia pronóstica, ya que el tejido remanente se beneficia de un mayor aporte de oxígeno y es donde tanto la RT como la QT pueden actuar con mayor efectividad(38).
La RT externa posquirúrgica ha mostrado mejorar los resultados de la cirugía. En cuanto a los campos de RT se sabe que la RT local radical obtiene iguales resultados terapéuticos que la holocraneal, con menos efectos secundarios(19,20,39).
En nuestra serie, un número importante de pacientes recibieron RT holocraneal y el equipo empleado fue de Cobalto 60, cuando hoy día se sabe que la misma debe ser efectuada con campos reducidos y con acelerador lineal, con una planificación 3D.
Debemos resaltar que la presencia de infiltración tumoral bihemisférica puede requerir la indicación de campos holocraneanos en algunos pacientes. Afortunadamente estos casos son infrecuentes.
En un intento de mejorar estos resultados, diferentes ensayos han utilizado distintos citostáticos, como monodroga o en forma de poliquimioterapia, demostrando desde el metaanálisis de Fine que existe un beneficio significativo en la administración de QT adyuvante(22).
En el año 2005 fueron publicados por Stupp y colaboradores, los resultados del estudio randomizado fase III que comparó cirugía seguida de RT contra cirugía seguida de RT y temozolomida concurrente, y luego en adyuvancia durante seis meses, mostrando un aumento en la sobrevida libre de progresión, mediana de sobrevida y en la sobrevida global en el brazo que recibió QT. La mediana de sobrevida fue de 12 y 15 meses y la sobrevida global a dos años de 10,4% y 26,5%, sin y con temozolomida, respectivamente, todas diferencias estadísticamente significativas (p<0,001)(36), por lo cual desde entonces se ha convertido en el nuevo estándar.
Más recientemente y con un seguimiento a cinco años, se mantiene el beneficio del brazo que incluyó a la temozolomida, con una sobrevida a cinco años de 9,8% contra 1,9% para la RT exclusiva(37).
Debemos destacar que nuestra serie es pretemozolomida, y que este agente no ha sido comparado en estudios randomizados con los agentes utilizados por nosotros.
]]> En nuestra casuística hemos encontrado que los síntomas más frecuentes como forma de presentación fueron los trastornos motores (déficit motor), las afasias y los episodios convulsivos, iguales a los descritos en la literatura(1). No hubo predominio en cuanto al sexo, a diferencia de otros estudios donde existe un predominio masculino.En lo referente a la localización predominaron las localizaciones frontales y temporales, pero en varios casos se observó su extensión a más de una topografía, siendo la distribución en cuanto a hemisferio, izquierdo o derecho, equitativa.
Los análisis de sobrevida mostraron un beneficio con la adición de quimioterapia tanto en la comparación con la cirugía (p=0,0001), como con la cirugía más RT (p=0,001). La mediana de sobrevida para los pacientes tratados con cirugía, RT y QT fue similar a la descrita en la literatura(23,27).
Se obtuvo un discreto beneficio en la sobrevida con la exéresis completa o subtotal con respecto a la parcial, pero sin significación estadística.
Llamativamente, cuando analizamos la sobrevida en relación con los campos de RT recibida, encontramos un beneficio estadísticamente significativo a favor de los que recibieron campos reducidos comparada a la holocraneana, que podría estar vinculado a una mejor planificación de tratamiento, llegando a dosis más altas sobre el lecho tumoral sin poder descartar que la extensión tumoral sea el principal factor, reconociendo que pacientes con tumores más voluminosos suelen presentar peor estado neurológico, reconocido factor con valor pronóstico negativo.
Se describe como factor de buen pronóstico la menor edad y en nuestra serie los pacientes menores de 60 años presentaron un beneficio en sobrevida en el límite de la significación estadística.
El estado neurológico posoperatorio y el tratamiento multimodal incluyendo QT resultaron factores pronósticos independientes en esta serie.
Destacamos que la sobrevida global fue de 46,6 semanas, también acorde a los datos aportados por otros autores, aunque menores que los resultados de Stupp.
Las limitaciones de este trabajo, que pueden explicar parcialmente esta discrepancia, incluyen su naturaleza retrospectiva, el uso de diferentes agentes quimioterápicos y los avances posteriores tanto en el área de la imagenología como de planificación y administración de RT(1,2,36,37).
En nuestra serie solo 9% de los pacientes recibió tratamiento oncoespecífico en el momento de la recidiva, quizás debido a que la mayoría había recibido RT como primera línea y en cuanto a la QT, se contaba con un arsenal reducido, a lo que debe agregarse la discusión del beneficio de la QT como segunda línea en el período analizado.
]]> El presente reporte resultará fundamental en el futuro, cuando con un adecuado tiempo de seguimiento intentemos comparar esta cohorte de pacientes con aquellos tratados a partir del año 2005 con temozolomida.Conclusiones
En este estudio ratificamos el valor pronóstico independiente del estado neurológico posoperatorio y de la inclusión de QT en el tratamiento del GBM.
A pesar de no constituir un estudio randomizado, este trabajo nos permite valorar los resultados obtenidos en el tratamiento de pacientes con GBM previo al advenimiento de temozolomida en nuestro hospital universitario, que es centro de referencia nacional.
Agradecimientos
Agradecemos al Dr. Jorge Pouso, Ex Jefe del Departamento de Enseñanza e Investigación de la Dirección Nacional de Sanidad de las Fuerzas Armadas, por su colaboración en el análisis estadístico.
Summary
Introduction: glioblastoma multiforme (GBM) is the most agressive kind of gliomas. The 5-year survival rate for exclusive surgical treatment is null. Additional chemotherapy and radiotherapy increases survival.
Objective: to evaluate the impact of treatment in the survival of patients suffering from GBM.
Method: patients with a histological diagnosis of GBM who were seen at the Neuro-Oncology Unit of the Clínicas Hospital, from 1980 through 2000. Clinical, paraclinical and patronymic data was collected, the same as information on the evolution of medical records. Survival rates were calculated through the Kaplan Meier and Mantel Cox method.
]]> Results: 65 patients with an average age of 58 years old were studied, (range: 6-79). All of them underwent surgery (complete in 22 patients, subtotal in 9, partial in 32 and biopsy in 2 patients). Ninety two percent of patients were treated with radiotherapy and 25% with chemotherapy. Median survival was 46.6 weeks and global survival one year after was 28%. The probability for survival one year after was 0 in patients who were treated only with surgery; 0.23 in those who also received radiotherapy and 0.62 with chemotherapy QT (p=0,0001).Multivariable analysis identified the following independent variables: multimodal treatment including chemotherapy (p=0,003) and a good postoperative general condition (p=0,007).
Conclusions: median survival in this series was similar to that described in literature, there existing a longer survival rate for patients with a good neurologic condition who are treated with radiotherapy and chemotherapy after surgery.
Resumo
Introdução: o glioblastoma multiforme (GBM) é a forma mais agressiva dos gliomas. A sobrevida aos cinco anos é nula quando o paciente recebe exclusivamente tratamento cirúrgico. Observa-se um aumento da sobrevida quando ademais da cirurgia se agrega radioterapia (RT) e quimioterapia (QT).
Objetivo: avaliar o impacto do tratamento na sobrevida de pacientes portadores de GBM.
Pacientes e métodos: foram incluídos todos os pacientes com diagnóstico histológico de GBM atendidos na Unidade de Neuro-Oncologia do Hospital de Clínicas, de 1980 a 2000. Dos prontuários dos pacientes foram coletados os dados de identificação, clínicos, resultados de exames e estudos e os relacionados com a evolução do caso. A sobrevida foi calculada utilizando o método de Kaplan Meier e Mantel Cox.
Resultados: foram estudados 65 pacientes com idade média de 58 anos (rango: 6-79 anos). Todos os pacientes (100%) foram submetidos à cirurgia (completa em 22 pacientes, subtotal em 9, parcial em 32 e biopsia em 2). Noventa e dois por centos (92%) receberam RT pós-operatória e 25% QT. A mediana de sobrevida foi de 46,6 semanas e a sobrevida global aos 12 meses foi de 28%. A probabilidade de sobrevida aos 12 meses foi zero nos pacientes que foram submetidos exclusivamente à cirurgia; 0,23 nos que se agregaram RT, e 0,62 nos tratados com QT (p=0,0001). A análise multivariada identificou como variáveis independentes: o tratamento multimodal incluindo quimioterapia (p=0,003) e bom estado neurológico pós-operatório (p=0,007).
Conclusões: a mediana de sobrevida desta serie foi similar às descritas na literatura, existindo uma sobrevida maior nos pacientes com bom estado neurológico tratados com cirurgia seguida de RT e QT.
Bibliografía
]]>1. Jemal A, Murray T, Ward E, Samuels A, Tiwari RC, Ghafoor A, et al. Cancer statistics, 2005. CA Cancer J Clin 2005; 55(1):10-30.
2. Vasallo JA, Barrios E, De Stefani E, Ronco A. Atlas de Incidencia por Cáncer en Uruguay: período 1996-1997. Montevideo: Comisión Honoraria de Lucha contra el Cáncer, 2001. p. 150-1.
3. Kleihues P, Cavenee K, eds. World Health Organization classification of tumours: pathology and genetics. Tumours of the nervous system. Lyon: IARC Press, 2000. 314 p.
4. Gordon Firing S, Garbino C. Clasificación e histogénesis de los tumores primitivos del sistema nervioso central. In: Tratamiento de los tumores primitivos del sistema nervioso central: nuestra experiencia desde 1975 a 1993. Montevideo: Oficina del Libro AEM, 1995. p. 19-29.
5. Rodríguez R, Luongo A, Mañana G, Wilson E. Tumores primarios del sistema nervioso central. In: Musé IM, Viola A, Sabini G, eds. Aspectos prácticos de la clínica oncológica. Montevideo: Sudamericana, 2004. p. 411-8.
]]>6. Blake LC, Maravilla KR. Computed Tomografhy. In: Berger M, Wilson CB, eds. The gliomas. Philadelphia: WB Saunders, 1999. p. 242-74.
7. Preston Martin S. Epidemiology. IEn: Berger M, Wilson CB, eds. The gliomas. Philadelphia: WB Saunders, 1999. p. 2-11.
8. Matías Riu J. Diagnóstico por imagen de las neoplasias intracraneales. In: Rosell R, Ariza A, Ley A, eds. Tumores del sistema nervioso central: epidemiología, nosología y terapéutica. Barcelona: Doyma, 1993. p. 31-53.
9. Gold RL, Dillon WP. Magnetic resonance imaging. In: Berger M, Wilson CB, eds. The gliomas. Philadelphia: WB Saunders, 1999. p. 275-93.
10. Levin VA, Kyristsis AP. Gliomas, medulloblastoma and CNS germ cell tumors. In: Cavalli F, Hansen HH, Kaye SB, eds. Textbook of medical oncology. 2 ed. London: Martin Dunitz, 2000. p. 493-520.
11. Kowalczuk A, Macdonald RL, Amidei C, Dohrmann G 3rd, Erickson RK, Hekmatpanah J, et al. Quantitative imaging study of extent of surgical resection and prognosis of malignant astrocytomas. Neurosurgery 1997; 41(5):1028-36; discussion 1036-8.
12. Brandes AA. State of the art treatment of high-grade brain tumors. Semin Oncol 2003; 30(6 Suppl 19):4-9.
13. Shrieve DC, Deen DF, Larson DA. Basic Principles of Radiobiology and Radiotherapy. In: Berger M, Wilson CB, eds. The gliomas. Philadelphia: WB Saunders, 1999. p. 464-97.
14. Leibel SA, Sheline GE. Radiotherapy in the treatment of cerebral astrocytomas. In: Thomas, D GT, ed. Neuro-oncology: primary malignant brain tumours. London: Edward Arnold, 1990. p. 193-221.
15. Biete A, Verger E, Conill C. Radioterapia en el tratamiento de los tumores del sistema nervioso central. In: Rosell R, Ariza A, Ley A, eds. Tumores del sistema nervioso central: epidemiología, nosología y terapéutica. Barcelona: Doyma, 1993. p. 65-81.
16. National Cancer Institute. NCI/PDQ(r) Pacientes: Tumores cerebrales en adultos: Tratamiento (PDQ(r)). Disponible en: http://www.oncolink.org/types/article.cfm?c=2&s=4&ss= 32&id=9320 [Consulta: 11 oct de 2010]
17. Fink K, Schold S. Tumor dissemination and management. In: Berger M, Wilson CB, eds. The gliomas. Philadelphia: WB Saunders, 1999. p. 636- 48.
18. Fiveash JB, Spencer SA. Role of radiation therapy and radiosurgery in glioblastoma multiforme. Cancer J 2003; 9(3):222-9.
19. Walker MD, Alexander E Jr, Hunt WE, MacCarty CS, Mahaley MS Jr, Mealey J Jr, et al. Evaluation of BCNU and/or radiotherapy in the treatment of anaplastic gliomas: a cooperative clinical trial. J Neurosurg 1978; 49(3):33-43.
20. Walker MD, Green SB, Byar DP, Alexander E Jr, Batzdorf U, Brooks WH, et al. Randomized comparisons of radiotherapy and nitrosoureas for the treatment of malignant glioma after surgery. N Engl J Med 1980; 303(23):1323-9.
21. Green SB, Byar DP, Walker MD, Pistenmaa DA, Alexander E Jr, Batzdorf U, et al. Comparisions of carmustine, procarbazine, and high dose methylprednisolone as additios to surgery and radiotherapy for treatment of malignan gliomas. Cancer Treat Rep 1983; 67(2):121-32.
]]>22. Fine HA, Dear KB, Loeffler JS, Black PM, Canellos GP. Meta- analysis of radiation therapy with and without adjuvant chemotherapy for malignant gliomas in adults. Cancer 1993; 71(8):2585-97.
23. Hildebrand J, Sahmoud T, Mignolet F, Brucher JM, Afra D. Adjuvant therapy with dibromodulcitol and BCNU increases survival of adults with malignant gliomas: EORTC Brain Tumor Group. Neurology 1994; 44(8):1479-83.
24. Medical Research Council Brain Tumor Working Party. Randomized trial of procarbazine, lomustine, and vincristine in the adjuvant treatment of high-grade astrocytoma: a Medical Research Council Trial. J Clin Oncol 2001; 19(2):509-18.
25. Stewart LA. Chemotherapy in adult high-grade glioma: a systematic review and meta-analysis of individual patient data from 12 randomized trials. Lancet 2002; 359(9311): 1011-8.
26. Rodríguez R, Alonso I, Suárez L, Gordon-Firing S, Aguiar S. Gliomas astrocitarios malignos. Estudio randomizado fase III comparando cirugía con radioterapia vs cirugía y quimioterapia con tenipósido. Arch Inst Neurol 2000; 3(2):78-86.
]]>27. Huncharek M, Muscat J, Geschwind JF. Multi-drug versus single agent chemotherapy for high grade astrocytoma; results of a meta-analysis. Anticancer Res 1998; 18(6B):4693-7.
28. Yung WK, Albright RE, Olson J, Fredericks R, Fink K, Prados MD, et al. A phase II study of temozolomide vs. procarbazine in patients with glioblastoma multiforme at first relapse. Br J Cancer 2000; 83(5):588-93.
29. Brandes AA, Ermani M, Basso U, Paris MK, Lumachi F, Berti F, et al. Temozolomide in patients with glioblastoma at second relapse after first line nitrosourea-procarbazine failure: a phase II estudy. Oncology 2002; 63(1):38-41.
30. Yung WK. Temozolomide in malignant gliomas. Semin Oncol 2000; 27(3 Suppl 6):27-34.
31. Prados MD. Future directions in the treatment of malignant gliomas with temozolomide. Semin Oncol 2000; 27(3 suppl 6):41-6.
]]>32. Prados MD, Levin V. Biology an treatment of malignant glioma. Semin Oncol 2000; 27(3 Suppl 6):1-10.
33. Osoba D, Brada M, Yung WK, Prados M. Health-related quality of life in patients treated with Temozolomide versus Procarbazine for recurrent glioblastoma multiforme. J Clin Oncol 2000; 18(7):1481-91.
34. Dinnes J, Cave C, Huang S, Milne R. A rapid and systematic review of the effectiveness of temozolomide for the treatment of recurrent malignant glioma. Br J Cancer 2002; 86(4):501-5.
35. Stupp R, Dietrich PY, Ostermann Kraljevic S, Pica A, Maillard I, Maeder P, et al. Promising survival for patients with newly diagnosed glioblastoma multiforme treated with concomitant radiation plus temozolomide followed by adjuvant temozolomide. J Clin Oncol 2002; 20(5):1375-82.
36. Stupp R, Mason WP, van den Bent MJ, Weller M, Fisher B, Taphoorn MJ, et al. Radiotherapy plus Concomitant and adjuvant Temozolomide for Glioblastoma. N Engl J Med 2005; 352(10):987-96.
]]>37. Stupp R, Hegi ME, Mason WP, van den Bent MJ, Taphoorn MJ, Janzer RC, et al. Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial. Lancet Oncol 2009; 10(5):459-66.
38. Kelly PJ, Olsen MH, Wrght AE. Stereotactic implantation of iridium 192 into CNS neoplasms. Surg Neurol 1978; 10(6):349-54.
39. Gordon-Firing S, Ferrari A, Rodríguez R, Alonso I, Garbino C. Tumores del sistema nervioso central. In: Vázquez T. Los cánceres más frecuentes. Montevideo: Oficina del Libro AEM, 2000. Tomo 2; p.141-88.
]]>