Primer informe en Uruguay de la vitrificación de embriones como alternativa real a la técnica de congelación lenta
Dres. Diana Vaamonde*, Roberto Suárez Serra†, Ariel Ahumada‡, Carlos Duarte§, Cecilia Torres¶, Sergio Oehninger††
Resumen
Introducción: la vitrificación es una técnica de criopreservación de las denominadas "rápidas". En comparación con los tradicionales procesos de congelación lenta, la estrategia de vitrificación permite la eliminación total de la formación de cristales tanto intracelular como extracelularmente. Permite poner las células directamente en el crioprotector y sumergirlas en N2 líquido. Su aplicación en el mundo ha ido creciendo exponencialmente y se puede aplicar tanto a ovocitos como a embriones en cualquier estadio.
Objetivos: revisión de la técnica de vitrificación y presentación de la experiencia de dos años en el Centro Iberoamericano de Reproducción Asistida, la primera en Uruguay.
Material y método: se incluyeron 17 pacientes de las que se han vitrificado y desvitrificado embriones. Se usó el método comercial Cryotop con las soluciones de vitrificación de Kitazato.
Conclusiones: la vitrificación como método de criopreservación se muestra prometedor y como buen sustituto de las técnicas de congelación lentas, debido a su alta tasa de éxito, su fiabilidad y la rapidez de ejecución, con resultados reproducibles.
Palabras clave: CRIOPRESERVACIÓN - métodos.
VITRIFICACIÓN.
Keywords: CRYOPRESERVATION - methods.
VITRIFICATION.
* Docente del Departamento de Ciencias Morfológicas. Facultad de Medicina, Universidad de Córdoba, España.
† Director Médico del Centro Iberoamericano de Reproducción Asistida. Uruguay. Presidente de la Sociedad Uruguaya de Reproducción Humana.
]]> ‡ Biólogo del Centro Iberoamericano de Reproducción Asistida. Director y Biólogo de Procrearte. Buenos Aires, Argentina.§ Co Director del Centro Iberoamericano de Reproducción Asistida. Uruguay.
¶ Bióloga del Centro Iberoamericano de Reproducción Asistida. Uruguay.
†† Director, The Jones Institute for Reproductive Medicine, Eastern Virginia Medical School, Norfolk, Virginia, USA. Consultante Centro Iberoamericano de Reproducción Asistida.
Correspondencia: Dr. Roberto Suárez Serra
Centro Iberoamericano de Reproducción Asistida. Montevideo, Uruguay.
Correo electrónico: rsuarez@mednet.org.uy
Recibido: 6/5/10.
Aceptado: 4/10/10.
Conflicto de intereses: los autores del presente artículo Roberto Suárez Serra, Ariel Ahumada, Carlos Duarte, Cecilia Torres, Sergio Oehninger trabajan en el Centro Iberoamericano de Reproducción Asistida.
]]>
Introducción
La preocupación por la criopreservación del material reproductivo ha seguido una trayectoria prácticamente paralela al desarrollo de las técnicas de reproducción asistida. Las técnicas de reproducción asistida (TRA) vienen realizándose desde la década de 1980. En el momento que se empiezan a realizar las TRA con supraovulación surge una imperiosa necesidad de criopreservar los embriones sobrantes tras la transferencia embrionaria. Esta necesidad derivada de los problemas tanto éticos como logísticos para ofrecer futuras tentativas con un costo inferior, hace que crezca la necesidad de desenvolver protocolos de congelación que sean eficaces. La preocupación por la preservación de la fertilidad, bien en pacientes que quisieran postergar la descendencia o bien en pacientes oncológicos que podrían ver su potencial reproductivo alterado o destruido tras los tratamientos, surge también. La criopreservación abarca ahora no sólo los embriones sino también los gametos o células sexuales.
Tras el nacimiento de Louise Brown en 1978, más de 3 millones de niños han nacido mediante la aplicación de las TRA(1). En 2009, se estima que unos 700.000 hayan nacido de embriones criopreservados(2). En 1985 se publica la preservación, por vitrificación libre de formación de hielo, de embriones de ratón y se postula como una alternativa real a los protocolos tradicionales de enfriamiento lento/calentamiento rápido(3). Este protocolo lento se venía usando comúnmente con resultados medianamente exitosos, desde que en 1983 se publicó el primer embarazo con embrión descongelado de ocho células(4). Con este protocolo, el tiempo que lleva el proceso varía entre 90 minutos y cinco horas. Durante su ejecución el congelamiento incluye la formación de cristales de hielo, tanto intra como extracelulares, al mismo tiempo que un aumento en la concentración de sustancias disueltas. Debido a que ambos fenómenos pueden ser nocivos para la viabilidad del embrión, la congelación tradicional debe mantener un equilibrio muy fino entre ambos fenómenos que puede dar lugar a daños por formación de hielo, daños osmóticos, fractura de la zona y los blastómeros y alteraciones del citoesqueleto(5).
Se ha comprobado que la vitrificación evita esos problemas(5). En la vitrificación se produce una solidificación de los solutos parecida al vidrio sin la formación de cristales de hielo(3). Este hecho se produce por la vía de dos mecanismos: aumentar las concentraciones de crioprotectores o aumentar las tasas de enfriamiento, o ambas(5).
La vitrificación empezó usándose para criopreservación principalmente de ovocitos y blastocistos, debido a que la mayoría de los embriólogos se niegan a exponer los embriones a las altas concentraciones (30% a 50%) de crioprotectores requeridas para conseguir el estado vitrificado. Sin embargo, hoy los protocolos se han mejorado y no se necesita tanta cantidad de crioprotector, pudiendo usarse la técnica sin reservas(6).
El propósito del presente trabajo fue: a) hacer una revisión y exposición de los hechos más significativos relacionados con la vitrificación para aclarar mitos y confusiones, y b) presentar los datos obtenidos desde que se empezó a implantar la técnica hace dos años en el Centro Iberoamericano de Reproducción Asistida.
]]> Revisión de la literaturaFenómenos físicos y químicos de la vitrificación
Por debajo de temperaturas de -130 °C(7) cualquier líquido que permanezca sin congelar entre los cristales de hielo pasa a una transición de vidrio. Las moléculas se pegan unas a otras mediante uniones de hidrógeno débiles. En este estado, las moléculas, en vez de moverse libremente, simplemente vibran en un lugar. Dado que las moléculas no se mueven libremente, se para toda reacción química y se preserva la vida. Para que las células vivas sobrevivan a este proceso se deben añadir los crioprotectores, moléculas tales como el glicerol, que penetran dentro de las células y limitan el porcentaje de agua que se convierte en hielo durante la congelación.
Luyet ya describió que la cristalización es incompatible con la vida y debería ser evitada en la mayor medida posible(8). Así, en 1984, Fahy y colaboradores(9) propusieron la adición de cantidades tan elevadas de crioprotector que la formación de hielo fuese completamente prevenida a cualquier temperatura. Por debajo de la temperatura de transición del vidrio, el material vendría a ser un sólido vidrioso, es decir, un sólido con la estructura molecular de un vidrio, libre de formación de hielo. Este proceso se denominó vitrificación. La congelación a velocidades ultrarrápidas se consideró igualmente como una opción para eliminar la formación de hielo y crear un estado de vidrio. La definición física de vitrificación es la solidificación de una solución; el agua se enfría rápidamente y se forma un estado de vidrio desde una fase líquida a baja temperatura, no por la cristalización de hielo sino por una elevación extrema de la viscosidad durante el enfriamiento. Según el grupo de Fahy, "la viscosidad de la muestra aumenta hasta que las moléculas se inmovilizan y la muestra ya no es más un líquido sino que tiene propiedades de sólido"(9). Estos conceptos constituyeron la idea de vitrificación. En contraste a los protocolos de congelación lenta, durante la vitrificación toda la solución permanece sin cambiar, el agua no se precipita y no se forman cristales de hielo(10).
Es útil distinguir entre vitrificación reversible y vitrificación morfológica. Mientras que la vitrificación reversible es aquella en la que el material se recupera del proceso de vitrificación en un estado viable, la vitrificación morfológica es aquella en la que hay una buena preservación estructural pero las enzimas u otras biomoléculas importantes se dañan por el procedimiento(1).
El hecho de que la vitrificación sea el resultado de altas tasas de enfriamientos con altas concentraciones de crioprotector resulta problemático biológicamente hablando y técnicamente difícil(11). Por tanto, la velocidad de enfriamiento y calentamiento y la concentración de crioprotector son las variables claves en la vitrificación. Debido a las limitaciones que ambas variables imponen (límite técnico en la velocidad y límite de toxicidad del crioprotector), debe existir un equilibrio entre ambas variables para garantizar la eliminación de formación de cristales tanto intracelulares como extracelulares.
La ventaja que ofrece el aumento en las tasas de enfriamiento y calentamiento es la de una necesidad disminuida en la cantidad de crioprotector, disminuyendo así tanto el daño tóxico como osmótico; además, proporciona que el paso por las zonas peligrosas de temperatura (de 15 ºC a -5 ºC) sea rápido y se disminuya el daño de chilling (daño por enfriamiento)(12). Este aspecto es muy importante para las estructuras sensibles, especialmente las que tienen alto contenido en lípidos(13). El aumento en las tasas de enfriamiento y calentamiento se puede alterar de tres maneras: minimizando la solución alrededor del material, minimizando el aislante térmico (contacto directo entre N2 y el crioprotector), evitar la formación de vapor de N2. Como hemos comentado, la formación de cristales de hielo dentro de las células causa daño o muerte celular, o ambos. Para proteger del daño chilling se intenta quitar la mayor cantidad de agua intracelular que sea posible, antes de la congelación, para que la formación de cristales de hielo dentro de la célula sea mínima, intentando asegurar así la viabilidad celular poscongelación. Sin embargo, si se extrae agua en exceso, puede haber un daño celular debido a un ambiente intracelular altamente concentrado. Los crioprotectores son los compuestos que actúan para conseguir la deshidratación celular deseada. Pueden dividirse en agentes permeables (entran en la célula y desplazan el agua) y no permeables (permanecen fuera de la célula pero sacan el agua por ósmosis). Normalmente se usa una combinación de ambos tipos de crioprotectores; el crioprotector más comúnmente usado en vitrificación es el etilenglicol (EG) que parece tener un bajo efecto tóxico(14,15), a pesar de que algunos autores han sugerido que puede no ser un buen crioprotector para embriones en pronúcleo, y una rápida difusión junto con un rápido equilibrio intra-extracelular(16). Se han reportado nacimientos normales con la aplicación de este crioprotector(17,18), por lo que su uso parece bien justificado.
Además del crioprotector propiamente dicho, las soluciones de vitrificación contienen otras moléculas y soluciones tampón que tienen un efecto protector sobre las células. Con la combinación de moléculas se consigue también una disminución del crioprotector(19); para tal efecto se añaden otras moléculas no permeables que permanecen en el área extracelular y también se puede usar una combinación de dos crioprotectores y exposición paso a paso de las células a la solución. En general, las soluciones de vitrificación contienen una combinación casi equimolar de EG y dimetilsulfóxido (DMSO). El DMSO es, al igual que el EG, un crioprotector permeable. Los tampones más usados son HEPES o los basados en fosfato. Otras moléculas que modifican la solución de vitrificación son los disacáridos como la sacarosa y fructosa, entre otros(20), o macromoléculas tales como polímeros que pueden constituir una matriz viscosa que ayuda en la prevención de la cristalización(21). Algunos de los métodos diseñados para la vitrificación, sin entrar a detallarlos, han sido la pipeta de denudación flexipet (FDP), tal vez el método más empleado sea el Cryotop ideado por Kuwayama (método de volumen mínimo), entre los sistemas "abiertos" y, por otra parte, el High Security Vitrification Kit-HSV entre los sistemas "cerrados".
]]>La vitrificación con distintas muestras
Con respecto a los ovocitos hay que mencionar que la vitrificación parece ser una alternativa real y efectiva a la congelación lenta. Hasta ahora, a pesar de haberse conseguido embarazos(22-25), los resultados eran inconsistentes, haciendo que la congelación ovocitaria no se practique rutinariamente. Los ovocitos deben tolerar contracciones y expansiones volumétricas, pero son más vulnerables a la cristalización que los embriones de cualquier estadio, debido a una permeabilidad reducida de las membranas citoplasmáticas de estos(26). Los ovocitos son altamente sensibles a la hinchazón osmótica, sea durante la etapa de retirada del crioprotector, sea justo tras el calentamiento(27). Sin embargo, la vitrificación ha demostrado ser más eficaz que el protocolo lento con respecto a tasas de supervivencia y desarrollo posterior del embrión y tasa de nacimientos(28).
Con respecto a los zigotos, es destacable que este estadio es muy favorable para la criopreservación, bien sea lenta o por vitrificación, debido a que la reacción cortical y endurecimiento posterior de la zona pelúcida parece conferir al oolema una mayor estabilidad para resistir la baja temperatura y los cambios osmóticos. A pesar de que según algunos autores el EG es tóxico para este estadio(16), este problema, de existir, parece quedar resuelto con las menores cantidades de crioprotector y la alta tasa de enfriamiento de los protocolos actuales(5).
Los aparentemente buenos resultados obtenidos en la aplicación de la vitrificación en embriones en estadio de células y blastocistos parecen señalar hacia un aumento en la aplicación de la técnica, hecho que puede dar paso a un uso mayor del cultivo largo para evitar los embarazos múltiples dado que la preservación de blastocistos dará buen resultado(2,29). Por otra parte, permitirá a la paciente un éxito mayor en las criotransferencias y una menor necesidad de ciclos múltiples.
Osada y colaboradores(30) estudiaron la eficacia clínica del Cryotop con respecto a transferencia en fresco de blastocistos, observando que 98,6% sobrevivió y 55,6% (275/495) quedaron embarazadas. El porcentaje de embarazo fue superior en el grupo de criotransferencias que en el de transferencias en fresco. Con respecto a los blastocistos, hay que destacar que la probabilidad de formación de cristales de hielo es directamente proporcional al volumen del blastocele y directamente proporcional a la viscosidad y tasa de enfriamiento. Por tanto, se ha observado una disminución en la tasa de supervivencia tras la vitrificación a medida que el volumen de la cavidad aumentaba. Como la vitrificación puede endurecer la zona, algunos autores aconsejan realizar eclosión asistida antes de la transferencia(31). Como es lógico, tanto en la criopreservación en estadio celular como en la de blastocistos es de suma importancia la calidad de los embriones, determinando la supervivencia del proceso de criopreservación y el desarrollo ulterior del embrión descongelado, al igual que la implantación y las tasas de embarazo evolutivo. Otras muestras objeto de vitrificación son el tejido ovárico y los espermatozoides; sin embargo, no son objeto del presente trabajo y, por tanto, no trataremos sobre ellos. Eso sí, se debe destacar que los espermatozoides no son un buen material pues debido al choque osmótico no resisten bien la vitrificación.
El método Cryotop
]]> El Cryotop es un método de vitrificación de volumen mínimo, probablemente el método más usado en el mundo(32,33). Consiste en un soporte especial que se compone de una tira de polipropileno delgada y estrecha (0,4 mm ancho, 20 mm largo, 0,1 mm espesor) unida a un soporte de plástico duro. Con el fin de proteger el soporte del daño mecánico durante el almacenaje, se protege con un capuchón plástico alargado de 3 cm; en este capuchón se inserta la tira de polipropileno. Al minimizar el volumen de la solución de vitrificación en la que están los ovocitos o embriones se aumentan las tasas de enfriamiento y calentamiento y se disminuye la formación de cristales de hielo(11). Se disminuye también el daño de chilling que ocurre entre los +15 ºC(13) y los -5 ºC al pasar la muestra rápidamente por esta zona de temperatura. La tasa para evitar este daño debe ser de unos 20.000 C/min(34). Aparentemente con Cryotop se consigue una tasa de hasta 40.000 C/min. Al usar un volumen mínimo (volumen de solución de vitrificación cargado en soporte menor a 0,1 ml), se puede evitar daño por fractura de la zona pelúcida y de las membranas celulares, daño relativamente común con la congelación por métodos convencionales; otros métodos de volumen mínimo son el MSD (gota de tamaño mínimo) y el Cryoloop. Una variedad de soluciones crioprotectoras pueden ser usadas con el método Cryotop y los parámetros de equilibrio y dilución se pueden variar según los requisitos específicos de las especie o el estadio de desarrollo.En general, parece que una proporción equimolar de DMSO y EG provee la combinación más efectiva, usando un equilibrio de dos pasos y una suplementación con sacarosa en la concentración final. El etilenglicol, dadas sus propiedades como crioprotector altamente permeable y de toxicidad moderada, es considerado como un componente estándar de las soluciones de vitrificación de mayor éxito. Su combinación con DMSO fue usada por primera vez con éxito por Ishimori y colaboradores(35), reportándose posteriormente que el DMSO aumentaba la permeabilidad del etilenglicol(36).
Material y método
Pacientes
Se incluyeron 17 pacientes de las que se han vitrificado y desvitrificado embriones. El número total de pacientes con embriones vitrificados es superior, si bien, al no haberse procedido a su desvitrificación y transferencia posterior, no han sido incluidas para el análisis de datos. Las pacientes tenían una edad media de 33,5 ± 3,4 años. Las pacientes fueron informadas tal sobre el uso de material humano y firmaron un documento de consentimiento informado.
Procedimiento
]]>Las pacientes se sometieron a hiperestimulación ovárica controlada. A partir del día 3 del ciclo se inició estimulación con r–FSH, seguida, al día 12, de la aplicación de hCG. Unas 36 horas después se realizó la aspiración folicular por vía transvaginal ecoguiada. Tras cultivo embrionario se realizó la transferencia en fresco en D3, D4 o D5. Tras realizar la transferencia de embriones en fresco se procedió a vitrificar los embriones sobrantes, sea en estadio de células (D3), en proceso de compactación (D4), o en blastocisto (D5). Tanto el cultivo embrionario como la transferencia han sido realizados con medios Global (Life Global, IVFOnline; Guelph, ON, Canadá.)
Para el proceso de vitrificación/desvitrificación se usó el método comercial Cryotop con las soluciones de vitrificación de Kitazato (Cryotop; Kitazato Bio Pharma Co, Fuji-shi, Japón).Una vez finalizado el proceso, la calidad fue dividida en regular y buena.
Vitrificación: el procedimiento de dos pasos, aunque ya descrito extensivamente en una serie de trabajos previos(2,5,32,37), se explica brevemente. Tras un equilibrio con EG (7,5%) y DMSO (7,5%) (en ningún caso se excederá un tiempo total de 15 minutos) se pasa el material a la solución de vitrificación que contiene EG (15%), DMSO (15%), y sacarosa (0,5 mol/l), y se carga el material con un capilar de vidrio fino, depositándolo sobre la tira de polipropileno con un volumen <0,1 ml.
Tras depositar el material, casi toda la solución se extrae para dejar sólo una fina película cubriendo el material y la muestra se sumerge rápidamente en nitrógeno líquido (este paso no debe exceder los 60 segundos).
Seguidamente se procede a poner el capuchón, protegiendo así la tira plástica y, por ende, al material vitrificado. Tras este paso la muestra se almacena en nitrógeno líquido.
Desvitrificación: durante el proceso de descongelación se procede a quitar el capuchón protector mientras el soporte está aún sumergido en nitrógeno líquido. La tira de polipropileno se sumerge directamente en un medio a 37 ºC que contiene sacarosa con el fin de contrarrestar el desequilibrio del choque osmótico causado por los crioprotectores acumulados intracelularmente. Esta solución de descongelación (TS) se usa en volumen de 0,5 a 1ml (en placa de cuatro pozos o de pozo central).
Los embriones se pasan secuencialmente por soluciones de dilución (DS) y de lavado (WS) en volumen de 300 ml (en placa provista por la propia compañía) previas al paso al medio definitivo, bien para mantenerlos en cultivo, bien para transferir el material.
Análisis estadístico
]]>Se han utilizado métodos estadísticos tradicionales para calcular media (+SD) y porcentaje. Además, se han usado las pruebas c² para las variables cualitativas (dos categorías), y la prueba T student para muestra independientes para la variable edad. Todos los cálculos fueron realizados con el paquete estadístico SPSS (versión 1.3).
Resultados
Con una media de embriones vitrificados de 2,71 (±0,69), la tasa de supervivencia global de los embriones tras la desvitrificación fue de 93,4%; por otra parte, la tasa final de embarazo, con una media de embriones transferidos de 2,41 (±0,62), fue de 47,1%.
En relación con la edad de las pacientes se ha observado una diferencia estadísticamente significativa entre las que han obtenido embarazo y las que no (embarazadas = 30,0 ±2,51 versus no embarazadas = 34,0 ±1,93 años; p<0,05).
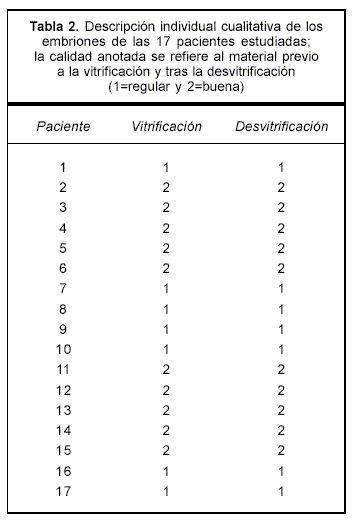
Al analizar la posible relación entre las variables embarazo y calidad de la vitrificación, se ha observado que no existe dependencia (p>0,05). El porcentaje de embarazo en función de la calidad se presenta en la tabla 1.

Por último se muestran los casos individuales (n=17) con respecto al análisis de la calidad anotada del material previo a la vitrificación y tras la desvitrificación (tabla 2).
]]>
Discusión
Nuestros resultados obtenidos con la vitrificación de embriones humanos son muy satisfactorios como muestran los resultados, obteniendo 47,1% de tasa de embarazo, con una media de embriones transferidos de 2,41; según nuestro conocimiento, estos son los primeros resultados obtenidos con esta técnica en Uruguay.
Tal como apuntan Kuwayama y colaboradores(32,33), hemos constatado que el método Cryotop es relativamente fácil de aprender (corta curva de aprendizaje), además de simple y fiable, los resultados son consistentes y las variaciones interoperario mínimas. Más aun, las soluciones y parámetros de equilibrio/dilución pueden aplicarse a los ovocitos MII, zigotos y embriones humanos, lo que evita que haya más de un protocolo de congelación dependiendo del estadio de desarrollo embrionario y permite estandarizar y optimizar los protocolos y, por tanto, la fiabilidad del método y el tiempo.
El principio de volumen mínimo de CryotopTM aumenta la tasa de enfriamiento y calentamiento (hasta 40.000 C/min), lo cual puede contribuir a la tasa de supervivencia mejorada y consistente, y a las tasas de desarrollo tanto in vitro como in vivo.
Parece que la vitrificación fuese la gran desconocida o malentendida pues, a pesar de la extensa literatura disponible sobre la técnica (más de 500 artículos en diez años), aún es considerada como experimental por muchos autores(38). Hasta ahora, con respecto a la técnica, los principales problemas han sido la falta de reproducibilidad(29), al igual que diferencias en la supervivencia, calidad y tasa de desarrollo tras la descongelación, aspectos respecto a los cuales no hay una clara información. Si bien los datos parecen indicar que sus resultados en ningún caso son inferiores a los de la congelación tradicional, existen problemas en torno a la técnica empezando por su simple definición. Si bien muchos artículos la describen simplemente como la aplicación de altas concentraciones de crioprotectores y de altas tasas de enfriamiento, se debe tener en cuenta que estas variables modifican la una a la otra, de tal modo que se puede vitrificar con menos crioprotector aumentando la tasa de enfriamiento y viceversa(6,11). Ahora bien, lejos de todos los parámetros susceptibles de modificación, la vitrificación, por su propia definición, es meramente una solidificación libre de hielo, vítrea y transparente de soluciones basadas en agua a temperaturas bajo cero(8).
Las disparidades de resultados respecto a tasas de supervivencia y desarrollo bien podrían deberse a los distintos soportes usados para vitrificar, con propiedades diferentes a la hora de la transferencia de temperatura. Además, el hecho de que se hayan formulado tantas soluciones de vitrificación diferentes, no ayuda a que se perfeccione una única metodología.
Hay que tener en cuenta que existen muchas variables en el proceso de vitrificación que pueden influir enormemente sobre la efectividad y el potencial de mejorar las tasas de supervivencia del material vitrificado, lo cual ha evitado la estandarización universal del protocolo. A saber: I) tipo y concentración del crioprotector (prácticamente todos son tóxicos); II) temperatura de la solución de vitrificación durante el procedimiento; III) tiempo de exposición a la concentración final de crioprotector antes de sumergirlo en N2 líquido; IV) tipo de soporte usado para vitrificación (influye sobre la película de vapor que se forma y la tasa de enfriamiento), y V) calidad y estadio de desarrollo del material.
]]> Con respecto a la vitrificación del agua intracelular para evitar la formación de cristales y daño de chilling, hay dos procedimientos principales: aumentar la diferencia de temperatura entre las muestras y el medio de vitrificación y usar materiales con rápida transferencia de calor. Más aun, se debe tener en cuenta que la tasa real de transferencia de calor durante el procedimiento puede variar ostensiblemente dependiendo del soporte, el perfeccionamiento técnico, y el movimiento durante la inmersión(5). Además, también hay que tener en cuenta que cada célula tiene su tasa de enfriamiento óptima. Los ovocitos tienen más propensión al daño por chilling que los embriones de cualquier estadio.Sin embargo, a pesar de los malentendidos y la falta de claridad, la criopreservación se muestra prometedora para la criopreservación de ovocitos y embriones(37,38), y el método Cryotop parece ofrecer los mejores resultados hasta la fecha. Como ya se comentó es un método abierto de vitrificación de volumen mínimo.
Los resultados obtenidos con el Cryotop, según Kuwayama y colaboradores(32,39), son espectaculares, con una tasa de supervivencia morfológica de 100% con embriones en estadio de pronúcleos, llegando 52% de estos a estadio de blastocisto, siendo estas tasas superiores a las de la criopreservación convencional. Por otra parte, con una muestra de 6.328 blastocistos humanos, la tasa de supervivencia fue de 90%, resultando en 53% de embarazos clínicos y 45% de nacidos vivos. Sin duda, estos son los valores más exitosos documentados usando vitrificación. Lieberman y colaboradores(29), por su parte, han publicado una tasa de embarazo con vitrificación de blastocistos en D5 de 48,7% versus 42,8% con métodos tradicionales. Los resultados para embriones en D6 fueron también de aproximadamente 43%. Si bien según estos autores no queda claro que la vitrificación ofrezca resultados mejores, queda totalmente manifiesto que sin duda los resultados son, al menos, equiparables. Nuestros resultados pasan a confirmar y apoyar el éxito de la vitrificación como método de elección para la criopreservación de embriones, a pesar de que nuestros resultados no sean tan altos como los del grupo de Kuwayama.
El mismo grupo, vitrificando ovocitos en MII, obtuvo una tasa de supervivencia morfológica de 95%, con una tasa de fertilización normal por ICSI de 91% y llegando a blastocisto el 50% de estos, resultando en una tasa de embarazo de 41%(32). Si bien nosotros hemos realizado vitrificación de ovocitos, aún no hemos procedido a su descongelación, por lo cual no poseemos datos para poder comparar. Según estos autores, aproximadamente 50 bebés han nacido fruto de la vitrificación con el método Cryotop, lo que ha convertido a este método en el más exitoso hasta el momento de los métodos de vitrificación.
Por otra parte, no podemos olvidar la importancia atribuida por muchos entendidos al contacto con el N2 líquido; si bien hoy día es un requisito, en la mayoría de los protocolos puede evitarse aunque algunos autores abogan que no es tan posible la contaminación como algunos preconizan(40). Sea como fuere, uno de los argumentos en contra de la vitrificación es la posibilidad de contagio debido al contacto de la muestra con el N2 líquido; en este sentido, el método Cryotop, que es un método abierto, está expuesto a tales juicios en contra. Desafortunadamente, la mayoría de los métodos actuales de vitrificación, al igual que el Cryotop, aún comparten y presentan estos problemas. Ahora bien, si se ha reportado la posible infección embrionaria tras la exposición artificial a altas concentraciones de virus, la posibilidad real de un ambiente tan adverso es prácticamente inexistente. Es más, en ningún caso se ha documentado la contaminación real en la clínica(37). Por tanto, parece que el peligro real es mucho menor al enfatizado por los críticos. No obstante, en algunos países se empiezan a considerar opciones para evitar que pueda pasar. Si bien el peligro de contaminación por N2 es real, tampoco debe sobreestimarse. En cualquier caso es preferible eliminar este peligro y con este fin han surgido muchos intentos en los últimos años(33,36).
Así pues se están ideando nuevos soportes, por ejemplo el CryoTip o Vitritip(33), que es un capilar estrecho que puede sellarse tras la carga con una solución de volumen mínima; sin embargo, parece que los resultados ofrecidos con respecto a tasas de desarrollo de ovocitos humanos son ligeramente inferiores a los obtenidos con el Cryotop. En el presente año, Lieberman ha publicado resultados muy similares, sin diferencia estadísticamente significativa, usando el método Cryotop y el HSV(2). Alternativamente se están tomando otras precauciones como filtrar o esterilizar el N2, separar las fases de congelación y almacenaje protegiendo con sellado tras la congelación y previo al almacenaje y la aparición de otros dispositivos.
El peligro del N2 existe, pero no es tan probable como apuntan algunos autores, ya que los efectos tóxicos y osmóticos por las últimas combinaciones y concentraciones de crioprotectores no son mayores a los de la congelación convencional, con el coadyuvante de un menor tiempo de exposición a los crioprotectores que pueden ser tóxicos, especialmente en relación al factor temperatura. Considerando la buena estadística respecto a la supervivencia y al desarrollo posterior, tanto in vitro como in vivo, la técnica puede considerarse como segura y eficaz.
Conclusiones
]]> A tenor de todo lo expuesto y de los datos observados en nuestra propia experiencia, la vitrificación se muestra como un método de criopreservación prometedor y como buen sustituto de las técnicas de congelación lentas. Si bien puede variar según el método, la vitrificación ofrece muchas ventajas y beneficios, tales como eliminación de formación de cristales de hielo al aumentar la tasa de enfriamiento y disminución del efecto tóxico y osmótico de los crioprotectores al disminuir su concentración. Todo esto permite reducir el riesgo de daño por chilling,y esto permite una mayor tasa de supervivencia del embrión. En nuestra experiencia el método Cryotop parece un método seguro, rápido y fiable, con resultados reproducibles. Debido a la conveniencia del método, pero también a sus inquietudes, especialmente sobre bioseguridad, pensamos que la técnica alcanzará en los años venideros un mayor nivel de eficacia clínica y uso.Summary
Introduction: vitrification is a cryopreservation technique that forms part of the so called "fast" cryopreservation techniques. Compared to traditional slow freezing processes, vitrification enables the total elimination of both intracellular and extracellular crystal formation.
It allows for placing the cells directly on the cryoprotector and submersing them in liquid nitrogen. Its application around the world has exponentially grown and the technique may be applied both to ovocytes and embryos at all stages.
Objectives: to carry out a review of the vitrification technique, the first one to be conducted in Uruguay, and to present the two-year experience at the Ibero-American Center for Assisted Reproduction.
Method: we included 17 patients in our study, the embryos of which have been vitrified and unvitrified. We used the commercial Cryotop method with the Kitazato vitrification solutions.
Results: with an average of 2,71 (±0,69) vitrified embryos per patients, global embryo survival rate after vitrification was 93,4%. With an average of 2,41 (±0,62) embryos transferred , the final pregnancy rate was 47,1%. The average age of patients who succeeded in getting pregnant is lower (average 30,0 ±2,51) than those who fail to get pregnant. .
Conclusions: vitrification as a cryopreservation method appears to be a promising technique and seems to be a good substitute for show freezing technique, due to its high-success rates, its reliability and execution speed, with replicable results.
]]>Résume
Introduction: la vitrification est une technique de cryoconservation des dénommées "rapides". En comparaison avec les processus traditionnels de congélation lente, la stratégie de vitrification permet d’éliminer totalement la formation de cristaux aussi bien au niveau intracellulaire qu’extracellulaire. Elle permet de mettre les cellules directement dans le cryoprotecteur et de les submerger dans du N2 liquide. Son application dans le monde a augmenté de façon exponentielle et elle peut être appliquée aussi bien à des ovocytes qu’a des embryons quelque soit l’étape à laquelle ils sont.
Objectifs: révision de la technique de vitrification et de présentation de l’expérience de deux années, au Centre Ibéro-américain de Reproduction Assistée, la première en Uruguay.
Matériel et méthode: on a inclus 17 patientes dont les embryons on a vitrifié et dévitrifié. On a utilisé la méthode commerciale Cryotop avec les solutions de vitrification de Kitazato
Résultats: avec une moyenne d’embryons vitrifiés de 2,71 (±0,69) par patiente, le taux de survie globale des embryons après la dévitrification a été de 93,4%. Avec une moyenne d’embryons transférés de 2,41 (±0,62), le taux final de grossesse a été de 47,1%. L’âge des patientes auquel on réussit une grossesse est inférieur (moyenne 30,0 ±2,51) que celui de celles chez lesquelles on ne réussit pas.
Conclusions: la vitrification comme méthode de cryopréservation se montre prometteur et est un bon substitut des techniques de congélation lentes, dû à son taux élevé de réussite, sa fiabilité et la rapidité d’exécution, avec des résultats reproductibles.
Resumo
Introdução: a vitrificação é uma técnica de criopreservação do grupo das chamadas técnicas "rápidas". Comparada com os processos tradicionais de congelação lenta, a vitrificação permite eliminar totalmente a formação de cristais tanto intra como extracelulares. Permite também colocar as células diretamente no crioprotetor e submergi-las em N2 líquido. Em todo o mundo sua aplicação vem crescendo exponencialmente e pode ser utilizada tanto com ovócitos como a embriões em qualquer estágio.
]]> Objetivos: revisão da técnica de vitrificação e apresentação da experiência de dois anos no Centro Iberoamericano de Reprodução Assistida, a primeira no Uruguay.Material e método: foram incluídas 17 pacientes que cujos embriões haviam sido vitrificados e desvitrificados. O método comercial Cryotop com soluções de vitrificação de Kitazato foi utilizado.
Resultados: A média de embriões vitrificados foi de 2,71 (±0,69) por paciente com uma taxa de sobrevivência global dos embriões depois da desvitrificação de 93,4%. Com uma média de embriões transferidos de 2,41 (±0,62), a taxa final de gravidez foi de 47,1%. A idade das pacientes que engravidaram (média 30,0 ±2,51) era menor que a das que não engravidaram.
Conclusões: a vitrificação se apresenta como um método de criopreservação prometedor e um bom substituto das técnicas de congelação lenta devido às altas taxas de sucesso, sua confiabilidade e rapidez para sua execução, com resultados reproduzíveis
Bibliografía
1. De Mouzon J. Session 50 – IVF Monitoring in Europe and Worldwide Hum Reprod 2006; 21(suppl 1): i76.
2. Liebermann J. Vitrification of human blastocysts: an update. Reprod Biomed Online 2009; 19(Suppl 4): 105-14.
3. Rall WF, Fahy GM. Ice-free cryopreservation of mouse embryos at -196 degrees C by vitrification. Nature 1985; 313(6003): 573-5.
4. Trounson A, Mohr L. Human pregnancy following cryopreservation, thawing and transfer of an eight-cell embryo. Nature 1983; 305(5936): 707-9.
5. Vajta G, Kuwayama M. Improving cryopreservation systems. Theriogenology 2006; 65(1): 236-44.
6. Fahy GM, Wowk B, Wu J, Paynter S. Improved vitrification solutions based on the predictability of vitrification solution toxicity. Cryobiology 2004; 48(1): 22-35.
7. Mazur P. Freezing of living cells: mechanisms and implications. Am J Physiol 1984; 247(3 Pt1): C125-42.
8. Luyet B, Hodapp A. Revival of frog’s spermatozoa vitrified in liquid air. Proc Meet Soc Exp Biol 1938; 39: 433-4.
]]>9. Fahy GM, MacFarlane DR, Angell CA, Meryman HT. Vitrification as an approach to cryopreservation. Cryobiology 1984; 21(4): 407-26.
10. Fahy GM. Vitrification: a new approach to organ cryopreservation. Prog Clin Biol Res 1986; 224: 305-35.
11. Rall WF. Factors affecting the survival of mouse embryos cryopreserved by vitrification. Cryobiology 1987; 24(5): 387-402.
12. Arav A, Zeron Y, Leslie SB, Behboodi E, Anderson GB, Crowe JH. Phase transition temperature and chilling sensitivity of bovine oocytes. Cryobiology 1996; 33(6): 589-99.
13. Ghetler Y, Yavin S, Shalgi R, Arav A. The effect of chilling on membrane lipid phase transition in human oocytes and zygotes. Hum Reprod 2005; 20(12): 3385-9.
]]>14. Kasai M, Mukaida T. Cryopreservation of animal and human embryos by vitrification. Reprod BioMed Online 2004; 9(2): 164-70.
15. Kasai M, Komi JH, Takakamo A, Tsudera H, Sakurai T, Machida T. A simple method for mouse embryo cryopreservation in a low toxicity vitrification solution, without appreciable loss of viability. J Reprod Fertil 1990; 89(1): 91-7.
16. Emiliani S, Van den Bergh M, Vannin AS, Biramane J, Englert Y. Comparison of ethylene glycol, 1,2-propanediol and glycerol for cryopreservation of slow-cooled mouse zygotes, 4-cell embryos and blastocysts. Hum Reprod 2000; 15(4): 905-10.
17. Zhu SE, Kasai M, Otoge H, Sakurai T, Machida T. Cryopreservation of expanded mouse blastocysts by vitrification in ethylene glycol-based solutions. J Reprod Fertil 1993; 98(1): 139-45.
18. Yokota Y, Sato S, Yokota M, Ishikawa Y, Makita M, Asada T, et al. Successful pregnancy following blastocyst vitrification. Hum Reprod 2000; 15(8): 1802-3.
]]>19. Critser JK, Agca Y, Gunasena KT. The cryobiology of mammalian oocytes. In Karow AM, Critser JK, eds. Reproductive Tissue Banking: scientific principles. New York: Academic Press, 1997: 329-57.
20. Kuleshova LL, MacFarlane DR, Trounson AO, Shaw JM. Sugars exert a major influence on the vitrification properties of ethylene glycol-based solutions and have a low toxicity to embryos and oocytes. Cryobiology 1999; 38(2): 119-30.
21. Kuleshova LL, Shaw JM, Trounson AO. Studies on replacing most of the penetrating cryoprotectant by polymers for embryo cryopreservation. Cryobiology 2001; 43(1): 21-31.
22. Chen C. Pregnancy after human oocyte cryopreservation. Lancet 1986; 1(8486): 884-6.
23. van Uem JF, Siebzehnrübl ER, Schuh B, Koch R, Trotnow S, Lang N. Birth after cryopreservation of unfertilized oocytes. Lancet 1987; 1(8535): 752-3.
]]>24. Tucker MJ, Wright G, Morton PC, Massey JB. Birth after cryopreservation of immature oocytes with subsequent in vitro maturation. Fertil Steril 1998; 70(3): 578-9.
25. Porcu E, Fabbri R, Seracchioli R, Ciotti PM, Magrini O, Flamigni C. Birth of a healthy female after intracytoplasmic sperm injection of cryopreserved human oocytes. Fertil Steril 1997; 68(4): 724-6.
26. Ruffing NA, Steponkus PL, Pitt RE, Parks JE. Osmometric behavior, hydraulic conductivity, and incidence of intracellular ice formation in bovine oocytes at different developmental stages. Cryobiology 1993; 30(6): 562-80.
27. Pedro PB, Zhu SE, Makino N, Sakurai T, Edashige K, Kasai M. Effects of hypotonic stress on the survival of mouse oocytes and embryos at various stages. Cryobiology 1997; 35(2): 150-8.
28. Hunter JE, Fuller BJ, Bernard A, Jackson A, Shaw RW. Vitrification of human oocytes following minimal exposure to cryoprotectants; initial studies on fertilization and embryonic development. Hum Reprod 1995; 10(5): 1184-8.
]]>29. Liebermann J, Tucker MJ. Comparison of vitrification and conventional cryopreservation of day 5 and day 6 blastocysts during clinical application. Fertil Steril 2006; 86(1): 20-6.
30. Osada H, Aono F, Kuwayama M, Morita H, Teramoto S, Kato O. Clinical efficiency of vitrification on blastocysts transfer cycles. Fertil Steril 2003; 80(Suppl 3): S63.
31. Vanderzwalmen P, Bertin G, Debauche Ch, Standaert V, Bollen N, van Roosendaal E, et al. Vitrification of human blastocysts with the Hemi-Straw carrier: application of assisted hatching after thawing. Hum Reprod 2003; 18(7): 1504-11.
32. Kuwayama M, Vajta G, Kato O, Leibo SP. Highly efficient vitrification method for cryopreservation of human oocytes. Reprod BioMed Online 2005; 11(3): 300-8.
33. Kuwayama M, Vajta G, Ieda S, Kato O. Comparison of open and closed methods for vitrification of human embryos and the elimination of potential contamination. Reprod BioMed Online 2005; 11(): 608-14.
]]>34. Vajta G, Holm P, Kuwayama M, Booth PJ, Jacobsen H, Greve T, et al. Open pulled straw (OPS) vitrification: a new way to reduce cryoinjuries of bovine ova and embryos. Mol Reprod Dev 1998; 51(1): 53-8.
35. Ishimori H, Saeki K, Inai M, Nagao Y, Itasaka J, Miki Y, et al. Vitrification of bovine embryos in a mixture of ethylene glycol and dimethyl sulfoxide. Theriogenology 1993; 40(2): 427-33.
36. Isachenko V, Montag M, Isachenko E, Dessole S, Nawroth F, van der Ven H. Aseptic vitrification of human germinal vesicle oocytes using dimethyl sulfoxide as a cryoprotectant. Fertil Steril 2006; 85(3): 741-7.
37. Vajta G, Nagy ZP. Are programmable freezers still needed in the embryo laboratory? Review on vitrification. Reprod BioMed Online 2006; 12(6): 779-96.
38. Michelmann HW, Nayudu P. Cryopreservation of human embryos. Cell Tissue Bank 2006; 7(2): 135-41.
]]>39. Kuwayama M. Highly efficient vitrification for cryopreservation of human oocytes and embryos: the Cryotop method. Theriogenology 2007; 67(1): 73-80.
40. Bielanski A, Vajta G. Risk of contamination of germplasm during cryopreservation and cryobanking in IVF units. Hum Reprod 2009; 24(10): 2457-67.