Farmacogenética y reacción adversa a medicamentos: valor predictivo del polimorfismo en el gen de la uridindifosfato glucuronosil transferasa 1A1
Mag. Marcelo Vital*, Quím. Federico André†, Dra. Patricia Esperón‡
Cátedra de Biología Molecular, Departamento de Bioquímica Clínica,
Facultad de Química. Universidad de la República, Avda. General Flores 2124, Montevideo, Uruguay
Introducción: las reacciones adversas a medicamentos constituyen un problema fundamental para los servicios de salud, la industria farmacéutica y los organismos reguladores. Gran parte de estas reacciones son relativamente leves y desaparecen al modificar la dosis, pero otras son más graves, pudiendo llegar a la muerte del individuo. El irinotecán es un agente citotóxico activo en cáncer colorrectal y pulmonar. Está asociado a una severa toxicidad hematológica y gastrointestinal, impredecibles en la práctica. Su metabolito activo (SN-38) es detoxificado mediante la enzima UDP-glucuronosiltransferasa-1A1 (UGT1A1). La variación en la actividad de esta enzima ha sido relacionada con polimorfismos en el gen UGT1A1, produciendo los efectos adversos observados. El polimorfismo más importante se presenta en la región promotora y consiste en un número variable de repeticiones timina-adenina. El alelo mayoritario tiene seis repeticiones (TA)6, siendo el polimorfismo de siete repeticiones la variante alélica más frecuente.
Objetivo: diseño de un ensayo molecular para el estudio de las variantes alélicas de la región promotora del gen UGT1A1.
Material y método: se seleccionó un grupo de 50 voluntarios sin vínculo familiar. Las determinaciones moleculares se realizaron mediante amplificación y posterior secuenciación de la región promotora.
Resultados y conclusiones: se logró la puesta a punto del diagnóstico molecular propuesto y se determinó que 8% de esa población es homocigoto (TA)7. Planteamos la ventaja de incorporar los resultados de este ensayo molecular en la toma de decisiones terapéuticas y así tender a una farmacoterapia personalizada en medicina oncológica.
Palabras clave: AGENTES ANTINEOPLÁSICOS - efectos adversos. IRINOTECÁN. GLUCURONOSILTRANSFERASA - efectos de drogas.
VARIACIÓN GENÉTICA - efectos de drogas.
Keywords: ANTINEOPLASTIC AGENTS - adverse effects.
IRINOTECAN.
GLUCURONOSYLTRANSFERASE - drug effects.
GLUCURONOSYLTRANSFERASE - genetics.
GENETIC VARIATION - drug effects.
* Magister en Quimica. Asistente de Biología Molecular, Facultad de Química, Universidad de la República. Uruguay.
† Quimico. Uruguay.
]]> ‡ Doctora en Quimica. Profesor Agregado de Biologia Molecular Facultad de Quimica. Universidad de la República. Uruguay.Correspondencia: Dra. Patricia Esperón
Avda. General Flores 2124. CP 11800. Montevideo, Uruguay.
Correo electrónico: pesperon@fq.edu.uy
Recibido: 7/1/10.
Aceptado: 29/3/10.
Introducción
]]> Las reacciones adversas y los fracasos terapéuticos son efectos perjudiciales producidos a menudo debido a polimorfismos genéticos de proteínas que afectan la absorción y el metabolismo de los fármacos.El aporte que trae la farmacogenética a este tema consiste en el conocimiento de las variantes genéticas y su influencia en el modo que respondemos frente a ciertos medicamentos. A partir de esta información es posible identificar a aquellos pacientes que se beneficiarán por cambios en los regímenes terapéuticos de modo de reducir la incidencia de reacciones adversas. Esta aproximación a la terapia personalizada posibilita una óptima y temprana racionalización del tratamiento, revirtiendo las ineficiencias de la metodología de ensayo y error usada tradicionalmente.
La dosificación de medicamentos antitumorales se ha realizado hasta el momento de forma empírica. Pequeños ensayos fase I predicen una dosis tolerable, y los estudios posteriores perfeccionan esa predicción. Sin embargo, debido a la variabilidad interindividual, una proporción de pacientes experimenta inevitablemente una mayor toxicidad frente a dosis estándar de una población.
El irinotecán (CPT-11), introducido en estudios clínicos a principios de 1990, es un eficaz agente antitumoral. Las toxicidades más importantes dosis-dependiente de la terapia con irinotecán son la diarrea y neutropenia severas, ambos factores limitantes de la terapia. El método actual de dosificación basado en la superficie corporal no se correlaciona con el metabolismo y eliminación del irinotecán, dejando a los pacientes en riesgo de desarrollar toxicidad grave(1).
En los últimos años se ha descripto el potencial de los análisis farmacogenéticos para mejorar el índice terapéutico en la terapia del cáncer(2). Hoy día se sabe que el desarrollo de toxicidad asociada al irinotecán es fundamentalmente dependiente de los polimorfismos de las enzimas metabolizadoras de fármacos.
El irinotecán se administra como pro fármaco, el cual es convertido en 7-etil-10-hidroxicamptotecina (SN-38), con aproximadamente 100 a 1.000 veces mayor toxicidad. SN-38 es un potente inhibidor de la topoisomerasa I, lo que provoca rupturas en el ácido desoxirribonucleico (ADN), que conducen en última instancia a la muerte celular. SN-38 se inactiva por acción de las enzimas uridindifosfato glucuronosil transferasas (UGTs), principalmente UGT1A1, y los citocromos CYP3A4 y CYP3A5(3). La eliminación depende de las proteínas transportadoras de fármacos presentes en el canalículo biliar(4). Una vez en el lumen intestinal, el metabolito inactivo (SN-38G) puede reactivarse por la acción de enzimas bacterianas y absorberse nuevamente aumentando el efecto tóxico (figura 1).
El irinotecán presenta efectos mielosupresores con consecuencias clínicas muy importantes. En un ensayo fase III con irinotecán, los pacientes fueron tratados en dos regímenes distintos para evaluar la eficacia y tolerancia de los mismos. Independientemente del régimen de administración seleccionado, siempre se manifestaron neutropenia grado 3 o 4, o diarrea, o ambas(5). Previamente, fue reportado durante un ensayo fase I una relación inversa entre la glucuronidación de SN-38 y las tasas de frecuencia de diarrea(6). Esto condujo a la hipótesis de que la toxicidad asociada a irinotecán podía ocurrir en algunos pacientes debido a las variaciones en la forma en que metabolizaban el fármaco. Los altos índices de toxicidad pueden conducir a la deshidratación, las infecciones, la necesidad de fármacos adicionales, la hospitalización e incluso a la muerte. Existe una fuerte evidencia entre la variación en la actividad de la enzima UGT1A1 con los niveles elevados y prolongados de SN-38 en plasma, dando lugar a los efectos adversos del tratamiento.
UGT1A1 pertenece a la superfamilia de enzimas microsomales de fase II y se localizan en la membrana del retículo endoplasmático en el hígado y tejidos extrahepáticos(7). Su gen se ubica en la posición 2q37, posee siete exones y el producto proteico es de 528 aminoácidos. Hasta el momento se han descripto más de 30 variantes genéticas, muchas de las cuales afectan el funcionamiento de la enzima. Una de ellas se encuentra en la TATA-box de la región promotora del gen, donde se observa una variabilidad del número de repeticiones de dinucleotidos timina-adenina (TA). El aumento del número de repeticiones lleva a una disminución en la tasa de iniciación de la transcripción y, por tanto, disminuye la expresión de la proteína reduciendo la desintoxicación de irinotecán(8).
El alelo más común (o "nativo" UGT1A1*1) tiene seis repetidos. Además se han identificado tres variantes alélicas con cinco, siete, y ocho repeticiones. El polimorfismo (TA)7 (UGT1A1*28) se encuentra en 10% de individuos homocigotos (7/7) en población de América del Norte. Los polimorfismos (TA)5 y (TA)8 (UGT1A1*33 y UGT1A1*34, respectivamente) son menos comunes y se encuentran principalmente en individuos de origen africano. La tabla 1 resume los datos reportados sobre la frecuencia de los diferentes polimorfismos del promotor de UGT1A1 en diferentes grupos étnicos(9). Estudios in vivo sobre terapia con irinotecán a dosis estándar han mostrado una asociación entre el polimorfismo UGT1A1*28 con valores farmacocinéticos y efectos adversos (principalmente diarrea y neutropenia)(10).
En 2005, la Food And Drug Administration avaló los resultados que permiten identificar en forma prospectiva a los pacientes que se encuentran en riesgo de presentar efectos adversos asociados al uso de dosis estándar de irinotecán. Los pacientes con el genotipo homocigoto (TA)7 tienen un riesgo 9,3 veces mayor de desarrollar neutropenia grado 4 que aquellos con los genotipos homocigoto (TA)6 y heterocigoto (TA)6/7. A partir de estos datos, la información para la prescripción de irinotecán cambió y en el prospecto se recomienda una reducción de dosis inicial de por lo menos un nivel para los pacientes homocigotos (TA)7(11). Para los pacientes heterocigotos, si bien se advierte que pueden tener cierto riesgo de desarrollar neutropenia, no se sugiere la reducción de la dosis. Esta medida resultó en un avance con respecto a cómo los enfoques de la farmacogenómica pueden permitir reducir los riesgos de la quimioterapia.
]]> Nos propusimos como objetivo de este trabajo la puesta a punto de un ensayo molecular para determinar las variantes alélicas de la región promotora del gen UGT1A1. De esta manera es posible identificar el subgrupo de pacientes en riesgo de presentar efectos adversos asociados a estos polimorfismos genéticos durante el tratamiento con irinotecán. Nuestra intención es que estos datos sean tenidos en cuenta en el momento de tomar decisiones sobre la elección del tipo de medicación y dosis a utilizar en el tratamiento quimioterápico.Material y método
Sujetos
El análisis del número de repetidos se llevó a cabo a partir de 50 muestras de ADN en voluntarios sanos, sin vínculo familiar, que consintieron en participar en el estudio. El proyecto de investigación fue aprobado por el Comité de Ética de la Facultad de Química.
Diagnósticos moleculares
]]> Los análisis genéticos se realizaron con ADN genómico obtenido a partir de sangre total (100-200 ml). Se utilizó kit comercial para realizar la extracción de ADN siguiendo las indicaciones del fabricante. El ADN aislado fue sometido a una amplificación por reacciones en cadena de la polimerasa (PCR) realizada en un volumen final de 25 mL y utilizando 100 ng de ADN, 200 mM/L de cada nucleótido, 0,5U de Taq polimerasa (Fermentas Lituania), 2 mL de buffer Taq 10x conteniendo 2 mM de MgCl2, y 0,5 mM de cebadores. La secuencia de los cebadores utilizada fue previamente descripta y se le realizaron leves modificaciones(12).Los productos amplificados fueron purificados y las determinaciones de los cambios respecto a UGT1A1*1 se realizaron por análisis de la secuencia (servicio de secuenciado automático por la empresa Macrogen, Corea).
Estadística
Las frecuencias genotípicas se calcularon mediante conteo y a partir de ellas se obtuvieron las frecuencias alélicas. Se aplicó el test chi cuadrado con un nivel de significancia de 0,05 para comparar las frecuencias obtenidas en este estudio con las reportadas.
Resultados y discusión
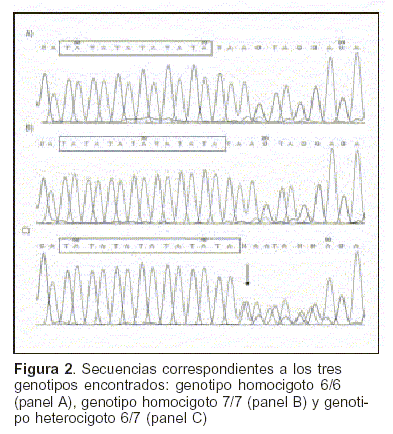
De los 50 individuos estudiados, 22 (44%) presentan alguna de las variantes alélicas mencionadas. La distribución genotípica encontrada fue de 56% (28), 36% (18) y 8% (4) para los genotipos homocigoto (TA)6, heterocigoto (TA)6/7 y homocigoto (TA)7, respectivamente (figura 2). Estos valores son muy similares a los encontrados para la población de Sardinia (Italia)(13), pero no resultan comparables con el resto de la población europea, asiática y africana (tabla 1). Aplicando el test chi cuadrado, se verificó que la distribución genotípica no difiere de la esperada para una población que se encuentra en equilibrio de Hardy-Weinberg.
]]>

Las frecuencias alélicas calculadas para los alelos UGT1A1*1 y UGT1A1*28 fueron de 0,74 y 0,26, respectivamente (figura 3). Si comparamos nuestros resultados, estos resultan comparables con los reportados para una población caucásica(9).
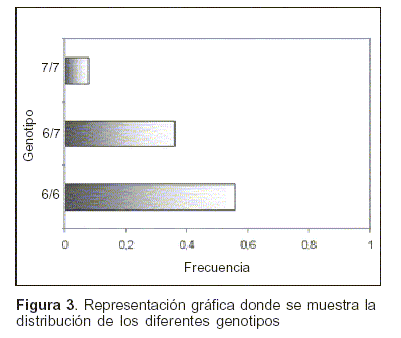
No se encontraron individuos con el número de repeticiones menos frecuentes (TA)5 y (TA)8, probablemente debido al tamaño pequeño de la muestra.
Conclusiones
El desarrollo de la farmacogenómica se ha constituido en una herramienta valiosa a la hora de seleccionar racionalmente una terapia en particular, identificando pacientes cuyo perfil genético molecular sugiera incapacidad o severo déficit en la detoxificación de fármacos. La identificación de variantes en los genes implicados en este proceso ayuda en la gestión de atención al paciente mediante la determinación de cuáles pacientes deben evitar cierta medicación y quiénes deben recibir una dosis diferente. Esta estrategia podría potencialmente reducir los costos médicos y mejorar el proceso de desarrollo de medicamentos.
Gran parte de la variabilidad interindividual respecto a la toxicidad frente al irinotecán puede explicarse por el polimorfismo UGT1A1*28. Los pacientes que son homocigotos para este alelo tienen un mayor riesgo de desarrollar neutropenia grave al recibir irinotecán, en especial en régimen de 300-350 mg/m2.
]]> El interés en el estudio de las variantes alélicas de UGT1A1 no sólo está dado por el uso creciente de irinotecán en oncología, sino además porque estos resultados pueden ser extrapolados para otros fármacos que también utilizan la glucuronidación como vía de detoxificación(14).La total individualización de la quimioterapia antineoplásica representa un objetivo todavía lejano en la práctica clínica, por lo que los pacientes se hallan expuestos a severa toxicidad o a ineficacia terapéutica, o ambas, habiendo pocos elementos determinantes para predecir la terapéutica más adecuada. Con el objetivo de lograr una terapia individualizada, la información genética aporta un dato adicional que puede ser usado en combinación con otras características del individuo (como la edad, función hepática, función renal, medicaciones concomitantes, etcétera).
Con este propósito, realizamos un estudio sobre una muestra de 50 individuos, que aunque no significa la verdadera representación de nuestra población, sirve como ejemplo para demostrar que existe un porcentaje considerable de individuos que presentan el cambio en homocigocia (8%). Estos individuos son los que podrían estar en riesgo de desarrollar efectos adversos ante la eventualidad de ser sometidos a una terapia con irinotecán. La individualización del tratamiento para ellos resulta ventajosa, ya que son los grupos menos representados los que están en riesgo de sufrir los efectos adversos frente a dosis estándar de este fármaco.
El análisis de otras variantes en el gen de UGT1A1(15-16) podría ser informativo con el fin de crear un haplotipo, de forma de realizar una asociación aun más significativa entre un conjunto de variantes y la aparición de efectos adversos.
En suma, disponemos en nuestro país de un ensayo molecular para realizar el estudio de las variantes alélicas de la región promotora del gen UGT1A1. El determinar el genotipo del paciente antes de iniciar la terapia se vuelve un enfoque realista para lograr la disminución de las incidencias de la neutropenia y la diarrea asociadas al tratamiento con irinotecán. Teniendo en cuenta la severa toxicidad causada y los beneficios obtenidos al reducir la dosis inicial de irinotecán, parece plausible llevar a cabo un estudio del genotipo de UGT1A1 en los pacientes que se encuentran próximos a recibir terapia con este fármaco.
Summary
Introduction: adverse reactions to drugs constitute an essential problem for health services, the pharmaceutical industry and the regulatory bodies. Most of these reactions are relatively mild and they disappear when dosage is modified, although others are more serious and they may result in death. Irinotecan is an active cytotoxic agent in colorectal and lung cancer. It is associated to severe hematological and gastrointestinal toxicity, unpredictable in practice. Its active metabolite (SN-38) is detoxified by the uridine diphosphate glucoronosyltransferase 1A1enzyme (UGT1A1). (UGT1A1). Variation in the activity of this enzyme has been associated to polymorphisms in the UGT1A1 gene, what results in the adverse reactions observed. The most important polymorphisms appear in the polymorphism of the promoting region, which consists in a variable repetition of thymine-adenine repetitions. The main allele has six repetitions (TA)6, being the seven repetition polymorphism the most frequent allelic variant.
Objetive: to design a molecular test to study allelic variants of the promoting region in the UGT1A1 gene.
Method: We selected a group of 50 volunteers with no family bonds. Amplification and subsequent sequencing of the promoting region were used to determine molecules.
]]> Results: we managed to update the suggested molecular diagnosis and determined that 8% of this population is a homozygote (TA)7. We propose the advantage of incorporating the results of this molecular test for the making of therapeutic decisions and thus make progress toward a more personalized oncologic medicine.Résumé
Introduction: les réactions adverses aux médicaments constituent un problème fondamental pour les services de santé, l’industrie pharmaceutique et les organismes pertinents. La plupart de ces réactions sont légères et disparaissent une fois la dose modifiée, mais d’autres sont plus graves et peuvent aboutir à la mort de l’individu. L’irinotécan est un agent cytologique actif au cancer colorectal et pulmonaire. Il est associé à une sévère toxicité hématologique et gastro-intestinal, pas prédictive. Son métabolite actif (SN-38) est détoxiqué au moyen de l’ enzyme UDP- glucuronyltransférase-1A1 (UGT1A1). La variation à l’activité de cette enzyme est en rapport avec des polymorphismes au gène UGT1A1, ce qui produit les effets adverses observés. Le polymorphisme le plus important se présente à la région promotrice, étant un nombre variable de répétitions thymine adénine. L’allèle majoritaire a six répétitions (TA)6, le polymorphisme à sept répétitions étant la variante allénique la plus fréquente.
Objectif: dessin d’un essai moléculaire pour l’étude des variantes alléniques de la région promotrice du gène UGT1A1.
Matériel et méthode: 50 volontaires choisis sans lien familial. Les déterminations moléculaires ont été réalisées au moyen d’amplification et une postérieure séquence de la région promotrice.
Résultats et conclusions: on a réussi la mise au point du diagnostic moléculaire proposé et on a déterminé que 8% de cette population est homozygote (TA)7. On remarque l’importance d’incorporer les résultats de cet essai moléculaire lors de la prise de décisions thérapeutiques, ce qui mènerait à une pharmacothérapie personnalisée en médecine oncologique.
Resumo
Introdução: as reações adversas a medicamentos são um problema importante para os serviços de saúde, a indústria farmacêutica e os organismos reguladores. Muitas destas reações são relativamente leves e desaparecem com a modificação da dose, porém outras são mais graves podendo levar à morte do paciente. O irinotecan é um agente citotóxico ativo em câncer colorretal e pulmonar. Está associado à toxicidade hematológica e gastrointestinal grave, imprevisível na prática. Seu metabólito ativo (SN-38) é detoxificado pela enzima UDP-glucuronosiltransferase-1A1 (UGT1A1). A variação da atividade desta enzima foi relacionada com polimorfismos no gene UGT1A1, produzindo os efeitos adversos observados. O polimorfismo mais importante se apresenta na região promotora e consiste num número variável de repetições timina-adenina. O alelo mais numeroso tem seis repetições (TA)6, sendo que o polimorfismo de sete repetições é a variante alélica mais frequente.
]]> Objetivo: projeto de um ensaio molecular para estudar as variantes dos alelos da região promotora do gene UGT1A1.Material e método: um grupo de 50 voluntários sem vínculo familiar foi selecionado. As determinações moleculares foram realizadas por amplificação e posterior seqüenciação da região promotora.
Resultados e conclusões: foi possível realizar o diagnóstico molecular proposto e determinar que 8% da população estudada era homozigota. (TA)7. Discutimos a vantagem de incorporar os resultados deste ensaio molecular na tomada de decisões terapêuticas e dessa forma estabelecer uma tendência à farmacoterapia personalizada em oncologia.
Bibliografía
1. Mathijssen RH, Verweij J, de Jonge MJ, Nooter K, Stoter G, Sparreboom A. Impact of body-size measures on irinotecan clearance: alternative dosing recommendations. J Clin Oncol 2002; 20(1): 81-7.
2. Deeken JF, Figg WD, Bates SE, Sparreboom A. Toward individualized treatment: prediction of anticancer drug disposition and toxicity with pharmacogenetics. Anti-Cancer Drugs 2007; 18(2): 111-26.
3. Gagné JF, Montminy V, Belanger P, Journault K, Gaucher G, Guillemette C. Common human UGT1A polymorphisms and the altered metabolism of irinotecan active metabolite 7-ethyl-10-hydroxycamptothecin (SN-38). Mol Pharmacol 2002; 62(3): 608-17.
4. Dean M, Hamon Y, Chimini G. The human ATP-binding cassette (ABC) transporter superfamily. J Lipid Res 2001; 42(7): 1007-17.
5. Fuchs CS, Moore MR, Harker G, Villa L, Rinaldi D, Hecht JR. Phase III comparison of two irinotecan dosing regimens in second-line therapy of metastatic colorectal cancer. J Clin Oncol 2003; 21(5): 807-14.
6. Gupta E, Lestingi TM, Mick R, Ramírez J, Vokes EE, Ratain MJ. Metabolic fate of irinotecan in humans: correlation of glucuronidation with diarrhea. Cancer Res 1994; 54(14): 3723-5.
7. Ando Y, Saka H, Ando M, Sawa T, Muro K, Ueoka H, et al. Polymorphisms of UDP-glucuronosyltransferase gene and irinotecan toxicity: a pharmacogenetic analysis. Cancer Res 2000; 60(24): 6921-6.
8. Bosma PJ, Chowdhury JR, Bakker C, Gantla S, de Boer A, Oostra BA, et al. The genetic basis of the reduced expression of bilirubin UDP-glucuronosyltransferase 1 in Gilbert’s syndrome. N Engl J Med 1995; 333(18): 1171-5.
9. Beutler E, Gelbart T, Demina A. Racial variability in the UDP-glucuronosyltransferase 1 (UGT1A1) promoter: A balanced polymorphism for regulation of bilirubin metabolism? Proc Natl Acad Sci USA 1998; 95(14): 8170-4.
10. Iyer L, Das S, Janisch L, Wen M, Ramírez J, Karrison T, et al. UGT1A1*28 polymorphism as a determinant of irinotecan disposition and toxicity. Pharmacogenomics J 2002; 2(1): 43-7.
11. Innocenti F, Undevia SD, Iyer L, Chen PX, Das S, Kocherginsky M, et al. Genetic variants in the UDP-glucuronosyltransferase 1A1 gene predict the risk of severe neutropenia of irinotecan. J Clin Oncol 2004; 22(8): 1382-8.
12. Fang JL, Lazarus P. Correlation between the UDP-glucuronosyltransferase (UGT1A1) TATAA box polymorphism and carcinogen detoxification phenotype: significantly decreased glucuronidating activity against benzo(a)pyrene-7,8-dihydrodiol(-) in liver microsomes from subjects with the UGT1A1*28 variant. Cancer Epidemiol Biomarkers Prev 2004; 13(1): 102-9.
13. Ratain MJ, Di Rienzo A, Iyer L, inventors. Methods for detection of promoter polymorphism in a UGT gene promoter. Origin: AUSTIN, TX US. IPC8 Class: AA61K31435FI. USPC Class: 514283. Patent application number: 2009031 8487.
14. Rodríguez-Nóvoa S, Martín-Carbonero L, Barreiro P, González-Pardo G, Jiménez-Nácher I, González-Lahoz J, et al. Genetic factors influencing atazanavir plasma concentrations and the risk of severe hyperbilirubinemia. AIDS 2007; 21(1): 41-6.
15. Innocenti F, Grimsley C, Das S, Ramírez J, Cheng C, Kuttab-Boulos H, et al. Haplotype structure of the UDP-glucuronosyltransferase 1A1 promoter in different ethnic groups. Pharmacogenetics 2002; 12(9): 725-33.
16. Côté JF, Kirzin S, Kramar A, Mosnier JF, Diebold MD, Soubeyran I, et al. UGT1A1 polymorphism can predict hematologic toxicity in patients treated with irinotecan. Clin Cancer Res 2007; 13(11): 3269-75.