Impacto clínico de la tomografía de emisión
por positrones (PET) en pacientes oncológicos y su potencial aplicación en el contexto sanitario y académico nacional
Dr. Omar Alonso*
Centro de Medicina Nuclear. Hospital de Clínicas. Facultad de Medicina. Universidad de la República. Montevideo, Uruguay
Resumen
La tomografía de emisión de positrones (PET) es una técnica de medicina nuclear que tiene la capacidad de detectar el cáncer por medio de mecanismos basados en las alteraciones moleculares de los procesos neoplásicos. En esta revisión se describen las aplicaciones oncológicas del PET y se analiza la potencial aplicación de esta tecnología en el contexto sanitario y académico nacional. El trazador más utilizado en oncología es un análogo de la glucosa marcado con flúor: 18F-2-flúor-2-desoxi-D-glucosa (FDG). De esta forma, el PET detecta la retención tumoral de FDG, debido al mayor índice glucolítico de las células cancerosas. Además, los tomógrafos PET permiten el estudio de todo el cuerpo en el mismo acto exploratorio y algunos equipos se encuentran acoplados a sistemas de tomografía axial computarizada (PET-TAC). Mediante PET-FDG es posible diagnosticar, estadificar y reestadificar la mayoría de los cánceres, con exactitudes diagnósticas cercanas a 90%, superior a los valores aportados por las técnicas imagenológicas convencionales. Además, es posible conocer precozmente la respuesta a los tratamientos oncológicos y obtener información pronóstica relevante.
Palabras claves: TOMOGRAFÍA POR EMISIÓN DE POSITRONES - utilización.
]]> TOMOGRAFÍA POR EMISIÓN DE POSITRONES - métodos.FLUORODESOXIGLUCOSA F 18 - uso diagnóstico.
NEOPLASMAS - diagnóstico.
* Profesor Agregado de Medicina Nuclear, Facultad de Medicina. Universidad de la República. Montevideo, Uruguay
Correspondencia: Dr. Omar Alonso
Centro de Medicina Nuclear. Hospital de Clínicas. Av. Italia s/n
Montevideo, Uruguay
E-mail: oalonso@hc.edu.uy
Recibido: 2/5/06.
Aceptado: 1/8/06.
]]>Introducción
La tomografía de emisión de positrones (PET) es una técnica imagenológica de medicina nuclear que requiere la inyección de un trazador radiactivo, emisor de positrones. Al igual que la medicina nuclear convencional, el principio de esta técnica se basa en el concepto de la cinética de trazadores, posibilitando la detección de procesos fisiopatológicos que resultan de cambios bioquímicos. Sin embargo, se diferencia claramente de los procedimientos convencionales de la especialidad al permitir visualizar los cambios mencionados en el nivel de organización molecular de los sistemas biológicos. Esto es debido a que los "trazadores" o radioisótopos utilizados son en sí mismo "sondas moleculares," es decir moléculas idénticas o indistinguibles de los sustratos bioquímicos fundamentales.
Los radioisótopos emisores de positrones son elementos básicos de la química orgánica como: 11C, 13N, 15O y 18F. En consecuencia, es posible marcar fácilmente cualquier molécula biológica por sustitución o mediante halogenación con 18F. Las moléculas a marcar pueden ser metabolitos, como la glucosa o sus análogos, aminoácidos, ácidos grasos, agua, oxígeno y moléculas afines a receptores celulares diversos.
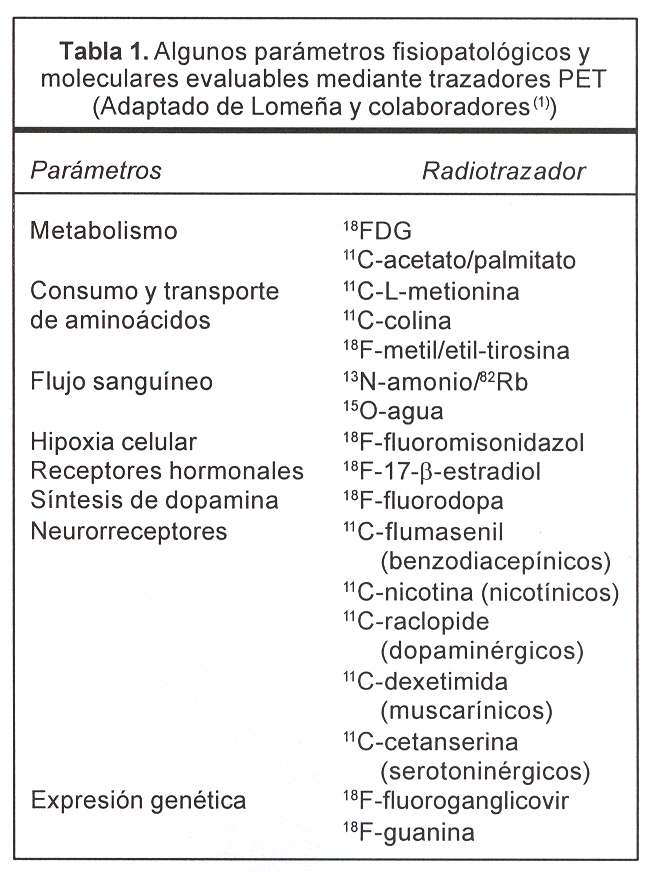
En consecuencia, es posible evaluar in vivo procesos vinculados con cambios metabólicos, de flujo sanguíneo, de consumo de oxígeno, del grado de unión entre agonistas y receptores, entre otros. En la tabla 1 se recogen algunos de los parámetros que puede visualizar y medir el PET, con sus radiofármacos correspondientes.
Una característica importante de los isótopos emisores de positrones es que son producto de ciclotrón (equipo acelerador de partículas) y, debido a su vida media muy corta (2-110 minutos), el laboratorio de radiofarmacia, para la síntesis de los compuestos, y la cámara PET, para la adquisición de las imágenes, deben estar situados a corta distancia. Los positrones corresponden a electrones con carga positiva que algunos radioisótopos liberan desde su núcleo en su decaimiento radiactivo. Esta partícula viaja algunos milímetros en el tejido antes de colisionar con un electrón. De esta colisión se aniquila la masa completa del positrón y del electrón liberando dos fotones de 511 Kev. Estos fotones viajan en direcciones opuestas, interactuando con detectores opuestos de la cámara o tomógrafo PET (figura 1). De esta forma, la localización del evento radiactivo puede ser determinada con exactitud. Estos equipos pueden adquirir imágenes en dos y tres dimensiones, en forma de estudios estáticos o dinámicos y reconstruyen imágenes volumétricas que se presentan como tomografías sectoriales o de cuerpo entero, con una muy buena resolución espacial, que puede llegar a los 4,0 mm(1).
El PET es actualmente una realidad. La transición desde el ámbito de la investigación básico y clínico, donde fuera empleada por más de 25 años, al escenario asistencial ha sido realizada exitosamente en los últimos diez años. En este sentido, existe vasta evidencia (más de 15.000 publicaciones arbitradas) en relación con los beneficios clínicos de la técnica(2). El impacto en el manejo clínico de los pacientes ha sido de tal magnitud que algunos autores consideran al PET como el desarrollo más importante de las técnicas imagenológicas de los últimos veinte años(3).
El propósito de esta revisión es el de proveer a los médicos clínicos de un marco conceptual básico de forma de poder comprender las aplicaciones clínicas del PET en el manejo de pacientes con enfermedad oncológica. Asimismo, analizaremos brevemente la potencial aplicación de esta tecnología en el ámbito sanitario y académico nacional.
18Flúor-desoxi-glucosa (FDG): radiofármaco PET
de mayor uso clínico
El 18F se ha empleado para marcar la desoxiglucosa a fin de producir el principal radiotrazador de uso actual: la FDG (18F-2-flúor-2-desoxi-D-glucosa). Este radiofármaco es el único con aplicación clínica e indicaciones establecidas, según criteros de la medicina basada en la evidencia(1). Esto ha sido posible por las características metabólicas y la rápida síntesis de la molécula, junto con una vida media adecuada del 18F (110 min).
La FDG es transportada al interior de las células por el mismo mecanismo que la glucosa no marcada, por difusión pasiva facilitada por proteínas transportadoras, siendo después fosforilada a 18FDG-6-fosfato por las enzimas hexoquinasa y glucoquinasa. Ésta queda atrapada en las células porque no puede continuar la vía metabólica de la glucosa.
La utilización de la FDG en la evaluación de pacientes oncológicos se basa en la concentración aumentada de este trazador en el interior de las células tumorales por varias razones(4):
- aumento en el número de dichas moléculas;
- aumento de la actividad de las isoenzimas de la hexoquinasa;
- disminución de la actividad de la glucosa-6-fosfatasa.
Por otra parte, la FDG permite, además, explorar otros procesos patológicos pertenecientes a tejidos que utilizan preferentemente glucosa como fuente energética. Tal es el caso del miocardio y el cerebro, lo cual ha permitido la utilización clínica de la técnica en la evaluación de pacientes con distintas enfermedades del sistema nervioso central y con cardiopatía isquémica(5).
Otras moléculas marcadas con emisores de positrones también pueden tener un papel importante en la evaluación de otras enfermedades: aminoácidos, purinas y pirimidinas, trazadores de flujo sanguíneo, de hipoxia, entre otras. En este sentido, el 11C es un radioisótopo emisor de positrones de enorme potencial, capaz de marcar una gran variedad de biomoléculas. A modo de ejemplo, el PET con 11C-metionina es capaz de evaluar el metabolismo amino-acídico tisular, siendo útil en varios tipos de tumores cerebrales primarios, particularmente los gliomas(1).
En adelante nos referiremos a las aplicaciones clínicas del PET con FDG.
Aplicaciones oncológicas del PET
El PET tiene aplicaciones clínicas relevantes en tres grandes áreas: oncología, cardiología y neurología. Las aplicaciones oncológicas constituyen 90% de su uso actual, de forma que esta tecnología representa una herramienta fundamental en el manejo clínico de pacientes con cáncer(6). En efecto, el PET está cambiando la metodología de estudio y seguimiento de estos pacientes, obligando a una re-evaluación de los métodos de estadificación convencional realizados mediante tomografía axial computarizada (TAC) y resonancia magnética (RM).
]]> En forma general, podemos señalar que la tomografía PET se puede usar en la evaluación de pacientes oncológicos para(1,7):- Distinguir entre tumores benignos y malignos en donde las imágenes anatómicas sean dudosas y existan contraindicaciones relativas para la biopsia.
- Identificar un tumor primario desconocido en pacientes con enfermedad metastásica.
- Establecer el grado de malignidad de un tumor.
- Establecer el estadio de la enfermedad al diagnóstico y en la recaída (reestadificación).
- Evaluar la existencia de enfermedad recurrente o residual.
- Establecer la topografía de las lesiones metastásicas en pacientes con niveles elevados o en ascenso de marcadores tumorales.
- Evaluar la respuesta a la terapia oncológica.
- Planificación de la radioterapia.
Es importante no confundir las indicaciones clínicas del PET con utilidad claramente demostrada con las financiadas por los sistemas sanitarios extranjeros, las cuales son más estrictas, menos numerosas, y sujetas a controles económicos rigurosos, dependiente de cada sistema de salud. La tabla 2 muestra a modo de ejemplo las indicaciones aprobadas por Medicare (sistema público estadounidense) y por la Agencia de Evaluación de Tecnologías Sanitarias (AETS) de España .
]]> Diagnóstico de malignidad en lesiones conocidasSe ha demostrado que el PET-FDG posee una elevada sensibilidad y elevado valor predictivo negativo (mayor a 90%), para la determinación de malignidad de pacientes con nódulo pulmonar solitario (NPS)(8,9). Se han asociado resultados falsos negativos a lesiones menores a 1 cm, tumores bronquioloalveolares y carcinoides. Asimismo, lesiones infecciosas y granulomatosas pueden captar FDG. De esta forma, algunos autores describen valores de especificidad cercanos a 80%(8). La mayoría de los autores aconseja realizar esta técnica en pacientes en los cuales exista discordancia entre la probabilidad pretest de malignidad y los hallazgos de la TAC, en pacientes con probabilidad pretest intermedia y con alto riesgo de complicaciones quirúrgicas y en pacientes con NPS que hayan mostrado crecimiento mediante radiografía de tórax o TAC(5,10). Es importante recordar que el PET-FDG no es solamente útil en la visualización del NPS, sino que además permite cambiar el manejo clínico de los pacientes al detectar enfermedad ganglionar y metastásica insospechada(8).
El PET ha demostrado también utilidad para diferenciar lesiones pancreáticas benignas de malignas. Se han reportado valores de sensibilidad entre 71%-100% (media: 92%) y de especificidad entre 64%-100% (media: 82%)(11). Esta técnica ha sido recomendada en pacientes con lesiones hipoecogénicas en la ecografía o hipodensas en la TAC con incremento en las concentraciones de CA-19.9(12), en pacientes con tumores pancreáticos de naturaleza indeterminada sin hiperglicemia y sin evidencia serológica de enfermedad activa inflamatoria(13), y en la evaluación de lesiones pancreáticas quísticas(14). Recientemente, Heinrich y colaboradores demostraron en una serie de 51 pacientes, valores de sensibilidad similares del PET y la TAC helicoidal (cercanos a 90%). Sin embargo, la especificidad del PET resultó mayor (69%) que la correspondiente a la TAC (21%)(15).
Se ha demostrado también que el PET tiene un gran potencial en la diferenciación de masas adrenales malignas de las benignas en pacientes con diagnóstico previo de cáncer y en aquellos en los cuales el diagnóstico fue realizado incidentalmente mediante TAC o RM. Se reportaron valores entre 93%-99% y 92%-96% para la sensibilidad y especificidad, respectivamente(16,17). Además la técnica demostró una sensibilidad de 88% y especificidad de 96% en pacientes con masas adrenales indeterminadas por la TAC(16).
Metástasis de tumores de origen desconocido
En pacientes con metástasis de tumor primario desconocido (MPD), se realizan frecuentemente múltiples estudios imagenológicos convencionales y procedimientos invasivos costosos, los cuales sólo logran identificar la lesión primaria en 20%-30% de los casos(9). El PET ha conseguido localizar el tumor primitivo en 24%-53% de pacientes con MPD(1,9,18,19). Recientemente, Scott y colaboradores han demostrado, mediante evaluación con PET, un cambio de conducta clínica en 38% de pacientes con este síndrome(18). El impacto clínico de esta técnica es importante en pacientes con enfermedad metastásica resecable, como ocurre en casos con adenopatías cervicales o supraclaviculares, y en pacientes con metástasis diseminadas en los que la localización del tumor primitivo permite una quimioterapia más dirigida(1,19). Además, el PET permite en estos pacientes realizar una estadificación más exhaustiva, no siendo infrecuente el hallazgo de localizaciones metastásicas desconocidas(5).
Recientemente, algunos autores han documentado una mayor sensibilidad del PET-CT en comparación con el PET dedicado, con valores de sensibilidad de hasta 57%(20,21).
]]> EstadificaciónEn el año 2003, Gould y colaboradores confirmaron en su metaanálisis la superioridad del PET con respecto a la TAC en la estadificación mediastinal del carcinoma de pulmón a células no pequeñas (CPCNP), con una sensibilidad y especificidad promedio de 85% y 90% para el PET y de 61% y 79% para la TAC, respectivamente(10). En este sentido, el PET ha demostrado también mejores valores diagnósticos que la ecografía transesofágica para la estadificación regional(22). El elevado valor predictivo negativo de esta técnica ha llevado a algunos autores a postular que cuando la misma es negativa para compromiso mediastinal los pacientes pueden ser sometidos directamente a toracotomía, evitándose procedimientos estadificadores invasivos. Verhagen y colaboradores, recientemente documentaron un valor predictivo negativo global del PET para la estadificación mediastinal de 71%. No obstante, el mismo desciende a 17% en el grupo de pacientes con PET positivo para ganglios hiliares o con tumores centrales, o ambos(23). Esto es debido a problemas vinculados con la resolución espacial de la técnica en la diferenciación del tumor primario y ganglios captantes adyacentes. Por tal motivo, estos autores recomiendan la mediastinoscopía en este grupo. El valor predictivo positivo del PET es elevado. De todas formas, se pueden encontrar resultados falsos positivos vinculados a procesos inflamatorios o granulomatosos. En consecuencia, en pacientes con un PET positivo para compromiso mediastinal, es necesario confirmar la presencia de un estadio N2 o N3 mediante mediastinoscopía(8).
El diagnóstico de metástasis extratorácicas no sospechadas permite evitar a los pacientes cirugías innecesarias. Las mismas están presentes en más de 10% de los estudios PET de pacientes con CPCNP en el momento de la evaluación inicial(5,23). Por otra parte, la técnica puede determinar la naturaleza de lesiones indeterminadas presentes en estudios convencionales, lo cual ocurre en 7%-19% de los pacientes. De esta forma, el PET permite cambiar la conducta clínica en 25%-52%, siendo lo más común la identificación de mayor extensión de la enfermedad(8).
El valor clínico del PET en el cáncer de pulmón a células pequeñas ha sido menos estudiado. Recientemente, Brink y colaboradores, en un trabajo prospectivo de 120 pacientes, demostraron la capacidad de la técnica en cambiar el estadio inicial de los pacientes en 12% de los casos. La mayoría de estos cambios (71%) correspondió a un aumento del estadio(24).
También se ha validado la utilidad del FDG-PET en la estadificación de pacientes con linfoma. Con la excepción de algunos subtipos de linfomas no Hodgkin, la mayoría presenta moderada-alta captación de glucosa(25). Comparado con el centellograma con galio, el PET posee mayor resolución espacial, mayor sensibilidad (especialmente en abdomen y hueso), menor dosis absorbida por el paciente y una duración del estudio mucho más corta: dos horas para el PET versus 3-7 días para el galio(26). Recientemente, Isasi y colaboradores describieron en un metaanálisis realizado con 25 trabajos, una sensibilidad y especificidad media del PET de 90% y 91%, respectivamente. En este estudio, los pacientes con enfermedad de Hodgkin presentaron mayor sensibilidad y menor especificidad medias que las correspondientes a los pacientes con linfomas no Hodgkin: 93%-88% versus 88%-94%, respectivamente(27). Asimismo, existe amplia evidencia que demuestra la superioridad diagnóstica del PET frente a la TAC, con valores de exactitud diagnóstica de la primera técnica que superan en 11%-24% a los correspondientes a la segunda(28,29). En una revisión sistemática publicada en 2003, el PET logró cambiar el estadio en 24% de pacientes, modificando el abordaje terapéutico en 13% de los casos. De los pacientes, 90% pasaron a estadios superiores, mientras que sólo 10% lo hicieron a estadios inferiores(30).
Varios investigadores han estudiado el valor del PET en el manejo clínico de pacientes con melanoma. La técnica ha demostrado un relevante papel en el diagnóstico de enfermedad metastásica. Sin embargo, la estrategia del ganglio centinela (GC) presenta una mayor sensibilidad para el diagnóstico de compromiso ganglionar regional en pacientes con melanoma clínicamente localizado(31). Por otra parte, es indiscutido el valor del PET en la evaluación de enfermedad sistémica. En una revisión realizada por Schwimmer y colaboradoares(32), el PET demostró una sensibilidad y especificidad media de 92% y 90%, respectivamente. Cuando el PET se suma a la información aportada por la TAC en la estadificación inicial de pacientes con melanoma de alto riesgo, se ha descripto un cambio en el manejo clínico de los pacientes de hasta 90% debido a la detección de lesiones metastásicas clínicamente ocultas(33). Varios autores han demostrado valores de sensibilidad y especificidad mayores para el PET en comparación con los correspondientes a las técnicas imagenológicas convencionales(31,34).
La TAC y la RM son las técnicas de elección para valorar la invasión local de un tumor primitivo de cabeza y cuello (TCC). La mayoría de los trabajos publicados muestra mayores valores diagnósticos del PET para la estadificación ganglionar regional en comparación a las técnicas imagenológicas convencionales(5). Sin embargo, la biopsia del GC es la técnica de elección debido a su mayor sensibilidad para la detección de micrometástasis(35). Recientemente, Kovács y colaboradores(36) propusieron que la alta especificidad del PET, junto con la alta sensibilidad de la estrategia del GC, permitía el uso de ambas técnicas en la estadificación prequirúrgica de pacientes con TCC clínicamente N0. Además del valor del PET en la estadificación locorregional de estos pacientes, la técnica permite detectar metástasis a distancia desconocidas o segundos tumores primarios, los cuales están presentes en aproximadamente 3%-8% de pacientes con TCC(37).
En la evaluación de pacientes con cáncer de esófago, existe acuerdo en considerar que el PET detecta mejor el tumor primario y las metástasis sistémicas que los métodos convencionales de imagen(38,39). En efecto, en tumores localmente avanzados esta técnica puede detectar 15%-20% de pacientes con metástasis a distancia, evitando la realización de procedimientos quirúrgicos potencialmente mórbidos(40). Un estudio reciente demostró una exactitud de 83% para el PET, 60% para la TAC y 58% para la ecografía transesofágica en la estadificación ganglionar regional de estos pacientes(41).
El PET ha sido propuesto como una técnica de gran utilidad en la estadificación preoperatoria de pacientes con cáncer de colon y recto, con elevada sensibilidad para la detección de metástasis a distancia, especialmente hepáticas(39). Recientemente, se ha señalado el valor del PET en la estadificación de tumores rectales avanzados en pacientes candidatos a terapia neoadyuvante preoperatoria. En 17% de los casos se contraindicó la cirugía y en 4% se modificó la planificación de la radioterapia. El estadio tumoral fue modificado en 39% de este grupo de pacientes(42).
Reestadificación
]]> La reestadificación o estadificación en la recaída es de gran relevancia clínica ya que la reintervención quirúrgica puede curar potencialmente un porcentaje de pacientes con cáncer. En este sentido, una de las aplicaciones clínicas más claras del PET ha sido en la evaluación de pacientes con cáncer de colon y recto con incremento sucesivo del antígeno carcino-embrionario (CEA) y con negatividad de métodos de imágenes convencionales(39). Asimismo, la técnica ha resultado de gran utilidad en la evaluación de pacientes con enfermedad hepática secundaria, candidatos a resecciones curativas. Un metaanális reciente demostró una sensibilidad y especificidad media de 88% y 96%, respectivamente, para diagnóstico de enfermedad hepática y de 92% y 95% para el diagnóstico de enfermedad extrahepática, respectivamente. Estos valores resultaron ser significativamente superiores a los correspondientes a la TAC. Además, el PET permitió un cambio en el manejo clínico de pacientes en 32% de los casos(43).Varios autores han destacado el valor del PET en el seguimiento de pacientes con melanoma estadio III y IV de alto riesgo(31). En pacientes con recaídas conocidas, el PET ha demostrado sitios no sospechados de la enfermedad, posibilitando una alteración en los planes terapéuticos en hasta 20% de los casos(32). Fuster y colaboradores(44) compararon la exactitud del PET y las técnicas convencionales de imágenes para la detección de enfermedad recurrente en 156 pacientes. La sensibilidad y especificidad del PET fue de 74% y 86%, respectivamente, comparada con los respectivos valores de las técnicas convencionales: 58% y 45%. La exactitud global del PET fue de 81% comparada con 52% de las otras técnicas.
En el cáncer epidermoide de cabeza y cuello, Schmidt y colaboradores (45) demostraron la utilidad del PET en la reestadificación. La técnica presentó valores de exactitud diagnóstica de 89%, 96% y 98% para la detección de recurrencias locales, identificación de metástasis ganglionares regionales y diagnóstico de metástasis a distancia, respectivamente.
El PET ha demostrado utilidad clínica en el seguimiento de pacientes con cáncer diferenciado de tiroides con sospecha de recurrencia o metástasis, o ambas, determinada por niveles elevados de tiroglobulina sérica (mayor a 10 ng/ml) y perfilografía con radioyodo negativa(46). En efecto, en esta situación algunos autores han encontrado una sensibilidad cercana a 90%(47). Por otra parte, una revisión reciente de la literatura documentó el valor clínico de esta técnica en el diagnóstico de enfermedad recurrente o metastásica en pacientes con cáncer medular y anaplásico de tiroides, con valores de sensibilidad entre 66%-100% y de especificidad entre 79%-90%, siendo estos mayores que los correspondientes a las técnicas de imágenes convencionales(48).
En el cáncer de mama, un metaanálisis reciente ha reportado valores de sensibilidad y especificidad medias de 93% y 82%, respectivamente, para el diagnóstico de recurrencias locorregionales y metástasis a distancia(49). En este sentido, Weir y colaboradores encontraron una sensibilidad de 89% y una especificidad de 88%, para el diagnóstico de enfermedad recurrente(50). Asimismo, estos autores encontraron que 30% de las pacientes con recaída locorregional presentaban metástasis a distancia diagnosticadas por PET. Resultados similares fueron reportados por Van Oost y colaboradores(51). Por otra parte, la técnica ha demostrado utilidad en pacientes con enfermedad oculta, evidenciada solamente por la elevación de marcadores tumorales. En este contexto, se han reportado valores de sensibilidad mayor a 90%, con especificidad variable entre 73%-75%(52,53).
Al igual que en el caso anterior, los estudios PET efectuados en pacientes con cáncer de ovario han demostrado gran potencial clínico, con muy buenos resultados para el diagnóstico de enfermedad recurrente basada en la elevación de marcadores tumorales o en aquellos casos en donde las pruebas imagenológicas convencionales no son concluyentes(54,55). En un estudio reciente, Murakami y colaboradores documentaron mediante el uso combinado de PET y CA-125, una sensibilidad de 98% para el diagnóstico de enfermedad recurrente(55).
Diagnóstico de enfermedad residual
Como es sabido, un cambio en el volumen tumoral no es un indicador sensible ni específico para la evaluación correcta de la respuesta al tratamiento. La evaluación mediante PET de la naturaleza de las masas residuales postratamiento ayuda a evitar la administración de terapias citotóxicas innecesarias a pacientes con masas necróticas, y permite la indicación precoz de terapias alternativas más apropiadas en pacientes con tumores persistentes. Este es uno de los usos más promisorios del PET, siendo muy probable su transferencia a la rutina clínica asistencial en un futuro próximo(56).
En pacientes con linfoma, el principal dilema en la evaluación de la respuesta al finalizar la quimioterapia de primera línea lo constituye la presencia de masas residuales en un grupo importante de pacientes(26). Las limitaciones de las técnicas de imágenes convencionales en la caracterización de estas masas están bien documentadas(25,26). Una revisión reciente demostró que el valor predictivo negativo (VPN) del PET en pacientes con enfermedad de Hodgkin y linfomas no Hodgkin es elevado, con valores variables entre 81%-100%, mostrando así la habilidad de esta técnica para identificar pacientes de muy buen pronóstico. Sin embargo, la misma revisión demostró un valor predictivo positivo (VPP) variable entre 25% y 100%. Se ha demostrado también que el número de falsos positivos disminuye con la experiencia del observador en la evaluación de masas residuales(26).
Cerca de 25% de pacientes con seminoma pueden presentar metástasis retroperitoneales (seminomas tipo "bulky"). Si bien estas lesiones son quimiosensibles, cerca de 80% de los pacientes presentan masas residuales luego del tratamiento, detectadas mediante TAC. Además, la indicación quirúrgica es técnicamente difícil por asociarse a una reacción desmoplásica y a fibrosis. Algunos centros han decidido realizar cirugía en pacientes con masas bien delineadas, mayores de 3,0 cm, las cuales se asocian con 30%-40% de tumor residual(9,57). Recientemente, Becherer y colaboradores demostraron en un estudio prospectivo multicéntrico de evaluación de masas residuales posquimioterapia, valores de sensibilidad y especificiad de 80% y 100% para el PET y de 73% y 73% para la TAC, respectivamente. El PET resultó además excelente para excluir malignidad en lesiones mayor de 3,0 cm(58).
]]>Equipos híbridos PET-TAC ("PET-CT")
El PET es usualmente indicado conjuntamente con la TAC, la cual constituye la técnica imagenológica estándar para la mayoría de los pacientes oncológicos. El uso combinado de ambas herramientas permite aumentar la exactitud diagnóstica, presentando beneficios clínicos potenciales para el diagnóstico y la estadificación de los pacientes.
En los últimos años se han introducido con éxito equipos híbridos PET-TAC, que llevan acoplados un sistema de detectores PET y un sistema de rayos X para TAC de alta resolución. Este último componente puede ser idéntico a una TAC convencional de forma que los equipos PET-TAC modernos se encuentran disponibles con tomógrafos helicoidales de 2, 4, 8 o 16 cortes. En efecto, este sistema integrado permite adquirir en un mismo estudio una TAC diagnóstica y un estudio PET en forma secuencial, realizando una simple traslación entre los dos sistemas. De esta forma se logran imágenes que combinan la información morfológica de la TAC con la funcional que brinda el estudio PET, permitiendo evaluar al paciente oncológico mediante un único estudio.
Varios trabajos recientes han demostrado el valor incremental de los estudios PET-TAC en relación con los estudios PET. En tal sentido, la técnica híbrida ha permitido: mejorar la detección de lesiones tanto en los estudios PET como en la TAC; mejorar la localización de focos de FDG, permitiendo diferenciar la captación patológica de la fisiológica y una localización más precisa de los focos malignos. Estos beneficios han sido claramente documentados en pacientes con tumores de cabeza y cuello, con cáncer de pulmón, de esófago y con tumores abdominales y pélvicos(59,60).
Además, la información obtenida por estos equipos tienen el potencial de introducir cambios significativos en los campos de tratamiento de radioterapia. Esto puede ser logrado a través de la definición precisa de los márgenes tumorales biológicos, distinguiendo tejido tumoral viable de aquel no viable y permitiendo una modulación de la dosis suministrada al paciente(61,62). Varios estudios clínicos prospectivos han demostrado recientemente esta estrategia y su utilidad clínica(62).
Costo-beneficio
Cualquier evaluación socioeconómica de una tecnología médica costosa debe sustentarse en dos principios básicos de los servicios de salud: primero, el acceso a la atención sanitaria es un derecho de todos los ciudadanos que no debe depender de la riqueza o del salario del individuo, y, segundo, el objetivo de los servicios de salud es maximizar el impacto sobre la salud de la población con los recursos que la sociedad coloca a disposición de dichos servicios(63).
En la actualidad resulta clave analizar el valor de las técnicas en relación con los costos implícitos en prevención, diagnóstico y tratamiento de las enfermedades y en qué medida se pueden traducir en un ahorro creciente de recursos. Varios autores han demostrado que las técnicas PET correctamente indicadas resultan costo-efectivas, lográndose un ahorro significativo de recursos, variable según la enfermedad, pero en promedio de 1.397 dólares por paciente(56,64). No obstante, hay que considerar con cautela la extrapolación de estos resultados a otros sistemas de salud.
]]> El ahorro mencionado se debe fundamentalmente al uso más efectivo de otros métodos diagnósticos y terapéuticos. El ejemplo más claro es el uso racional de la cirugía exploratoria, evitando procedimientos quirúrgicos innecesarios o inapropiados a la luz de los hallazgos del PET(56).
Summary
Positron Emission Tomography (PET) is a medical nuclear technique that may prevent cancer using mechanisms to alter neoplastic process.
In this review we describe oncologic applications of PET and analyze the national sanitary and academic context where those could take place. The most used trazer in oncology is a fluor marker glucose analogue: 18F-2-fluor-2-desoxi-D-glucose (FDG). In that way, PET may detect tumor retention of FDG due to a mayor glucolitic index of cancer cells.
Also, PET tomography allows to study the entire body in the same exploration and some are coupled to a Computarized axial tomography (CAT/PET). Diagnosis and categorization of stages could be determine in 90% of patients with cancer using PET-FDG, a higher percent compared to the obtained by conventional imaging techniques. Moreover, responses to treatment and relevant prognostic information could be known in advance.
Résumé
La tomographie d’émission de positron (PET) est une technique de médecine nucléaire qui permet la détection du cancer au moyen de mécanismes basés sur les atteintes moléculaires des processus néoplasiques. Dans cette révision, on décrit les applications oncologiques du PET et on analyse l’usage potentiel de cette technologie dans le contexte sanitaire et académique national. Le traceur le plus utilisé en oncologie est un analogue de la glucose marqué avec fluor: 18F-2-fluoro-deoxy-D-glucose (FAG). C’est ainsi que le PET détecte la retenue tumorale de FDG, due à l’indice glu colitique plus élevé des cellules cancéreuses. D’ailleurs, les tomographes PET permettent l’étude de tout le corps dans la même action exploratoire et certains équipements sont assemblés au système de tomographie axiale (PET-TAC). Au moyen du PET-FDG, on peut diagnostiquer, classer et reclasser la plupart des cancers, avec une exactitude de 90% environ, supérieure aux valeurs apportées par les techniques d’imagerie conventionnelle. Par ailleurs, on peut connaître précoce-ment la réponse aux traitements oncologiques et obtenir une information pronostique relevante.
]]> Resumo
A tomografia por emissão de pósitrons (PET) é uma técnica de medicina nuclear com capacidade para detectar neoplasias por mecanismos baseados nas alterações moleculares dos processos cancerosos. Nesta revisão se descrevem as aplicações oncológicas do PET e se analisa a aplicação potencial desta tecnología no contexto sanitário e acadêmico nacional. O traçador mais utilizado em oncologia é um análogo da glicose marcado com fluor: 18F-2-fluor-2-desoxi-D-glicosa (FDG). O PET detecta a retenção tumoral de FDG devido ao índice glicolítico maior das células cancerosas. Os tomográfos PET permitem ademais, estudar todo o corpo no mesmo ato exploratório e alguns equipamentos estão acoplados a sistemas de tomografia axial computada (PET-TAC). Utilizando PET-FDG é possível diagnosticar, fazer e refazer o estadiamento a maioria dos processos cancerosos, com exatitude diagnóstica próxima ao 90%, superior aos valores obtidos com técnicas imagenológicas convencionais. Ademais é possível conhecer precocemente a resposta aos tratamentos oncológicos e obter informação prognóstica relevante.
Bibliografía
1. Lomeña JF, Simó M. Indicaciones de la tomografía por emisión de positrones. Med Clin (Barc) 2003; 120: 742-9.
2. Intercollegiate Standing Committee on Nuclear Medicine. Positron emission tomography: a strategy for provision in the UK. A report of the Intercollegiate Standing Committee on Nuclear Medicine. London: Royal College of Physicians of London, 2003: 69 p. Obtenido de: www.rcplondon.ac.uk/pubs/wp_pet.pdf (Consultado: 22 abr 2006).
3. Lenzo N. The Australian government’s review of positron emission tomography: evidence-based policy decision-making in action. Med J Aust 2004; 181: 516-7.
]]>4. Saha GB, MacIntyre WJ, Go RT. Cyclotrons and positron emission tomography radiopharmaceuticals for clinical imaging. Semin Nucl Med 1992; 22: 150-61.
5. Ho CL. Clinical PET imaging - an Asian perspective. Ann Acad Med Singapore 2004; 33: 155-65.
6. Suárez JP, Maldonado A, Domínguez ML, Serna JA, Kostvinseva O, Ordovás A, et al. La tomografía por emisión de positrones (PET) en la práctica clínica oncológica. Oncología (Barc) 2004; 27: 479-89.
7. Schillaci O, Simonetti, G. Fusion imaging in nuclear medicine-applications of dual-modality systems in oncology. Cancer Biother Radiopharm 2004; 19: 1-10.
8. Schrevens L, Lorent N, Dooms C, Vansteenkiste J. The role of PET scan in diagnosis, staging and management of non-small cell lung cancer. Oncologist 2004; 9: 633-43.
]]>9. Ruiz G, Romero C, Carreras JL. Valor de la tomográfica por emisión de positrones mediante 18F-fluoro-2-desoxi-D-glucosa (PET-FDG) en el diagnóstico de las neoplasias. Med Clin (Barc) 2005; 124: 229-36.
10. Gould MK, Sanders GD, Barnett PG, Rydzak CE, Maclean CC, McClellan. MB, et al. Cost-effectiveness of alternative management strategies for patients with solitary pulmonary nodules. Ann Intern Med 2003;138: 724-35.
11. Zimny M, Schumpelick V. Fluorodeoxyglucose positron emission tomography (FDG-PET) in the differential diagnosis of pancreatic lesions. Chirurg 2001;72: 989-94.
12. Papos M, Takacs T, Tron L, Farkas G, Ambrus E, Szakall S, et al. The possible role of F-18 FDG positron emission tomography in the differential diagnosis of focal pancreatic lesions. Clin Nucl Med 2002; 27: 197-201.
13. Diederichs CG, Staib L, Vogel J, Glasbrenner B, Glatting G, Brambs HJ, et al. Values and limitations of 18F-fluorodeoxyglucose-positron-emission tomography with preoperative evaluation of patients with pancreatic masses. Pancreas 2000; 20: 109-16.
]]>14. Sperti C, Pasquali C, Decet G, Chierichetti F, Liessi G, Pedrazzoli S. F-18-fluorodeoxyglucose positron emission tomography in differentiating malignant form benign pancreatic cysts: a prospective study. J Gastrointest Surg 2005; 9: 22-8.
15. Hienrich S, Goerres GW, Schafer M, Sagmeister M, Bauerfeind P, Pestalozzi BC, et al. Positron emission tomography/computed tomography influences on the management of respectable pancreatic cancer and its cost-effectiveness. Ann Surg 2005; 242: 235-43.
16. Jana S, Zhang T, Milstein DM, Isasi CR, Blaufox MD. FDG-PET and CT characterization of adrenal lesions in cancer patients. Eur J Nucl Med Mol Imaging 2006; 33: 29-35.
17. Metser U, Miller E, Lerman H, Lievhitz G, Avital S, Even-Sapir E. 18F-FDG PET/CT in the Evaluation of Adrenal Masses. J Nucl Med 2006; 47: 32-7.
18. Scott CL, Kudaba I, Stewart JM, Hicks RJ, Rischin D. The utility of 2-deoxy-2-[F-18] fluoro-D-glucose positron emission tomography in the investigation of patients with disseminated carcinoma of unknown primary origin. Mol Imaging Biol 2005; 7: 236-43.
]]>19. Miller FR, Hussey D, Beeram M, Eng T, McGuff HS, Otto RA. Positron emission tomography in the management of unknown primary head and neck carcinoma. Arch Otolaryn-gol Head Neck Surg 2005; 131: 626-9.
20. Gutzeit A, Antoch G, Kuhl H, Egelhof T, Fischer M, Hauth E, et al. Unknown primary tumors: detection with dual-modality PET/CT-initial experience. Radiology 2005; 234: 227-34.
21. Nanni C, Rubello D, Castelucci P, Farsad M, Franchi R, Toso S, et al. Role of 18F-FDG PET-CT imaging for the detection of an unknown primary tumour: preliminary results in 21 patients. Eur J Nucl Med Mol Imaging 2005; 32: 589-92.
22. Toloza EM, Harpole L, McCrory DC. Noninvasive staging of non-small cell lung cancer: a review of the current evidence. Chest 2003; 123(Suppl 1): 137S-146S.
23. Verhagen AF, Bootsma GP, Tjan-Heinjnen VC, van der Wilt GJ, Cox AL, Brouwer MH, et al. FDG-PET in staging lung cancer: how does it change the algorithm?. Lung Cancer 2004; 44: 175-81.
]]>24. Brink I, Schumacher T, Mix M, Ruhland S, Stoelben E, Digel W, et al. Impact of [18F]FDG-PET on the primary staging of small-cell lung cancer. Eur J Nucl Med Mol Imaging 2004; 31: 1614-20.
25. Israel O, Keidar Z, Bar-Shalom R. Positron emission tomography in the evaluation of lymphoma. Semin Nucl Med 2004; 34: 166-79.
26. Meyer RM, Ambinder RF, Stroobants S. Hodgkin’s lymphoma: evolving concepts with implications for practice. Hematology Am Soc Hematol Educ Program 2004; 184-202.
27. Isasi CR, Lu P, Blaufox MD. A metaanalysis of 18F-2-deoxy-2-fluoro-D-glucose positron emission tomography in the staging and restaging of patients with lymphoma. Cancer 2005; 104: 1066-74.
28. Stumpe KD, Urbinelli M, Steinert HC, Glanzmann C, Buck A, von Schulthess GK. Whole-body positron emission tomography using fluorodeoxyglucose for staging of lymphoma: effectiveness and comparison with computed tomography. Eur J Nucl Med 1998; 25: 721-8.
29. Freudenberg LS, Antoch G, Schutt P, Beyer T, Jentzen W, Muller SP, et al. FDG-PET/CT in re-staging of patients with lymphoma. Eur J Nucl Med Mol Imaging 2004; 31: 325-9.
30. Ruiz-Hernández G, Carreras Delgado JL, García Conde J. Tomografía por emisión de positrones en pacientes con linfoma: perspectivas futuras. Hematología 2003; 6: 133-48.
31. Kumar R, Alavi A. Clinical applications of fluorodeoxy-glucose-positron emission tomography in the management of malignant melanoma. Curr Opin Oncol 2005; 17: 154-9.
32. Schwimmer J, Essner R, Patel A, Jahan SA, Shepherd JE, Park K, et al. A review of the literature for whole-body FDG PET in the management of patients with melanoma. Q J Nucl Med 2000; 44: 153-67.
33. Klein M, Freedman N, Lotem M, Marciano R, Moshe S, Gimon Z, et al. Contribution of whole body F-18-FDG-PET and lymphoscintigraphy to the assessment of regional and distant metastases in cutaneous malignant melanoma: A pilot study. Nuklearmedizin 2000; 39: 56-61.
34. Friedman KP, Wahl RL. Clinical use of positron emission tomography in the management of cutaneous melanoma. Semin Nucl Med 2004; 34: 242-53.
35. Muylle K, Castaigne C, Flamen P. 18-F-fluoro-2-deoxy-D-glucose positron emission tomographic imaging: recent developments in head and neck cancer. Curr Opin Oncol 2005; 17: 249-53.
36. Kovacs AF, Dobert N, Gaa J, Menzel C, Bitter K. Positron emission tomography in combination with sentinel node biopsy reduces the rate of elective neck dissections in the treatment of oral and oropharyngeal cancer. J Clin Oncol 2004; 22: 3973-80.
37. Schoder H, Yeung HW. Positron emission imaging of head and neck cancer, including thyroid carcinoma. Semin Nucl Med 2004; 34: 180-97.
38. Rasanen JV, Sihvo EI, Knuuti MJ, Minn HR, Luostarinen ME, Laippala P, et al. Prospective analysis of accuracy of positron emission tomography, computed tomography, and endoscopic ultrasonography in staging of adenocarcinoma of the esophagus and the esophagogastric junction. Ann Surg Oncol 2003; 10: 954-60.
39. Hustinx R. PET imaging in assessing gastrointestinal tumors. Radiol Clin North Am 2004; 42: 1123-39.
40. Larson SM, Schoder H, Yeung H. Positron emission tomography/computerized tomography functional imaging of esophageal and colorectal cancer. Cancer J. 2004; 10: 243-50.
41. Choi JY, Lee KH, Shim YM, Lee KS, Kim JJ, Kim SE, et al. Improved detection of individual nodal involvement in squamous cell carcinoma of the esophagus by FDG PET. J Nucl Med 2000; 41: 808-15.
42. Heriot AG, Hicks RJ, Drummond EG, Keck J, Mackay J, Chen F, et al. Does positron emission tomography change management in primary rectal cancer?: A prospective assessment. Dis Colon Rectum 2004; 47: 451-8.
43. Wiering B, Krabbe PF, Jager GJ, Oyen WJ, Ruers TJ. The impact of fluor-18-deoxyglucose-positron emission tomography in the management of colorectal liver metastases. Cancer 2005; 104: 2658-70.
44. Fuster D, Chiang S, Johnson G, Schuchter LM, Zhuang H, Alavi A. Is 18F-FDG PET more accurate than standard diagnostic procedures in the detection of suspected recurrent melanoma?. J Nucl Med 2004; 45: 1323-7.
45. Schmidt M, Schmalenbach M, Jungehulsing M, Theissen P, Dietlein M, Schroder U, et al. 18F-FDG PET for detecting recurrent head and neck cancer, local lymph node involvement and distant metastases: Comparison of qualitative visual and semiquantitative analysis. Nuklearmedizin 2004; 43: 91-101.
46. Ruiz Franco-Baux JV, Borrego Dorado I, Gómez Camarero P, Rodríguez Rodríguez JR, Vázquez Albertino RJ, Navarro González E, et al. F-18-fluordeoxy-glucose positron emission tomography on patients with differentiated thyroid cancer who present elevated human serum thyroglobulin levels and negative I-131 whole body scan. Rev Esp Med Nucl 2005; 24: 5-13.
47. Palmedo H, Bucerius J, Joe A, Strunk H, Hortling N, Meyka S, et al. Integrated PET/CT in differentiated thyroid cancer: diagnostic accuracy and impact on patient management. J Nucl Med 2006; 47: 616-24.
48. Khan N, Oriuchi N, Higuchi T, Endo K. Review of fluorine-18-2-fluoro-2-deoxy-D-glucose positron emission tomography (FDG-PET) in the follow-up of medullary and anaplastic thyroid carcinomas. Cancer Control 2005; 12: 254-60.
49. Isasi CR, Moadel RM, Blaufox MD. A meta-analysis of FDG-PET for the evaluation of breast cancer recurrence and metastases. Breast Cancer Res Treat 2005; 90: 105-12.
50. Weir L, Worsley D, Bernstein V. The value of FDG positron emission tomography in the management of patients with breast cancer. Breast J 2005; 11: 204-9.
51. Van Oost FJ, Van Der Hoeven JJ, Hoekstra OS, Voogd AC, Coebergh JW, Van De Poll-Franse LV. Staging in patients with locoregionally recurrent breast cancer: current practice and prospects for positron emission tomography. Eur J Cancer 2004; 40: 1545-53.
52. Grahek D, Montravers F, Kerrou K, Aide N, Lotz JP, Talbot JN. 18 F FDG in recurrent breast cancer: diagnostic performances, clinical impact and relevance of induced changes in management. Eur J Nucl Med Mol Imaging 2004; 31: 179-88.
53. Suárez M, Pérez-Castejon MJ, Jiménez A, Domper M, Ruiz G, Montz R, et al. Early diagnosis of recurrent breast cancer with FDG-PET in patients with progressive elevation of serum tumor markers. Q J Nucl Med 2002; 46: 113-21.
54. García Velloso MJ, Boán García JF, Villar Luque LM, Aramendia Beitia JM, López García G, Richter Echeverría JA. Tomografía por emisión de positrones con F-18-FDG en el diagnóstico de recurrencia del cáncer de ovario: Comparación con TAC y CA 125. Rev Esp Med Nucl 2003; 22: 217-23.
55. Murakami M, Miyamoto T, Iida T, Tsukada H, Watanabe W, Shida M, et al. Whole-body positron emission tomography and tumor marker CA125 for detection of recurrence in epithelial ovarian cancer. Int J Gynecol Cancer 2006; 16(Suppl 1): 99-107.
56. Juweid ME, Cheson BD. Positron-emission tomography and assessment of cancer therapy. N Engl J Med 2006; 354: 496-507.
57. Quek ML, Simma-Chiang V, Stein JP, Pinski J, Quinn DI, Skinner DG. Postchemotherapy residual masses in advanced seminoma; current management and outcomes. Expert Rev Anticancer Ther 2005; 5: 869-74.
58. Becherer A, De Santis M, Karanikas G, Szabo M, Bokemeyer C, Dohmen BM, et al. FDG PET is superior to CT in the prediction of viable tumour in post-chemotherapy seminoma residuals. Eur J Radiol 2005; 54: 284-8.
59. Messa C, Bettinardi V, Picchio M, Pelosi E, Landoni C, Gianolli L, et al. PET/CT in diagnostic oncology. Q J Nucl Med Mol Imaging 2004; 48: 66-75.
60. Coleman RE, Delbeke D, Guiberteau MJ, Conti PS, Royal HD, Weinreb JC, et al. Concurrent PET/CT with an integrated imaging system: intersociety dialogue from the joint working group of the American College of Radiology, the Society of Nuclear Medicine, and the Society of Computed Body Tomography and Magnetic Resonance. J Nucl Med 2005; 46: 1225-39.
61. Messa C, Di Muzio N, Picchio M, Gilardi MC, Bettinardi V, Fazio F. PET/CT and radiotherapy. Q J Nucl Med Mol Imaging 2006; 50: 4-14.
62. Ell PJ. The contribution of PET/CT to improved patient management. Br J Radiol 2006; 79: 32-6.
63. Guerrero Pupo JC, Amell Muñoz I, Cañedo Andalia R. Tecnología, tecnología médica y tecnología de la salud: algunas consideraciones básicas. Acimed 2004; 12(4). Obtenido en: http://scielo.sld.cu/scielo.php?pid=1024-943520040004& script=sci_issuetoc (Consultado: 22 abr 2006).
64. González P, Massardo T, Canessa J, Humeres P, Jofre MJ. Clinical application of positron emission tomography (PET). Rev Med Chile 2002; 130 (5): 569-79. Obtenido de: http://www.scielo.cl/scielo.php?pid=0034-988720020005& script=sci_issuetoc (Consultado: 22 abr 2006).