Beretta Andrés1, Bassahum Daniel1, Musselli Raquel1
1INIA La Estanzuela, Laboratorio de Suelos, Plantas y Aguas. Ruta 50 km 11, 70.000 Colonia, Uruguay
Correo electrónico: aberetta@inia.org.uy
Recibido: 9/10/13 Aceptado: 10/9/14
]]> Resumen
En la determinación del pH en suelo hay que considerar el tiempo de lectura y si realizar las medidas en reposo o agitando la mezcla suelo:agua . Este estudio comparó la medición de pH en el sobrenadante de la mezcla suelo:agua (1:2,5) luego de 15 minutos de reposo, con la alternativa de medir durante la agitación y en menor tiempo. Los procedimientos de medición de pH fueron: i) 3 minutos de agitación + 15 minutos de reposo y medición en el sobrenadante sin agitar (protocolo del laboratorio de INIA La Estanzuela); ii) lo mismo con medición en agitación de la mezcla durante 1, 2 y 3 minutos luego del reposo; iii) medición con agitación de la mezcla durante 1, 2 y 3 minutos sin reposo previo. Los valores de pH durante la agitación inicial fueron superiores a los del sobrenadante luego del reposo. Estas diferencias disminuyeron de 5,38 % a 3,91 % con tres minutos de agitación. No hubo diferencias en el valor de pH a los tres minutos de agitación con o sin reposo previo de 15 minutos. Las lecturas durante la agitación inicial de tres minutos, con tres repeticiones por muestra, presentaron un CV= 1,41 %. Medir el pH a los tres minutos de agitación sería una medición precisa y con una exactitud aceptable.
Palabras clave: TIEMPO DE REPOSO, SOBRENADANTE, pHMETRO
Summary
Measure Soil pH at Rest or Stirring the Soil:water Mixture?
For soil pH measurement is necessary consider the reading time and read during stirring the mix soil:water or read in repose. We compared the measurement of pH in the supernatant from the soil mix: water (1:2.5) after 15 minutes rest or stirring sample and measure at less time. The procedures for pH measure were: i) stirred during 3 minutes + 15 minutes of rest and measuring in supernatant without stirring; ii) after stirring the mixture for 1, 2 and 3 minutes after 3 minutes of stirring + 15 minutes rest; iii) during the stirring of the mixture for 1, 2 and 3 minutes without rest. The higher soil pH values were obtained during initial stirring. These differences decreased from 5.38 % to 3.91 % after three minutes of stirring. There were no differences in pH values after three minutes of stirring with or without previous rest. There was no effect of 15 minutes rest. Measurement of soil pH at the end of the initial two minutes of stirring, with three repetitions, showed a CV = 1.41 %. The soil pH measurement at the end of three minutes of stirring the soil:water mixture would be acceptable.
Introducción
En la medición de pH utilizando electrodo de actividad específica hay varios factores a considerar: la relación suelo:agua, la fuerza iónica en la solución, la posición del electrodo en la suspensión, y agitado o reposo de la muestra durante la medición (Conyers y Davey, 1988; Miller y Kissel, 2010). Thomas (1996) indica que al hacer las mediciones de pH en agua, hay diferencias entre medir en el suelo decantado, en el sobrenadante o durante la agitación de la muestra, pero lo importante es reportar los resultados habiendo realizado las mediciones con el mismo criterio.
Al colocar el electrodo en el sedimento, los valores de pH son generalmente inferiores a los del sobrenadante, debido a la capacidad de intercambio catiónico y la fuerza iónica generada por los cationes en solución (Coleman y Thomas, 1967; McLean, 1982; Kalra y Maynard, 1991). Las mediciones de pH pueden realizarse luego de la sedimentación de las arenas, mientras las arcillas están en suspensión o en el filtrado del suelo (Schofield y Taylor, 1955). Algunos autores recomiendan leer el pH en el líquido sobrenadante (Kalra y Maynard, 1991; Little, 1992; Sumner, 1994; Hendeshot et al., 2008). Eckert y Sims (2009), por el contrario, recomiendan leer el pH en el sedimento y advierten que hay que tener cuidado de no colocar el electrodo en el sobrenadante. Sumner (1994), advierte que se cometen grandes errores de medición al leer el pH durante la agitación, ya que esta práctica logra mayor precisión en los resultados pero perjudica la exactitud. Tisdale y Nelson (1975) recomiendan colocar el electrodo en el sedimento, con el fin de disminuir el efecto salino de la solución y realizar las mediciones durante la agitación suave de la mezcla. Van Lierop (1990) recomienda hacer las mediciones de pH durante la agitación de la muestra en el caso de suelos alcalinos, con lo que se lograría mayor rapidez y exactitud en la medición. En el caso de suelos ligeramente ácidos no es necesario agitar y la mezcla suelo:agua debe dejarse decantar 15 a 30 minutos antes de realizar la medición en el sedimento.
El tiempo de equilibrio de la mezcla suelo:agua antes de la medición puede afectar los valores medidos de pH. Conyers y Davey (1988) recomiendan no exceder las 24 horas para no provocar solubilización de sales que puedan interferir en el potencial iónico y recomienda un período de equilibrio cercano a una hora. Little (1992) recomienda agitar durante una hora la mezcla suelo:agua y luego dejar reposar 20 minutos antes de la medición. Schofield y Taylor (1955) recomiendan 15 minutos de equilibrio. Kalra y Maynard (1991) y Eckert y Sims (2009) recomiendan 30 minutos de reposo. McLean (1982), al leer el pH en una relación suelo:agua de 1:1, recomienda leer durante la agitación de la mezcla, posteriormente a un reposo de 10 minutos.
El objetivo de este trabajo fue comparar la medición de pH en reposo, según el protocolo del laboratorio del INIA La Estanzuela, con la alternativa de medir durante la agitación de la muestra y un menor tiempo de equilibrio suelo:agua.
]]>Materiales y métodos
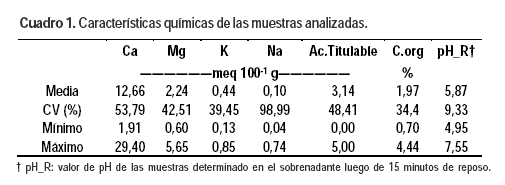
Se utilizaron 53 muestras de suelos, cuyas características se resumen en el Cuadro 1. Las muestras fueron previamente secadas a 40 °C durante 48 h y molidas hasta pasar por malla de 2 mm. A estas muestras se les midió el pH acorde al protocolo realizado por INIA La Estanzuela, sugerido por Capurro et al. en «Técnicas empleadas en análisis de rutina en el laboratorio del proyecto suelos-mayo 1978» (no publicado) y por Gavlak et al. (2003). Para esto se pesaron 20 g de suelo y se les agregó 50 mL de agua desionizada. La mezcla suelo:agua se agitó durante tres minutos y se dejó reposar 15 minutos. El pH se midió en el sobrenadante sin agitar (pH_R). A 31 de estas mismas muestras, posteriormente a la agitación de 3 minutos + 15 minutos de reposo, se les midió el pH mientras se las agitó durante 1 minuto (pH_RA1min), 2 minutos (pH_RA2min) y 3 minutos (pH_RA3min). En 35 muestras se midió el pH durante la agitación de la mezcla desde el minuto 1 (pH_A1min), minuto 2 (pH_A2min) y minuto 3 (pH_A3min).

Las mediciones se realizaron con pHmetro combinado con cuerpo de epoxy (Thermo Sientific_9165NWP). La calibración del equipo se realizó con soluciones buffer de pH 7 y 4, acorde a lo indicado por el fabricante.
Los valores entre mediciones se compararon por análisis de regresión y por medias apareadas, para tener una idea de la exactitud de la medición mientras se agita la muestra. En los análisis de regresión se consideró la variable x como la medición pH_R y como variable y las diferentes alternativas propuestas. La precisión de medir el pH mientras se agita la muestra se evaluó mediante el coeficiente de variación obtenido en las mediciones pH_A3min en 21 muestras de suelos que se midieron por triplicado.
]]>Resultados y discusión
El promedio de los valores de pH_A1min, pH_A2min y pH_A3min superaró los valores promedio de pH_R en 0,27, 0,24 y 0,16 respectivamente, acorde a la comparación de medias apareadas. Los modelos de regresión ajustados para las tres técnicas poseen coeficiente b menor a uno, pero el coeficiente a fue mayor a cero, lo que agregó un valor constante a las mediciones durante la agitación de las muestras (Cuadro 2). Esta tendencia no concuerda con los menores valores esperados según lo expuesto por Smiley y Coock (1972), Tisdale y Nelson (1975) o Thomas (1996), que sugieren que los coloides en suspensión provocan un descenso de pH respecto a la medición en el sobrenadante.

Durante la agitación de la muestra por pocos minutos (uno a tres) puede que no se haya alcanzado el equilibrio químico entre el suelo y el agua, ya que las diferencias fueron significativamente menores a mayor tiempo de agitado. Varios autores recomiendan valores de contacto del suelo con el agua de 15 minutos o superiores, para alcanzar un equilibrio en la reacción de la mezcla (Schofield y Taylor, 1955; McLean, 1982; Kalra y Maynard, 1991; Little, 1992; Eckert y Sims, 2009).
Durante la agitación de la muestra luego del reposo de 15 minutos, sin embargo, los valores de pH también fueron mayores a los leídos en el sobrenadante durante el reposo. Los valores promedio de pH_RA1min, pH_RA2min y pH_RA3min, superaron en 0,18, 0,14 y 0,14 respectivamente los valores de pH_R. No hubo diferencias entre pH_A1min y pH_RA1min, entre pH_A2min y pH_RA2min o entre pH_A3min y pH_RA3min. Las diferencias entre pH_A1min y pH_RA3min y entre pH_A2min y pH_RA3min se pudieron deber a que en uno o dos minutos de agitación no se alcanzó un equilibrio en la mezcla suelo:agua y la membrana del electrodo.
]]> Estas diferencias no se deberían a problemas de tiempo de equilibrio de la mezcla suelo:agua. Las diferencias entre las lecturas pH_A1min, pH_A2min, pH_A3min y pH_R se pudieron deber, por lo tanto, a que la membrana del electrodo demoró en alcanzar un equilibrio con la mezcla y/o a que el electrodo se posicionó muy cerca de la superficie del suelo y la solución sobrenadante en las lecturas en reposo. Con 15 minutos de reposo, además, no se alcanzó un sobrenadante sin partículas en suspensión, lo cual según Conyers y Davey (1988) podría provocar valores de pH inferiores a los esperables si el sobrenadante no tuviese estas partículas. Al colocarse la membrana cercana a la superficie del suelo decantado se podría estar midiendo valores de pH inferiores a los reales, debido al efecto salino (Smiley y Coock, 1972; Sumner, 1994).Las diferencias entre los valores pH_A1min, pH_A2min, pH_A3min y pH_R disminuyeron al aumentar los valores de pH_R, r= -0,49, r= -0,47 y r= -0,44 respectivamente (Figura 1). Esta tendencia pudo deberse a que a valores bajos de pH los suelos presentan menos cationes de intercambio, ya que los valores de pH_R tuvieron un coeficiente de correlación de 0,77 con la suma de total de bases. El menor contenido de bases pudo generar mayores diferencias entre el supernadante y el sedimento. Las diferencias relativas entre estas mediciones descendieron con el aumento de tiempo de agitación, de un valor absoluto promedio de 5,38 %, 4,37 % y 3,91 % al medir en el primer, segundo o tercer minuto de agitación respectivamente. Al dejar reposar la muestra durante 15 minutos y luego leer el pH durante la agitación, las diferencias relativas no se correlacionaron con los valores de pH_R (Figura 2). La magnitud absoluta de estas diferencias promedió 3,11 %, 2,75 % y 2,68 % según las lecturas hayan sido realizadas durante la agitación de uno, dos o tres minutos respectivamente. El descenso observado solo fue significativo entre la agitación de uno y dos minutos. Las diferencias relativas generadas por la lectura pH_A3min respecto a las mediciones pH_R, no difirieron de las generadas por las lecturas pH_RA3min, por lo que no hubo efecto del reposo de 15 minutos al medir el pH agitando la mezcla suelo:agua.
Las mediciones pH_A3min tuvieron un coeficiente de variación de 1,04 % (n=63, el máximo valor observado fue de 1,33 % (n=3). El coeficiente de variación de las mediciones en reposo de las diferentes muestras de control utilizadas por nuestro laboratorio ha sido de 1,3 a 6,3 % (n=3), mientras que si consideramos una base de 79 mediciones logramos descender el coeficiente de variación de las muestras control a 1,4 %. Kalra y Maynard (1991) sugieren que las mediciones de pH (1:2 suelo:agua) deben poseer una precisión de al menos cinco por ciento. El orden de magnitud de los coeficientes de variación aquí determinados concuerda con los aceptados por Kalra (1995).
]]> Conclusión
La medición pH_A3min tendría una precisión y una exactitud aceptables. Las diferencias encontradas entre estas mediciones y las de pH_R no introducirían errores significativos al interpretar los resultados. Medir el pH al cabo de los tres primeros minutos de agitación de la muestra permite realizar el análisis en menor tiempo con un resultado aceptable.
Agradecimientos
Al equipo de trabajo del Laboratorio de Suelos, Plantas y Aguas de INIA La Estanzuela.
Bibliografía
Coleman NT, Thomas GW. 1967. The basic chemistry of soil acidity. En: Pearson RW, Adams F. [Eds]. Soil acidity and liming. vol. 12. Wisconsin : American Society of Agronomy. pp. 1-41.
Conyers MK, Davey BG. 1988. Observations on some routine methods for soil pH determination. Soil Science, 145: 29-36.
Eckert D, Sims JT. 2009. Recommended soil pH and lime requirement test. En: Recommended Soil Testing Procedures for the Northeastern United States. Newark : Agricultural Experiment Stations of Connecticut. (Northeastern Regional Publication ; 493). pp. 16-21.
Gavlak RG, Horneck DA, Miller RO, Kotuby-Amacher J. 2003. Soil pH and Electrical Conductivity. En: Soil, Plant and Water Reference Methods for the Western Region. 2nd ed. Colorado : Colorado State University. (WCC-103 Publication). pp. 37-47.
Hendershot WH, Lalande H, Duquette M. 2008. Soil reaction and exchangeable acidity. En: Carter MR, Gregorich EG. [Eds.]. Soil Sampling and Methods of Analysis. 2nd ed. Boca Raton: CRC Press. pp. 173-178.
Kalra Y. 1995. Determination of pH of Soil by Different Methods : Collaborative Study. Journal of AOAC International, 78(2): 310-324.
Kalra YP, Maynard DG. 1991. Methods manual for forest soil and plant analysis. Edmonton, Alberta: Forest Canadian, Northwest Region, Northern Forestry Centre. 116p.
Little IP. 1992. The Relationship between Soil pH Measurements in Calcium Chloride and Water Suspensions. Australian Journal Soil Research, 30: 587-592.
McLean EO. 1982. Soil pH and lime requirement. En: Page AL, Miller RH, Keeney DR. [Eds]. Methods of soil analysis: Part 2 Chemical and microbiological properties. 2nd ed. Madison: American Society of Agronomy. (Agronomy Monograph ; 9). pp. 199-223.
Miller RO, Kissel DE. 2010. Comparision of soil pH methods on soils of North America. Soil Science of America, 74(1): 310-316.
Schofield RK, Taylo AW. 1955. The measurement of soil pH. Soil Science Society American Proceedings, 19: 164-167.
Smiley RW, Coock RJ. 1972. Use and Abuse of the Soil pH Measurement. Phytopathology, 62(1): 192-194 .
Sumner ME. 1994. Measurement of soil pH: Problems and solutions. Communication in Soil Science and Plant Analysis, 25: 859-879.
Thomas GW. 1996. Soil pH and soil acidity. En: Sparks DL. [Ed]. Methods of soil analysis: Part 3 Chemical methods. Madison: Soil Science Society of America. (Soil Science Society of America Book ; 5). pp. 475- 490.
Tisdale S, Nelson W. 1975. Soil Fertility and Fertilizers. 3rd ed. New York: Macmillan. 694p.
Van Lierop W. 1990. Soil pH and lime requirement determination. En: Westerman RL. [Ed]. Soil testing and plant analysis. 3rd ed. Madison: Soil Science Society of America. (Soil Science Society of America Book ; 3). pp. 73 - 126.
]]>