Episodios adversos a medicamentos, detectados en dos servicios de internación pediátrica del Centro Hospitalario Pereira Rossell
DRAS. STELLA GUTIéRREZ 1, MARIZEL REPETTO 2
1. Profesora Adjunta de Clínica Pediátrica. Ex Profesora Adjunta del Departamento de Farmacología y Terapéutica.
2. Ex Profesora Adjunta de Clínica Pediátrica
Clínicas Pediátricas “A” y “B” y Departamento de Farmacología y Terapéutica de la Facultad de Medicina
Fecha recibido: 12 de julio 2004
Fecha aprobado: 28 de diciembre 2004
Los episodios adversos son consecuencia inevitable del tratamiento farmacológico. Abarcan tanto las reacciones adversas a medicamentos como los daños causados por errores en la prescripción, dispensación y administración de medicamentos.
Objetivo: describir los episodios adversos diagnosticados en dos servicios de internación pediátrica del Centro Hospitalario Pereira Rossell (CHPR).
Metodología: se realizó un estudio descriptivo con los niños hospitalizados en las Clínicas Pediátricas A y B del CHPR en los años 2000 y 2001. Se registraron los episodios adversos producidos durante la internación en ficha precodificada a tales efectos. Se determinó el número total de efectos producidos y los medicamentos involucrados.
Resultados: se detectaron 70 episodios adversos a 69 medicamentos en 67 niños que representaron un 0,8% del total de niños ingresados en ese período. De ellos 21 fueron reacciones predecibles y 49 no predecibles. Dentro de las primeras se identificaron 10 por sobredosis, cuatro por efectos secundarios y siete por efectos colaterales. Dentro de las segundas, 49 por hipersensibilidad. Los medicamentos más involucrados fueron los antibióticos seguidos de los anticonvulsivantes. No se registraron casos fatales y pocos revistieron gravedad potencial.
Conclusión: los episodios adversos se detectaron en forma frecuente, en particular para antibióticos y anticonvulsivantes. Su notificación y evaluación deben formar parte de la práctica médica habitual para mejorar la calidad de asistencia y brindar la máxima seguridad al paciente. La educación en este sentido a nivel de programas del currículo médico de pre y posgrado mejorará el número total de registros y la calidad de los informes.
Palabras clave: TOXICIDAD DE MEDICAMENTOS
NIñO HOSPITALIZADO
Summary
Adverse events are an inevitable consequence of pharmacologic treatment.They involve either adverse reactions to drugs or any harmful result of their prescription, dispensation or administration. ]]>
Objective: to assess adverse events diagnosed in 2 pediatric services from Pereira Rossell Hospital Center.
Methods: a descriptive study was realized with children admitted in pediatric clinics “A” and “B” both 2000 and 2001. Adverse events taken place during hospitalization were registered in a precoded form.All adverse events and drugs involved were registered.
Results: 70 adverse events were detected to 69 drugs in 67 children which represents 0,8% of hospitalized children during that period: 21 were predictable adverse reactions and 49 were impredictable adverse reactions. From the predictable ones,10 were the result of overdosage, 4 secondary effects and 7 colateral effects. From the impredictable ones, 49 of hypersensibility. The group of drugs most frequently involved were antibiotics and after anticonvulsivants.There were no fatal cases and few were particulary severe.
Conclusion: adverse events in hospitalized patients were frequently detected particulary for antibiotics and anticonvulsants drugs. Their notification and evaluation must be part of the daily medical practice to improve assistance and give the safe option to the patient. Education in this field for pre and post graduated will increase number and quality of the reports.
Key words: DRUG TOXICITY
HOSPITALIZED CHILD
Introducción
Las reacciones adversas son tan antiguas como la misma historia pero la identificación de problemas de seguridad relacionados con los medicamentos comienza a fines del siglo XIX (1,2).
Según la OMS, el efecto adverso es un efecto nocivo no intencional que ocurre cuando un medicamento se utiliza en el hombre a dosis normalmente empleadas con fines profilácticos, diagnósticos o terapéuticos (3). Esta definición excluye el error como fuente de efectos adversos y las reacciones a contaminantes y constituyentes inactivos.
]]> Las reacciones adversas se definen como la consecuencia no deseada de la administración de un fármaco durante un ciclo terapéutico o después del mismo (4). Se trata de una reacción perjudicial o no deseable ocasionada por el uso de un producto medicinal que exige tratamiento específico o modificación del régimen de dosificación o suspensión del producto y que puede reiterarse en caso de futura administración.Si bien los términos efecto adverso y reacción adversa son intercambiables, el efecto se refiere al medicamento y la reacción al paciente.
El evento o acontecimiento o episodio adverso es un resultado adverso que ocurre en el curso de un tratamiento farmacológico pero donde no existe necesariamente una relación de causalidad con el fármaco (5-7).
Para atribuir a un medicamento la aparición de un efecto adverso debe existir una relación de causalidad (8). La clínica de las reacciones adversas es extraordinariamente polimorfa ya que pueden simular cualquier enfermedad conocida, modificar el curso de una enfermedad o incluso dar lugar a patologías anteriormente no descritas (9).
Las reacciones adversas son consecuencia inevitable del tratamiento farmacológico. Su notificación, registro, análisis y evaluación sistemática constituyen la farmacovigilancia que comienza una vez que el medicamento se encuentra en fase 4 (disponibilidad en el mercado, uso librado a grandes poblaciones). Comprende un conjunto de métodos que tiene por objeto la identificación, evaluación cuantitativa del riesgo y la valoración cualitativa clínica de los efectos del uso agudo o crónico de los medicamentos en el conjunto de la población o subgrupos específicos de ella (5). Permite, no solamente la detección de reacciones adversas ya conocidas, sino también la detección de aquellas que no han sido aún identificadas por su baja frecuencia, antes del registro del medicamento en cuestión.
La notificación espontánea de reacciones adversas a los medicamentos es un sistema de seguridad para limitar la toxicidad de los productos farmacéuticos comercializados. La Food and Drug Administration (FDA) estima que el 90% de los efectos adversos serios o fatales no son reportados (10).
En pediatría, los eventos adversos se observan en 4,7 a 16,8% de los niños hospitalizados en salas de internación (11,12), pudiendo aumentar hasta 30% en unidades de terapia intensiva. Abarcan tanto reacciones adversas a medicamentos como daños causados por errores en la prescripción, la dispensación y la administración de medicamentos en el proceso de monitoreo de la respuesta terapéutica.
En 1991, Rawlins y Thompson clasificaron las reacciones adversas en dos categorías: predecibles y no predecibles (13). Las primeras constituyen el 80% de todos los efectos adversos, dependen de la dosis y se relacionan con la acción farmacológica conocida del producto. Pueden predecirse a partir del conocimiento de las acciones farmacológicas del fármaco implicado. Comprenden los efectos tóxicos por sobredosis, los efectos colaterales (efecto no buscado, facultativo, pero inherente a la propia acción farmacológica del medicamento), los efectos secundarios (no relacionados con su acción farmacológica primaria, consecuencia indirecta, obligatoria de la acción de un medicamento) y los producidos por interacciones medicamentosas. Las segundas se presentan en una población susceptible. No dependen de la dosis ni guardan relación alguna con la acción farmacológica del producto. En su desarrollo los factores genéticos y ambientales son importantes. Comprenden los efectos idiosincráticos (respuesta cualitativamente anormal, no inmunológica, que no se espera se produzca según la acción farmacológica conocida del producto) y por hipersensibilidad (reacción cualitativamente anormal inesperada mediada por una reacción inmune).
Objetivo
Describir los episodios adversos diagnosticados durante los años 2000 y 2001 en dos servicios de Internación Pediátrica del Centro Hospitalario Pereira Rossell (CHPR).
]]> MétodosSe realizó un estudio descriptivo que incluyó todos los niños hospitalizados en las Clínicas Pediátricas A y B del CHPR en los años 2000 y 2001.
Se registraron los episodios adversos producidos durante la internación. Se recogieron los siguientes datos: edad del niño, peso, descripción del efecto adverso y evolución del mismo, medicamento sospechado en la reacción adversa y medicamentos administrados simultáneamente. Se envió copia de la ficha al Centro Nacional de Farmacovigilancia nº 61 de la Organización Mundial de la Salud (OMS) con el fin de indexar los casos clínicos y realizar una correcta imputabilidad de los mismos según los códigos establecidos por el Centro Mundial de Uppsala, Suecia.
Se determinó el número total de efectos producidos, el tipo de reacción (predecible o no predecible) y los medicamentos involucrados.
Se describen brevemente algunos de los casos.
Resultados y comentarios
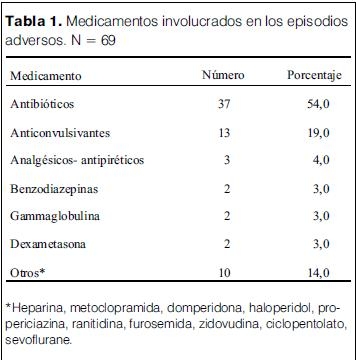
Durante los años 2000 y 2001 se detectaron 70 episodios adversos a 69 medicamentos en 67 niños hospitalizados en las Clínicas Pediátricas “A” y “B” del Hospital Pediátrico del CHPR (tabla 1). Estos niños representan el 0,8 % del total de egresos de dichas clínicas en el mismo período *.
* Datos obtenidos del informe anual de las Clínicas Pediátricas A y B, presentado y aprobado por el Consejo de la Facultad de Medicina.
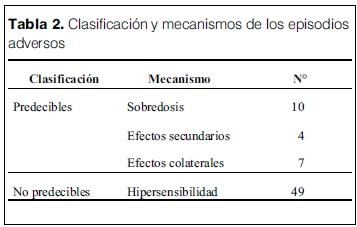
]]> Los episodios adversos detectados se clasificaron en predecibles (n=21) y no predecibles (n=49). Sus mecanismos se muestran en la tabla 2.
Los medicamentos involucrados en los episodios adversos predecibles se muestran en la tabla 3.
A continuación se describen y comentan los episodios adversos agrupados por su mecanismo.
Sobredosis
1. Niña de 7 años portadora de encefalopatía con epilepsia en tratamiento con fenobarbital que consulta por depresión neuropsíquica. Fenobarbitalemia de 146 µg/ml. La intoxicación por fenobarbital se produjo por error en una farmacia que expendió comprimidos de 100 mg en vez de 15 mg. A las 48 horas de suspendida la medicación y luego de recibir suero bicarbonatado 1/6 molar i/v, la fenobarbitalemia bajó a 55 µg/ml. A los cinco días, con fenobarbitalemia de 13 µg/ml, se reinició el tratamiento. La alcalinización de la orina aumenta el grado de ionización del fenobarbital por lo que disminuye la reabsorción tubular y aumenta su excreción urinaria. La relación entre concentración plasmática de fenobarbital y efectos adversos varía según el grado de desarrollo de tolerancia de cada individuo. Para una misma sobredosis, la intoxicación será mejor tolerada en el individuo con tratamiento crónico que en aquel que no ha podido aún desarrollar tolerancia (14).
2. Niño de 2 años, epiléptico en tratamiento con fenobarbital. Ingresa por aumento de convulsiones, con fenobarbitalemia en rango terapéutico. Recibe fenitoína intravenosa, dosis carga de 20 mg/kg seguida de una dosis de mantenimiento de 10 mg/kg cada 12 horas. Al segundo día presenta ataxia, tendencia al sueño, nistagmo horizontal, hipotonía, dismetría y telebradiquinesia una hora después de recibir la tercera dosis. La concentración plasmática en ese momento fue de 44 µg/ml.
3. Adolescente de 14 años, epiléptica en tratamiento con ácido valproico desde hace dos años. Ingresa por cefalea, vómitos y convulsiones tonicoclónicas reiteradas. Tomografía de cráneo y estudio del LCR normales. La dosificación plasmática de ácido valproico fue de 136 µg/ml. Se suspendió este medicamento y se realizó tratamiento con fenitoína intravenosa para yugular las convulsiones. La desaparición de los síntomas ocurrió a las 24 horas de suspendido el fármaco. No quedó claro la causa de la intoxicación.
]]> 4. Niño de 2 años epiléptico, tratado con fenobarbital al cual se agrega clobazam a la dosis de 5 mg/cada 12 horas. Doce días después ingresa por depresión neuropsíquica, ataxia e hipotonía. La dosificación plasmática de benzodiazepinas fue de 140,6 µg/ml y la de fenobarbital de 22 µg/ml. A las 24 horas de suspendido el clobazam mejoró la sintomatología.5. Niña de 5 años, monorrena, que ingresa a la unidad de cuidados intensivos por crisis de asma severa requiriendo asistencia ventilatoria mecánica por 11 días. Durante ese período recibió midazolam para sedación a 0,6 mg/kg. Al quinto día de suspendida la medicación comienza con mutismo, llanto incontrolado, alucinaciones, hipotonía generalizada, marcha inestable e hiporreflexia que duraron 20 días, con desaparición gradual de la sintomatología. La concentración plasmática de benzodiazepinas a los 11 días de haber finalizado el tratamiento era de 45 ng/ml y a los 20 días, ya asintomática, de 35 ng/ml. Dos tipos de reacciones se presentan en este caso, una por sobredosis y otra, el síndrome de abstinencia, ya descrito en algunos reportes luego del tratamiento con este fármaco (14). Si bien el midazolam se metaboliza en el hígado, su principal metabolito, el 1-hidroximetilmidazolam de igual acción farmacológica, pero menos activo, se excreta por vía renal. Es una benzodiazepina de vida media corta pero su clearance puede disminuir en caso de administración intravenosa prolongada particularmente en el menor de 3 años. La azoemia y creatininemia en este caso eran normales.
6. Niño de 3 años, peso 16 kg, que recibe metoclopramida 40 gotas (5,2 mg) cada 12 horas por vómitos. Una hora después de recibir la tercera dosis presenta crisis oculógiras con lateralización de cuello. Fue tratado con difenhidramina intravenosa, antihistamínico H1 de acción sedante y efectos antimuscarínicos. Su administración reduce la frecuencia de reacciones distónicas extrapiramidales. La metoclopramida es un antagonista de los receptores dopaminérgicos pudiendo ocasionar síntomas extrapiramidales, sobre todo en niños, adolescentes y ancianos. La mayoría de las distonías se asocian con dosis mayores a las recomendadas, siendo la dosis habitual de 0,1 a 0,2 mg/kg/dosis cada 6 horas.
7. Niño de 2 años cursando gastroenteritis que recibe domperidona 1 gota/kg (500 µg/kg) cada 6 horas. Al tercer día, agrega somnolencia, lateralización de cuello e hipertonía a predominio de miembros superiores por lo que ingresa. Recibe hidratación intravenosa, difenhidramina y se suspende la domperidona. Presenta buena evolución. La domperidona es un antagonista dopaminérgico al igual que la metoclopramida, cuya penetración a través de la barrera hematoencefálica es menos rápida y de menor entidad. La dosis pediátrica es de 200 a 400 µg/kg de peso cada 6 a 8 horas.
8 y 9. Adolescente de 14 años que comienza a recibir haloperidol 5 mg cada 6 horas por agitación secundaria a lesión encefálica por accidente de tránsito. A la tercera dosis presenta episodio de distonía aguda que cede con la administración de difenhidramina intravenosa. A las 24 horas de suspendido el haloperidol, se inicia propericiazina (10 mg/día), un segundo neuroléptico con acción más sedante que el haloperidol. Instala hipertonía de cuatro miembros con fenómeno de rueda dentada, por lo que se agrega biperideno, antimuscarínico útil para los efectos extrapiramidales de las fenotiazinas. La vida media plasmática del haloperidol es de 12 a 38 horas por lo que probablemente se sumó la acción de ambas drogas. Las reacciones distónicas de los neurolépticos predominan en el niño y adolescente. La dosis de haloperidol aconsejada para niños es de 25 a 50 µg/kg/día en dos dosis.
10. Niña de 6 años en hemodiálisis desde hace 7 meses por insuficiencia renal crónica, que presenta, 5 horas luego de la diálisis, petequias y equímosis generalizadas. Se realizaron los siguientes exámenes: KPTT incoagulable, tiempo de protrombina 10%, fibrinógeno 125 mg/dl y recuento plaquetario 311.000 elementos/mm3. Con diagnóstico de intoxicación por heparina, recibe una transfusión de plasma fresco, 1 ml de sulfato de protamina y vitamina K intravenosa 10 mg, con desaparición de la signología. La heparina a altas dosis aumenta la tasa de reacción entre trombina y antitrombina e inhibe los factores de las vías intrínseca y común como el IXa, Xa, XIa, XIIa y calicreína por lo que se altera el KPTT, el tiempo de protrombina y la agregabilidad plaquetaria.
La mayoría de las sobredosis aquí constatadas fueron de causa iatrogénica, resultado de un tratamiento médico.
Efectos secundarios
1. Adolescente de 13 años con pansinusitis rápidamente progresiva. Comienza con vancomicina intravenosa 500 mg cada 6 horas a pasar en una hora. Al final de la primera dosis, erupción máculoeritematosa generalizada que luego desaparece espontáneamente. En las próximas dosis, la duración de la infusión fue de 90 minutos sin reiterar el efecto. La administración rápida de vancomicina produce liberación de histamina dando el síndrome del “hombre rojo”. Este efecto se evita administrando la misma en infusión de 5 mg/ml en un plazo de 60 minutos para dosis de 500 mg o de 100 minutos para dosis de 1 g. El síndrome de hombre rojo puede ir acompañado de hipotensión arterial (15).
2. Niño de 7 años hospitalizado por neumonía con dolor epigástrico. Interpretado como probable gastritis, recibe ranitidina intravenosa. A los cinco minutos de la administración instala mareos, palidez y náuseas de 30 minutos de duración. Este fármaco es capaz de desencadenar a nivel cardiovascular bradicardia y bloqueo auriculoventricular en pacientes susceptibles, particularmente cuando se lo administra por vía parenteral.
]]> 3. Niño de 3 años con convulsiones febriles reiteradas en tratamiento con fenobarbital desde hace tres meses. Ingresa por nueva convulsión febril. Durante el interrogatorio se constata hiperactividad que la madre nota desde hace un mes. Se decide la suspensión gradual del fármaco.El fenobarbital produce reacciones paradojales tanto en el anciano como en el niño con irritabilidad e hiperactividad.
4. Recién nacido de 5 días, hijo de madre VIH positiva, que ingresa por vómitos reiterados luego de la administración oral de zidovudine 2 mg/kg cada 6 horas. Se disminuye la dosis a 1,5 mg/kg con buena tolerancia. Los efectos adversos más frecuentes de este antiretroviral son anemia y vómitos. Son efectos dosis dependientes y reversibles.
Efectos colaterales
1. Niño de 3 años con diagnóstico de gastritis en tratamiento con antiácidos desde hace 2 meses. Cursa hace 3 días gastroenterocolitis recibiendo ibuprofeno como antipirético. Ingresa por episodio de hematemesis. La endoscopía muestra múltiples lesiones erosivas a nivel del cuerpo gástrico.
2 y 3. Niños de 2 y 5 años tratados con ampicilina intravenosa por neumonía con empiema y calmados con ibuprofeno cada 6 horas. Desde el inicio, dolor epigástrico que cede al cambiar a paracetamol.
La inhibición no selectiva de la ciclooxigenasa, en particular la COX1, por fármacos analgésicos-antipiréticos-antiinflamatorios no esteroideos se vincula con los efectos gastrointestinales al desaparecer la acción citoprotectora de las prostaglandinas en la mucosa gastrointestinal. Sin embargo, no todos estos fármacos presentan el mismo riesgo de lesión gastrointestinal. La dipirona y el paracetamol presentan menor riesgo, en cambio el ibuprofeno a dosis analgésicas tiene riesgo leve, aumentando el mismo a dosis antiinflamatorias
4. Niño de 1 año portador de ductus arterioso persistente con repercusión hemodinámica que inicia su tratamiento con furosemida a 1 mg/kg dosis cada 8 horas y captopril. Al 10º día de tratamiento presenta deshidratación. En ese momento no presentaba vómitos ni deposiciones anormales. Luego de rehidratado, se disminuyó la dosis a 1 mg/kg/día con buena evolución posterior.
5. Lactante de 2 meses cursando segunda infección respiratoria baja grave, en tratamiento con salbutamol y dexametasona desde hace 12 días. Se constata edema de párpados y miembros. Desaparece a los tres días de suspendida la dexametasona.
6. Lactante de 9 meses cursando laringotraqueobronquitis grave. Recibe dexametasona intravenosa por 15 días. En los controles se comprueba cifras tensionales elevadas en varias oportunidades. Se comienza con furosemide y se suspende la dexametasona pasando a prednisolona que se disminuye gradualmente. A los 10 días se suspende el furosemide.
]]> La dexametasona es un glucocorticoide de gran potencia antiinflamatoria y escaso efecto mineralocorticoideo. Su vida media biológica es prolongada de 36 a 72 horas por lo que sólo debe utilizarse en tratamientos cortos. A pesar del escaso efecto mineralocorticoide, en estos niños determinó retención de agua y sodio provocando edemas e hipertensión arterial.Dentro del grupo de reacciones adversas no predecibles se identificaron 49 por hipersensibilidad (tabla 2), 36 de las cuales correspondieron a antibióticos (dos niños con dos reacciones de hipersensibilidad cada uno) (tabla 4).
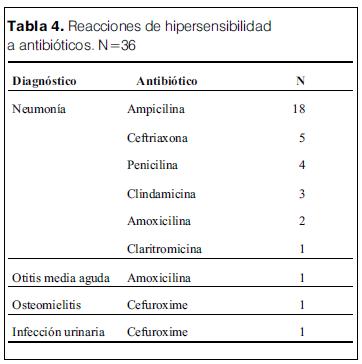
Las reacciones de hipersensibilidad a antibióticos son secundarias al propio fármaco o a sus metabolitos. Pueden clasificarse según el tiempo que media entre el antibiótico y el inicio de los síntomas en inmediatas (antes de la hora de haber sido administrado): aceleradas (1 a 72 horas luego de la administración) y tardías (luego de las 72 horas) (16).
Reacciones inmediatas: un niño epiléptico de 6 años en tratamiento con fenobarbital, vigabatrin y carbamazepina, hospitalizado por neumonía, presentó, a los minutos de su primera dosis de penicilina, erupción máculopapulosa generalizada y edema angioneurótico siendo trasladado a la unidad de cuidados intensivos donde agregó insuficiencia renal aguda y toque hepatocítico. Posteriormente presentó buena evolución. El término anafilaxia describe una reacción inmediata de tipo I, mediada por IgE, en un individuo previamente sensibilizado. El niño había recibido en varias oportunidades amoxicilina sin ningún efecto adverso.
Reacciones aceleradas: se registraron nueve. Ocho presentaron rash máculopapuloso generalizado y uno urticaria. Uno de los niños presentó además angioedema y sibilancias. La reacción duró entre dos y tres días. Todos fueron tratados con clorfeniramina y cambio de antibiótico dentro de la misma familia de betalactámicos.
Reacciones tardías: se registraron 22, todos con rash máculopapuloso. Un niño presentó, además de la erupción descrita, petequias generalizadas con recuento plaquetario normal, interpretadas como vasculitis; un niño presentó fiebre simultáneamente con la erupción. La aparición de las reacciones tardías tuvo una mediana de 10 días luego del inicio del antibiótico con un rango entre 3 a 20 días; su duración presentó una mediana entre 2 y 3 días.
Cinco niños presentaron fiebre por antibióticos a clindamicina, ampicilina, penicilina, ceftriaxona. La fiebre apareció con una mediana de 13 días del inicio del tratamiento (rango entre seis y 20) y duró tres días (rango entre dos y seis).
Las reacciones tardías de hipersensibilidad corresponden a los tipos II, III y IV de la clasificación de Gell y Coombs. Sin embargo, los rash máculopapulosos obedecen en la mayoría de los casos a reacciones idiopáticas cuyo mecanismo inmunológico subyacente es desconocido (17).
]]> La fiebre por antibióticos puede alcanzar temperaturas altas, ser continua, remitente o intermitente y acompañarse de chuchos. La reacción febril suele desaparecer entre las 24 y 36 horas de concluir la administración del fármaco pero puede persistir durante varios días (14). Es una reacción humoral en la que se forma un complejo Ag-Ac (reacción tipo III de Gell y Coombs) en respuesta al medicamento o a sus metabolitos. Se produce liberación de pirógenos endógenos desde los leucocitos, que llevan a la aparición de la fiebre (18).Las reacciones de hipersensibilidad son los efectos adversos más comunes de los betaláctamicos y en orden aproximado de frecuencia decreciente las manifestaciones de alergia incluyen erupción maculopapulosa, urticaria, fiebre y broncoespasmo con una incidencia entre 0,7 y 10%. La ampicilina es el más frecuentemente involucrado (14).
Ocho niños presentaron las siguientes reacciones de hipersensibilidad a los anticonvulsivantes:
a) Hepatitis
1. Niño de 3 años, epiléptico, tratado con fenobarbital y vigabatrin al cual se le agrega ácido valproico por persistencia de convulsiones. Al mes reingresa por persistencia de convulsiones. Se solicita funcional hepático de control que muestra: bilirrubina total 1,73 mg/dl, bilirrubina directa 1,06, TGO 90,4 U/L, TGP 79,7 U/L y Colinesterasa 194. Se suspende el ácido valproico. A los 20 días, el funcional hepático muestra: bilirrubina total 0,79, bilirrubina directa 0,45, TGO 47 U/L y TGP 61 U/L.
2. Niño de 8 años, con epilepsia secundaria a contusión cerebral tratado con carbamazepina. A los 20 días se solicita hemograma y funcional hepático de control que muestran: leucocitosis 4.000 elementos/mm3, TGO 84 U/L y TGP 72 U/L. Continúa con carbamazepina con exámenes normales a los 20 días.
3. Adolescente de 13 años, epiléptica tratada con fenitoína desde hace 6 años y carbamazepina desde hace 1 mes. Se solicita hemograma de control normal y funcional hepático que muestra: TGO 78 y TGP 88 U/L. A los 20 días, el funcional hepático era normal continuando con la medicación.
El ácido valproico en monoterapia puede ocasionar aumento gradual y asintomático de transaminasas en los primeros meses de tratamiento. La hepatitis fatal no es precedida por anomalías de la función hepática y se asocia con politerapia, edad menor de 2 años y encefalopatía previa (1,19).
La carbamazepina puede producir anomalías hepáticas, en particular aumento de transaminasas, en 5 a 10% de los casos y leucopenia y trombocitopenia en 10% al inicio del tratamiento, que desaparece en los primeros meses y no requiere la suspensión de la misma.
b) Síndrome de Stevens-Johnson
]]> Adolescente de 13 años tratado con fluoxetina y alprazolam desde hace un año por depresión que ingresa por alteración del humor. Se le agrega carbamazepina. Reingresa al mes por erupción generalizada, irritación conjuntival y lesiones de boca. Se diagnostica síndrome de Stevens-Johnson y se suspende la carbamazepina.El síndrome de Stevens-Johnson es una reacción cutánea extensa, generalizada, con lesiones en diana que se necrosan formando vesículas y ampollas con afectación de dos o más mucosas. Las lesiones de piel no son muy dolorosas. Las lesiones oculares (ulceración corneal, uveítis anterior) pueden dejar secuelas. La mortalidad es del 5%.
c) Síndrome de hipersensibilidad
1. Niño de 8 años con diagnóstico de epilepsia inicia tratamiento con fenitoína. A los 15 días comienza con fiebre diaria sin foco clínico evidente y a los 20 días agrega erupción máculopapuloeritematosa e irritación conjuntival por lo que ingresa. Al examen se constatan adenopatías mayores de 1 cm en todos los territorios. Se realiza hemograma que muestra glóbulos blancos 3.700 elementos/mm3, con glóbulos rojos y plaquetas normales. Se suspende la fenitoína. La fiebre desaparece a los 13 días; a los 20 días las adenopatías disminuyen de tamaño y mejora la irritación conjuntival. Se otorga el alta con persistencia de la erupción, que desaparece totalmente al mes.
2. Niño de 11 años con diagnóstico de epilepsia, que inicia tratamiento con carbamazepina. A los 10 días comienza con fiebre y adenopatías generalizadas, por lo que ingresa. No se suspende la medicación. Agrega a los 10 días erupción máculopapuloeritematosa, lesiones de boca y ano. El hemograma es normal y el funcional hepático muestra aumento de transaminasas. Se suspende la carbamazepina comenzando la mejoría progresiva a los 13 días.
3. Niño de 7 años, epiléptico que inicia tratamiento con fenitoína. Comienza a los 3 días con fiebre alta, adenopatías generalizadas y erupción máculopapuloeritematosa por lo que ingresa. El recuento leucocitario era de 4.300 elementos/mm3, con resto de las series normales. Se suspende la fenitoína con mejoría y desaparición de la erupción a la semana. Se agrega carbamazepina durante la internación. A las 48 horas vuelve a instalar la erupción agregando compromiso de boca y aumento del tamaño de las adenopatías. El hemograma muestra recuento leucocitario de 3.100 elementos/mm3. Se suspende la carbamazepina. El cuadro retrocede totalmente a los 20 días.
El síndrome de hipersensibilidad a fármacos se define por la presencia de reacción cutánea acompañada de fiebre (ambas presentes en 87% de los casos), aumento de transaminasas de severidad variable (51% de los casos), linfadenopatías(75%), anomalías hematológicas (30%), nefritis intersticial (11%). Se produce entre 7 y 28 días del inicio del tratamiento pudiendo aparecer hasta 3 meses después del inicio del mismo (1). En caso de reexposición, la reacción puede aparecer en uno a dos días. Su incidencia va entre 1/1000 y 1/10.000. Los familiares de primera línea son más propensos a presentar esta reacción cuando reciben estos anticonvulsivantes. La reactividad cruzada entre fenobarbital, fenitoína y carbamazepina es del 75%. Su presencia exige la suspensión inmediata del fármaco. La mortalidad es del 10% (20).
d) Eritema multiforme
Niña de 9 años, epiléptica, que inicia tratamiento con fenitoína. A los 16 días ingresa por eritema máculopapuloeritematoso generalizado a predominio de miembros superiores e inferiores que comenzó dos días antes. Algunas lesiones presentan centro purpúrico. Mucosas normales. Hemograma y funcional hepático normales.
El eritema multiforme se define como una reacción cutánea de inicio agudo, simétrica, caracterizada por máculas eritematosas, pápulas, vesículas, ampollas o placas de aspecto urticariano que predominan en la cara extensora de miembros superiores. La lesión típica es en diana caracterizada por un halo eritematoso con un centro purpúrico. A veces se acompaña de lesiones bucales pero las demás mucosas están respetadas. Es más frecuente luego de infecciones que de fármacos. Su curso es benigno.
]]> Se observaron las siguientes reacciones de hipersensibilidad a otros medicamentos:1. Lactante de 2 meses que ingresa por convulsión en apirexia. Se le administra ciclopentolato en gotas oftálmicas como midriático para realizar el fondo de ojo. A la hora comienza con edema de párpados, rash facial y erupción eritematomicropapulosa en tronco. Recibe clorfeniramina intravenosa cada cuatro horas con desaparición de la reacción en 8 horas. La administración de este anticolinérgico no se recomienda en el lactante tierno. Su toxicidad sistémica ha sido notificada en varias oportunidades con aparición de taquicardia, náuseas y lagrimeo.
2. Niña de 1 año con diagnóstico de empiema paraneumónico que ingresa a block quirúrgico para colocación de drenaje de tórax. En el acto intraoperatorio, mientras recibe sevoflurano, anestésico general inhalatorio, comienza con erupción que rápidamente se generaliza y síndrome canalicular obstructivo. Recibe antihistamínicos, corticoides, salbutamol y aminofilina con buena evolución.
3 y 4. Dos niños de 5 años, ingresados con diagnóstico de púrpura trombocitopénico autoinmune recibieron 1 g/kg dosis de gammaglobulina intravenosa. A la hora y a las dos horas respectivamente del inicio de la infusión comienzan con fiebre, que desciende con ibuprofeno vía oral en un caso y dipirona intravenosa en el segundo. Los efectos adversos de la gammaglobulina intravenosa son habitualmente leves y agudos. Incluyen eritema facial, naúseas, vómitos, sudoración, cefalea y fiebre. La suspensión o enlentecimiento de la infusión por 15 a 30 minutos lleva a la desaparición de los síntomas luego de lo cual la gammaglobulina es readministrada (20).
Más de un mecanismo inmunopatológico puede estar involucrado en una reacción clínica. El riesgo de hipersensibilidad se incrementa con factores genéticos, enfermedades concurrentes (mononucleosis infecciosa, inmunodeficiencias), vía y dosis del fármaco (la vía parenteral y dosis elevadas), edad (mayor riesgo entre 20 a 40 años) y antecedentes de reacciones adversas (4 a 6 veces mayor si tuvo reacción alérgica previa)
Conclusiones
Los episodios adversos a medicamentos en sala de internación se detectaron en forma frecuente, en particular para antibióticos y anticonvulsivantes. Predominaron los efectos no predecibles a diferencia de lo que ocurre habitualmente (7). Este fenómeno puede estar relacionado al servicio médico quirúrgico para tratamiento de niños con empiema, los cuales reciben antibioticoterapia prolongada.
No se registró ningún caso de muerte y pocos revistieron gravedad potencial.
La notificación de los efectos adversos y la evaluación de los mismos deben formar parte de la práctica médica habitual con el objetivo de mejorar la calidad de asistencia y brindar la máxima seguridad al paciente.
La educación en este sentido mejorará el registro del número total de efectos notificados y la calidad de los informes. En base a ello, es fundamental incluir esta metodología en programas del currículum médico de pre y posgrado (2).
]]> AgradecimientosA las profesoras Ana María Ferrari y Carolina Seade por su invalorable ayuda en la redacción y comentarios de este artículo.
Bibliografía
1. Routledge P. 150 years of pharmacovigilance. Lancet 1998; 351: 1200-1.
2. Feely J, Williams D. Detección de reacciones adversas a los medicamentos: primera parte. Adverse Drug Reaction Bulletin. Carta Médica. Supl. de Noticias oct 2002 nº 117: 54-7.
3. World Health Organization. International Drug Monitoring. World Health Organization. Tech. Rep. 425, 1969.
4. Sly SM. Reacciones adversas a fármacos. En: Behrman RE, Kliegman RM, Jenson HB. Nelson Tratado de Pediatría. 16 ed. Madrid: Mc Graw-Hill, 2000: 754-8.
5. Edwards I R, Aronson JK. Adverse Drugs Reactions: definitions,diagnosis and management. Lancet 2000; 356: 1255-9.
6. Bates DW, Cullen DJ, Laird N, Petersen L, Small S, Servi D, et al. Incidence of Adverse Drug Events and Potential Adverse Drug Events. JAMA 1995; 274: 29-34.
7. Laporte JR. Principios básicos de investigación clínica, 2ºed. Barcelona: Comunicación en Ciencias de la Salud, 2001.
8. Laporte JR, Capellà D. Mecanismos de producción y diagnóstico clínico de los efectos indeseables producidos por medicamentos. En: Principios de epidemiología del medicamento. 2ºed. Barcelona: Masson-Salvat, 1993: 95-102.
9. Laporte JR. Reacciones adversas a medicamentos y fármacovigilancia. Med Clin (Barc) 1989; 92: 536-8.
10. Moore T, Weiss S, Kaplan S, Blaisdell C. Reported Adverse Drug Events in Infants and Children Under 2 Years of Age [artículo en línea]. Pediatrics 2002; 110(5).
http://www.pediatrics.org/cgi/content/full/110/5/e53 /[consulta,22 marzo 2003].
11. Weiss J, Krebs S, Hoffmann C, Werner U, Neubert A, Brune K et al. Survey of Adverse Drug Reactions on a Pediatric Ward: A Strategy for Early and Detailed Detection. Pediatrics 2002; 110: 254-7.
12. Rylance G, Armstrong D. Episodios adversos causados por medicamentos en los niños. Adverse Drug Reaction Bulletin.Carta Médica. Supl. de Noticias may 1998 nº 92: 62-4.
13. Rawlins M, Thompson W, Davies D. Mechanisms of adverse drug reactions. En: .Textbook of adverse drug reactions,1ºed. New York: Oxford University Press, 1991: 18-45.
]]>14. McNamara J. Fármacos eficaces para el tratamiento de las epilepsias. En: Hardman J, Limbird L, Molinoff P, Ruddon R, Goodman A. Goodman & Gilman. Las Bases Farmacológicas de la Terapéutica. 9ºed. México: Interamericana McGraw-Hill, 1996: 491-519.
15. Martindale.The Complete Drug Reference. 33th Ed Pharmaceutical Press. London-Chicago, 2002.
16. Boguniewicz M and Leung D. Hypersensitivity reactions to antibiotics commonly used in children. Pediatr Infect Dis J 1995; 14: 221-31.
17. Salkind A, Cuddy P, Foxworth J. Is this patient allergic to penicillin? JAMA 2001; 285: 2498-505.
18. Hanson M. Drug fever. Postgraduate Medicine 1991; 89(5): 167-8.
]]>19. Armijo Simón JA, Herranz Fernández J L. Fármacos antiepilépticos. Medicine 1998; 7(99): 4605-16.
20. Griebel M. Acute Management of Hypersensitivity Reactions and Seizures. Epilepsia 1998; 39(Suppl 7): S17-21.
21. Patel J, Ogra P. Antiviral chemotherapy. En: Pediatric Pharmacology. Therapeutic Principles in Practice. 2ºed. Philadelphia: WB Saunders, 1992: 377-8.
Correspondencia: Dra. Stella Gutiérrez ]]>
Bvar Artigas 2524/101 - CP 11600. Montevideo, Uruguay.
E-mail: maressol@chasque.apc.org