ARTÍCULO DE REVISIÓN
Exposición al humo de tabaco y trombosis
DR. PABLO ASADURIAN 1
1. Ex Profesor Adjunto de Cardiología, Ex Profesor Adjunto de Medicina. Miembro del Grupo CLATH (Grupo Latinoamericano de Trombosis y Hemostasis).
PALABRAS CLAVE:
TABAQUISMO
CONTAMINACIÓN POR HUMO DE TABACO
FACTORES DE RIESGO ]]>
TROMBOSIS
KEY WORDS:
SMOKING
TOBACCO SMOKE POLUTTION
RISK FACTORS
THROMBOSIS
El tabaquismo es un factor de riesgo principal de aterosclerosis y de trombosis arterial aguda, asimismo existe evidencia que permite vincularlo con el riesgo de trombosis venosa. Se estima que aproximadamente 1,6 millones de personas al año mueren de causa cardiovascular vinculada al tabaco, constituyendo 22% de las muertes de EEUU. El riesgo de muerte del fumador respecto al no fumador se sitúa entre 1,65 y 2 (1,2).
Ya en 1973 aparecieron artículos en revistas internacionales en los cuales se planteaba el efecto protrombótico arterial y el desarrollo de aterosclerosis debido al tabaquismo (3). Actualmente 40% de las muertes vinculadas al tabaco son de causa cardiovascular (4).
La exposición al humo del cigarrillo favorece la trombosis por diversos mecanismos tanto a nivel de la pared vascular como a nivel de la sangre. A nivel vascular debemos mencionar la disfunción endotelial, el daño oxidativo sobre las mitocondrias de los miocitos, la proliferación de células musculares lisas. A nivel sanguíneo, la hiperagregabilidad plaquetaria, la disminución de la expresión del inhibidor del factor tisular, el aumento de los niveles de fibrinógeno y el aumento de la viscosidad sanguínea (5-7).
]]> A continuación analizaremos con mayor detalle estos mecanismos, para abordar luego algunos aspectos clínicos de la relación entre tabaco y enfermedades tromboembólicas.1. MECANISMOS DE LA HIPERTROMBICIDAD VINCULADA AL TABAQUISMO
DISFUNCIóN ENDOTELIAL
El endotelio vascular pasó de ser considerado un simple epitelio con función de barrera a transformarse en uno de los órganos más importantes, al que se le reconocen funciones dirigidas a mantener la estabilidad de la hemostasis, junto a propiedades vasodilatadoras y antitrombóticas. Sus funciones vasodilatadoras disminuyen las resistencias vasculares periféricas y mejoran las condiciones del flujo sanguíneo. Su superficie, para un individuo de 70 kg, es de aproximadamente 2.000 a 4.000 m2, equivalente a más de dos canchas de tenis, con un peso entre 1 kg y 3 kg (8).
El endotelio se regenera a punto de partida de progenitores endoteliales circulantes, los que son derivados de la médula ósea. El tabaquismo disminuye los progenitores circulantes, por lo que reduce la capacidad de regeneración del endotelio, mientras que la cesación produce un repunte de estos progenitores.
El endotelio sano elabora sustancias vasoactivas, vasodilatadoras como el óxido nítrico (ON), prostaciclinas y péptido natriurético, entre otras, aumentando el diámetro vascular y reduciendo la resistencia al flujo. Cuando el endotelio se enferma, disminuyen las sustancias protectoras, aumentan la endotelina y el tromboxano, elevando las resistencias vasculares, lo que facilita el desarrollo y progresión de la aterosclerosis y de la cardiopatía isquémica.
Otra función endotelial influenciada por el tabaco es la angiogénesis. La nicotina del humo de tabaco promueve la neovascularización, lo que determina un crecimiento tumoral mayor entre los fumadores que en los no fumadores, a la vez que promueve el crecimiento de la placa aterosclerótica a expensas del desarrollo de microvasos en la vasa vasorum de la misma. Algo similar ocurre en la retina, produciendo neovascularización que lleva al deterioro visual más acelerado de los fumadores respecto a los no fumadores.
En suma, la exposición al humo de tabaco produce disfunción endotelial, promueve la inflamación, proliferación celular y trombosis, lo que redunda en mayor progresión aterosclerótica.
EFECTOS SOBRE LAS PLAQUETAS
]]> El turnover plaquetario se acelera en fumadores y la trombosis se asocia más con la producción de plaquetas reticuladas que con el aumento del número absoluto de las mismas. La excreción urinaria de metabolitos del tromboxano (2,3 dinor tromboxano B2 y 11-dehydro tromboxano B2) son marcadores de activación plaquetaria in vivo, que en pacientes fumadores se incrementan de un modo dosis dependiente. Por este motivo el humo del tabaco produce activación plaquetaria y mayor respuesta de las mismas al shear stress (9).La cesación del tabaquismo se asocia a un descenso rápido de los niveles de metabolitos del tromboxano en orina, lo que se observa a los pocos días de la misma, aunque no llegue a niveles de no fumadores.
En estudios de laboratorio, la agregación plaquetaria es mayor en fumadores (10). Asimismo, la reducción en la agregabilidad plaquetaria, luego de 14 días de abstinencia, se revierte rápidamente al volver a fumar. Los niveles de metabolitos de tromboxano en orina hablan de activación plaquetaria, el uso de bajas dosis de ácido acetilsalicílico reduce la eliminación de los mismos en orina vía bloqueo de la COX 1.
Aunque derivado de las plaquetas, el óxido nítrico (ON) es un inhibidor moderado de la activación plaquetaria in vitro, el que además reduce el reclutamiento de plaquetas al trombo en crecimiento. La producción de ON por parte de las plaquetas de pacientes con síndrome coronario agudo es menor que la de pacientes con angina crónica, y es menor en fumadores que en no fumadores (10). Este hallazgo se acompaña de una reducción de los niveles de glutatión-a intraplaquetrio, marcador de estrés oxidativo y de incremento de la agregabilidad plaquetaria. Los niveles de ON y glutatión-a se recuperan al tiempo de abandonar el cigarrillo, pero caen rápido al restituir el tabaco (11). La sensibilidad plaquetaria al ON en fumadores está disminuida en horas de la mañana, momento en que el infarto de miocardio es más frecuente (12).
El humo del cigarrillo contiene abundantes radicales libres, lo que incrementa el estrés oxidativo que puede medirse in vivo por el aumento de los niveles de isoprostanos, los que disminuyen con la cesación tabáquica. Takajo y colaboradores (9) demostraron niveles elevados de isoprostanos y bajos de glutatión en plaquetas de fumadores. Gorlach y colaboradores en el año 2000 demostraron activación plaquetaria inducida por estrés oxidativo de células del músculo liso vascular, asociado a aumentos de la expresión de factor tisular. El isoprostano IPF2a-III disminuye la actividad del ON plaquetario, y algunos investigadores especulan que tiene un papel importante en el desarrollo de resistencia al ácido acetilsalicílico en pacientes con cardiopatía isquémica.
EFECTOS SOBRE LA HEMOSTASIS
La exposición aguda al humo de cigarrillo produce aumento de los niveles plasmáticos del factor tisular (13), lo que sugiere que aumentan los biomarcadores protrombóticos, estimulando en forma directa la trombosis. Además acelera la producción de fibrina, lo que ha sido determinado mediante tromboelastograma. En este contexto la red de fibrina tiene una estructura diferente, más densa y con fibras más finas que son más resistentes a la fibrinólisis. Se cree que en la base de este proceso se halla la modificación funcional que produce el humo del tabaco sobre el fibrinógeno, mediado por efecto de los radicales libres que regulan a la baja a los antioxidantes endógenos.
La anormalidad en la formación, estructura y estabilidad de la fibrina producida por la exposición aguda al humo de tabaco ha sido descrita en algunas disfibrinogenemias, lo que sugiere un mecanismo similar.
Las moléculas de adhesión S VCAM y SICAM aumentan en los fumadores. Estas moléculas evidencian la existencia de actividad inflamatoria a nivel endotelial y son responsables de acelerar la ateroinflamación (8).
Los fumadores cursan con niveles elevados de factores Von Willebrand y tisular; este último activa la cascada de la coagulación, mientras que el primero favorece la adhesión plaquetaria a la pared del vaso.
]]> Entre los fumadores existe reducción de la respuesta fibrinolítica con disminución de la lisis espontánea del trombo, lo que obedece a que el activador tisular del plasminógeno (tPA) está disminuido, al tiempo que se produce un aumento del inhibidor del activador tisular del plasminógeno (PAI-1). Al interferir con las funciones del tPA y del PAI-1 se produce una disminución de la actividad fibrinolítica, los que se asocia con eventos cardiovasculares (13).ELEMENTOS FORMES DE LA SANGRE Y ACTIVIDAD INFLAMATORIA
Otros efectos en los elementos formes de sangre favorecen condiciones de hipertrombicidad. El tabaquismo aumenta el hematocrito, la masa globular y la viscosidad sanguínea en relación con los niveles de monóxido de carbono y carboxihemoglobina. Con el abandono del tabaquismo, el hematocrito puede disminuir, pero la viscosidad y deformación globular pueden persistir. La hiperviscosidad parece incrementar más el riesgo de stroke que el de infarto de miocardio, aun luego de ajustarlo para otros factores como hipertensión arterial y dislipemia (14). También se observan efectos sobre el hematocrito de hijos de madres que fuman más de 20 cigarrillos/día durante el embarazo, con incremento del índice de hipoxemia fetal, policitemia y complicaciones neurológicas, comparado con hijos de madres no fumadoras.
El humo del cigarrillo también actúa en los polimorfonucleares, aumentando las mieloperoxidasas, incrementa la expresión de integrinas CD11b, CD15 y CD63, marcadores de activación leucocitaria. Esto, junto a la elevación de las moléculas de adhesión ICAM-1, VCAM, P-selectina y E-selectina evidencian la actividad inflamatoria.
A nivel de los monocitos aumenta la expresión de integrinas CD11b y CD18, incrementando la adhesividad a células endoteliales, lo que favorece su pasaje al subendotelio y la diferenciación a macrófago promoviendo la aterogénesis.
El fibrinógeno aumenta en fumadores, disminuyendo tras el abandono del hábito. El aumento del fibrinógeno se correlaciona directamente con enfermedad coronaria (15) e incrementa la incidencia de trombosis venosa (16).
En fumadores aumentan los niveles de proteína C reactiva (PCR) respecto a no fumadores, este aumento es dosis dependiente y se correlaciona con actividad inflamatoria crónica y aterogénesis (17). El aumento de la actividad inflamatoria se mantuvo incluso con el ajuste de otros factores de riesgo como perfil lipídico, diabetes, enfermedad cardiovascular, edad, sexo y raza. Recién después de cinco años de abandono del tabaco los niveles de PCR llegan a niveles similares al de los no fumadores.
2. ASPECTOS CLÍNICOS
INFARTO AGUDO DE MIOCARDIO Y MUERTE SúBITA
]]> El infarto agudo de miocardio (IAM) ocurre a edades más tempranas en los fumadores que en los no fumadores. A su vez, los fumadores que se presentan con IAM tienen menos factores de riesgo cardiovascular, menor cantidad y severidad de lesiones coronarias y mejores resultados en la terapia de reperfusión por fibrinólisis que los no fumadores.El humo del cigarrillo aumenta el riesgo de muerte súbita en mayor medida que el de angina. Esto parece explicarse porque la angina depende más de un fenómeno hemodinámico, mientras que la muerte súbita depende más de la trombosis. La muerte súbita es 2,5 veces más frecuente en fumadores que en no fumadores (18). Entre los individuos fallecidos por muerte súbita en los que se demostró trombosis la incidencia de tabaquismo fue de 75%, mientras que cuando la misma estuvo vinculada a un accidente de placa, la presencia de tabaquismo era de 41%.
Dado que los fumadores desarrollan el IAM con menor carga aterogénica que los no fumadores, en ellos tienen un papel más relevante las alteraciones de la coagulación de la sangre.
TROMBOSIS VENOSA
La tríada descrita por Virchow en 1856 y modificada por Aschoff en 1924, consistente en alteraciones de la coagulación de la sangre, alteraciones del flujo con estasis y alteración de la pared vascular, sigue teniendo vigencia como predisponente para la trombosis venosa.
La evidencia que vincula el tabaco con la trombosis venosa es menos consistente que su contraparte arterial. Sin embargo el estudio MEGA, que compara 3.989 pacientes con enfermedad tromboembólica venosa con 4.900 sanos, concluye que el fumar tiene un riesgo relativo (RR) de trombosis venosa de 1,43; IC 95% 1,28-1,60. El mismo se incrementa mucho en mujeres jóvenes fumadoras que reciben anticonceptivos orales (RR de 8,8), comparado con mujeres no fumadoras que no toman anticonceptivos. El riesgo de este grupo de mujeres es mayor que el de las que padecen trombofilia (19).
El tabaco parece aumentar el riesgo de enfermedad tromboembólica venosa en el análisis del registro nacional danés, que comprendió 27.178 hombres y 29.875 mujeres entre 50 y 64 años de edad, con un seguimiento a diez años. Hubo 617 eventos tromboembólicos, de los cuales 58% eran trombosis venosas profundas y 42% embolia pulmonar (20). Luego de ajustar el riesgo por otras variables, como consumo de alcohol, índice de masa corporal, sedentarismo y terapia de reemplazo hormonal, las mujeres fumadoras tuvieron 52% más de eventos que las no fumadoras y los hombres fumadores tuvieron 32% más de riesgo. Los ex fumadores tenían el mismo riesgo que los no fumadores, lo que sugiere que la exposición al humo del cigarro promueve trombosis.
En el estudio de las nurses norteamericanas, las fumadoras de más de 35 cigarrillos/día tuvieron doble riesgo de hipertensión pulmonar que las mujeres no fumadoras (21). El estudio de los hombres nacidos en 1913, mostró que el riesgo de enfermedad tromboembólica venosa se triplicó en fumadores de más de 15 cigarrillos/día, algo que no se verificó en el estudio Framingham analizando las autopsias (22).
3. EXPOSICIÓN AL HUMO AMBIENTAL Y TROMBOSIS
]]> En lo que respecta a los fumadores de segunda mano, los niveles de fibrinógeno y factor VII de la coagulación de hijos de padres fumadores fueron mayores que en hijos de padres no fumadores (23), lo que evidencia un estado protrombótico. También se demostraron niveles de PAI-1 menores en hijos de fumadores, lo que sugiere disminución de la fibrinólisis.Los niveles de trombomodulina (factor de efecto antitrombótico producida por el endotelio vascular) es menor en hijos de fumadores, lo que evidencia actividad protrombótica. No hubo diferencias en los niveles de factor de von Willebrand. Además, los metabolitos de tromboxano urinario aumentan en hijos de fumadores, alcanzando niveles similares al de los fumadores luego de una exposición de seis horas. Por lo tanto, muchos efectos del tabaquismo activo también se ven en los individuos expuestos involuntariamente al humo del cigarrillo.
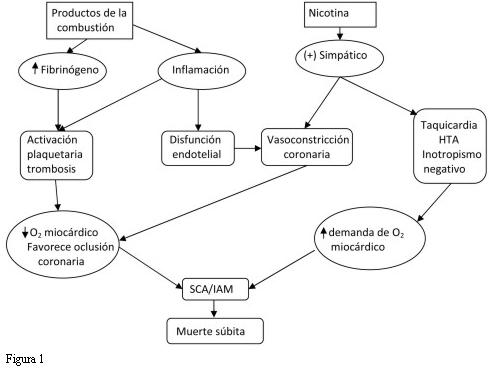
En la figura 1 se resumen los efectos del tabaco sobre la trombosis.
BIBLIOGRAFíA
1. Dagenais GR, Yi Q, Lonn E, Sleight P, Ostergren J, Yusuf S; HOPE Trial Investigators. Impact of cigarette smoking in high-risk patients participating in a clinical trial. A substudy from the Heart Outcomes Prevention Evaluation (HOPE) trial. Eur J Cardiovasc Prev Rehabil 2005; 12: 75-81.
]]>2. Thun MJ, Day-Lally CA, Calle EE, Flanders WD, Heath CW. Excess mortality among cigarette smokers: changes in a 20-year interval. Am J Public Health 1995; 85: 1223-30.
3. Levine PH. An acute effect of cigarette smoking on platelet function: a possible link between smoking and arterial thrombosis. Circulation 1973; 48: 619-23.
4. Campbell RA, Machlus KR, Wolberg AS. Smoking out the cause of thrombosis. Arterioscler Thromb Vasc Biol 2010; 30: 7-8.
5. Armani C, Landini L Jr, Leone A. Molecular and biochemical changes of the cardiovascular system due to smoking exposure. Curr Pharm Des 2009; 15: 1038-53.
6. Schroeter MR, Sawalich M, Humboldt T, Leifheit M, Meurrens K, Berges A, et al. Cigarette smoke exposure promotes arterial thrombosis and vessel remodeling after vascular injury in apolipoprotein E-deficient mice. J Vasc Res 2008; 45: 480-92.
]]> 7. Barua RS, Ambrose JA, Saha DC, Eales-Reynolds LJ. Smoking is associated with altered endothelial– derived fibrinolytic and antithrombotic factors: an in vitro demonstration. Circulation 2002; 106: 905-8.8. U.S. Department of Health and Human Services. How tobacco smoke causes disease: the biology and behavioral basis for smoking-attributable disease. A report of the surgeon general [monografía en Internet]. Atlanta: CDC; 2010. Disponible en: http://www.surgeongeneral.gov/library (consultado 17/11/2011)
9. Rubenstein D, Jesty J, Bluestein D. Differences between mainstream and sidestream cigarette smoke extracts and nicotine in the activation of platelets under static and flow conditions. Circulation 2004; 109: 78-83.
10. Takajo Y, Ikeda H, Haramaki N, Murohara T, Imaizumi T. Augmented oxidative stress of platelets in chronic smokers: mechanisms of impaired platelet-derived nitric oxide bioactivity and augmented platelet aggregability. J Am Coll Cardiol 2001; 38: 1320-7.
11. Morita H, Ikeda H, Haramaki N, Eguchi H, Imaizumi T. Only two-week smoking cessation improves platelet aggregability and intraplatelet redox imbalance of long-term smokers. J Am Coll Cardiol 2005; 45: 589-94.
12. Sawada M, Kishi Y, Numano F, Isobe M. Smokers lack morning increase in platelet sensitivity to nitric oxide. J Cardiovasc Pharmacol 2002; 40: 571-6.
13. Sambola A, Osende J, Hathcock J, Degen M, Nemerson Y, Fuster V, et al. Role of risk factors in the modulation of tissue factor activity and blood thrombogenicity. Circulation 2003; 107: 973-7.
14. Lee AJ, Fowkes FG, Rattray A, Rumley A, Lowe GD. Haemostatic and rheological factors in intermittent claudication: the influence of smoking and extent of arterial disease. Br J Haematol 1996; 92: 226-30.
15. Paramo JA, Beloqui O, Roncal C, Benito A, Orbe J. Validation of plasma fibrinogen as a marker of carotid aterosclerosis in subjects free of clinical cardiovascular disease. Haematologica 2004; 89: 1226-31.
16. Vayá A, Mira Y, Martínez M, Villa P, Ferrando F, Estellés A, et al. Biological risk factors for deep vein thrombosis. Clin Hemorheol Microcirc 2002; 26: 41-53.
17. Bakhru A, Erlinger TP. Smoking cessation and cardiovascular disease risk factors: results from the Third National Health and Nutrition Examination Survey. PLoS Med 2005;2e160
18. Goldenberg I, Jonas M, Tenenbaum A, Boyko V, Matetzky S, Shotan A, et al. Current smoking, smoking cessation, and the risk of sudden cardiac death in patients with coronary artery disease. Arch Intern Med 2003; 163: 2301-5.
19. Pomp E, Rosendaal F, Doggen C. Smoking increases the risk of venous thrombosis and acts synergistically with oral contraceptive use. Am J Hematol 2008; 83: 97-102.
20. Severinsen MT, Kristensen SR, Johnsen SP, Dethlefsen C, Tjønneland A, K Overvad K. Smoking and venous thromboembolism: a Danish follow-up study. J Thromb Haemost 2009; 7: 1297-303.
21. Goldhaber SZ, Grodstein F, Stampfer MJ, Manson JE, Colditz GA, Speizer FE, et al. A prospective study of risk factors for pulmonary embolism in women. JAMA 1997;277:642-645
22. Hansson PO, Eriksson H, Welin L, Svärdsudd K, Wilhelmsen L. Smoking and abdominal obesity: Risk factors for venous thromboembolism among middle-aged men: ''The study of men born in 1913''. Arch Intern Med 1999;159:1886-1890
23. Stavroulakis GA, Makris TK, Hatzizacharias AN, Tsoukala C, Kyriakidis MK. Passive smoking adversely affects the haemostasis/fibrinolytic parameters in healthy nonsmoker offspring of healthy smokers. Thromb Haemost 2000; 84: 923-4.