
Trasplante autólogo de progenitores hematopoyéticos en pacientes con mieloma múltiple: análisis de factores pronósticos y sobrevida. Experiencia del Hospital Británico
Dres. Carolina Oliver*, Silvia Pierri†, Sebastián Galeano‡,
Ada Caneiro§, Laura Bello§, Jorge Di Landro*, Andrew Miller¶, Regis Gai††, Pablo Mux퇇
Resumen
Introducción: el trasplante autólogo de progenitores hematopoyéticos (TAPH) es considerado estándar en el tratamiento de primera línea en pacientes con mieloma múltiple (MM) menores de 65 años.
Objetivo: analizar la sobrevida global (SG) y sobrevida libre de eventos (SLEv) de los pacientes con MM trasplantados en el Hospital Británico.
Material y método: se realizó un estudio retrospectivo de los pacientes que recibieron un primer TAPH.
Resultados: entre el 1º de julio de 1999 y el 30 de junio de 2010 se realizaron 56 TAPH a 48 pacientes con MM. Del análisis de los pacientes al primer TAPH, 46% eran mujeres y 54% hombres. La mediana de edad fue de 54 años (32-65 años). El 73% eran IgG, 17% IgA y 10% de cadenas livianas. El 60,4% logró una RC/nRC (RC, RC no confirmada y VGPR) posTAPH. Con una media de seguimiento de 58,6 meses (5,84-186,56), la mediana de SG fue de 121,8 meses (IC 95%: 70,1-173,54 meses). No se hallaron diferencias significativas en SG entre los pacientes que lograron RC/nRC posTAPH y quienes no lo lograron (log Rank p=0,162). La mediana de SLEv fue de 56 meses (IC 95%: 42,2-70,4 meses).
Conclusiones: el TAPH es una herramienta fundamental en el tratamiento de los pacientes con MM y es un procedimiento seguro en la Unidad de Hematología del Hospital Británico.
]]> Palabras clave: TRASPLANTE DE CÉLULAS MADRE HEMATOPOYÉTICAS. TRASPLANTE AUTÓLOGO.MIELOMA MÚLTIPLE.
Keywords: HEMATOPOIETIC STEM CELL TRANSPLANTATION.
TRANSPLANTATION, AUTOLOGOUS.
MULTIPLE MYELOMA.
*Asistente Interina de Cátedra de Hematología. Hospital de Clínicas. Facultad de Medicina. Universidad de la República. Uruguay.
† Ex Profesor Adjunto de Cátedra de Hematología. Hospital de Clínicas. Facultad de Medicina. Universidad de la República. Uruguay.
‡ Ex Asistente de Cátedra de Hematología. Hospital de Clínicas. Facultad de Medicina. Universidad de la República. Uruguay.
§ Ex Profesor Adjunto de Cátedra de Medicina Transfusional. Ex director del Banco Nacional de Sangre. Uruguay.
¶ Hematólogo. Unidad de Hematología del Hospital Británico.
]]> †† Médico hemoterapeuta. Unidad de Hematología del Hospital Británico. Uruguay.‡‡ Director de Unidad de Hematología del Hospital Británico. Ex Profesor Agregado de Cátedra de Hematología. Hospital de Clínicas. Facultad de Medicina. Universidad de la República. Uruguay.
Correspondencia: Dra. Ana Carolina Oliver Solimano
Av. Italia 2420. Unidad de Hematología. Hospital Británico.
Correo electrónico:
carolinaoliver@adinet.com.uy
Recibido: 20/7/110.
Aceptado: 28/10/11.
Conflicto de intereses: los autores declaran que no existen conflictos de intereses.
Introducción
]]> En los últimos 15 años ha habido un importante progreso en el tratamiento del mieloma múltiple (MM). El trasplante autólogo de progenitores hematopoyéticos (TAPH) ha sido considerado como el gold estándar en el tratamiento de primera línea en pacientes con MM menores de 65 años a partir de tres trabajos randomizados publicados entre 1996 y el 2004, los cuales demostraron beneficios en términos de sobrevida global (SG), remisión completa (RC) y sobrevida libre de eventos (SLEv). El primer trabajo que mostró mejoría en la SG y en sobrevida libre de enfermedad (SLE) con TAPH fue publicado por Attal M y colaboradores. Fue un estudio prospectivo y aleatorizado en 200 pacientes con MM menores de 65 años que comparó quimioterapia (QT) convencional con TAPH. La SG estimada a cinco años fue de 52% en el grupo con TAPH versus 12% en el grupo con tratamiento convencional (p=0,03)1). En el Medical Research Council Myeloma VII Trial, publicado por Child J y colaboradores, se seleccionaron 407 pacientes menores de 65 años con MM. Se comparó QT estándar versus TAPH, en el grupo de pacientes que recibieron QT intensa con infusión de progenitores hematopoyéticos se logró un aumento de la SG media de casi un año, 54 meses (95% IC 44,9 a 65,2) versus 42,3 meses (95% IC 33,1 a 51,6) (p<0,01)(2). En el estudio publicado por Palumbo A y colaboradores, la SG a tres años fue de 77% para el grupo con TAPH y 62% para el grupo tratado con QT (p<0,01)(3). Si bien estos tres trabajos son la base del uso actual del TAPH en primera línea dados los beneficios en SG, hay otros trabajos que no lo pudieron demostrar(4-6). Esto se debe a que en estos trabajos se incluyeron solo pacientes quimiosensibles o en una franja muy acotada de edad. Estos hechos se vieron reflejados en la revisión sistemática y metaanálisis de estudios randomizados publicada en el año 2007, que incluyó a 2.411 pacientes tratados con TAPH o QT convencional, donde se demostró una mejor sobrevida libre de progresión (SLP) a favor del TAPH sin impacto significativo en la SG(7).El tratamiento de condicionamiento aceptado es el melphalán a una dosis de 200 mg/m2 sin irradiación corporal total (ICT). La ICT no mostró ventajas en términos de remisión o SG y sí mayor toxicidad(8).
A pesar de los beneficios alcanzados con el uso del TAPH, no se ha logrado llegar a la cura de esta enfermedad, por lo que se han evaluado diferentes estrategias para lograr mejores resultados, entre ellas proceder al TAPH como consolidación luego de la inducción o en el momento de la recaída, o el uso del TAPH en tándem o el trasplante alogénico(9-14). El uso de estas modalidades es controversial y continúa en investigación.
El descubrimiento de nuevos fármacos como talidomida, lenalidomida y bortezomib, y su uso en combinación entre sí o con corticoides, doxorrubicina o ciclofosfamida, ha logrado aumentar el número de RC pre y posTAPH, hecho actualmente reconocido como un factor pronóstico independiente en términos de SG y SLP en esta enfermedad(15-17).
Material y método
En el Hospital Británico se comenzaron a trasplantar pacientes con MM en el año 1998, el primer paciente recibió un trasplante alogénico. En el período comprendido entre el 1º de julio de 1998 y el 30 de junio de 2010 se realizaron 56 TAPH a 48 pacientes con MM en la Unidad de Trasplante de Médula Ósea del Hospital Británico del Uruguay. Ocho pacientes recibieron un segundo TAPH luego de recaída o progresión. Se analizaron retrospectivamente los 48 pacientes que recibieron un primer TAPH luego de terapia de inducción a la remisión mediante la revisión de historias clínicas.
Los tratamientos de inducción realizados fueron: en 27 pacientes talidomida-dexametasona; en 30 pacientes vincristina-doxorrubicina-dexametasona (VAD); en cinco melphalán-prednisona; en dos interferón-alfa (INF-alfa); en dos bortezomib-dexametasona; en uno fludarabina; en siete radioterapia (RT), y en uno ciclofosfamida-vincristina-doxorrubicina-dexametasona (CVAD). La mediana de tratamientos previos fue de 1 (1-4); 66,7% recibieron un tratamiento previo; 25% dos; 6,3% tres, y 2% cuatro.
De los 48 pacientes, 10,4% fueron trasplantados en 1ª RC; 10,4% en 1ª RC no confirmada (PEF sin pico monoclonal, pero no se cuenta con inmunofijación); 8,3% en 1ª muy buena remisión parcial (VGPR); 68,8% en 1ª remisión parcial (RP), y 2,1% en 2ª RP.
La movilización de stem cells se realizó con factores estimulantes de colonias de granulocitos (G-CSF) en 47 pacientes y la media para la movilización fue de cinco días (2-11 días). Se utilizó para la aféresis un procesador Cobe Spectra. Un paciente recibió progenitores hematopoyéticos por cosecha de médula ósea. Todos los pacientes recibieron como condicionamiento pretrasplante melphalán 100 mg/m2 por dos días. La mediana de CD 34 fue de 4,6/kg x 106 (0,89-8,8). La mediana de mononucleares fue de 10/kg x 108 (7,02-38,6).
En todos los pacientes se realizó aislamiento en habitación con cámara de flujo laminar y se hizo profilaxis de Pn. jiroveci con trimetroprín-sulfametoxazol y de infección viral por herpes virus con aciclovir. Durante el período de neutropenia todos los pacientes recibieron profilaxis con fluconazol y ciprofloxacina. Todos los pacientes recibieron factores de crecimiento granulocitarios y eritropoietina.
]]> Se utilizaron los criterios de respuesta del International Myeloma Working Group Uniform Response Criteria(18).El análisis de los datos se realizó con el paquete estadístico G-Stat 2.0.
Resultados
De los 48 pacientes, 22 (46%) eran de sexo femenino y 26 (54%) de sexo masculino. La mediana de edad al debut fue de 54 años (32-65 años). La mediana de latencia entre el debut y el 1º TAPH fue de 9,9 meses (3,2-62,5 meses). El 37,5% de los pacientes procedían de centros del interior de Uruguay y 62,5% de Montevideo.
Con respecto al tipo de MM, 73% eran IgG, 17% IgA y 10% de cadenas livianas (6% lambda y 4% kappa del total) (tabla 1). Debutaron en estadio I A 10,5%, en II A 25%, en III A 58,5% y en III B 6%; 94% no presentaron insuficiencia renal al debut.
Se cuenta con los datos para el cálculo del ISS al debut de 26 pacientes. De ellos, 50% tenía un ISS I, 27% un ISS II y 23% un ISS III. Con respecto a la citogenética de MO, hay datos en 12 pacientes. De estos 12, solo un paciente presentó un citogenético de mal pronóstico. Un paciente de los 48 tenía amiloidosis asociada demostrada por biopsia y en uno se diagnosticó amiloidosis en el seguimiento postrasplante.
Como resultado del condicionamiento con melphalán se asistió a la mielosupresión, con un nadir de glóbulos blancos al día +5 (1-9), de glóbulos rojos (GR) al día +8 (1-14) y de plaquetas al día +1 (0-8). La recuperación medular medida por el nivel del PMN 500/mm3 fue en el día +10 (9-24). Treinta y seis pacientes (75%) debieron recibir una o más transfusiones de GR durante el período de aplasia. La mediana de número de transfusiones de GR fue de 2 (0-12). El 98% (47 pacientes) recibieron uno o más concentrados de plaquetas de donante único (CPDU). La mediana de CPDU administrados fue de 3 (0-32). La mediana de la última transfusión de GR fue el día +9 (2-38) y la de plaquetas el día +10 (6-42).
De los 48 pacientes, 32 (66,7%) tuvieron fiebre durante el período de aplasia. La mediana de días de fiebre fue de 1 (0-8); 6/32 tuvieron neutropenia febril documentada microbiológicamente, se hallaron: tres Staphylococcus coagulasa negativo, una Cándida Albicans, un Clostridium difficcile y un E. coli. Estos pacientes resolvieron su infección con el tratamiento adecuado sin otras complicaciones. Los focos clínicos infecciosos demostrados en el período de aplasia fueron diez (por orden de frecuencia): seis infecciones en zona de catéter Hickman; dos neumopatías agudas, una de las cuales evolucionó a sepsis; una sepsis de origen intestinal; una diverticulitis. En una de las bolsas de stem cells se halló Brevundinoma (pseudo) vesicularis.
Doce pacientes no requirieron tratamiento ATB empírico u específico más allá de la profilaxis infecciosa. La mediana de número de planes ATB utilizados fue de 1. El 42% requirió un solo plan, 25% dos planes, y 4,2% requirieron tres o cuatro planes.
La mediana de días de G-CSF utilizados posTAPH fue de 9 (6-30). La mediana de días al alta, medida desde el día de la infusión hasta el alta, fue de 15 (12-49).
]]> La mortalidad relacionada al TAPH en este grupo de 48 pacientes fue 0 (tabla 2).La mejor respuesta alcanzada, evaluada a los tres meses postrasplante, fue: en 11 (22,9%) pacientes RC, en 18 RC no confirmadas (37,5%), en tres VGPR (6,3%), en diez RP (20,8%), en cinco progresión (10,4%), y en uno no se ha evaluado. El 60,4% logró una RC/nRC posTAPH.
Se evaluaron las respuestas pre y posTAPH en los pacientes con VAD y TD dado que fueron los tratamientos más utilizados en esta serie y fueron, cada uno de ellos, estándares terapéuticos en distintas épocas (tabla 3 y figura 1 y figura 2).

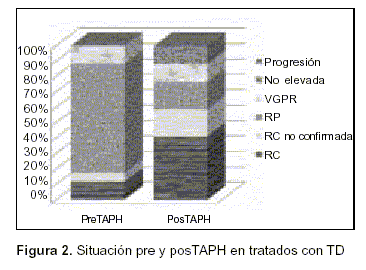
De los 48 pacientes, a 34 (71%) se les realizó mantenimiento. Los mantenimientos fueron con talidomida a 32 pacientes, INF a uno y dexametasona a un paciente.
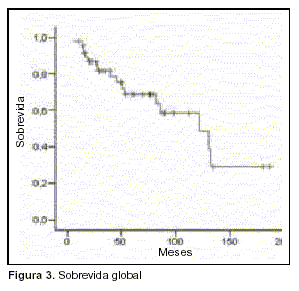
A la fecha de cierre de este análisis: 31 pacientes están vivos (64,6%), de los cuales nueve tuvieron una o más recaídas y siete progresaron. Con una media de seguimiento de 58,6 meses (5,84-186,56), la mediana de SG del total de pacientes con TAPH es de 121,8 meses (IC 95%: 70,1-173,54 meses). La SG a tres años es de 81%, a cuatro años 75% y a cinco años 68% (figura 3).
]]>
El International Staging System for Multiple Myeloma (ISS) que toma en cuenta el valor de la beta2-microglobulina (B2-M) y la albúmina se pudo calcular en 26 pacientes. Una B2-M menor de 3,5 mg/L y albúmina mayor o igual a 3,5 g/dL corresponde a un ISS I, una B2-M mayor o igual a 5,5 mg/L es un ISS III y los valores intermedios de B2-M o albúmina menor a 3,5 g/dL es un ISS II. El 50% eran ISS I, el 27 % ISS II y 23% ISS III. Se halló una diferencia significativa en SG entre los pacientes con diferentes grupos de riesgo (log Rank p=0,002). La mediana de SG para ISS I no se ha alcanzado, la estimada es de 93,7 meses (IC 95%: 87-100,5 meses), la mediana de SG para ISS II fue de 86,3 meses (IC 95%: 30,4-142,27 meses), y para ISS III 14,95 meses (IC 95%: 10,2-19,57 meses) (figura 4).
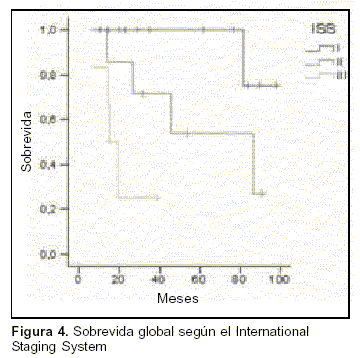
No se hallaron diferencias estadísticamente significativas en SG entre los pacientes que lograron RC/nRC (RC, RC no confirmada y VGPR) posTAPH y quienes no lo lograron (log Rank p=0,162). A pesar de que el número de pacientes es pequeño, se ve una tendencia a mayor SG de los pacientes que lograron RC/nRC posTAPH en los primeros años. La mediana de SG para los que lograron RC/nRC fue de 129,8 meses (IC 95%: 61,3-198,2) y para los que no, 86,3 meses (IC 95%: 0-180 meses). La SG a cinco años fue de 74% para el grupo que logró RC/nRC y de 56% para los que no (figura 5).
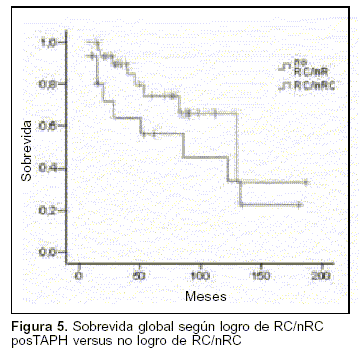
La mediana de SLEv (progresión, recaída o muerte por la enfermedad) fue de 56 meses (IC 95%: 42,2-70,4 meses). La SLEv a tres años fue de 69% y a siete años de 25%.
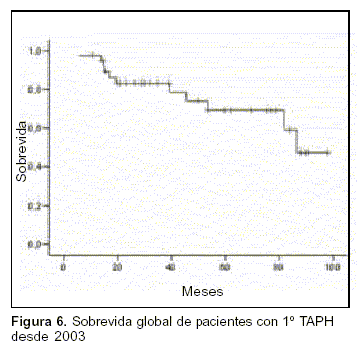
Treinta y ocho pacientes recibieron el 1º TAPH desde el año 2003 al momento. La mediana de SG estimada en este subgrupo de pacientes es de 86,3 meses. La SG a tres años en este subgrupo es de 83% y a cinco años de 69%. La mediana de seguimiento es 37 meses (5,84-97,77) (figura 6).
]]>
Discusión
El TAPH es una herramienta terapéutica fundamental y estándar en el manejo de los pacientes con MM. En el Hospital Británico se comenzaron a trasplantar pacientes con MM en el año 1998.
La mortalidad relacionada al TAPH a los 100 días en estos 56 procedimientos fue 0%, según los datos publicados por el CIBMTR (Center for International Blood and Marrow Transplant Research), en el año 2007-2008 fue menor a 3% a nivel internacional(19). Los datos reportados con respecto a la mielosupresión y la recuperación de la hematopoyesis son similares a los reportados a nivel internacional(20,21).
Existen tres trabajos que comparan los regímenes talidomida/dexametasona versus VAD. Se logra RC en 13% de los pacientes con el uso de estos planes(22). En estos trabajos se demostraron beneficios de TD versus VAD como tratamiento de inducción en términos de respuesta: al menos VGPR 30% versus 15%(23), 35% versus 13%(24) y al menos RP 76% versus 52%. También se demostraron mejores resultados postrasplante: al menos VGPR 44% versus 42% y 68% versus 49%. No se demostró diferencia estadísticamente significativa en SG a cinco años al comparar estos regímenes, si bien en el trabajo publicado por Cavo hubo una tendencia a mayor SG con el uso de TD (69% versus 53% a cinco años). Las respuestas obtenidas en nuestra serie son similares a las reportadas en estos trabajos. La SG a cinco años tiene también una tendencia a ser mejor con TD versus VAD, 80% versus 66%, pero sin diferencia estadísticamente significativa.
Con una media de seguimiento de 58,6 meses la mediana de SG en el grupo de pacientes trasplantados fue de 121,8 meses, SG muy superior a los datos publicados por Child (54 meses). La SG a tres años fue de 81%, similar a la publicada por Palumbo, pero superior a los datos aportados por el CIBMTR, cuyas cifras son de 68% a los tres años(19). Pensamos que esto es debido a que se trata de una población muy heterogénea de pacientes, tanto por el tiempo previo al TAPH, los tratamientos y líneas utilizadas, y sesgado por los primeros pacientes trasplantados, dado que solamente se trasplantaban pacientes en RC o RP mayor, sin comorbilidades y con un excelente estado general. Por esto se procedió a analizar el grupo de 38 pacientes trasplantados desde el 1º de enero de 2003 al 30 de junio de 2010, se seleccionó este grupo ya que en 2003 se comenzó a trasplantar, si no existía contraindicación, a todos los pacientes menores de 65 años portadores de MM luego de una inducción de la remisión independientemente del éxito logrado con la misma. En este grupo de pacientes, con una media de seguimiento de 37 meses (5,84-97,77), la SG estimada es de 86,3 meses, con SG a tres años de 83% y a cinco años de 69%, datos más acorde con los conocidos internacionalmente, de todas maneras la media de seguimiento es corta y el número de pacientes es limitado, por lo que pueden existir estas diferencias.
La SLEv en nuestra serie fue de 56 meses, superior a los datos internacionales que refieren una mediana entre 25 y 42 meses(2,4,5). También fue superior a los datos aportados en los trabajos de Attal y Palumbo(1,3). Esto podría explicarse por las mismas consideraciones que se realizaron para SG y que sería una diferente población en los estudios.
El índice ISS ha sido validado en pacientes de diferentes poblaciones, edades, tratados o no con trasplante, y ha demostrado su simplicidad y validez en predecir sobrevida. Con un ISS I la mediana de SG es de 62 meses, con ISS II 44 meses y con ISS III 29 meses. En nuestra población, a pesar de ser escaso el número de pacientes evaluables, se observó también una diferencia estadísticamente significativa en SG entre los diferentes grupos de riesgo.
El impacto de lograr la RC en MM ha sido demostrado luego del inicio del uso del TAPH en esta patología. La mayoría de los estudios que evalúan TAPH han demostrado que es beneficioso lograr una buena remisión en términos de SG o al menos de SLP(2,3,25,26). En esta serie observamos una tendencia a mayor SG al lograr RC/nRC posTAPH. El número de pacientes es bajo pero se observa una diferencia marcada en los primeros diez años del debut. La SG a los cinco años es similar a la obtenida en el trabajo del grupo francés(27): 74% versus 61% en este último y 74% versus 56% en esta serie.
Conclusiones
]]> El TAPH es una herramienta fundamental en el tratamiento de los pacientes con MM. Es un procedimiento seguro en nuestra unidad del Hospital Británico. La SG en el total de pacientes analizados en esta serie es de 121,8 meses y la SLEv es de 56 meses; pensamos que estos resultados están sesgados por una selección de pacientes realizada en los primeros años de uso de la técnica. En concordancia con los datos reportados a nivel internacional hay una tendencia a mejores resultados en los pacientes que logran la RC/nRC y en quienes tienen un ISS de bajo riesgo.Summary
Introduction: autologic transplant of hematopoietic progenitors is regarded as the standard in the first line treatment of patients with multiple myeloma (MM) younger than 65 years old.
Objective: to analyse global survival and incident free survival in patients with multiple myeloma transplanted at the British Hospital.
Method: we conducted a retrospective study of patients who received the first autologic transplant of hematopoietic progenitors.
Results: 56 autologic transplants of hematopoietic progenitors were performed from July 1, 1999 through June 30, 2010 in 48 patients with MM. Upon analysis of patients after the first transplant, 46% were women and 54% were men. Median age was 54 years old (32-65 years old). 73% were IgG, 17% were IgA and 10% were light chains.60.4% achieved CR/nCR (CR), non- confirmed CR and VGPR) after transplant. With an average follow-up of 58.6 months (5.84-186.56), the median global survival was 121.8 months (IC 95%: 70.1-173.54 months). No significant differences were found in the global survival in patients who achieved CR/nCR after autologic transplant of hematopoietic progenitors and those who failed to achieve it (log Rank p=0.162. The median incident-free survival was 56 months (IC 95%: 42.2-70.4 months).
Conclusions: autologic transplant of hematopoietic progenitors is an essential tool to treat patients with MM and it is a safe procedure at the Hematology Unit of the British Hospital.
Resumo
Introdução: o transplante autólogo de progenitores hematopoiéticos (TAPH) é considerado um padrão no tratamento de primeira linha de pacientes menores de 65 anos com mieloma múltiple (MM).
Objetivo: analisar a sobrevida global (SG) e sobrevida livre de eventos (SLEv) dos pacientes com MM transplantados no Hospital Britânico.
]]> Material e método: um estudo retrospectivo dos pacientes que receberam um primeiro TAPH foi realizado.Resultados: no período 1º de julho de 1999 a 30 de junho de 2010 foram realizados 56 TAPH a 48 pacientes com MM. A análise dos dados dos pacientes no primeiro TAPH mostrou que 46% eram mulheres e 54% homens. A mediana da idade foi 54 anos (32-65 anos). 73% eram IgG, 17% IgA e 10% de cadeias leves. 60,4% conseguiram uma RC/nRC (RC, RC não confirmada e VGPR) pósTAPH. Com una media de seguimento de 58,6 meses (5,84-186,56), a mediana de SG foi de 121,8 meses (IC 95%: 70,1-173,54 meses). Não foram encontradas diferenças significativas na SG entre os pacientes que conseguiram RC/nRC pósTAPH e os que não a conseguiram (log Rank p=0,162). A mediana de SLEv foi 56 meses (IC 95%: 42,2-70,4 meses).
Conclusões: o TAPH é uma ferramenta fundamental para o tratamento de pacientes com MM e é um procedimento seguro na Unidade de Hematologia do Hospital Britânico.
Bibliografía
1. Attal M, Harousseau JL, Stoppa AM, Sotto JJ, Fuzibet JG, Rossi JF, et al. A prospective, randomized trial of autologous bone marrow transplantation and chemotherapy in multiple myeloma: Intergroupe Français du Myélome. N Engl J Med 1996; 335(2): 91-7.
2. Child JA, Morgan GJ, Davies FE, Owen RG, Bell SE, Hawkins K, et al. Medical Research Council Adult Leukaemia Working Party. High-dose chemotherapy with hematopoietic stem-cell rescue for multiple myeloma. N Engl J Med 2003; 348(19): 1875-83.
3. Palumbo A, Bringhen S, Petrucci MT, Musto P, Rossini F, Nunzi M, et al. Intermediate-dose melphalan improves survival of myeloma patients aged 50 to 70: results of a randomized controlled trial. Blood 2004; 104(10): 3052-7.
]]>4. Bladé J, Rosiñol L, Sureda A, Ribera JM, Díaz-Mediavilla J, García-Laraña J, et al. High-dose therapy intensification compared with continued standard chemotherapy in multiple myeloma patients responding to the initial chemotherapy: long-term results from a prospective randomized trial from the Spanish Cooperative Group PETHEMA. Blood 2005; 106(12): 3755-9.
5. Fermand JP, Katsahian S, Divine M, Leblond V, Dreyfus F, Macro M, et al. High dose therapy and autologous blood stem cell transplantation compared with conventional treatment in myeloma patients aged 55 to 65 years: long-term results of a randomized control trial from the Group Myelome-Autogreffe. J Clin Oncol 2005; 23(36): 9227-33.
6. Barlogie B, Kyle RA, Anderson KC, Greipp PR, Lazarus HM, Hurd DD, et al. Standard chemotherapy compared with high-dose chemoradiotherapy for multiple myeloma: final results of phase III US Intergroup trial S9321. J. Clin Oncol 2006; 24(6): 929-36.
7. Koreth J, Cutler CS, Djulbegovic B, Behl R, Schlossman RL, Munshi NC, et al. High dose therapy with single autologous transplantation versus chemotherapy for newly diagnosed multiple myeloma: a systematic review and metaanalysis of randomized controlled trials. Biol Blood Marrow Transplant 2007; 13(2): 183-96.
8. Moreau P, Facon T, Attal M, Hulin C, Michallet M, Maloisel F, et al. Intergroupe Francophone du Myélome. Comparison of 200 mg/m2 melphalan and 8 Gy total body irradiation plus 140 mg/m2 melphalan as conditioning regimens for peripheral blood stem cell transplantation in patients with newly diagnosed multiple myeloma: final analysis of the Intergroupe Francophone du Myélome 9502 randomized trial. Blood 2002; 99(3): 731-5.
]]>9. Attal M, Harousseau JL, Facon T, Guilhot F, Doyen C, Fuzibet JG, et al. Single versus double autologous stem-cell transplantation for multiple myeloma. N Engl J Med 2003; 349(26): 2495-502.
10. Cavo M, Tosi P, Zamagni E, Cellini C, Tacchetti P, Patriarca F, et al. Prospective, randomized study of single compared with double autologous transplantation for multiple myeloma: Bologna 96 clinical study. J Clin Oncol 2007; 25(17): 2434-41.
11. Crawley C, Iacobelli S, Björkstrand B, Apperley JF, Niederwieser D, et al. Reduced-intensity conditioning for myeloma: lower nonrelapse mortality but higher relapse rates compared with myeloablative conditioning. Blood 2007; 109(8): 3588-94.
12. Fermand JP, Ravaud P, Chevret S, Divine M, Leblond V, Belanger C, et al. High-dose therapy and autologous peripheral blood stem cell transplantation in multiple myeloma: Up-front or rescue treatment? Results of a multicenter sequential randomized clinical trial. Blood 1998; 92: 3131-6.
13. Facon T, Mary JY, Harousseau JL. Front-line or rescue autologous bone marrow transplantation (ABMT) following a first course of high dose melphalan (HDM) in multiple myeloma (MM). Preliminary results of a prospective randomized trial (CIAM) protocol. Blood 1996; 88(1): 685a.
]]>14. Barlogie B, Kyle R, Anderson K. Comparable survival in multiple myeloma (MM) with high dose therapy (HDT) employing MEL 140 mg/m2 1 TBI 12 Gy autotransplants versus standard dose therapy with VBMCP and no benefit from interferon (IFN) maintenance: results of intergroup Trial S9321. Blood 2003; 102: 42a.
15. Alexanian R, Weber D, Giralt S, Dimopoulos M, Delasalle K, Smith T, et al. Impact of complete remission with intensive therapy in patients with responsive multiple myeloma. Bone Marrow Transplant 2001; 27(10): 1037-43.
16. Lahuerta JJ, Mateos MV, Martínez-López J, Rosiñol L, Sureda A, de la Rubia J, et al. Influence of pre- and post-transplantation responses on outcome of patients with multiple myeloma: sequential improvement of response and achievement of complete response are associated with longer survival. J Clin Oncol 2008; 26(35): 5775-82.
17. van de Velde HJ, Liu X, Chen G, Cakana A, Deraedt W, Bayssas M. Complete response correlates with long-term survival and progression free survival in high-dose therapy in multiple myeloma. Haematologica 2007; 92(10): 1399-406.
18. Durie BG, Harousseau JL, Miguel JS, Bladé J, Barlogie B, Anderson K, et al. International uniform response criteria for multiple myeloma. Leukemia 2006; 20(9): 1467-73.
]]>19. Center for International Blood & Marrow Transplant Research. Disponible en: http://www.cibmtr.org/pages/index.aspx. [Consulta: 26/5/2011].
20. Papanikolaou X, Maltezas D, Repousis P, Athanassopoulos A, Alexia S, Megalakaki K, et al. High dose chemotherapy and autologous stem cell transplantation in patients with multiple myeloma: the experience of a single haematological unit. J BUON 2008; 13(2): 193-7.
21. Majolino I, Vignetti M, Meloni G, Vegna ML, Scimè R, Tringali S, et al. Autologous transplantation in multiple myeloma: a GITMO retrospective analysis on 290 patients. Haematologica 1999; 84(9): 844-52.
22. Cavo M, Zamagni E, Tosi P, Tacchetti P, Cellini C, Cangini D, et al. Superiority of thalidomide and dexamethasone over vincristine-doxorubicin-dexamethasone (VAD) as primary therapy in preparation for autologous transplantation for multiple myeloma. Blood. 2005; 106(1): 35-9.
23. Cavo M, Di Raimondo F, Zamagni E, Patriarca F, Tacchetti P, Casulli AF, et al. Short-Term Thalidomide Incorporated Into Double Autologous Stem-Cell Transplantation Improves Outcomes in Comparison With Double Autotransplantation for Multiple Myeloma. J Clin Oncol 2009; 27(30): 5001-7.
]]>24. Macro M, Divine M, Uzunhan Y. Dexamethasone + Thalidomide (Dex/Thal) compared to VAD as a Pre-Transplant Treatment in Newly Diagnosed Multiple Myeloma (MM): A Randomized Trial.. Blood 2006; 108: 22a.
25. Lenhoff S, Hjorth M, Turesson I, Westin J, Gimsing P, Wislöff F, et al. Intensive therapy for multiple myeloma in patients younger than 60 years: Long-term results focusing on the effect of the degree of response on survival and relapse pattern after transplantation. Haematologica 2006; 91(9): 1228-33.
26. Kim JS, Kim K, Cheong JW, Min YH, Suh C, Kim H, et al. Complete remission status before autologous stem cell transplantation is an important prognostic factor in patients with multiple myeloma undergoing upfront single autologous transplantation. Biol Blood Marrow Transplant 2009; 15(4): 463-70.
27. Harousseau JL, Avet-Loiseau H, Attal M, Charbonnel C, Garban F, Hulin C, et al. Achievement of at Least Very Good Partial Response Is a Simple and Robust Prognostic Factor in Patients With Multiple Myeloma Treated With High-Dose Therapy: Long-Term Analysis of the IFM 99-02 and 99-04 Trials. J Clin Oncol 2009; 27(34): 5720-6.
]]>