
Dres. Walter Pedreira1, Leonardo Anzalone2, Marcelo Álvez3,
Tec. Alina Cafferatta4
Laboratorio Clínico del Centro de Asistencia del Sindicato Médico del Uruguay. Sección Bacteriología del Laboratorio de Atención Primaria del Servicio de Asistencia Externa del Ministerio de Salud Pública.
Resumen
La infección urinaria baja es una enfermedad frecuente en mujeres, con una evolución favorable pero alta morbilidad.
La fosfomicina es un derivado del ácido fosfónico que altera la pared bacteriana. Su actividad abarca la mayoría de los agentes uropatógenos con una resistencia de 1% en Escherichia coli, el uropatógeno más importante. La sal de trometamol mejora la absorción de la fosfomicina obteniéndose concentraciones urinarias con rango terapéutico durante tres días luego de una dosis de 3 g.
Objetivos: conocer la eficacia clínica/microbiológica y la seguridad de una monodosis de fosfomicina/trometamol (Fosfurol) de 3 g en mujeres con infección urinaria baja no complicada.
Material y método: se realizó un estudio prospectivo multicéntrico, randomizado y no comparativo. Se estudiaron 54 pacientes que concurrieron a las policlínicas de Atención Primaria de Salud Pública y de un centro asistencial privado con sintomatología de infección urinaria baja sin haber recibido antibióticos en los 15 días anteriores. Se recolectó la orina para la evaluación mediante tira reactiva de elementos anormales y la siembra para bacteriuria cuantitiva. A las pacientes con infección urinaria se les administró una monodosis de fosfomicina trometamol de 3 g. Las cepas aisladas se identificaron y se estudió la sensibilidad a este antimicrobiano. Se realizó un seguimiento clínico y microbiológico en la semana 1 y 3 de la primera consulta.
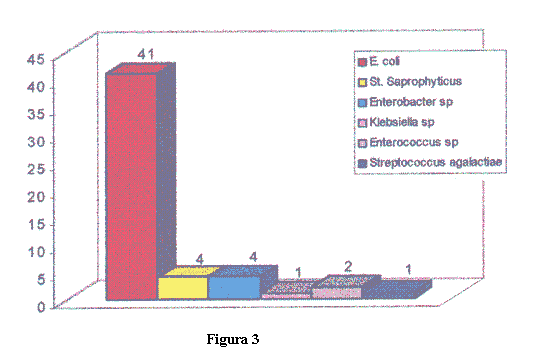
]]> Resultados: se aislaron los siguientes gérmenes: 41 Escherichia coli, 4 Staphylococcus saprophyticus, 4 Proteus sp, 1 Enterococcus sp, 2 Klebsiella sp, 1 Streptococcus agalactiae y 1 Enterobacter sp. Sólo tres cepas de Staphylococcus saprophyticus y una cepa de Klebsiella sp presentaron resistencia in vitro.En la visita 2 se encontraron 50 erradicaciones, 4 persistencias microbiológicas, 49 curas clínicas y 4 fallas. En la visita 3 se encontraron 49 erradicaciones, 1 recidiva, 49 curas clínicas, 1 recaída. Ninguna paciente presentó candidiasis después del tratamiento ni efectos secundarios con significación clínica.
Conclusiones: la baja resistencia in vitro a la fosfomicina de los gérmenes urinarios estudiados junto con la muy buena eficacia clínico-microbiológica y la tolerancia a este antimicrobiano lo muestran como una terapéutica útil en el tratamiento de infecciones urinarias no complicadas en mujeres.
Palabras clave: INFECCIONES URINARIAS - quimioterapia.
FOSFOMICINA - uso terapéutico.
TROMETAMOL - uso terapéutico.
1. Ex Prof. Agdo. de la Cátedra de Bacteriología y Virología. Facultad de Medicina. Microbiólogo Jefe de la Sección Bacteriología del Laboratorio Clínico del Centro de Asistencia del Sindicato Médico del Uruguay.
2. Prof. Adj. del Departamento de Laboratorio Clínico del Hospital de Clínicas. Ex Prof. Adj. de la Cátedra de Bacteriología y Virología.
Microbiólogo Jefe de la Sección Bacteriología del Laboratorio de Atención Primaria del Servicio de Salud de Asistencia Externa (SSAE)-Ministerio de Salud Pública.
]]> 3. Médico posgrado en infectología.4. Técnica del Laboratorio de Asistencia Externa - SSAE.
Institución responsable: Ministerio de Salud Pública - Administración de Servicios de Salud del Estado (ASSE) - SSAE.
Fuente de apoyo parcial - Laboratorio Libra.
Correspondencia: Dr. Leonardo Anzalone
Cantoni - Ramos 4407 apto. 605 Montevideo. Uruguay.
E-mail: lanzalone@conectate.com.uy
Recibido: 22/5/02.
Aceptado: 9/5/03.
]]> IntroducciónLas infecciones urinarias en las mujeres son frecuentes. Se estima que una mujer experimentará por lo menos un episodio de infección urinaria en su vida; de 3% a 5% de las mujeres en edad genital activa tendrán una infección urinaria y de 0,5% a 1% tendrán infecciones recurrentes. De 25% a 35% de las mujeres entre 20 y 40 años tendrán una infección urinaria. Esta infección conlleva una apreciable morbilidad; la duración de los síntomas es promedialmente de 6,4 días, las alteraciones en la actividad de 2,4 días y el ausentismo laboral de 1,5 días(1).
Los factores de riesgo mayores son:
- edad,
- actividad sexual,
- higiene sexual poscoito,
- embarazo,
- historia de infección urinaria reciente,
- uso de antibióticos betalactámicos en el mes previo.
La topografía, la existencia o no de síntomas y ciertos factores agregados del huésped tales como vejiga neurógena, malformaciones, diabetes, cálculos, etcétera, dificultan el establecimiento al inicio de una terapéutica efectiva en todos los casos ya sea en lo que concierne a la elección de fármacos efectivos en la vía urinaria como a la duración de la misma. Esta situación se complica por la elevada tasa de resistencia a los antimicrobianos (betalactámicos, sulfas, nitrofuranos y un incremento actual a las quinolonas) de los gérmenes productores de infección urinaria (E. coli y otras enterobacterias)(2).
]]> También se ha señalado el hecho de que no todos los fármacos son eficaces en el contexto clínico evolutivo puesto que si un antibiótico no tiene impacto sobre la flora intestinal, si no alcanza concentraciones adecuadas en el tejido renal o en el introito vaginal, puede sólo actuar en el episodio puntual pero no prevenir las recurrencias tan frecuentes en las pacientes de sexo femenino(1).Por último, los síntomas clínicos si bien son orientadores nunca pueden excluir una infección urinaria alta aunque sea superficial y sin gravedad. Ellas representan 10% de los episodios de infecciones urinarias catalogadas como bajas.
Existen múltiples pautas de tratamiento con diferentes fármacos, dosis y duración.
La duración del tratamiento en la infección urinaria se determina de acuerdo a la presunta topografía y a la existencia o no de factores complicantes.
Para la infección urinaria baja sin factores complicantes se utilizan cursos de tres a cinco días y para la infección urinaria alta con o sin factores complicantes se utilizan pautas de hasta 14 días(1). Las tasas de eficacia de una dosis única como encare terapéutico dependen de una adecuada anamnesis que permita la inclusión de las pacientes en la categoría de IU baja sin factores complicantes. En general en esta población las tasas de curación exceden 98% y son comparables a los esquemas de tres a cinco días de duración(3,4).
Los antimicrobianos útiles para el tratamiento de dosis única deberán tener:
- espectro antimicrobiano que abarque todos los patógenos de infección urinaria (concentración inhibitoria mínima [CIM] baja),
- actividad bactericida (concentración mínima bactericida [CMB] baja).
- farmacocinética: alta concentración urinaria, alta concentración renal, baja tasa de excreción. Concentraciones por encima de la CIM por más de 48 horas en la orina vesical,
- escasos efectos colaterales,
]]> - alta complacencia por parte del paciente.Estudios clínicos previos han constatado la eficacia de algunos fármacos como trimetoprima/sulfametoxazol, quinolonas fluoradas como fleroxacina, pefloxacina(5).
Han demostrado también la poca eficacia de los betalactámicos para esta terapéutica debido a la alta tasa de resistencia y a su rápida eliminación urinaria.
Desde 1969 está disponible la fosfomicina como sal soluble en agua (fosfomicina-trometamina).
Se trata de un antibiótico bactericida contra la mayoría de las cepas bacterianas, tanto gramnegativas como grampositivas causantes de infección urinaria. Actúa bloqueando las etapas iniciales de la síntesis de la pared celular en especial en presencia de un pH ácido(6). Posee también, a concentraciones subinhibitorias, la capacidad de disminuir la adherencia bacteriana a las células del urotelio tanto en bacterias sensibles como resistentes. Presenta un efecto bactericida a concentraciones superiores a la CIM con 99% de letalidad cuando la concentración duplica la CIM en un lapso de tres a ocho horas luego de ser administrado(7). Se destaca un efecto posantibiótico de tres horas y la disminución de la adherencia de bacterias sensibles y resistentes, por ejemplo Pseudomonas aeruginosa(7). La emergencia de variantes bacterianas resistentes es muy baja (10-7 a 10-9). A concentraciones estándar, la aparición de mutantes resistentes de Escherichia coli es poco probable; sin embargo, éstas se observan a concentraciones urinarias menores o iguales a 200 mg/l(8). Es menos activa frente a Klebsiella sp. y Staphylococcus saprophyticus. La resistencia por cepas mutantes no es probablemente un problema en el tratamiento de infecciones urinarias sin factores complicantes. Si bien aparecen mutantes resistentes postratamiento en la flora fecal, no se aíslan luego de pasado el mes de tratamiento. La característica más relevante de este antimicrobiano es que no presenta resistencia cruzada con otros antimicrobianos. Las cepas resistentes a ampicilina, cefalosporina de primera generación o trimetoprima/sulfametoxazol son sensibles a fosfomicina; esto es debido a su diferente estructura química y mecanismo de acción sobre la bacteria(9-12).
La nueva formulación de la fosfomicina-trometamol (FOT) tiene también las condiciones de un antibiótico ideal para el tratamiento con monodosis de una infección urinaria. El agregado de la sal de trometamol favorece la absorción digestiva de la fosfomicina debido a que la sal de trometamina evita que la fosfomicina sea inactivada por la acidez estomacal y aumenta la biodisponibilidad por vía oral más de tres veces con respecto a la fosfomicina en su formulación clásica (sal cálcica) por la misma vía. Posee un gran volumen de distribución y una pobre unión a proteínas plasmáticas. La farmacocinética sérica es lineal no dosis dependiente con una concentración máxima a las 2 horas de la ingesta. La concentración en próstata, pared vesical y vesículas seminales es similar a la sérica. La excreción renal es exclusiva sin transformaciones y por filtración glomerular(6,7,13). Estos hechos plantean que después de dos a cuatro horas de una monodosis de 3 g la concentración urinaria es 350 veces mayor que la mínima concentración necesaria para la inhibición de E. coli y la misma permanece elevada (por encima de la CIM de uropatógenos) durante 3,5 días(7) (figura 1).
Este fármaco presenta una excelente actividad in vitro, evidenciada en los estudios nacionales de 1995 a la fecha(9) (tabla 1) y estudios internacionales(10-12), que favorece su utilización.
Los resultados de estudios tan alentadores motivaron a los autores a realizar un estudio de eficacia clínica.
]]> Objetivos- Comprobar la eficacia clínica y microbiológica de un plan terapéutico de una única dosis de fosfomicina-trometamol (Fosfurol (r)) en las pacientes con infección urinaria baja sin factores complicantes.
- Evaluar la tasa de efectos colaterales causados por ese fármaco.
- Determinar la concentración inhibitoria mínima (CIM) de los patógenos comúnmente involucrados en la causa de la infección urinaria a este antimicrobiano.
Material y método
Método experimental
Estudio prospectivo, multicéntrico, randomizado y no comparativo. Se estudiaron 54 pacientes que concurrieron a las policlínicas de Atención Primaria de Salud Pública (Ministerio de Salud Pública) y de un centro asistencial privado con sintomatología de infección urinaria baja sin ingesta de antibióticos en los 15 días anteriores.
Selección de las pacientes
1) Criterios de inclusión: se incluyeron mujeres comprendidas entre 15 y 55 años con diagnóstico presuntivo de infección urinaria baja sin factores complicantes.
2) Criterios de exclusión: se excluyeron del estudio todas las pacientes que tuvieran algún indicio de padecer una infección urinaria alta o fueran portadoras de factores complicantes.
]]> Criterios de exclusión:- Diabetes.
- Embarazo y lactancia.
- infección urinaria alta, fiebre de 38,5ºC, dolor en fosas lumbares y vómitos que persistan por más de tres a cuatro días.
- Otros elementos complicantes: cálculos, vejiga neurógena, inmunopatías en general.
- Hipersensibilidad a fármacos.
Procedimientos
Se obtuvo un consentimiento informado de todas las pacientes que integraron el estudio. Se les informó acerca del método de estudio y de la necesidad de un seguimiento.
Se realizaron tres visitas, la primera de captación (visita número 1) y dos de seguimiento y control (visitas número 2 y número 3). La visita número 2 se realizó entre los días 6-9 y la visita número 3 entre los días 21-30; tomando como día 1 el día de la captación de la paciente (fichas de trabajo).
]]> En la visita número 1 se realizó un chequeo clínico y el llenado de la ficha correspondiente. Se buscaron elementos orientadores de infección urinaria mediante la utilización de tiras reactivas de diez parámetros (Multistix(r), Bayer). Se determinó la presencia de esterasas leucocitarias, nitritos, proteinuria o hematuria, o ambas(14-16). Se realizó la toma para bacteriuria cuantitativa a efectos de confirmar el diagnóstico presuntivo de infección urinaria y aislar el agente etiológico involucrado. El criterio diagnóstico utilizado fue el de Kass y Stamm modificado para interpretación de bacteriurias, considerándose positivos aquellos cultivos con recuentos monomicrobianos mayores a 100.000 unidades formadoras de colonias por ml (UFC/ml) de orina o recuentos menores acompañados de sintomatología o leucocitos, o ambos, sangre o nitritos en la orina, o ambos(17). La identificación se realizó según criterios convencionales(18).A aquellas pacientes con infección urinaria se les administró una monodosis de 3,5 g de fosfomicina/trometamol (Fosfurol (r)).
Se estudió el comportamiento del agente aislado frente a los antibióticos comúnmente usados en infecciones urinarias mediante disco difusión por técnica de Kirby-Bauer, frente a ampicilina, cotrimoxazol, nitrofurantoína, cefalotina, ciprofloxacina, norfloxacina y fosfomicina-trometamol. Para este último fármaco se utilizaran discos de 200 µg más glucosa 6 fosfato (G6P). Los criterios de interpretación fueron de NCCLS (National Commitee for Clinical Laboratory Standars) 1997 y para la fosfomicina se consideraron sensibles halos mayores de 16 mm (CIM < 64 mg/l), intermedios 12-15 mm (128 mg/l) y resistentes menores de 12 mm (> 128 mg/l) según normas estadounidenses(19).
Se incluyeron como controles de los estudios de sensibilidad las cepas de referencia E. coli (ATCC 25922) y S. aureus (ATCC 25923).
Se determinó la CIM mediante un test cuantitativo de difusión en agar, (E-Test(r) Epsilometer AB-BioDisk) para la fosfomicina-trometamol.
Sabiendo que en menos de 10% de los episodios de infección urinaria no se erradicará completamente el agente (aproximadamente ese es el porcentaje de infección urinaria alta que no se puede diferenciar de infección urinaria baja), se optó por un nuevo agente antimicrobiano para el tratamiento (por ejemplo, quinolonas fluoradas). Se planteó también su utilización frente a fracasos clínicos y aislamientos de cepas resistentes a la fosfomicina-trometamol.
En el resto de las visitas se realizó un chequeo clínico junto con el llenado de las fichas correspondientes a esas visitas y se determinó la presencia de infección urinaria mediante bacteriuria cuantitativa (figura 2).
Evaluación clínica
]]>Curación: desaparición de los síntomas y signos luego del tratamiento.
Mejoría: marcada reducción de los síntomas sin llegar a la desaparición total al final del tratamiento (primera o segunda semanas).
Recaída: reaparición de los síntomas con bacteriuria postratamiento, pudiendo corresponder a reinfección o recidiva.
Falla: persistencia o empeoramiento de los síntomas.
No evaluable: imposibilidad de seguimiento.
Evaluación microbiológica
Curación: desaparición del uropatógeno inicial.
Persistencia: no desaparición del germen inicial en la primera visita (ocho a diez días).
Recidiva: reaparición del agente presunto después de una primera muestra negativa inicial (dentro del mes).
]]> Reinfección: reaparición de un agente diferente después de una primera muestra negativa inicial (dentro del mes).Luego de la obtención de un urocultivo negativo no se consideró una falla del tratamiento.
Seguridad
Efectos adversos: fueron considerados por las pacientes. Se catalogaron como leves, moderados o severos, y se consignó su duración. En base a estos datos se evaluó la tolerabilidad del fármaco pudiendo ser éste excelente, regular o malo.
Los efectos adversos pueden ser: diarrea, náuseas, vómitos, erupción cutánea, dolor abdominal, disturbios sensoriales.
Resultados
Se enrolaron en el estudio 54 pacientes que cumplían con los criterios de inclusión-exclusión y que presentaban una infección urinaria. Los agentes bacterianos encontrados se muestran en la figura 3. Los resultados de sensibilidad de los microorganimos aislados se observan en la tabla 2. Los rangos de CIM para fosfomicina-trometamol de los aislamientos se presentan en la tabla 3. De los agentes encontrados sólo tres cepas de Staphylococcus saprophyticus y una cepa de Klebsiella sp. presentaron resistencia in vitro a la fosfomicina-trometamol acompañada de falla clínica y persistencia del germen. La cepa de Klebsiella pneumoniae se aisló de una paciente que había recibido en dos ocasiones tratamientos con fosfomicina-trometamol con resultados exitosos en los cinco meses previos. La respuesta microbiológica luego del tratamiento se observa en la tabla 4. La presunta recidiva microbiológica correspondió a una E. coli sensible a fosfomicina-trometamol.
La tabla 5 muestra la respuesta clínica y la evolución de estas pacientes.
Es importante destacar que ninguna paciente presentó Candidiasis luego del tratamiento ni efectos secundarios severos. Ninguna paciente presentó erupción cutánea ni vómitos; tres pacientes (3/54) presentaron distensión abdominal con dolor que no requirió tratamiento; dos (2/54) presentaron una disminución transitoria en la consistencia de las materias fecales.
]]>
Discusión y conclusiones
En esta población controlada, E. coli fue el agente más frecuentemente involucrado (41/54), seguido lejanamente por Staphylococcus saprophyticus y Proteus sp. Otros agentes fueron hallados en muy baja frecuencia. Fosfomicina-trometamol fue el antimicrobiano más activo in vitro frente a los microoganismos aislados. Nuestros resultados reafirman que este antimicrobiano puede ser utilizado como tratamiento empírico inicial en pacientes con infecciones urinarias ambulatorias sin factores complicantes. Clínicamente la tasa de fracasos se relacionó con determinados microorganismos que presentan una sensibilidad disminuida a este fármaco, como Klebsiella pneumoniae y Staphylococcus saprophyticus, según se demostró en nuestro estudio previo referido a la sensibilidad in vitro de agentes de infección urinaria (tabla 1)(9).
Las fallas clínico-microbiológicas se correspondieron a la resistencia in vitro y respondieron favorablemente al tratamiento alternativo con quinolonas fluoradas (ciprofloxacina 500 mg cada 12 horas por cinco días).
En una paciente, en la tercera visita se constató la reaparición de los síntomas. Se aisló una cepa de E. coli con el mismo perfil fenotípico encontrado en la primera visita, por lo cual se catalogó como una presunta recidiva. Es de destacar que sin contar con estudios moleculares que tipifiquen esta cepa no podemos descartar que no se trate de una reinfección.
Nuestro estudio está en concordancia con los resultados publicados internacionalmente en la última década(20-22). Estudios clínicos comparativos de dosis únicas de este antibiótico en pacientes con infecciones urinarias no complicadas muestran porcentajes de curación clínica y bacteriológica ya sea a corto o a largo plazo postratamiento, comparables e incluso superiores a los obtenidos con otros antibióticos administrados en dosis únicas o múltiples(23-26). En un estudio comparativo randomizado doble ciego se comparó la dosis única de 3 g de fosfomicina-trometamol con un régimen de siete días de norfloxacina; los porcentajes de erradicación bacteriológica a los tres días postratamiento fueron de 90% y 80%, respectivamente(23). En mujeres se comparó esta monodosis contra siete días de tratamiento con nitrofurantoína; los resultados fueron de curación bacteriológica en 78% de las pacientes tratadas con monodosis de fosfomicina-trometamol y de 86% en los tratados con nitrofurantoína(27). Se han realizado diversos estudios doble ciego comparativos con respecto a otras monodosis, tales como 800 mg de norfloxacina(28) y 200 mg de trimetoprima(29) no encontrándose diferencias en los resultados de curación y evolución clínica. Resultados similares se encontraron comparando la monodosis de fosfomicina-trometamol con cinco días de amoxicilina-clavulánico(30), tres días de norfloxacina(25), cinco días de cefalexina(31) o tres días de trimetoprima-sulfametoxa-zol(32,33).
]]> La tolerancia y la seguridad de la monodosis con este antibiótico fueron muy buenas en nuestro estudio, con efectos colaterales leves y sin significación clínica. Naber en su estudio también encontró efectos colaterales leves como dispepsia, náuseas y cefaleas en porcentajes muy bajos, sin reacciones adversas severas(34). Este autor encontró que la frecuencia de efectos colaterales aumenta levemente cuando se tratan pacientes embarazadas(34).Las interacciones medicamentosas con fármacos como la metoclopramida reducen marcadamente la absorción y las concentraciones urinarias de fosfomicina-trometamol al igual que los alimentos que retrasan los picos séricos y urinarios en 8% a 10%(35). Otros fármacos como la cimetidina no generan cambios en su absorción(35).
La bacteriuria es una complicación importante en las mujeres embarazadas, tanto la bacteriuria sintomática como la asintomática. Su frecuencia varía de 3% a 10% con posibilidades de recurrencias en un grupo de ellas(36).
En un estudio multicéntrico randomizado, Zinner S(37), comparó la dosis única de 3 g con un tratamiento de siete días de ácido pipemídico en 291 pacientes embarazadas con bacteriurias sintomáticas y asintomáticas. Los porcentajes de curación al mes fueron de 93% y 90%, respectivamente; las recurrencias fueron similares (3%) y los efectos adversos fueron mínimos y leves 9% y 15%, respectivamente(37). Resultados similares fueron encontrados en un estudio comparativo con nitrofurantoína 200 mg/día en embarazadas asintomáticas(38). Otro estudio comparando la monodosis de fosfomicina-trometamol con tres días de cetibuten vía oral en embarazadas con cistitis mostró una cura y erradicación de uropatógenos en 90% y 95%, respectivamente, diferencia no estadísticamente significativa(36). La fosfomicina-trometamol no se ha asociado a efectos teratogénicos y es actualmente considerada como un fármaco clase B para la Food Drug Administration respecto a su uso en el embarazo. En pacientes embarazadas con infecciones recurrentes o pielonefritis su utilización no sería adecuada.
Existen pocos estudios en niños. Se utilizaron dosis únicas de 2 g y 1 g en menores de 1 año. Un estudio comparativo sobre 135 niños de 1 a 16 años comparando la monodosis contra dosis única de netilmicina 5 mg/kg intramuscular mostró una curación bacteriológica con orinas estériles al mes de 80% y 81%, respectivamente(39).
Ferraro y colaboradores evaluaron la eficacia clínica y la seguridad de monodosis de fosfomicina-trometamol en infecciones bajas no complicadas de ancianos comparándola con siete días de norfloxacina. La curación bacteriológica se logró en 76,6% de los pacientes tratados con monodosis y en 73,3% de los tratados con norfloxacina(40).
Distintos estudios muestran también a este antibiótico como una muy buena alternativa en la profilaxis de cirugía transuretral(41,42).
En suma, hay acuerdo general en que los esquemas acortados (tres días) se plantean en pacientes con infecciones bajas cuya presunción se logra con el interrogatorio de síntomas y signos. El diagnóstico de dichas infecciones se puede presumir con mayor certeza utilizando técnicas de screening, como ser aspecto de la orina, piuria, microhematuria, nitritos, determinados en consultorio mediante una tira reactiva de orina. Esta técnica alcanza un alto valor predictivo negativo(2,14-16). Se suma a esto la causa predecible, los patrones de resistencia conocidos, la tendencia a la curación espontánea y la ausencia de elementos complicantes. Siguiendo este algoritmo diagnóstico consideramos que en nuestro medio fosfomicina-trometamol debe ser considerada como una terapéutica antibiótica, basados en el creciente aumento de la resistencia a betalactámicos y quinolonas fluoradas.
Esta estrategia de tratamiento es adecuada para su utilización en los consultorios de los sistemas primarios de salud, debiendo contar con un seguimiento clínico-bacteriológico, tomando en cuenta que este gesto terapéutico es costo efectivo. Una falla temprana en el tratamiento orientará a una resistencia del agente involucrado, una infección urinaria parenquimatosa o la presencia de factores complicantes no detectados inicialmente. Esto puede determinar la implementación de un estudio oportuno y más exhaustivo en un número pequeño de pacientes con fracaso terapéutico luego del tratamiento.
La baja tasa de resistencia in vitro a fosfomicina frente a los gérmenes aislados de infección urinaria junto con la muy buena eficacia clínico-microbiológica de este antimicrobiano lo muestran como una terapéutica útil en el tratamiento de infecciones urinarias no complicadas en mujeres.
]]> También puede ser de utilidad para topografiar dicha infección. La presencia de una baja tasa de resistencia a fosfomicina, como la que se observa en nuestro estudio, plantea que frente a una falla terapéutica podemos atribuirla a una infección parenquimatosa en un porcentaje no despreciable. Esto se observa sobre todo al descartar la presencia de resistencia bacteriana en el control microbiológico posterior al fracaso clínico con el tratamiento empírico.En nuestro estudio, como los criterios clínicos de inclusión fueron muy estrictos, se encontraron cifras menores a las publicadas de fallas terapéuticas no vinculadas a la resistencia al fármaco (por ejemplo, infección urinaria parenquimatosa subyacente).
Summary
Low urinary infection is a frequent pathology in women with good prognosis but high morbility.
Fosfomycin is a phosphoric acid derivative able to alter bacterial wall. Its activity comprises most of the uropathogenic agents with a 1% resistance in Escherichia coli, the most important uropathogen. Trometamol facilitates absorbtion of fosfomycin obtaining urinary concentration with therapeutic range lasting for three days after a 3 g dose.
Objectives: to determine the clinical/microbiological efficacy and safety of a single-3 g dose of fosfomycin trometamol (Fosfurol) in women with low non-complicated urinary infection.
Methods: a multicenter, randomized, non-comparative prospective study was undertaken. Fifty-four patients of public health centers and one private clinic presented symptoms of low urinary infection without taking antibiotics the previous 15 days. Urine was collected using reactives for abnormal elements and cultures for bactriuria. Patients with urinary infection received a single-3 g dose of fosfomycin trometamol. Strains were identified and sensitivity was studied. A clinical and microbiological follow up was done at the first and third week.
Results: germens were isolated as follow: 41 Escherichia coli, 4 Staphylococcus saprophyticus, 4 Proteus sp, 1 Enterococcus sp, 2 Klebsiella sp, 1 Streptococcus agalactiae and 1 Enterobacter sp. Only 3 strains of Staphylococcus saprophyticus and one strain of Klebsiella sp presented resistance in vitro.
Conclusions: low fosfomycin resistance in vitro altogether with high clinical-microbiological efficacy and tolerance to this antimicrobian indicate that it is a useful therapeutic in treating non-complicated urinary infections in women.
Résumé
]]> L'infection urinaire basse est une pathologie fréquente chez les femmes, aynat une évolution favorable mais une haute morbidité.La phosphomycine est un dérivé de l'acide phosphonique qui altère la paroi bactérie. Son activité comprend la plupart des agents uropathogènes avec une résistance de 1% en Escherichia coli, l'uropathogène le plus important. Le sel de trométamol améliore l'absorption de la phosphomycine, obtenant des concentrations urinaires avec rang thérapeutique pendant trois jours après une dose de 3 g.
Buts: connaître l'efficacité clinique-microbiologique et la sécurité d'une monodose de phsphomycine/trométamol (Phosphurol) de 3 g ches des femmes avec infection urinaire basse pas compliquée.
Matériaux et méthode: on a réalisé une étude prospec-tive multicentrique et pas comparative. On a étudié 54 patientes qui sont allées aux polycliniques d'Assistance Primaire de la Santé Publique et d'un centre privé d'assistance, avec des symptômes d'infection urinaire basse sans avoir reçu d'antibiotiques pendant les 15 jours précédents. On a collecté l'urine pour l'évaluation au moyen de bande réactive d'éléments anormaux et la culture pour bactériurie quantitative. Aux patientes avec infection urinaire on a donné une monodose de phosphomycine trométamol de 3g. Les cèpes isolées ont été identifiées et on a étudié leur sensibilité face à cet antimicrobien. On a fait une suite clinique et microbiologique pendant la semaine 1 et 3 après la première consultation.
Résultats: on a isolé les germes suivants: 41 Escherichia coli, 4 Staphylococcus saprophyticus, 4 Proteus sp, 1 Enterococcus sp, 2 Klebsiella sp, 1 Streptococcus agalactiae et 1 Enterobacter sp. Seulement 3 cèpes de Staphylococcus saprophyticus et une cèpe de Klebsiella sp ont présenté résistance in vitro. À la visite 2 on a trouvé 50 éradications, 4 persistences microbiologi-ques, 49 guérisons cliniques et 4 failles. À la visite 3 on a trouvé 49 éradications, 1 récidive, 49 guérisons et 1 rechute. Aucune patiente n'a présenté candidose après le traitement ni des effets secondaires significatifs.
Conclusions: la basse résistance in vitro à la phospho-mycine des germes urinaires étudiés et l'efficacité clinique-microbiologique et la tolérance à cet antimicrobien, le signalent comme une thérapeutique utile dans le traitement des infections urinaires pas compliquées chez les femmes.
Bibliografía
1. Sobel JD, Kaye D. Urinary Tract Infections. In: Mandell GL, Bennett JE, Dolin R (ed). Principles and Practice of Infectious Disease. fifth ed. New York: Churchill Livignstone, 2000: 662-90.
]]>2. Anzalone L, Cafferatta A, Pascale C, Javier A, Píriz N, Gallo J. Infección urinaria comunitaria: detección rápida en consultorio y planteos de terapéutica antibiótica empírica a utilizar. Congreso Panamericano de Infectología, 9, Congreso Panamericano de SIDA 1, Congreso Guatemalteco de Enfermedades Infecciosas 4, Ciudad de Guatemala. 1999: 67.
3. Bailey RR. Review of published studies on single dose therapy of urinary tract infections. Infection 1990; 18 (Suppl 2): s53-6.
4. Caron F, Humbert G. Short-Term treatment of urinary tract infections: the french concept. Infection 1992; 20 (Suppl 4): s286- 90.
5. Bailey RR. Managment of lower urinary tract infections. Drugs 1993; 45(Suppl 3): s139-44.
6. Gialdroni Grassi G. Clinical Development of Fosfomycin Trometamol. Infection 1990; 18(Suppl 2): s57-s64.
]]>7. Bergan T. Degree of absorption, pharmacokinetics of Fosfomycin Trometamol and duration of urinary antibacterial activity. Infection 1990; 18(Suppl 2): s65-s69.
8. Greenwood D. Fosfomycin Trometamol: activity in vitro against urinary tract pathogens. Infection 1990; 18(Suppl 2): s 60-s63.
9. Pedreira W, Anzalone L, Cafferatta A, Monroy F, Viola M. Estudio comparativo de la actividad in vitro de fosfomicina trometamol frente a agentes aislados de mujeres con infección urinaria no complicada. Rev Urug Patol Clín 2000; 32: 20-3.
10. Smayevsky J, Rospide F, Incola F, Bantar C. Actividad comparativa in vitro de fosfomicina frente a microorganismos aislados de mujeres con infección urinaria no complicada. Centro de Educación Médica e Investigación Clínica, Buenos Aires, Argentina. Congreso Argentino de Microbiología 11, Buenos Aires, 1998: 132.
11. Barry AL. Antibacterial spectrum of fosfomycin trometamol. J Antimicrob Chemother 1995; 35: 228-30.
]]>12. Garau M, Latorre A, Alonso-Sanz M. Fosfomicina: un antibiótico infravalorado en infecciones urinarias por Escherichia coli. Enferm Infec Microbiol Clin 2001; 19: 462-6.
13. Patel SS, Balfour JA, Bryson HM. Fosfomycin trometamine. A review of its actibacterial activity, pharmacokinetic properties and therapeutic efficacy as a single dose oral treatment for uncomplicated lower urinary tract infections. Drugs 1997; 53(4): 637-56.
14. Winkens RAG, Leffers P, Trienekens TAM, Stobberingh EE. The validity of urine examination for urinary tract infections in daily practice. Fam Pract 1995; 12(3): 290-3.
15. Pels RJ, Bor DH, Woolhandler S, Himmelstein DU. Dipstick urinalysis screening of asymptomatic adults for urinary tract disorders. JAMA 1989; 262(9): 1221-4.
16. Pezzlo M. Detection of urinary tract infections by rapid methods. Clin Microbiol Rev 1988; 1: 268-86.
]]>17. Stamm WE. Quantitative urine cultures revisited. Eur J Clin Microbiol 1984; 3: 279-85.
18. Baron E, Piterson L, Finegold S. Urinary tract mechanisms. In: Bailey and Scotts. Diagnostic Microbiology, 10th ed. Philadelphia: Mosby, 1994: 249-57.
19. National Committee for Clinical Laboratory Standars. Performance Standard for Antimicrobial Disk Susceptibility Test. Fifth Edition; Approved Estándar. Villanova: NCCLS 1993: (Document M2- A5, Vol 13, No 24).
20. Gelfand M, Jhonson R. Single-dose Fosfomycin Tromethamine: evaluation in the treatment of uncomplicated lower urinary tract infection. Adv Ther 1997; 14(2): 49-63.
21. Moroni M. Monuril in lower uncomplicated urinary tract infections in adults. Eur Urol 1987; 13(Suppl I): 101-4.
]]>22. Stein GI. Single dose treatment of acute cistitis with fosfomycin tromethamine. Ann Pharmacother 1998; 32: 2. 215-9.
23. Boerema JBJ, Willems ThC. Fosfomycine Trometamol single dose versus multiple dose Norfloxacin over seven days for uncomplicated UTI in general practice. Infection 1990; 18(Suppl 2): s80-8.
24. Jardin A. A general practitioner multicenter study: Fosfofomycin Trometamol single dose versus Pipemidic Acid multiple dose. Infection 1990; 18(Suppl 2): s89-93.
25. Reynaert J, Van Eyek D, Vandepitte J. Single dose Fosfomycin Trometamol versus multiple dose Norfloxacin over three days for uncomplicated UTI in general practice. Infection 1990; 18(Suppl 2): s77-88.
26. Neu HC. Fosfomycin trometamol versus amoxycillin - single dose: multicenter study of urinary tract infections. Chemotherapy 1990; 36( Suppl I ): 19-23.
]]>27. Stein GE. Comparison of single-dose fosfomycin and a 7 day course of nitrofurantoin in female patientes whit uncomplicated urinary tract infection. Clin Therap 1998; 1: 864-72.
28. Selvaggi FP, Ditonno P, Traficante A, Battaglia M, Di Lorenzo V. Fosfomycin trometamol (Monuril) versus norfloxacin in single dose for adult female uncomplicated UTIs. Chemotherapy 1990; 36(Suppl I ): 31-3.
29. Harvard Davis R, O' Dowd TC, Holmes W, Smail J, Slack RCB. A comparative double-blind randomizes study of single dose fosfomycin trometamol with trimetoprim in treatment of urinary tract infections in general practice. Chemotherapy 1990; 36(Suppl I): 34-6.
30. Cooper J, Raeburn AL, Brumfitt W, Hamilton-Miller JMT. General practitioner study: fosfomycin trometamol versus amoxycillin clavulanate in acute urinary tract infections. Chemotherapy 1990; 36(Suppl I): 24-6.
31. Elhanan G, Tabenkin H, Yahalom R, Raz R. Single-dose fosfomycin trometamol versus 5 - day cephalexin regimen for treatment of uncomplicated lower urinary tract infections in women. Antimicrob Agents Chemother 1994; 38: 2612-4.
]]>32. Crocchilo P. Single-dose fosfomycin trometamol versus multiple-dose cotrimoxazole in the treatment of lower urinary tract infections in general practice. Chemotherapy 1990; 36(Suppl I): 37-40.
33. Naber KG, Thyroff-Friesinger U. Fosfomycin Trometamol versus Ofloxacin/Co- trimoxazole as single dose. Therapy of acute uncomplicated urinary tract infection in female: a multicentre study. Infection 1990; 18(Suppl 2): s70-6.
34. Naber K. The safety and tolerability of Fosfomycin Trometamol. Rev Contemp Pharmacother 1995; 6: 63.
35. Bergan T, Di Mario F, Mastropaolo G, Naccarato R. Pharmacokinetics of fosfomycin and influencia of cimetidine and metroclopramide on the bioavailability of of fosfomycin trometamol. In: Neu H, Williams JD (eds): New trends in urinary tract infections. Karger: Basel, 1988: 157-66.
36. Krcmery S, Horomec J, Demesova D. Treatment of lower urynary tract infection in pregnancy. Int J Antimicrob Agents 2001; 17: 279-82.
]]>37. Zinner S. Fosfomycine trometamol versus pipemidic acid in the treatment of bacteriuria in pregnancy. Chemotherapy 1990; 36(Suppl I): 50-2.
38. Thoumsin H, Aghayan M, Lambotte R. Single dose Fosfomycin Trometamol versus multiple dose Nitrofurantoin in pregnant women with bacteriuruia: preliminary results. Infection 1990; 18(Suppl 2): s94-7.
39. Principi N, Corda R, Bassetti D, Varese LA, Peratoner L. Fosfomycin trometamol versus netilmicin in children's lower urinary tract infections. Chemotherapy 1990; 36(Suppl I): 41-5.
40. Ferraro G, Ambrosi G, Bucci L, Palmieri G. Fosfomycin trometamol versus norfloxacin in the treatment of uncomplicated lower urinary tract infections of ederly. Chemotherapy 1990; (Suppl I): 46-9.
41. Di Siverio F, Ferrone G, Carati I. Prophylactic chemotherapy with Fosfomycin Trometamol during transurethral surgery and urological manoeeuvres. Results of a multicenter study. Infection 1990; 18(Suppl 2): s98-102.
]]>42. Baert I, Billiet I, Vandepitte J. Prophylactic chemotherapy with Fosfomycin trometamol versus placebo during transurethral prostatic resection. Infection 1990; 18(Suppl 2): s103-6.
]]>