Dres. Carlos Rivas*, Gonzalo Greif†, Cecilia Coitinho*,Luis Araújo‡, Paula Laserra‡, Carlos Robello §
* Departamento de Laboratorio. Comisión Honoraria para la Lucha Antituberculosa y Enfermedades Prevalentes. Centro de Referencia Nacional para Micobacterias. Ministerio de Salud Pública, Uruguay.
† Unidad de Biología Molecular del Institut Pasteur, Uruguay.
‡ Médicos neumólogos supervisores. Comisión Honoraria para la Lucha Antituberculosa y Enfermedades Prevalentes. Ministerio de Salud Pública, Uruguay.
§ Departamento de Bioquímica, Facultad de Medicina, Universidad de la República, Uruguay.
Correspondencia: Dra. Cecilia Coitinho. Laboratorio de Biología Molecular. Comisión Honoraria para la Lucha Antituberculosa y Enfermedades Prevalentes. Laboratorio Calmette. Bulevar Gral. Artigas 3175, Montevideo. Correo electrónico: ccoitinho@fmed.edu.uy
Recibido: 30/4/12. Aceptado: 7/9/12
Resumen
Se describen los primeros tres casos de tuberculosis pulmonar por Mycobacterium bovis en Uruguay. Uno de los enfermos poseía antecedentes de contacto con animales en un zoológico; el otro, portador del virus de inmunodeficiencia humana (VIH), estaba en contacto cotidiano con derivados cárnicos de ganado vacuno, el tercero poseía antecedentes de ingestión de leche no pasteurizada. En todos los casos se pudo confirmar la etiología mediante la aplicación rutinaria de técnicas de biología molecular en conjunto con la bacteriología convencional. A pesar de que se ha realizado la búsqueda sistemática de M. bovis en muestras clínicas que ingresan a nuestro laboratorio, hasta ahora no se habían podido reportar aislamientos de origen humano. La presencia de este microorganismo en muestras veterinarias en la última década permite esperar la aparición de nuevos casos en sujetos inmunocompetentes y pacientes VIH/SIDA. El antecedente de contacto estrecho con animales, especialmente ganado bovino, o con sus productos derivados, o ambos, debe alertar al clínico sobre la posibilidad de esta zoonosis en cuyo tratamiento se debe excluir la pirazinamida.
]]> Palabras clave: TUBERCULOSIS PULMONAR MYCOBACTERIUM BOVIS ZOONOSISKeywords: TUBERCULOSIS, PULMONARY MYCOBACTERIUM BOVIS ZOONOSES
Introducción
La tuberculosis continúa siendo una enfermedad de importancia tanto en el hombre como en los animales(1). Los agentes etiológicos integran un complejo (Mycobacterium tuberculosis complex) que incluye a M. tuberculosis, que es el agente de la tuberculosis humana (TBH), y M. bovis, que es el agente causal de la tuberculosis en animales, principalmente ganado bovino, aunque otros animales domésticos o salvajes, en cautiverio o vida libre, pueden ser afectados(2,3). El hombre puede infectarse y enfermar de tuberculosis por M. bovis (TBB) considerada, en estos casos, como una zoonosis(4).
En Latinoamérica, la TBB registra una muy baja incidencia, aunque la misma podría estar subestimada por las dificultades técnicas para un correcto aislamiento e identificación del agente(5). En Uruguay no se habían reportado casos de TBB, aunque no es posible descartar la existencia de casos no confirmados o erróneamente tipificados como TBH; los estudios bacteriológicos sistemáticos realizados a nivel nacional para aislamiento e identificación de M. bovis siempre fueron negativos, incidirían en este aspecto las medidas de control a nivel veterinario sumadas a la pasteurización de la leche y controles sanitarios de sus derivados. Durante el año 2011, por técnicas de biología molecular se detectaron cepas compatibles con M. bovis que fueron luego totalmente confirmadas por tipificación fenotípica y por secuenciación genómica en el Institut Pasteur de Montevideo (IPM). Nuestro objetivo es reportar estos casos clínicos y destacar los aspectos más interesantes de esta zoonosis que se presenta ahora en Uruguay.
Caso clínico 1
Paciente de 60 años, sexo masculino, de Paysandú, diabético tipo II, alcoholista moderado, fumador intenso que consulta en servicio de urgencia por fiebre alta (39ºC axilar), sudoración profusa, astenia y adinamia. La radiografía de tórax muestra una lesión nodular en lóbulo superior derecho. Se indican antibióticos y controles en policlínica para estudio. Consulta nuevamente a las 24 horas, febril, con desorientación témporo-espacial y un cuadro focal neurológico con hemiplejia derecha, parálisis facial y afasia. En urgencia instala convulsión tónico-clónica generalizada por lo que se traslada a cuidados intensivos con asistencia ventilatoria mecánica.
Antecedentes personales: hasta hace un año y medio trabajaba en el zoológico municipal, realizando la limpieza de las jaulas de animales.
Tomografía axial computada (TAC) de cráneo: sin lesiones.
TAC de tórax: se destaca lesión nodular cavitada de lóbulo superior derecho (LSD), derrame pleural bilateral y consolidación bibasal.
]]> Velocidad de eritrosedimentación (VES): 82 mm. Leucocitosis: 8.200 mm3. Proteína C reactiva : positiva.Estudio citoquímico del líquido céfalo-raquídeo (LCR) (muestra del primer ingreso): Pandy negativo, 8 leucocitos, 70% neutrófilos.
Estudio citoquímico de LCR (muestra del segundo ingreso): Pandy positivo, 145 leucocitos, 95% mononucleares.
Serología para VIH: negativa.
Se plantea tuberculosis pulmonar asociada a tuberculosis meníngea, por lo que se instala tratamiento empírico con plan según normas nacionales de tratamiento para la tuberculosis, y corticoides.
Bacteriología: examen microscópico directo de secreciones obtenidas por fibrobroconscopía: positivo para micobacterias. Cultivos para micobacterias: positivos.
Identificación bacteriana final (fenotípica y genotípica): Mycobacterium bovis sp. Sensibilidad a fármacos antituberculosos: isoniacida sensible, rifampicina sensible, estreptomicina sensible, etambutol sensible, pirazinamida resistente.
Completa tratamiento antituberculoso. Buena evolución con secuelas neurológicas.
Caso clínico 2
Paciente de 38 años, sexo masculino, domiciliado en Canelones, que ingresa a centro hospitalario por dolor torácico tipo puntada de costado, acompañado de tos, expectoración, fiebre, astenia y adinamia (síntomas iniciados en los 20 días previos). La radiografía de tórax muestra un infiltrado bilateral con derrame pleural. Se realiza pleuroscopía con toma biópsica.
]]> Antecedentes personales: desde el año 2008, por razones laborales, el paciente está en contacto cotidiano con huesos y vísceras de ganado vacuno y de pollos.Hemocultivos para gérmenes comunes: negativos.
Serología para VIH: positiva. Linfocitosis: 1.640 mm3, CD4: 303 (18,5%), carga viral: menor a 53 copias/ml.
Examen funcional y enzimograma hepático: sin valores alterados.
Bacteriología: baciloscopías de expectoración, negativas.
Examen microscópico directo de biopsia pleural: positivo para micobacterias. Cultivos para micobacterias: positivos.
Identificación bacteriana final (fenotípica y genotípica): Mycobacerium bovis sp. Sensibilidad a fármacos antituberculosos: isoniacida sensible, rifampicina sensible, estreptomicina sensible, etambutol sensible, pirazinamida resistente.
Se realiza tratamiento antituberculoso completo con buena adherencia y respuesta, se otorga alta; buena evolución.
Caso clínico 3
Paciente de 39 años, sexo femenino, domiciliada en Salinas, Canelones. Desocupada. Presenta un cuadro de un mes de evolución dado por: astenia, adinamia, anorexia y adelgazamiento, tos y expectoración escasas, sin síndrome de impregnación tóxica, sin disnea ni sangrados.
]]> La radiografía de tórax muestra opacidad inhomogénea con broncograma aéreo en tercio superior de ambos hemitórax, a predominio derecho. En lóbulo superior derecho lesión cavitada de 3 cm de diámetro mayor con nivel hidroaéreo.Antecedentes personales: ingestas de leche sin pasteurizar, directamente de un tambo familiar, durante un mes, hace un año atrás. La paciente vivió en zona rural de Montevideo durante su adolescencia, en contacto con animales de granja.
Hemograma: se destaca hemoglobina de 11,6 g/dl.
VES: 20 mm.
Serología para VIH: negativa.
Examen funcional y enzimograma hepático: sin valores alterados.
Bacteriología de expectoración: exámenes microscópicos directos y cultivos positivos para micobacterias. Identificación primaria: M. tuberculosis complex.
Identificación bacteriana final (fenotípica y genotípica): Mycobacerium bovis sp. Sensibilidad a fármacos antituberculosos: isoniacida sensible, rifampicina sensible, estreptomicina sensible, etambutol sensible, pirazinamida resistente.
Con resultados bacteriológicos primarios, inicia tratamiento antituberculoso según normas nacionales, buena evolución, continúa en tratamiento ajustado a identificación micobacteriana definitiva.
Identificación de los aislamientos clínicos
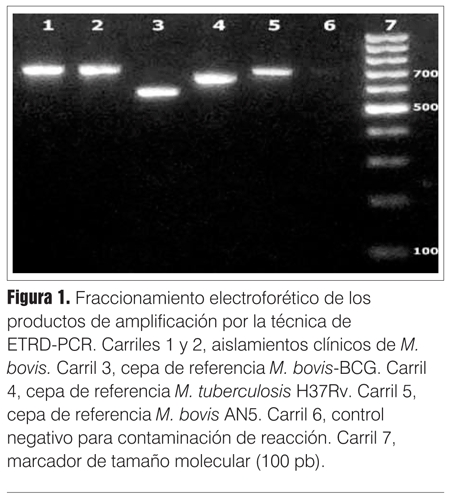
]]> El complejo Mycobacterium tuberculosis incluye varias especies genéticamente relacionadas (M. tuberculosis, M. bovis, M. bovis-BCG, M. africanum, M. microti, M. pinnipedi, M. caprae y M. canetti). De ellas, M. tuberculosis y M. bovis son de distribución universal y los patógenos más importantes. Ambas especies son de crecimiento lento (tres a ocho semanas en cultivos convencionales), pero existen algunas diferencias fenotípicas destacables (tabla 1). M. bovis es inhibido por el glicerol (nutriente común en los medios a base de huevos), lo cual dificulta la obtención de cultivos positivos. A diferencia de M. tuberculosis, no produce niacina ni posee nitrato reductasa, por lo que estas pruebas son negativas; el desarrollo de M. bovis es inhibido por la hidracida del ácido tiofeno-2-carboxílico (TCH) y es resistente a la pirazinamida (PZ) (carece de la enzima pirazinamidasa). Desde el punto de vista genotípico existen regiones del genoma de M. bovis que pueden ser amplificadas por la reacción en cadena de la polimerasa (PCR) y que permiten diferenciarlo de M. tuberculosis con gran precisión y rapidez. En nuestro laboratorio se realiza una PCR desarrollada "in house", basada en reportes de Djelouadji y colaboradores(6), que amplifica una de las repeticiones en tándem VNTR (Variable Number of Tandem Repeats) específicas del complejo M. tuberculosis y conocidas como MIRU (Mycobacterial Interespersed Repeat Units). Recientemente nuestro grupo utilizó esta técnica para la identificación de 800 aislados clínicos(7), donde además de mostrar una gran homogeneidad en los datos, se observaron diferencias en cuanto a los tamaños publicados por Djelouadji, encontrándose en nuestro país principalmente aislados de M. tuberculosis con tamaño de 600 y 824 pares de bases. Asimismo, en el caso de M. bovis, el tamaño fue de 672 pares de bases, tanto para la cepa de referencia como para los aislados clínicos presentados en este trabajo (figura 1). La confirmación por secuenciación del amplicón fue realizada para cada tamaño de amplificación obtenido, confirmando el número de repetidos variables en cada caso(7).
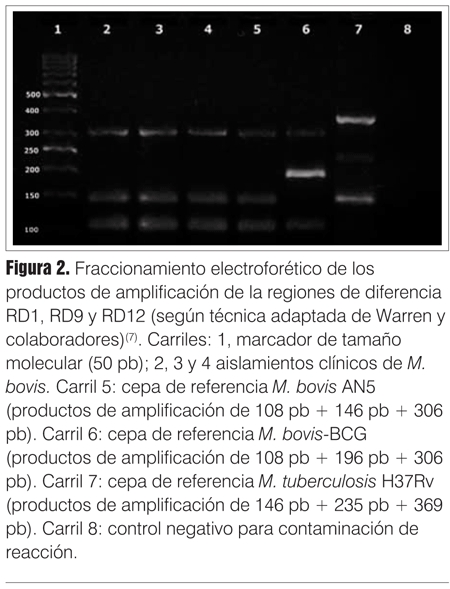
En los casos descriptos, la secuenciación de esta región fue indicativa de M. bovis, por lo cual se realizaron las pruebas bioquímicas y una PCR complementaria, adaptada de Warren y colaboradores(8), que amplifica las regiones de diferencia RD1, RD9 y RD12 para diferenciar especies dentro del complejo M. tuberculosis (figura 2). En este caso se espera obtener amplificaci&oa cute;n de 146, 235 y 369 bp en el caso de tratarse de M. tuberculosis , mientras que en el caso de M. bovis los tamaños esperados son 108,146 y 306 bp. En la figura 2 se observa cómo el patrón de bandas obtenido para los tres aislados clínicos se corresponde con el esperado para M. bovis, asimismo las cepas de referencia utilizadas como control presentaron el patrón esperado. En cuanto a la susceptibilidad a fármacos antituberculosos, a excepción de la PZ (característicamente resistente), al igual que M. tuberculosis las cepas salvajes son sensibles a isoniacida y rifampicina aunque pueden adquirir resistencia por mutación frente a tratamientos inadecuados.
Consideraciones clínicas y epidemiológicas
Desde el punto de vista clínico, imagenológico y paraclínico, la TBB es indistinguible de la TBH(9). La diferencia se plantea en relación con el tratamiento, ya que la PZ no es activa contra M. bovis y debe excluirse de cualquier esquema terapéutico.
Epidemiológicamente, los tres casos presentan distintos ejemplos de cómo puede adquirirse está zoonosis; el contacto con animales, domésticos o salvajes, el antecedente de exposición laboral (trabajadores en contacto con ganado, frigoríficos e industrias derivadas, veterinarios) y la ingestión de alimentos lácteos o derivados sin pasteurizar. Estos factores de riesgo deben orientar a la posibilidad de una tuberculosis humana por M. bovis. El microorganismo puede ingresar por inhalación a partir de aerosoles en ambientes contaminados o animales infectados, generando una TBB pulmonar, o por ingestión a partir de productos contaminados (leche y derivados) provocando formas extrapulmonares predominantemente linfáticas (cuello y axilas)(10); la transmisión humano-humano, aunque puede ocurrir, no es relevante. En los casos presentados existe una fuerte correlación entre la enfermedad y la exposición o la ingesta de alimentos lácteos no pasteurizados. La forma de presentación y la buena respuesta al tratamiento, sin la aparición de complicaciones u otras infecciones concomitantes, son características en pacientes inmunocompetentes; aunque raros, existen casos descriptos de TBB y VIH/SIDA(11), tal como ocurrió en uno de nuestros casos. El antecedente de contagio puede ser lejano en el tiempo ya que, al igual que en la TBH, después de la infección el microorganismo puede mantenerse latente durante años.
Discusión
La incidencia de la TBB (aunque es dificil estimarla correctamente) es muy baja en relación con la TBH, por lo que, en principio, todo paciente con tuberculosis debe ser considerado como caso de TBH hasta la identificación exacta de la especie de micobacteria aislada. Su forma de presentación y evolución son similares, pudiendo progresar, como en uno de los casos presentados, hacia formas neurológicas graves. Esta zoonosis está directamente relacionada con el grado de infección por M. bovis en animales de cría, especialmente en ganado bovino. Se estima que de los 374 millones de cabezas de ganado existentes en Latinoamérica y el Caribe, 70% radica en lugares donde las tasas de infección superan el 1%(12). En la región, solamente Ecuador, Brasil, Venezuela y Argentina han registrado casos de TBB; en este último país las cifras se sitúan entre 0,3% y 1% del total de casos de tuberculosis(5). Una publicación reciente(13) establece una prevalencia de 0,4% de M. bovis entre los casos de tuberculosis confirmados en Buenos Aires; el factor de riesgo más importante fue la exposición de carácter ocupacional. Reportes uruguayos confirman la presencia del patógeno a nivel de ganado; entre los años 1997 y 2010, 61,9% de los aislamientos de micobacterias en muestras ambientales o de animales correspondió a M. bovis(14). Según recomendaciones (Kantor y colaboradores)(15), las medidas para disminuir la tuberculosis de origen bovino en humanos deberían enfocarse en:
En consecuencia, los servicios de Salud Pública deberían orientarse a la detección de casos de TBB y al incremento de las medidas de protección y prevención en personas especialmente expuestas.
Summary
The study describes the first three cases of pulmonary tuberculosis caused by Mycobacterium bovis in Uruguay. One of the infected people had a history of being in contact with zoo animals, another one, an HIV carrier, was in daily contact with meat by-products, and the third one had a history of drinking unpasteurized milk. Molecular biology techniques and conventional bacteriology enabled the confirmation of the etiology in all cases. In spite of the systematic search for M. bovis in the clinical samples analysed in our laboratories, no isolation of Mycobacterium bovis from human cases had been reported until then. The presence of this microorganism in our veterinary samples during the last decade indicates we may continue to see new cases in immune competent people and HIV/AIDS patients. A history of close contact with animals, particularly bovines, with meat by-products, or both should warn clinicians about the possibility of this zoonosis, whose treatment should exclude pyrazinamide.
Resumo
]]> Os três primeiros casos de tuberculose pulmonar por Mycobacterium bovis no Uruguai são descritos. Um dos pacientes apresentava antecedentes de contacto com animais em um zoológico; o outro, portador de VIH, estava em contacto cotidiano com derivados de carne de gado bovino e o terceiro tinha antecedentes de ingestão de leite não pasteurizada. Foi possível confirmar a etiologia em todos os casos pela utilização de rotina de técnicas de biologia molecular juntamente com bacteriologia convencional. Apesar de que se realiza pesquisa sistemática de M. bovis nas amostras clínicas que chegam ao nosso laboratório, até esta oportunidade não havia sido possível registrar isolamentos de origem humano. A presença deste micro-organismo em amostras veterinárias na última década permite esperar o surgimento de novos casos em pessoas imunocompetentes e pacientes VIH/SIDA. O antecedente de contacto próximo com animais, especialmente gado bovino, ou com seus derivados, ou ambos, deve alertar o clínico sobre a possibilidade da presença desta zoonose em cujo tratamento a pirazinamida deve ser excluída.Bibliografía
1. Thoen CO, Lobue PA, Enarson DA, Kaneene JB, de Kantor IN. Tuberculosis: a re-emerging disease in animals and humans. Vet Ital 2009, 45(1):135-81.
2. Biet F, Boschiroli ML, Thorel MF, Guilloteau LA. Zoonotic aspect of Mycobacterium bovis and Mycobacterium avium-intracellulare complex (MAC). Vet Res 2005; 36(3):411-36.
3. O'Reilly LM, Daborn CJ. The epidemiology of Mycobacterium bovis infections in animals and man: a review. Tuber Lung Dis 1995; 76(Suppl 1):1-46.
4. Cosivi O, Grange JM, Daborn CJ, Raviglione MC, Fujikura T, Cousins D, et al. Zoonotic tuberculosis due to Mycobacterium bovis in developing countries. 1998. Emerg Infect Dis 1998; 4(1):59-70
5. de Kantor IN, Ambroggi M, Poggi S, Morcillo N, Da Silva Telles MA, Osório Ribeiro M, et al. Human Mycobacterium bovis infection in ten Latin America countries. Tuberculosis (Edinb) 2008; 88(4):358-65.
6. Djelouadji Z, Raoult D, Daffé M, Drancourt M. A single step sequencing method for the identification of Mycobacterium tuberculosis complex species. PLoS Negl Trop Dis 2008; 2(6):e253.
7. Coitinho C, Greif G, Robello C, van Ingen J, Rivas C. Identification of Mycobacterium tuberculosis complex by polymerase chain reaction of Exact Tandem Repeat-D fragment from mycobacterial cultures. Int J Mycobacteriol 2012; 1 (3):146-8.
8. Warren RM, Gey van Pittius NC, Barnard M, Hesseling A, Engelke E, de Kock M, et al. Differentiation of Mycobacterium tuberculosis complex by PCR amplification of genomic regions of difference. Int J Tuberc Lung Dis. 2006; 10(7):818-22.
9. Wedlock DN, Skinner MA, de Lisle GW, Buddle BM. Control of Mycobacterium bovis infections and the risk to human populations. Microbes Infect 2002; 4(4):471-80.
10. Moda G, Daborn CJ, Grange JM, Cosivi O. The zoonotic importance of Mycobacterium bovis. Tuber Lung Dis 1996; 77(2):103-8.
11. Valerga M, Viola C, Thwaites A, Bases O Ambroggi M, Poggi S, Marino R. Tuberculosis por Mycobacterium bovis en una mujer con SIDA. Rev Argen Microbiol 2005; 37(2):96-8.
12. de Kantor IN, Rittaco V. An update on bovine tuberculosis programmes in Latin American And Caribbean countries. Vet Microbiol 2006; 112(2-4):111-8.
13. Cordova E, Gonzalo X, Boschi A, Lossa M, Robles M, Poggi S, et al. Human Mycobacterium bovis infection in Buenos Aires: epidemiology, microbiology and clinical presentation. Int J Tuberc Lung Dis 2012; 16(3):415-7.
14. Castro Ramos M. Más de tres décadas de diagnóstico de tuberculosis y micobacteriosis animal en Uruguay. In: Primeiro Encontro de Saúde Animal. Santa María, Brasil: Comité de Saúde Animal de AUGM, 2010.
15. de Kantor IN, Paolicchi F, Bernardelli A, Torres PM, Canal A, Lobo JR, et al. Bovine Tuberculosis in Latin American Countries: current situation and recommendations. Workshop sponsored by OIE, 3rd Latin American Congress on Zoonoses. Buenos Aires, Argentina, June 19, 2008. Disponible en: http://www.rramericas.oie.int/in/proyectos/zoonosis/in_tuberculosis_recomendaciones_ago.html. [Consulta: 25 de mar de 2012].
]]>