
Expresión tumoral de HER-2, receptores de estrógenos y de progesterona y su relación con características clínico-patológicas en pacientes uruguayas con cáncer de mama
Dres. Lucía Delgado*, Rodrigo Fresco†, Guianeya Santander‡, Sergio Aguiar§, Natalia Camejo¶, Liliana Ferrero††, Valeria González‡‡, Silvina Heinzen§§, Andrea Martínez¶¶, Samantha Mauriz†††, Carlos Meyer‡‡, Gustavo Sena†††, Gonzalo Spera¶, Luis Ubillos††, Franco Xavier¶, Hugo Deneo‡‡‡, Marta Aghazarian§§§, Robinson Rodríguez¶¶¶, Graciela Sabini††††
Departamento e Institución responsables: Servicio de Oncología Clínica. Hospital de Clínicas "Dr. Manuel Quintela". Universidad de la República. Montevideo, Uruguay
Resumen
Introducción: el cáncer de mama (CM), principal causa de muerte por cáncer en la mujer uruguaya, constituye una enfermedad heterogénea. El estudio de la expresión tumoral del receptor del factor de crecimiento epidérmico-2 (HER2), el receptor de estrógenos (RE) y el receptor de progesterona (RP) permite reconocer subtipos con diferentes características clínico-patológicas y evolutivas.
Objetivos: conocer el perfil de expresión tumoral de HER2, RE y RP y su relación con características clínico-patológicas en pacientes uruguayas con CM.
Material y método: se revisaron las historias clínicas de pacientes intervenidas quirúrgicamente por CM invasivo en un período de dos años, seleccionándose las que contaban con la determinación de RE, RP y HER2 mediante inmunohistoquímica. Se comparó el perfil de expresión de estos marcadores con la edad al diagnóstico, tipo y grado histológico (GH) y estadio patológico (TNM).
]]> Resultados: se seleccionaron 197 pacientes cuyas características fueron edad media: 55 años, carcinoma ductal: 85%, GH 1-2: 59%, estadio: I-II: 75%, metástasis axilares: 51%, RE/RP+: 78%, HER2+: 10%. Se definieron tres subtipos: HER2- RE/RP+ (73%), HER2+ (10%) y triple negativo (TN) (17%). Los subtipos TN y HER2+ se asociaron con mayor grado histológico (p<0,05) y el TN con menor edad al diagnóstico (p<0,05) que el subtipo HER2-, RE/RP+.Conclusiones: el porcentaje de pacientes con CM invasivo subtipo HER2+ (10%) es menor que el reportado por otros estudios (17%-28%). En concordancia con estudios previos, los subtipos TN y HER2+ se correlacionaron con tumores más indiferenciados y el TN se presentó en pacientes más jóvenes.
Palabras clave: NEOPLASIAS DE LA MAMA -2 patología.
RECEPTOR erbB-2 - análisis.
RECEPTORES ESTROGÉNICOS.
RECEPTORES DE PROGESTERONA.
Keywords: BREAST NEOPLASMS - pathology.
RECEPTOR erbB-2 - analysis.
RECEPTORS, ESTROGEN.
RECEPTORS, PROGESTERONE.
]]>* Prof. Agda. del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
† Prof. Adj. del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
‡ Asistente del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Oncóloga Médica del Servicio de Oncología del Hospital Central de las Fuerzas Armadas. Uruguay.
§ Ex Prof. Adj. del Servicio de Oncología Radioterápica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
¶ Médico Residente del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
†† Médico Residente de Oncología Médica del Instituto Nacional del Cáncer, ASSE. Uruguay.
‡‡ Médico Residente del Depto. de Oncología Clínica del CASMU. Uruguay.
§§ Asistente del Dpto. Básico de Medicina, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
¶¶ Ex Médico Residente del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
]]> ††† Postgrado de Oncología Médica, Servicio de Oncología Clínica. Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.‡‡‡ Prof. Agdo. de la Cátedra de Anatomía Patológica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
§§§ Jefe del Departamento de Oncología Médica del Instituto Nacional del Cáncer, ASSE. Uruguay
¶¶¶ Jefe del Servicio de Oncología del Hospital Central de las Fuerzas Armadas. Médico especializado colaborador honorario del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
†††† Prof. Directora del Servicio de Oncología Clínica, Hospital de Clínicas, Facultad de Medicina, Universidad de la República. Uruguay.
Correspondencia: Dra. Lucía Delgado
Servicio de Oncología Clínica. Hospital de Clínicas
Avda. Italia s/n. CP 11600. Montevideo, Uruguay
Correo electrónico: ldelgado@hc.edu.uy
Recibido: 12/4/10.
]]> Aceptado: 2/8/10.Conflicto de intereses: los autores declaran que no existen conflictos de intereses.
Introducción
En nuestro país el cáncer de mama es la principal causa de muerte por cáncer en la mujer y, con exclusión del cáncer de piel no melanoma, es el cáncer más frecuente en el sexo femenino, dando cuenta de aproximadamente 1.800 casos nuevos y 600 muertes por año(1,2).
A pesar de los adelantos en el diagnóstico precoz y el desarrollo de tratamientos más efectivos, hasta 40% de las pacientes con cáncer de mama temprano recaerán y fallecerán a causa de la enfermedad(3). Más aun, pacientes que se presentan con un mismo estadio al diagnóstico pueden tener una evolución muy diferente(3).
]]> En los últimos años se han realizado avances significativos en la comprensión de esta heterogeneidad en la historia natural del cáncer mamario. En particular, la atención se ha centrado en la identificación de marcadores biológicos pronósticos y predictivos de la respuesta al tratamiento. En este sentido, la identificación de la proteína HER2 codificada por el oncogén erbB2 y su validación como marcador pronóstico y predictivo de la respuesta a terapias dirigidas y otros tratamientos sistémicos, ha complementado la información aportada por la determinación del receptor de estrógeno (RE) y del receptor de progesterona (RP) contribuyendo significativamente a ajustar el pronóstico y el tratamiento de las pacientes con cáncer mamario(3,4). El advenimiento de la tecnología de los microarreglos ha hecho posible el estudio del perfil de expresión génica (incluyendo la expresión de HER2, RE y RP), estableciéndose clasificaciones moleculares de la enfermedad(5-13). Así, en función de dicho perfil, es posible reconocer al menos cuatro subtipos biológicos de cánceres mamarios con características clínicas, patológicas y moleculares diversas, distinto pronóstico y manejo terapéutico. Estos han sido denominados luminal-A (HER2-, RE/RP+ y Ki67 bajo, entre otros marcadores), luminal-B (HER2-, RE/RP+ y Ki67 alto, entre otros marcadores), HER2-símil (HER2+, RE/RP+ o RE/RP-) y basal símil (KER2, RE-, RP)(5,13,14).Dada la complejidad y el alto costo de los estudios del perfil de expresión génica, se ha investigado la relación entre los subtipos moleculares y los subtipos que resultan de la combinación de HER2, RE y RP estudiados mediante inmunohistoquímica (IHQ), encontrándose una buena correlación entre la clasificación molecular y la IHQ(6,14,15). Esta última, además de tener valor pronóstico y predictivo, tiene un costo sensiblemente menor y se encuentra disponible para la práctica clínica estándar.
Es así que en la práctica clínica, la combinación de la expresión tumoral de estos tres marcadores ha pasado a tener papel pronóstico al menos tan importante como los clásicos factores pronósticos clínico-patológicos, a lo que se agrega su valor predictivo de la respuesta de varios tratamientos.
En el presente estudio el cáncer mamario fue clasificado en tres subtipos en base a la expresión tumoral positiva o negativa por IHQ de HER2, RE y RP:
1) HER2-, RE/RP+ = RE+/RP+, HER2-; RE-/RP+,Her2-; RE+/RP-, HER2-
2) HER2+ = RE+/RP+, HER2+; RE-/RP+, HER2+; RE+/RP, HER2+ RE-/RP-, HER2+
3) RE-, RP-, HER2- (triple negativo).
Son escasos los estudios latinoamericanos que han estudiado la frecuencia de sobreexpresión de HER2 en pacientes con CM(16-25). Por otra parte, sólo hemos encontrado un estudio latinoamericano, realizado en Brasil(25), dirigido a investigar la frecuencia de los subtipos de CM resultantes de la combinación de la expresión tumoral de HER2, RE y RP y la relación entre dichos subtipos y características clínico-patológicas de la enfermedad.
Objetivos
Estudiar en pacientes uruguayas la frecuencia de los subtipos de cáncer mamario definidos en base a la expresión tumoral de HER2, RE y RP evaluada mediante IHQ y comparar las características clínico-patológicas de los distintos subtipos.
]]> Material y métodoSe revisaron las historias clínicas de pacientes de sexo femenino que fueron intervenidas quirúrgicamente por cáncer de mama invasivo estadio I-III, entre marzo de 2006 y marzo de 2008, en los servicios de oncología de las instituciones de Montevideo en las que se desempeñan los autores, seleccionándose los casos con determinación de RE, RP y HER2 en el tumor primario. Se obtuvieron los siguientes datos: edad, tipo histológico, grado histológico, tamaño tumoral patológico, estado de los ganglios linfáticos axilares, estadio de acuerdo con la clasificación TNM(26) y estatus de HER2, RE y RP estudiados mediante IHQ.
Todos los estudios de IHQ fueron realizados como parte del trabajo rutinario de los departamentos de anatomía patológica de las instituciones donde se asistieron las pacientes. Los receptores de estrógenos y progesterona se determinaron mediante anticuerpos monoclonales y con el sistema de detección provisto por el fabricante. Los resultados de la inmunomarcación fueron considerados positivos cuando se informó inmunotinción nuclear en >1% de las células tumorales.
El nivel de sobreexpresión de HER2 fue determinado mediante Herceptest® (Dako, Carpinteria, CA, USA) en 95% de los casos. Los informes de los resultados de la inmunomarcación para HER2 se basaron en las recomendaciones vigentes en el período en que fueron estudiadas las pacientes, clasificándose los mismos en cuatro grados: 0, ausencia de tinción de membrana; 1+, tinción de membrana parcial y débil; 2+, tinción de membrana completa y débil en menos de 10% de las células cancerosas invasivas; 3+, tinción de membrana completa e intensa en más de 10% de las células cancerosas invasivas. Se consideró positivo el resultado con imnunotinción 3+.
En todos los análisis estadísticos se utilizó GraphPad InStat3 para Windows. Las diferencias en las características clínico-patológicas entre los distintos subtipos fueron analizadas utilizando análisis de varianza (ANOVA) para las variables cuantitativas y mediante chi-cuadrado/test exacto de Fisher de dos extremos para las variables categóricas. Se consideró estadísticamente significativo un valor de p<0,05.
El manejo de los datos se realizó manteniendo el anonimato de las pacientes.
Resultados
El análisis incluyó 197 pacientes de sexo femenino con cáncer de mama invasivo, 74 (38%) asistidas en el Instituto Nacional del Cáncer; 48 (24%) en el Hospital Central de las Fuerzas Armadas; 47 (24%) en el Centro de Asistencia del Sindicato Médico del Uruguay (CASMU), y 28 (14%) en el Hospital de Clínicas. Con respecto a la zona geográfica, procedieron de Montevideo 185 de las 197 pacientes (94%).
La edad media fue 55 años (DS: 11.55; rango: 24-85 años), siendo 67% mayor de 50 años. El resto de las características se muestra en la tabla 1. Aproximadamente la mitad de las pacientes presentó características clínico-patológicas favorables, tales como un pequeño tamaño tumoral (T<2cm: 46%), ganglios linfáticos axilares negativos (51%) y grado histológico bajo o intermedio (59%). Además, RE o RP, o ambas, fueron positivos en 78% de los casos.
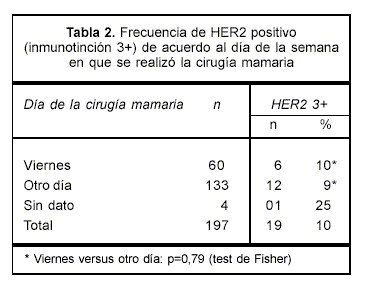
El resultado de la IHQ para la expresión tumoral de HER2 fue positivo (inmunomarcación 3+) solamente en 10% de las pacientes. No se observaron diferencias significativas en el porcentaje de HER2 3+ entre las instituciones participantes (Fisher, p=0,45). Dado que el tiempo de fijación de la pieza tumoral puede influir en el resultado de la IHQ se comparó la frecuencia de HER2 3+ en las pacientes intervenidas quirúrgicamente los viernes (probabilidad de fijación durante más de 48 horas) con la frecuencia de las que fueron intervenidas otros días de la semana, no observándose diferencias estadísticamente significativas (p=0,79) (tabla 2).
]]>
De las 197 pacientes, 144 (0,73) fueron HER2-, RE/RP+, 19 (0,10) fueron HER2+ y el resto (0,17) fueron clasificadas como triple negativas, es decir HER2-, ER/PR- (tabla 3).
Las diferencias en las características clínico-patológicas entre los tres subtipos se muestran en la tabla 4.
La edad al diagnóstico fue menor en las pacientes con el subtipo TN que en las pacientes con el subtipo HER2-, RE/RP+ (p<0,05). Además, el subtipo TN se asoció con mayor probabilidad de edad <40 años al diagnóstico (0,24) que el subtipo HER2+ (0,16) y el HER2-, RE/RP+ (0,10) (p=0,0268).

Se observó una asociación estadísticamente significativa entre el subtipo, el tipo histológico (p=0,0082) y grado histológico (p=<0,0001). La probabilidad de presentar tumores de tipo ductal infiltrante fue menor en las pacientes con el subtipo HER2-, RE/RP+ (80%) que en las pacientes con subtipo HER2+ (100%; p=0,0462) y TN (97%, p=0,0186). La casi totalidad (28/29) de los carcinomas de otra variedad histológica, en su mayor parte lobulillares (18/28), fueron observados en el subtipo HER2- RE/RP+.
Las pacientes con el subtipo HER2-, RE/RP+ tuvieron mayor probabilidad de tener tumores bien o moderadamente diferenciados (68%) que las pacientes con subtipo HER2 (26%; p=0,0016) y TN (41%, p=0,0013). Más aun, la frecuencia relativa de tumores grado histológico I fue 0,20 en el subtipo HER2-, RE/RP+, 0,10 en el subtipo HER2+ y 0 en el subtipo TN (p=0,035, test de chi-cuadrado).
No se encontró relación entre el subtipo tumoral y el resto de las características estudiadas (estadio, tamaño tumoral y estado de los ganglios linfáticos axilares).
Discusión
Nuestros resultados muestran diferencias estadísticamente significativas en algunas características clínicas y patológicas entre los tres subtipos definidos en base a la expresión tumoral de HER2, RE y RP mediante IHQ.
]]> La edad al diagnóstico fue menor en las pacientes con el subtipo TN y la proporción de pacientes menores de 40 años fue mayor entre las portadoras de dicho subtipo. Estos resultados son concordantes con los obtenidos en estudios previos que han incluido pacientes hispanas(27,28).Por otra parte, la probabilidad de presentar tumores de tipo ductal infiltrante y tumores pobremente diferenciados (grado histológico III) fue mayor en las pacientes con CM subtipo TN o HER2+, lo cual está de acuerdo con la mayor agresividad biológica de estos subtipos y es concordante con los hallazgos de estudios previos(15-25,27,28).
Con respecto a las posibles diferencias en el tamaño del tumor primario, el estado de la axila y el estadio TNM entre los subtipos definidos mediante estudio de IHQ, los reportes previos muestran resultados diversos(15,28). En el presente estudio no se encontraron diferencias significativas entre los distintos subtipos cuando se comparó la frecuencia de los estadios I-III, el tamaño tumoral y el estado de la axila.
En relación con la prevalencia de cada uno de los tres subtipos analizados, encontramos una frecuencia de tumores HER2 + por IHQ (inmunotinción 3+) inferior a la reportada en la literatura(15-25,28). En efecto, tanto en estudios europeos y norteamericanos como en estudios realizados en países de Latinoamérica, la prevalencia encontrada –con excepción de un estudio que reportó una frecuencia de 17%(24)– es igual o mayor a 20%(15-25,28). Por el contrario, la frecuencia de tumores RE/RP+ fue similar a la reportada en estudios previos, incluidos los datos de nuestro país(15-25,28-32).
Es bien sabido que además del umbral utilizado para interpretar un test como positivo, los principales factores que pueden afectar la exactitud y reproducibilidad de los estudios de IHQ son el tipo y la duración de la fijación del tejido y el anticuerpo utilizado(33). Así, además de la utilización de formol tamponado, para el estudio de HER2 se recomienda fijación durante más de 6 horas y menos de 48 horas(34).
Todos los estudios IHQ correspondientes a las pacientes incluidas en el presente estudio fueron realizados utilizando un tipo de fijación adecuada (formol tamponado). En relación con la duración de la fijación, considerando que en el caso de las pacientes intervenidas quirúrgicamente los viernes ésta podría ser superior a 48 horas, se comparó la prevalencia de estudios positivos observada en las pacientes intervenidas los viernes con la observada en las pacientes intervenidas otros días de la semana, no encontrándose diferencias significativas. Con respecto a los anticuerpos utilizados, se usó Herceptest en 95% de los casos. En consecuencia, los factores mencionados no parecen explicar el bajo porcentaje de pacientes con tumores HER2+ encontrados en nuestra serie.
Dado que tanto la edad y la raza han sido identificadas como factores predictores independientes del subtipo de CM(28,29), corresponde analizar si el bajo porcentaje observado en nuestro estudio podría explicarse por la selección de la muestra. En efecto, las pacientes incluidas son las que contaban con la determinación de RE/RP y también de HER2, lo cual puede introducir un sesgo tanto en relación con la extensión lesional como a la edad, ya que las pacientes con axila negativa y tumor primario <1 cm y las más añosas, no candidatas a tratamiento con terapias dirigidas contra HER2, podrían no contar con la determinación de la expresión tumoral de HER2. Dado que los estudios realizados muestran que el porcentaje de pacientes con tumores HER2 positivos es mayor en las pacientes con cáncer de mama estadio II y III y en las pacientes jóvenes(15,28,29), estos posibles sesgos no explicarían el bajo porcentaje de CM HER2+ encontrado en nuestro estudio.
Por último, es importante considerar que la sobreexpresión de HER2 se debe en general a amplificación del gen y que si bien se ha reportado una fuerte asociación entre la sobreexpresión de la proteína determinada por IHQ y la ampificación del gen determinada por FISH ("fluorescence in situ hybridization"), la tasa de discordancia puede alcanzar hasta 20%, predominando los falsos positivos(33). En efecto, el porcentaje de falsos positivos y falsos negativos para HER2 por IHQ versus HER2 por FISH puede alcanzar 22% y 9%, respectivamente(33). Así, si la expresión tumoral de HER2 se hubiera estudiado mediante FISH en todas nuestras pacientes y asumiéramos hasta 9% de falsos negativos y 0% de falso positivos, el porcentaje de HER2 positivos podría haber alcanzado 14%, porcentaje aun inferior al reportado en los estudios que evaluaron la expresión tumoral de HER2 mediante IHQ(15-25).
La prevalencia de los otros dos subtipos fue ligeramente superior a la reportada en población caucásica e hispana. De forma concordante con reportes previos en dichas poblaciones, la frecuencia de TN encontrada en nuestro estudio fue claramente inferior a la observada en población afro-americana(15-25,27-29).
Conclusiones
]]> Nuestros resultados muestran una prevalencia menor de sobreexpresión de HER2 en los cánceres mamarios invasivos de pacientes uruguayas que en las de pacientes de otros países, tanto europeos y norteamericanos como latinoamericanos. Por el contrario, la prevalencia de cánceres mamarios invasivos RE y RP positivos es similar.De acuerdo con estudios previos, el subtipo TN se asoció con menor edad al diagnóstico y al igual que el subtipo HER2+ con mayor grado histológico, lo cual es concordante con la mayor agresividad biológica de ambos subtipos.
Summary
Introduction: breast cancer, the main cause of death of Uruguayan women, is an heterogeneous disease. Study of the tumoral expression of the Human Epidermal growth factor Receptor-2 (HER2), the estrogen receptor and the progesterone receptor enables the recognition of sub-types with different clinical, and pathological characteristics and evolution.
Objectives: to learn about the HER2, estrogen receptor and progesterone receptor tumoral expression profile and their relationship with clinical-pathological characteristics in Uruguayan patients with breast cancer.
Method: we reviewed the medical record of patients who underwent surgery for invasive breast cancer within a two year period, and we selected those who had determination of estrogen receptor, progesterone receptor and HER2 through immune-histochemestry. We compared the expression profile of these markers with the age at the time of diagnosis, the histological type and degree and the pathological status.
Results: we selected 197 patients with the following characteristics: average age: 55 years old, ductal carcinoma: 85%, histological degree 1-2: 59%; stage I-II: 75%, axillary metastasis: 51%, progesterone receptor/estrogen receptors+ (RE/RP+): 78%, HER2+: 10%. Three subtypes were defined: HER2- RE/RP+ (73%), HER2+ (10%) and triple negative (TN) (17%). Subtypes TN and HER2+ were associated with a greater histological degree (GH) (p<0,05) and the TN with lower age at the time of diagnosis than the HER2-, RE/RP+ subtype.
Conclusions: the percentage of patients with HER2+ subtype invasive breast cancer (10%) is lower than the one reported in others studies. In accordance with previous studies, TN and HER2+ subtypes correlated with less differentiated tumors and TN subtype occurred in younger patients
Résumé
Introduction: le cancer de sein (CS), principal responsable de mort par cancer des uruguayennes, est une maladie hétérogène. L’étude de l’expression tumorale du récepteur du facteur de croissance épidermique 2 (HER-2), le récepteur d’oestrogène (RE) et le récepteur de progestérone (RP) permet de reconnaître des sous-types à caractéristiques cliniques pathologiques et évolutives variées.
]]> Objectif: connaître le profil de expression tumorale de HER-2, RE et RP et leur lien avec des données cliniques pathologiques chez des patientes uruguayennes atteintes de cancer de sein.Matériel et méthode: on fait la révision clinique des patientes atteintes de CS ayant subi une intervention chirurgicale pour une période de deux ans, choisissant celles portant la détermination de HER-2, RP et RE par immunohistochimie. On compare le profil de manifestation de ces marqueurs à l’âge au diagnostic, type et degré histologique (GH) et stade pathologique (TNM).
Résultats: 197 patientes furent sélectionnées dont voici les caractéristiques: 55 ans (moyenne), 85% carcinome ductal, 59% GH 1-2; 75% stade I- II; 51% métastase axillaire; 78% RE-RP +; 10% HER2+; trois sous-types furent définis: HER2- RE/RP+ (73%), HER2+ (10%) et triple négatif (TN) (17%).
Les sous-types TN et HER2+ furent associés à un degré histologique plus grand (p<0,05) et le TN à un âge plus bas au diagnostic (p<0,05) que le sous-type HER2-, RE/RP+.
Conclusions: le pourcentage de patientes avec CM invasif sous-type HER2+ (10%) est inférieur à celui reporté par d’autres études (17%-28%). En concordance avec des études préalables, les sous-types TN y HER2+ ont été mis en relation avec des tumeurs plus indifférenciées et le TN a été présent chez des patientes plus jeunes.
Resumo
Introdução: o câncer de mama (CM), principal causa de morte por câncer em mulheres uruguaias, é uma doença heterogênea. O estudo da expressão tumoral do receptor do fator de crescimento epidérmico-2 (HER2), do receptor de estrógeno (RE) e do receptor de progesterona (RP) permite reconhecer subtipos com diferentes características clínico-patológicas e de evolução.
Objetivos: conhecer o perfil de expressão tumoral de HER2, RE e RP e sua relação com as características clínico-patológicas em pacientes uruguaias com CM.
Material e método: os prontuários de pacientes submetidas a cirurgia por CM invasivo em um período de dois anos foram revisados. Foram selecionadas as que incluíam a determinação de RE, RP e HER2 por imuno-histoquímica. O perfil de expressão destes marcadores foi comparado com a idade no momento do diagnóstico, tipo e grau histológico (GH) e estádio patológico (TNM).
Resultados: foram selecionadas 197 pacientes cujas características eram idade media: 55 anos, carcinoma ductal: 85%, GH 1-2: 59%, estádio: I-II: 75%, metástases axilares: 51%, RE/RP+: 78%, HER2+: 10%. Foram definidos três subtipos: HER2- RE/RP+ (73%), HER2+ (10%) e triplo negativo (TN) (17%). Os subtipos TN e HER2+ estavam associados a um maior grau histológico (p<0,05) e o TN com menor idade no momento do diagnóstico (p<0,05) que o subtipo HER2-, RE/RP+.
]]> Conclusões: a porcentagem de pacientes com CM invasivo subtipo HER2+ (10%) é menor que o informado por outros estudos (17%-28%). No entanto houve concordância com estudos anteriores nos quais os subtipos TN e HER2+ estavam correlacionados com tumores mais indiferenciados e o TN em pacientes más jovens.Bibliografía
1. Comisión Honoraria de Lucha contra el Cáncer. Programa Vigilancia Epidemiológica. Registro Nacional de Cáncer. Informe Anual 2008. Disponible en: http://www.urucan.org.uy/uilayer/informe_2008.pdf (Consulta: 5/7/2010).
2. Comisión Honoraria de Lucha contra el Cáncer. Programa Vigilancia Epidemiológica. Registro Nacional de Cáncer. Tendencias de la mortalidad por cáncer de mama en mujeres 2002-2005.
3. Conzen SD, Grushko TA, Olopade OI. Cancer of the breast. In: Devita VT, Hellman S, Rosenberg SA, eds. Cancer: principles and practice of oncology. 8th ed. Philadelphia: Lippincott, 2008: 1595-605.
4. Nielsen DL, Andersson M, Kamby C. HER2-targeted therapy in breast cancer. Monoclonal antibodies and tyrosine kinase inhibitors. Cancer Treat Rev 2009; 35(2): 121-36.
5. Sotiriou C, Pusztai L. Gene-expression signatures in breast cancer. N Engl J Med 2009; 360(8): 790-800.
6. van de Vijver MJ, He YD, van’t Veer LJ, Dai H, Hart AA, Voskuil DW, et al. A gene-expression signature as a predictor of survival in breast cancer. N Engl J Med 2002; 347(25): 1999-2009.
7. Liu R, Wang X, Chen GY, Dalerba P, Gurney A, Hoey T, et al. The prognostic role of a gene signature from tumorigenic breast-cancer cells. N Engl J Med 2007; 356(3): 217-26.
8. Sørlie T, Perou CM, Fan C, Geisler S, Aas T, Nobel A, et al. Gene expression profiles do not consistently predict the clinical treatment response in locally advanced breast cancer. Mol Cancer Ther 2006; 5(11): 2914-8.
9. Carey LA, Perou CM, Livasy CA, Dressler LG, Cowan D, Conway K, et al. Race, breast cancer subtypes, and survival in the Carolina Breast Cancer Study. JAMA 2006; 295(21): 2492-502.
]]>10. Dolled-Filhart M, Rydén L, Cregger M, Jirström K, Harigopal M, Camp RL, et al. Classification of breast cancer using genetic algorithms and tissue microarrays. Clin Cancer Res 2006; 12(21): 6459-68.
11. Chang HY, Nuyten DS, Sneddon JB, Hastie T, Tibshirani R, Sørlie T, et al. Robustness, scalability, and integration of a wound-response gene expression signature in predicting breast cancer survival. Proc Natl Acad Sci USA 2005; 102(10): 3738-43.
12. Sorlie T, Tibshirani R, Parker J, Hastie T, Marron JS, Nobel A, et al. Repeated observation of breast tumor subtypes in independent gene expression data sets. Proc Natl Acad Sci USA 2003; 100(14): 8418-23.
13. Perou CM, Sørlie T, Eisen MB, van de Rijn M, Jeffrey SS, Rees CA, et al. Molecular portraits of human breast tumours. Nature 2000; 406(6797): 747-52.
14. Huber KE, Carey LA, Wazer DE. Breast cancer molecular subtypes in patients with locally advanced disease: impact on prognosis, patterns of recurrence, and response to therapy. Semin Radiat Oncol 2009; 19(4): 204-10.
]]>15. Onitilo AA, Engel JM, Greenlee RT, Mukesh BN. Breast cancer subtypes based on ER/PR and Her2 expression: comparison of clinicopathologic features and survival. Clin Med Res 2009; 7(1-2): 4-13.
16. Morales L, Reigosa A, Caleiras E, Mora R, Marrero N, Payares E, et al. Expresión del HER2/neu en pacientes venezolanas con cáncer de mama localmente avanzado. Invest Clin 2008; 49(1): 69-78.
17. Colón E, Reyes JS, González Keelan C, Climent-Peris C. Prevalence of steroid receptors and HER 2/neu in breast cancer biopsies of women living in Puerto Rico. P R Health J 2002; 21(4): 299-303.
18. Crabtree BE, Neme YY, Rivera S, Olivares G. Receptores hormonales, HER-2/neu y p53 en pacientes con cáncer de mama. GAMO 2005; 4(2): 29-33.
19. Brück P, Vilches Cisneros N, Ramos López E, Barboza Quintana O, Ancer Rodríguez J, Flores Gutiérrez JP. Expresión de Her2-neu en el adenocarcinoma ductal de la glándula mamaria: correlación con parámetros histopatológicos y expresión de receptores estrogénicos en pacientes mexicanas. Ginecol Obstet Mex 2006; 74(10): 516-22.
]]>20. Peredo R, Sastre G, Serrano J, Hunter Mellado R. Her-2/neu oncogene expression in Puerto Rican females with breast cancer. Cell Mol Biol (Noisy-le-grand) 2001; 47(6): 1025-32.
21. Gouvêa AP, Milanezi F, Olson SJ, Leitao D, Schmitt FC, Gobbi H. Selecting antibodies to detect HER2 overexpression by immunohistochemistry in invasive mammary carcinomas. Appl Immunohistochem Mol Morphol 2006; 14(1): 103-8.
22. González-Muller. Características patológicas asociadas al carcinoma de mama HER-2 positivo. An Fac Med Lima 2005; 66(2): 89-99.
24. Álvarez Goyanes R, Escobar Pérez X, Camacho Rodríguez R, Franco Odio S, de Armas Fernández M, Ropero Toirac R, et al. Prevalencia de HER2 en el cáncer de mama en Cuba. Cancerología 2009; 4: 135-41.
25. Fernandes RC, Bevilacqua JL, Soares IC, Siqueira SA, Pires L, Hegg R, et al. Coordinated expression of ER, PR and HER2 define different prognostic subtypes among poorly differentiated breast carcinomas. Histopathology 2009; 55(3): 346-52.
]]>26. American Joint Committee on Cancer. AJCC Cancer Staging Manual. 6th ed. New York: Springer, 2002.
27. Bauer KR, Brown M, Cress RD, Parise CA, Caggiano V. Descriptive analysis of estrogen receptor (ER)-negative, progesterone receptor (PR)-negative, and HER2-negative invasive breast cancer, the so-called triple-negative phenotype: a population-based study from the California cancer Registry. Cancer 2007; 109(9): 1721-8.
28. Parise CA, Bauer KR, Brown MM, Caggiano V. Breast cancer subtypes as defined by the estrogen receptor (ER), progesterone receptor (PR), and the human epidermal growth factor receptor 2 (HER2) among women with invasive breast cancer in California, 1999-2004. Breast J 2009; 15(6): 593-602.
29. Kwan ML, Kushi LH, Weltzien E, Maring B, Kutner SE, Fulton RS, et al. Epidemiology of breast cancer subtypes in two prospective cohort studies of breast cancer survivors. Breast Cancer Res 2009; 11(3): R31.
30. Artagaveytia N. Alteraciones moleculares vinculadas al proceso de transformación maligna de la glándula mamaria: Implicancias en la evolución clínica del cáncer mamario. 2006. Tesis de Doctorado de ProInBio.
]]>31. Sabini G, Delgado L, Suárez L, Musé IM. Cáncer de mama localizado. In: Musé IM, Viola A, Sabini G, eds. Aspectos prácticos de la Clínica Oncológica. Montevideo: Sudamericana, 2004: 235-50.
32. Vázquez T, Krygier G, Barrios E, Cataldi S, Vázquez A, Alonso R, et al. Análisis de sobrevida de una población con cáncer de mama y su relación con factores pronósticos: estudio de 1.311 pacientes seguidas durante 230 meses. Rev Med Urug 2005; 21(2): 107-21.
33. Press MF, Sauter G, Bernstein L, Villalobos IE, Mirlacher M, Zhou JY, et al. Diagnostic evaluation of HER-2 as a molecular target: an assessment of accuracy and reproducibility of laboratory testing in large, prospective, randomized clinical trials. Clin Cancer Res 2005; 11(18): 6598-607.
34. Wolff AC, Hammond ME, Schwartz JN, Hagerty KL, Allred DC, Cote RJ, et al. American Society of Clinical Oncology/College of American Pathologists guideline recommendations for human epidermal growth factor receptor 2 testing in breast cancer. J Clin Oncol 2007; 25(1): 118-45.