Recomendaciones para la prevención y el tratamiento de náuseas y vómitos inducidos por quimioterapia
Dres. Rodrigo Fresco*, Liliana Suárez‡
Resumen
Las náuseas y los vómitos son uno de los efectos adversos más frecuentes de la quimioterapia, y uno de los más temidos por los pacientes. El adecuado control de la emesis aguda y tardía redunda en una mejor calidad de vida y una mayor adhesión de los pacientes al tratamiento. A pesar de disponerse actualmente de estrategias antieméticas más efectivas, es frecuente su empleo inadecuado ya sea por su sobre o subutilización.
El objetivo de este trabajo es establecer guías precisas para la prevención y el tratamiento de náuseas y vómitos inducidos por quimioterapia, aplicables a nuestro medio, procurando mantener una adecuada relación costo-beneficio.
]]> Los factores de riesgo para las náuseas y vómitos inducidos por quimioterapia son dependientes del paciente y dependientes del tratamiento, siendo la emetogenicidad propia del plan de quimioterapia el más importante. En las situaciones de alto riesgo de náuseas y vómitos inducidos por quimioterapia (cisplatino, ciclofosfamida, adriamicina, entre otras), la combinación de un antagonista 5HT3 más corticoide previene más efectivamente la emesis aguda que otras combinaciones previamente empleadas. En la profilaxis de la emesis tardía no se ha demostrado la superioridad del uso de antagonistas 5HT3, por lo que su mayor costo no justifica su empleo inicial. En las situaciones de riesgo intermedio (5-Fu, taxanos, etopósido) el tratamiento con corticoides o metoclopramida sería suficiente, no recomendándose de inicio profilaxis de la emesis tardía. Para las situaciones de bajo riesgo (bleomicina, vinca) no se sugiere profilaxis de náuseas y vómitos inducidos por quimioterapia. Los antieméticos vía oral son igualmente efectivos que los intravenosos, por lo que por su costo y su conveniencia serían de preferencia.Palabras clave: emesis - prevención y control.
NÁUSEA - prevención y control.
quimioterapia - efectos adversos.
antieméticos.
* Asistente de Oncología Médica, Servicio de Oncología Clínica, Facultad de Medicina.
‡ Especialista en Oncología Médica. Asistente de Oncología Médica, Servicio de Oncología Clínica, Facultad de Medicina.
Correspondencia: Dr. Rodrigo Fresco
Cont. Echevarriarza 3535/408, CP 11.300. Montevideo, Uruguay.
E-mail: rfresco@hc.edu.uy
]]> Recibido: 16/10/03.Aceptado luego de modificaciones: 16/3/04.
Introducción
El manejo eficaz de náuseas y vómitos inducidos por quimioterapia (NVIQT) representa un desafío en el tratamiento del paciente con cáncer. La tendencia a utilizar regímenes quimioterápicos combinados cada vez más agresivos en ocasiones permite obtener mejores resultados terapéuticos, pero frecuentemente a costo de una mayor toxicidad.
En algunos casos el oncólogo tratante y el personal de enfermería tienden a minimizar el posible impacto de las NVIQT en la calidad de vida del paciente, fundamentalmente en lo que se refiere a las náuseas y los vómitos tardíos, es decir aquellos que aparecen luego de las 24 horas de administrada la quimioterapia. Contrariamente, desde la perspectiva del paciente, los vómitos fueron históricamente considerados el efecto secundario más severo de la quimioterapia(1). Los pacientes que experimentan NVIQT refieren, además, sufrir más anorexia, insomnio y fatiga que aquellos que no los experimentan(2), y en los casos más graves este efecto adverso puede hacer que el paciente no complete una quimioterapia potencialmente curativa. Además, un inadecuado manejo de las NVIQT puede precipitar la aparición de complicaciones potencialmente fatales como deshidratación, desequilibrios hidroelectrolíticos, síndrome de Mallory-Weiss, neumonía aspirativa, entre otras.
Globalmente, 70%-80% de los pacientes que reciben quimioterapia y no reciben antieméticos experimentarán NVIQT(3). Con tratamiento antiemético estos porcentajes disminuyen en forma considerable, pero la incidencia de náuseas continúa siendo significativa. De los pacientes, 50%-75% experimentan náuseas y 25%-55% vómitos luego de la quimioterapia, a pesar de un tratamiento antiemético eficaz(4,5). La alta frecuencia de este efecto adverso y sus posibles consecuencias determinan que su profilaxis y tratamiento sean una parte integral del manejo de los pacientes que reciben quimioterapia. El conocimiento del adecuado control de las mismas no sólo es fundamental para el oncólogo y hematólogo sino también para el internista, médico general, médico de familia, cirujano, etcétera.
Adicionalmente, debe tenerse en cuenta que el hecho de que un paciente que está recibiendo quimioterapia presente náuseas y vómitos no necesariamente implica que tenga NVIQT. Las náuseas y los vómitos pueden estar causados por hipertensión endocraneana, hipercalcemia, oclusión intestinal, etcétera, así como por causas más comunes como gastritis aguda, gastroenteritis, etcétera. Por lo tanto, debe pensarse en causas adicionales a las NVIQT en todo paciente oncológico que presente emesis, particularmente cuando las características de la misma no son las típicas de la emesis posquimioterapia.
Varios factores han contribuido a los avances terapéuticos en el área de las NVIQT, incluyendo el mejor conocimiento de la fisiopatología de la emesis, el reconocimiento del valor del tratamiento antiemético combinado de la necesidad de tratamientos específicos y diferenciales para la emesis aguda y la emesis tardía, y fundamentalmente el desarrollo de nuevos fármacos entre los que se destacan los antagonistas de los receptores de serotonina (antagonistas 5-HT3).
El más efectivo control de los vómitos con estos agentes determinó que estos dejaran de ser considerados por los pacientes el efecto adverso más severo y preocupante. Sin embargo, las náuseas pasaron a ocupar el primer lugar entre más de 70 síntomas físicos y no físicos experimentados por quienes reciben quimioterapia(4). Esto es debido, al menos en parte, a que los antagonistas 5HT3 han mejorado la prevención y el tratamiento de las náuseas y vómitos agudos pero su eficacia es menor en el control de las náuseas y los vómitos tardíos.
]]> A pesar de disponerse actualmente de estrategias antieméticas más efectivas que en el pasado, es frecuente su empleo inadecuado ya sea por su sobre o subutilización. Por lo tanto, el establecimiento de guías precisas para la prevención y el tratamiento de las NVIQT, aplicables en nuestro medio, se podrá traducir en un beneficio para los pacientes así como en una adecuada relación costo-beneficio.Clasificación de las NVIQT
Emesis aguda
Se define como las náuseas y los vómitos que ocurren en las primeras 24 horas luego de la administración de la quimioterapia. Con la mayoría de los agentes éstas comienzan 1-2 horas luego del tratamiento; sin embargo, con algunos fármacos es posible la aparición de la emesis aguda a las 9-18 horas luego de recibir la quimioterapia (por ejemplo, carboplatino, ciclofosfamida)(6).
Emesis tardía
]]> Se define como las náuseas y los vómitos que ocurren más allá de las 24 horas de la administración de la quimioterapia, pueden persistir por 6-7 días. El cisplatino es el fármaco que más frecuentemente produce este efecto. En ausencia de profilaxis, 65%-90% de los pacientes que reciben este cisplatino presentarán emesis tardía(7). Otros agentes como ciclofosfamida, carboplatino y adriamicina también tienen potencial de producir náuseas y vómitos tardíos en un tercio de los pacientes(8). Su reconocimiento y adecuado tratamiento son fundamentales para mejorar la tolerancia y adhesión a la quimioterapia.Emesis anticipatoria
En general comienza dentro de las 24 horas previas a la realización de la quimioterapia. Se ha reportado que luego del tercer o cuarto ciclo, 20%-40% de los pacientes presentan emesis anticipatoria(9).
Factores de riesgo
Varios factores propios del paciente, de la enfermedad y del tratamiento han sido descritos como de riesgo para la aparición de NVIQT. Indudablemente que el principal de ellos es el potencial emetógeno del plan de quimioterapia(10).
Emesis aguda: los factores que se han asociado con un mayor riesgo de emesis aguda incluyen: 1) náuseas y vómitos con ciclos o planes de quimioterapia previamente administrados; 2) pacientes menores de 50 años; 3) sexo femenino; 4) ausencia de historia de ingesta crónica y abundante de alcohol (por ejemplo, 100 g/día durante varios años); 5) antecedentes de emesis gravídica(8,11). El subgrupo de pacientes de mayor riesgo de NVIQT sería el de las mujeres jóvenes.
Emesis tardía: el principal factor de riesgo es el inadecuado control de la emesis aguda. En consecuencia, los factores que predisponen a la emesis aguda pueden considerarse también factores de riesgo de emesis tardía. La ausencia de náuseas y vómitos en las primeras 24 horas es un indicador de una baja probabilidad de emesis tardía. Por su parte, aquellos pacientes que presentan náuseas y vómitos tardíos durante el primer ciclo de quimioterapia, tienen mayor riesgo de presentarlos en los siguientes ciclos(12).
]]> Emesis anticipatoria: al igual que la emesis tardía, el principal factor de riesgo de la emesis anticipatoria es el pobre control de las náuseas y los vómitos agudos. La presencia de emesis posquimioterapia es un factor de riesgo de emesis anticipatoria, la cual rara vez se ve en pacientes que no han experimentado náuseas y vómitos postratamiento(8). El adecuado control de la emesis aguda, particularmente durante el primer ciclo de quimioterapia administrado, tiene un impacto favorable en la incidencia y severidad de la emesis anticipatoria(8,12).Fisiopatología de las NVIQT
La fisiopatología exacta de las NVIQT no es conocida. Los sistemas involucrados en la respuesta emética a los diferentes estímulos incluyen al sistema nervioso central (SNC), el tracto gastrointestinal y el sistema vestibular. Tradicionalmente, dos áreas del SNC han sido involucradas en la respuesta emética: 1) el centro del vómito, ubicado en la formación reticular lateral del bulbo, y 2) la zona de activación de quimiorreceptores ubicada en el piso del cuarto ventrículo cerca del área postrema. Esta última se encuentra fuera de la barrera hematoencefálica, y su estimulación por sustancias químicas presentes en la sangre o en el líquido cefalorraquídeo produce señales que son transmitidas al centro del vómito. Otras fuentes de estimulación del centro del vómito son el sistema vestibular, la faringe, el tracto gastrointestinal y la corteza cerebral. Los centros corticales podrían tener un papel relevante en la fisiopatología de la emesis anticipatoria(13). Estudios recientes han identificado un tercer área del SNC que está involucrada en la respuesta emética. Se trata del núcleo del tracto solitario, el cual se topografía en proximidad del área postrema y podría ser el principal área vinculada con la respuesta emética(14).
Los neurotransmisores involucrados en la fisiopatología de las NVIQT son dopamina, serotonina y sustancia P. Los primeros estudios se enfocaron en el papel del receptor dopaminérgico y llevaron al desarrollo de los antagonistas dopaminérgicos (por ejemplo, metoclopramida, domperidona). El uso de altas dosis de metoclopramida fue durante años el tratamiento estándar de las NVIQT. Sin embargo, en los años 1970 se observó que las altas dosis de este fármaco resultaban en una inhibición del receptor de serotonina más que del de dopamina. Esto llevó al desarrollo de los antagonistas de los receptores de serotonina, los cuales inhiben el receptor 5-HT3(13,15,16).
Los agentes quimioterápicos determinan la liberación de serotonina a partir de las células enterocromafines del tracto gastrointestinal, la cual estimula los receptores 5-HT3 de las aferencias vagales y esplácnicas cercanas. Este estímulo alcanza entonces el centro del vómito a través de aferentes vagales. El receptor 5-HT3 también ha sido identificado en al área postrema.
Más recientemente, los inhibidores del receptor NK-1 han demostrado resultados prometedores en el tratamiento de las NVIQT(17). Esto sugiere que la sustancia P, el ligando natural del receptor NK-1, también tiene un papel relevante en la respuesta emética.
La fisiopatología de la emesis tardía ha sido mucho menos estudiada y, por lo tanto, es menos comprendida. La serotonina no tendría un papel relevante en la fisiopatología de la emesis tardía, lo cual es apoyado por el hecho de que los antagonistas 5-HT3 son poco efectivos para su manejo. Factores inflamatorios intestinales podrían estar involucrados en su fisiopatología. Se ha visto, además, que los antagonistas del receptor NK-1 son efectivos para el control de la emesis tardía, por lo que la sustancia P también podría estar implicada en su patogenia(17).
Respecto a la emesis anticipatoria, se piensa que se trata de una respuesta condicionada vinculada con factores visuales, gustativos, olfatorios o ambientales, asociados con una quimioterapia administrada previamente.
]]> Clasificación de los agentes quimioterápicos según su emetogenicidadLa posibilidad de predecir adecuadamente el riesgo individual de presentar NVIQT permite adecuar el tratamiento para cada caso particular. Como mencionamos, el principal factor relacionado con el riesgo de emesis es la emetogenicidad propia del agente quimioterápico, a lo que se agrega la dosis empleada y el esquema de administración. Es así que la administración intravenosa en bolo suele asociarse con una mayor frecuencia de náuseas y vómitos que las infusiones prolongadas o los agentes quimioterápicos orales.
En el pasado se han desarrollado varios sistemas de clasificación de los agentes quimioterápicos según su potencial emetogénico, la mayoría de ellos con limitaciones importantes(18,19).
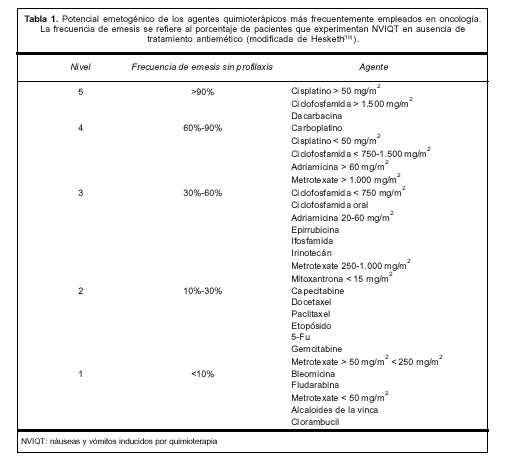
Hesketh desarrolló el sistema de clasificación más aceptado actualmente(10). Esta clasificación considera los efectos de la dosis, su ruta de administración, así como la emetogenicidad intrínseca de cada agente. Este sistema asigna cada uno de los agentes quimioterápicos a uno de cinco niveles de emetogenicidad. Cada nivel define el riesgo de emesis aguda en ausencia de una profilaxis antiemética efectiva (tabla 1).
Uno de los mayores aportes de la clasificación de Hesketh respecto a las anteriores es la posibilidad de predecir la emetogenicidad de los planes de poliquimioterapia. Frente a las combinaciones de fármacos se sugiere seguir los siguientes pasos: 1) identificar el fármaco con mayor nivel de emetogenicidad; 2) determinar la contribución de los otros agentes del plan según el siguiente esquema: a) los agentes del nivel 1 no contribuyen a la emetogenicidad del plan, b) el uso de uno o más agentes del nivel 2 incrementa la emetogenicidad del plan en un nivel, c) la adición de agentes de los niveles 3-4 incrementa la emetogenicidad del plan en un nivel por cada agente (tabla 2). A modo de ejemplo, la emetogenicidad del plan AC (ciclofosfamida 600 mg/m2 más adriamicina 60 mg/m2) es: 3 por la ciclofosfamida más 1 por el agregado de la adriamicina (es decir un fármaco del nivel 3), lo cual suma un punto adicional a la emetogenicidad del plan, la cual es entonces de 4. Por lo tanto, en ausencia de tratamiento antiemético se estima que 60%-90% de los pacientes que reciben este plan presentarán NVIQT (tabla 3).
En vista a simplificar las recomendaciones, los agentes y planes de la categoría 5 se clasifican como de alto riesgo de emesis, los de las categorías 4 y 3 como de moderado riesgo emético, y los de las categorías 2 y 1 como de bajo riesgo(10,12).
]]> Debe tenerse en cuenta que este y otros sistemas de clasificación tienen como objetivo predecir el riesgo de emetogenicidad aguda por lo que no deben aplicarse en la predicción del riesgo de emesis tardía.
Prevención y tratamiento de las NVIQT
El objetivo ideal de cualquier tratamiento antiemético es prevenir en forma completa la aparición de náuseas y vómitos. Varios estudios han demostrado que sólo el control absoluto de las NVIQT se correlaciona con la completa satisfacción de los pacientes respecto al control emético(20). Lamentablemente, a pesar de los avances observados en los últimos 20 años, este objetivo es difícil de alcanzar y como se mencionó, las náuseas continúan siendo un efecto adverso frecuente y preocupante en los pacientes que reciben quimioterapia(4).
Emesis aguda
Durante muchos años, los principales agentes farmacológicos para la prevención y el tratamiento de las náuseas y los vómitos agudos han sido los antagonistas dopaminérgicos, antihistamínicos, corticoesteroides, canabinoides y las benzodiacepinas. Si bien estos agentes ofrecen cierto grado de eficacia, también pueden causar efectos secundarios considerables. Desde la aparición de los antagonistas de los receptores de serotonina se dispone de una nueva clase de agentes con una mayor eficacia y menor frecuencia y severidad de efectos adversos.
]]> Numerosos estudios han confirmado la superioridad de estos fármacos en comparación con los antagonistas dopaminérgicos en el tratamiento de la emesis aguda inducida por quimioterapia con riesgo emético alto y moderado(21-24). Un beneficio adicional de los antagonistas 5-HT3 es el mantenimiento de su eficacia durante ciclos sucesivos de quimioterapia. Ha sido demostrada una disminución de la eficacia de la combinación metoclopramida y dexametasona con ciclos repetidos de quimioterapia(25), efecto que no se ha observado con la combinación de un corticoesteroide y un antagonista 5-HT3(26).A dosis equivalentes, los cuatro antagonistas 5-HT3 existentes (ondansetrón, granisetrón, dolasetrón, tropisetrón) son igualmente efectivos en la prevención de la emesis inducida por quimioterapia moderada o altamente emetizante, y la decisión de cuál utilizar debe basarse en su disponibilidad, conveniencia, costo y perfil de efectos adversos (el tropisetrón no está disponible en nuestro medio)(27-31). La tabla 4 muestra las dosis recomendadas de cada agente para la profilaxis de la emesis aguda. El uso de dosis menores a las recomendadas puede derivar en un inadecuado control de las NVIQT(8).
Varios ensayos randomizados han demostrado la equivalencia terapéutica entre las dosis únicas prequimioterapia de ondansetrón, dolasetrón y granisetrón y los esquemas multidosis a lo largo de las primeras 24 horas luego de la quimioterapia(5.32). Esto se asocia a una mayor conveniencia para el paciente y personal de salud, menor probabilidad de efectos adversos, y una mejor relación costo-beneficio. Además, a dosis biológicamente equivalentes, los preparados orales son igualmente eficaces que los intravenosos y se asocian a un menor costo y una más fácil administración(33,34).
En líneas generales, estos agentes comparten sus efectos adversos, representados fundamentalmente por cefalea leve, constipación, astenia, somnolencia y elevación reversible de las transaminasas. Sin embargo, existen algunos efectos adversos particulares para cada fármaco que deben ser tenidos en cuenta. El ondansetrón se asocia más frecuentemente que los otros fármacos del mismo grupo a efectos a nivel del SNc (alteraciones visuales, mareos)(33), mientras que el dolasetrón produce más frecuentemente que el granisetrón y ondansetrón efectos cardiovasculares. Entre éstos se destacan cambios electrocardiográficos, particularmente prolongación de los intervalos PR y QT(30,31), los cuales si bien en la mayoría de los casos son asintomáticos, determinan que el dolasetrón deba emplearse con precaución en pacientes con hipopotasemia, hipomagnesemia o cualquier otra condición que incremente el intervalo QT, así como en aquellos que reciben antiarrítmicos u otros fármacos que aumenten este intervalo.Adicionalmente, se ha demostrado que la combinación de antieméticos es más efectiva que la administración de agentes únicos. Esto es particularmente cierto para los planes con alto y moderado riesgo emético, donde la combinación de un antagonista 5-HT3 y un corticosteroide (usualmente dexametasona 20 mg intravenosa en dosis única prequimioterapia ([tabla 3]) logra un mejor control de la emesis aguda que cada agente por separado(23,35,36). Además, se ha demostrado que la combinación de un antagonista 5-HT3 y un corticosteroide es más eficaz que la de un corticosteroide con un antagonista dopaminérgico del tipo de la metoclopramida(36). Un estudio randomizado demostró una mayor eficacia y similar toxicidad con la dexametasona a dosis de 20 mg en comparación con dosis menores(37).
Otro grupo de agentes que se ha evaluado para la profilaxis y el tratamiento de las NVIQT son las benzodiacepinas. Estos fármacos tienen una actividad antiemética limitada y no deben ser empleados como agentes únicos. Debido a su acción ansiolítica pueden ser útiles en determinadas circunstancias particulares cuando son empleados en combinación con otros agentes más activos.
La tabla 5 resume las recomendaciones para la profilaxis de la emesis aguda inducida por quimioterapia según el riesgo de emetogenicidad del plan administrado.
Emesis tardía
]]> La emesis tardía suele ser más difícil de tratar que la emesis aguda. Debe tenerse en cuenta, además, que es un efecto adverso que usualmente el paciente experimenta en su domicilio, donde las posibilidades de control adecuado pueden ser menores y el impacto personal y familiar puede ser considerable. Por lo tanto, en todo caso en que exista riesgo de presentar náuseas y vómitos tardíos debe instruirse al paciente para el correcto uso de los fármacos antieméticos. Esto debe realizarse previo a la indicación del primer ciclo de quimioterapia dado que un adecuado control de las NVIQT disminuye el riesgo de emesis aguda, tardía y anticipatoria en los ciclos siguientes.Como mencionamos, la serotonina no jugaría un papel relevante en la patogenia de la emesis tardía. Por lo tanto, los antagonistas 5-HT3 no son tan efectivos para el control de este efecto adverso en comparación con su eficacia en el control de la emesis aguda.
Los corticoesteroides durante 3-4 días posquimioterapia parecen ser los agentes más activos para la prevención de la emesis tardía(31,38). Al igual que lo observado en la emesis aguda, la combinación de agentes antieméticos parece ser más efectiva que el uso de agentes únicos. La combinación de un antagonista 5-HT3 y corticoesteroide sería igualmente o menos efectiva que la de metoclopramida y dexametasona(39,40), por lo que por razones de costo esta última es de preferencia en la profilaxis y el tratamiento de la emesis tardía. Los antagonistas 5-HT3 estarían indicados como tratamiento de segunda línea cuando no se alcanza un buen control con la anterior combinación.
La tabla 5 resume las recomendaciones para la profilaxis de la emesis tardía inducida por quimioterapia según el riesgo de emetogenicidad del plan administrado.
Emesis anticipatoria
La mejor forma de prevenir la emesis anticipatoria es lograr un adecuado control de la emesis aguda y tardía. En caso de presentarse este efecto adverso, la terapia conductual puede ser efectiva(41).
]]> NVIQT a pesar de un tratamiento óptimoEs posible la aparición de NVIQT a pesar de una profilaxis y un tratamiento óptimos con las medidas anteriormente mencionadas. Este subgrupo de pacientes presenta un riesgo elevado de emesis anticipatoria, y si se han empleado los agentes más efectivos a dosis adecuadas es poco probable el control de las NVIQT en los siguientes ciclos de quimioterapia.
El manejo de estos pacientes representa un desafío particular. Descartadas otras causas que expliquen la presencia de náuseas y vómitos, en primer lugar debe revisarse si se empleó una estrategia antiemética apropiada en función del riesgo emetogénico del plan quimioterápico administrado. Si el paciente recibió una quimioterapia con bajo riesgo emetogénico debe emplearse un tratamiento antiemético similar a los recomendados para los pacientes de mayor riesgo. En quienes recibieron los fármacos por vía oral puede intentarse su administración por vía intravenosa, si bien no existe demostración que esto mejore los resultados. Dado que todos los antagonistas 5-HT3 tienen un mecanismo de acción similar es poco probable que la sustitución de un agente por otro de este grupo mejore significativamente el control de las NVIQT en ciclos posteriores.
En algunos casos particulares pueden realizarse modificaciones en el plan quimioterápico en vista a disminuir la severidad de las NVIQT. Entre estas estrategias se incluyen la sustitución de algún fármaco por otro igualmente efectivo pero menos emetogénico (por ejemplo, en algunos tumores sustituir cisplatino por carboplatino), y el alargamiento del tiempo de infusión de la quimioterapia. En el contexto adyuvante deben minimizarse las posibilidades de recaída por lo que se debe ser prudente con estas modificaciones para que no impacten negativamente en la eficacia de la quimioterapia. Contrariamente, en el contexto paliativo el énfasis debe ser puesto en la calidad de vida del paciente.
Conclusiones
El manejo de las NVIQT es un componente fundamental del tratamiento del paciente con cáncer y debe basarse fundamentalmente en la prevención más que en el tratamiento. El control efectivo de este efecto adverso permite una mejor calidad de vida del paciente, evita complicaciones potencialmente graves y facilita la adhesión al tratamiento quimioterápico.
La probabilidad de presentar NVIQT depende primariamente de la emetogenicidad intrínseca del plan de quimioterapia, por lo que la determinación precisa de la misma es fundamental para el manejo individual de cada paciente.
]]> La combinación de un antagonista 5-HT3 con un corticoesteroide es considerado actualmente el patrón de oro del tratamiento antiemético, alcanzando un control más efectivo de la emesis aguda inducida por quimioterapia altamente o moderadamente emetógena, con una mayor tolerabilidad en comparación con los planes basados en los antagonistas dopaminérgicos. El control efectivo de la emesis aguda reduce considerablemente el riesgo de emesis tardía y anticipatoria, cuyo manejo suele ser más dificultoso. En vista a disminuir los costos de atención oncológica, los antagonistas 5-HT3 administrados por vía oral alcanzan la misma eficacia que los intravenosos, con un menor costo y una mayor conveniencia.
Summary
Nausea and vomiting are among the most frequent adverse reactions of chemotherapy. Control of acute emesis and vomiting might improve quality of life and compliance to treatment. Althought many other anti-emetic strategies are more efficient, chemotherapy’s overuse and misuse are frequent.
The aim of the study is to determine precise and adjusted guidelines for the prevention and treatment of nausea and vomiting provoked by chemotherapy.
Emesis was the main risk factor for nausea and vomiting induced by chemotherapy. Like all risk factors, it depends on patients and treatment. A 5HT3 antagonist plus corticoid combination prevents acute emesis in situations at high risk for nausea and vomiting induced by chemotherapy (cisplatine, ciclofosfamide, adriamicine among others). 5HT3 antagonist for profilaxis of later emesis has not been proved as more efficient than other choices, its use –at least at the beginning of the treatment– is not recommended due to its high cost. Treatment with corticoids or metoclopramide is recommended for cases at intermediate risk (5-fu, taxane, eoposide). At low risk (belomicine, vinca) profilaxis of nausea and vomiting induced by chemotherapy is not suggested. Oral antiemetic is first-line choice because it is equally efficient than intravenous antiemetic, more convenient and availabe at low cost.
Résumé
]]> Les nausées et les vomissements sont parmi les effets adverses les plus fréquents de la chimiothérapie et parmi les plus redoutables chez les patients. Un bon contrôle de lémétie aigue et tardive détermine une meilleure qualité de vie et une plus grande collaboration du patient au traitement. Même si on dispose de stratégies antiémétiques plus efficaces, il est fréquent de voir qu’elles sont mal employées.Le but de ce travail est d’établir des guides précis pour la prévention et le traitement des nausées et des vomissements survenus par chimiothérapie, adaptés à notre réalité,tout en gardant une relation coût- bénéfice équilibrée.
Les facteurs de risque pour les nausées et les vomissements induits par chimiothérapie dépendent de chaque patient et du traitement, le plan chimiothéra-peutique restant le plus important. Dans les cas à plus grand risque de ces effets adverses (cisplatin, cyclo-phosphamide, adriamicine, entre autres) la combinaison d’un antagoniste 5HT3 plus corticoïde prévient plus efficacement les effets émétiques aigus que d’autres combinaisons avant utilisées. Pour les effets émétiques tardifs, on n’a pas prouvé la supériorité de l’emploi d’antagonistes 5HT3, si bien que son coût plus élevé ne justifie pas son emploi initiel. Dans les situations à risque moyen, (5-Fu, taxanos. Etoposide) le traitement avec corticoïdes ou métochlopramide suffirait, n’étant pas conseillable au début la prophylaxie des effets tardifs. Pour les situations à bas risque (bléomicine, vinca) on ne signale pas de prophylaxie des nausées et de vomissements induits par chimiothérapie. Les antiémétiques par la bouche sont aussi efficaces que par voie veineuse, et plus convenables par leur coût.
Bibliografía
1. Coates A, Abraham S, Kaye SB, Sowerbutts T, Frewin C, Fox RM, et al. On the receiving end—patient perception of the side-effects of cancer chemotherapy. Eur J Cancer Clin Oncol 1983; 19: 203-8.
2. Osoba D, Zee B, Warr D, Kaizer L, Latreille J, Pater J. Quality of life studies in chemotherapy-induced emesis. Oncology 1996; 53 (Suppl 1): 92-5.
3. Koski S, Venner P. Chemotherapy-induced nausea and vomiting. In: Nabholtz JM, Tonkin K, Aapro M, Buzdar A, ed. Breast cancer management: application of evidence to patient care. London: Martin Dunitz, 2000: 317-29.
4. Griffin AM, Butow PN, Coates AS, Childs AM, Ellis PM, Dunn SM, et al. On the receiving end. V: Patient perceptions of the side effects of cancer chemotherapy in 1993. Ann Oncol 1996; 7(2): 189-95.
5. Kaizer L, Warr D, Hoskins P, Latreille J, Lofters W, Yau J, et al. Effect of schedule and maintenance on the antiemetic efficacy of ondansetron combined with dexamethasone in acute and delayed nausea and emesis in patients receiving moderately emetogenic chemotherapy: a phase III trial by the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 1994; 12: 1050-7.
6. Osoba D, Warr DG, Fitch MI, Nakashima L, Warren B. Guidelines for the optimal management of chemotherapy-induced nausea and vomiting: a consensus. Can J Oncol 1995; 5: 381-400.
7. Kris MG, Gralla RJ, Clark RA. Incidence, course, and severity of delayed nausea and vomiting following the administration of high-dose cisplatin. J Clin Oncol 1985; 3: 1379-84.
8. Gralla RJ, Osoba D, Kris MG, Kirkbride P, Hesketh PJ, Lawrence WC, et al. Recommendations for the use of antiemetics: evidence-based, clinical practice guidelines. J Clin Oncol 1999; 17: 2971-94.
9. Boakes RA, Tarrier N, Barnes BW, Tattersall MH. Prevalence of anticipatory nausea and other side-effects in cancer patients receiving chemotherapy. Eur J Cancer 1993; 29A: 866-70.
10. Hesketh PJ. Defining the emetogenicity of cancer chemotherapy regimens: relevance to clinical practice. Oncologist 1999; 4: 191-6.
11. Gregory RE, Ettinger DS. 5-HT3 receptor antagonists for the prevention of chemotherapy-induced nausea and vomiting: a comparison of their pharmacology and clinical efficacy. Drugs 1998; 55: 173-89.
12. Schnell FM. Chemotherapy-induced nausea and vomiting: the importance of acute antiemetic control. Oncologist 2003; 8: 187-98.
13. Grunberg SM, Hesketh PJ. Control of chemotherapy-induced emesis. N Engl J Med 1993; 329: 1790-6.
14. Naylor RJ, Rudd JA. Mechanisms of chemotherapy/radiotherapy-induced emesis in animal models. Oncology 1996; 53 (Suppl 1): 8-17.
15. Andrews PL, Bhandari P. The 5-hydroxytryptamine receptor antagonists as antiemetics: preclinical evaluation and mechanism of action. Eur J Cancer 1998; 29A: S11-S16.
16. Cubeddu LX. Serotonin mechanisms in chemotherapy-induced emesis in cancer patients. Oncology 1996; 53 (Suppl 1): 18-25.
17. Hesketh PJ. Potential role of the NK1 receptor antagonists in chemotherapy-induced nausea and vomiting. Support Care Cancer 2001; 9(5): 350-4.
18. Laszlo J. Treatment of nausea and vomiting caused by cancer chemotherapy. Cancer Treat Rev 1982; 9 (Suppl B): 3-9.
19. Lindley CM, Bernard S, Fields SM. Incidence and duration of chemotherapy-induced nausea and vomiting in the outpatient oncology population. J Clin Oncol 1989; 7: 1142-9.
20. Aapro MS. Methodological issues in atiemetic studies. Invest N Drugs 1993; 11: 243-53.
21. Jantunen IT, Flander MK, Heikkinen MI, Kuoppala TA, Teerenhovi L, Kataja VV. Comparison of ondansetron with customary treatment in the prophylaxis of nausea and emesis induced by non-cisplatin containing chemotherapy. Acta Oncol 1993; 32: 413-5.
22. Jantunen IT, Kataja VV, Muhonen TT. An overview of randomised studies comparing 5-HT3 receptor antagonists to conventional anti-emetics in the prophylaxis of acute chemotherapy-induced vomiting. Eur J Cancer 1997; 33: 66-74.
23. Gebbia V, Testa A, Valenza R, Cannata G, Tirrito ML, Gebbia N. Oral granisetron with or without methylprednisolone versus metoclopramide plus methylprednisolone in the management of delayed nausea and vomiting induced by cisplatin-based chemotherapy. A prospective randomized trial. Cancer 1995; 76: 1821-8.
24. Navari RM, Province WS, Perrine GM, Kilgore JR. Comparison of intermittent ondansetron versus continuous infusion metoclopramide used with standard combination antiemetics in control of acute nausea induced by cisplatin chemotherapy. Cancer 1993; 72: 583-6.
25. Roila F, Tonato M, Basurto C. Protection from nausea and vomiting in cisplatin-treated patients: high-dose metoclopramide combined with methylprednisolone versus metoclopramide combined with dexamethasone and diphenydramine: study of the Italian Oncology Group for Clinical Research. J Clin Oncol 1989; 7: 1693-700.
26. Roila F. Control of acute cisplatin-induced emesis over repeat courses of chemotherapy. Italian Group for Antiemetic Research. Oncology 1996; 53 (Suppl 1): 65-72.
27. Gebbia V, Cannata G, Testa A, Curto G, Valenza R, Cipolla C, et al. Ondansetron versus granisetron in the prevention of chemotherapy-induced nausea and vomiting. Results of a prospective randomized trial. Cancer 1994; 74: 1945-52.
28. Beck TM, York M, Chang A, Navari R, Harvey WH, Meshad M, et al. Oral ondansetron 8 mg twice daily is as effective as 8 mg three times daily in the prevention of nausea and vomiting associated with moderately emetogenic cancer chemotherapy. S3A-376 Study Group. Cancer Invest 1997; 15: 297-303.
29. Bonneterre J, Hecquet B. Granisetron (IV) compared with ondansetron (IV plus oral) in the prevention of nausea and vomiting induced by moderately-emetogenic chemotherapy. A cross-over study. Bull Cancer 1995; 82: 1038-43.
30. Hesketh P, Navari R, Grote T, Gralla R, Hainsworth J, Kris M, et al. Double-blind, randomized comparison of the antiemetic efficacy of intravenous dolasetron mesylate and intravenous ondansetron in the prevention of acute cisplatin-induced emesis in patients with cancer. Dolasetron Comparative Chemotherapy-induced Emesis Prevention Group. J Clin Oncol 1996; 14: 2242-9.
31. Lofters WS, Pater JL, Zee B, Dempsey E, Walde D, Moquin JP, et al. Phase III double-blind comparison of dolasetron mesylate and ondansetron and an evaluation of the additive role of dexamethasone in the prevention of acute and delayed nausea and vomiting due to moderately emetogenic chemotherapy. J Clin Oncol 1997; 15: 2966-73.
32. Ettinger DS, Eisenberg PD, Fitts D, Friedman C, Wilson-Lynch K, Yocom K. A double-blind comparison of the efficacy of two dose regimens of oral granisetron in preventing acute emesis in patients receiving moderately emetogenic chemotherapy. Cancer 1996; 78: 144-51.
33. Perez EA, Hesketh P, Sandbach J, Reeves J, Chawla S, Markman M, et al. Comparison of single-dose oral granisetron versus intravenous ondansetron in the prevention of nausea and vomiting induced by moderately emetogenic chemotherapy: a multicenter, double-blind, randomized parallel study. J Clin Oncol 1998; 16: 754-60.
34. Clavel M, Bonneterre J, d’Allens H, Paillarse JM. Oral ondansetron in the prevention of chemotherapy-induced emesis in breast cancer patients. French Ondansetron Study Group. Eur J Cancer 1995; 31A: 15-9.
35. Goedhals L, Heron JF, Kleisbauer JP, Pagani O, Sessa C. Control of delayed nausea and vomiting with granisetron plus dexamethasone or dexamethasone alone in patients receiving highly emetogenic chemotherapy: a double-blind, placebo-controlled, comparative study. Ann Oncol 1998; 9: 661-6.
36. Heron JF. Single-agent granisetron for the prevention of acute cisplatin-induced emesis: a double-bind, randomized comparison with granisetron plus dexamethasone and high-dose metoclopramide plus dexamethasone. Semin Oncol 1995; 22 (4 Suppl 10): 24-30.
37. Italian Group for Antiemetic Research. Double-blind, dose-finding study of four intravenous dosis of dexamethasone in the prevention of cisplatin-induced acute emesis. J Clin Oncol 1998; 16: 2937-42.
38. Koo WH, Ang PT. Role of maintenance oral dexamethasone in prophylaxis of delayed emesis caused by moderately emetogenic chemotherapy. Ann Oncol 1996; 7: 71-4.
]]>39. Campora E, Giudici S, Merlini L, Rubagotti A, Rosso R. Ondansetron and dexamethasone versus standard combination antiemetic therapy. A randomized trial for the prevention of acute and delayed emesis induced by cyclophosphamide-doxorubicin chemotherapy and maintenance of antiemetic effect at subsequent courses. Am J Clin Oncol 1994; 17: 522-6.
40. Italian Group for Antiemetic Research. Ondansetron versus metoclopramide, both combined with dexamethasone in the prevention of cisplatin-induced delayed emesis. J Clin Oncol 1997; 15: 124-30.
41. Morrow GR, Morrell C. Behavioral treatment for the anticipatory nausea and vomiting induced by cancer chemotherapy. N Engl J Med 1982; 307: 1476-80.