
Dres. Rosario Goyetche*, Adriana Pérez*, Gretel Morena†,
Gonzalo Pérez†, Gustavo Giachetto‡, María Catalina Pírez§,
Ivonne Rubio¶, Alicia Montano¶, Ana Ferrari¶
Clínicas Pediátricas "A", "B", "C". Hospital Pediátrico,
Centro Hospitalario Pereira Rossell. Facultad de Medicina, Montevideo. Uruguay
Resumen
Introducción: en diciembre de 2001 se realizó la primera campaña de vacunación masiva con VA-MENGOCC-BCR en Uruguay. En la ciudad de Santa Lucía (departamento de Canelones) se vacunaron 5.366 niños de 2 a 19 años de edad. Esta vacuna es considerada inocua; las principales reacciones adversas notificadas son locales.
Objetivos: determinar la prevalencia y el tipo de reacciones adversas a la vacuna VA-MENGOCC-BCR en esta población.
Material y método: se tomó una muestra simple al azar por rango de muestreo de 744 niños. El registro de las reacciones adversas luego de la primera y segunda dosis se realizó a través de encuesta personal o telefónica 30 días luego de cada dosis.
]]> Resultados: se evaluaron 728 niños (98% de la muestra). El 53% (IC95 53% + 3,6) desarrolló algún tipo de reacción adversa: 30% luego de la primera dosis, 5% luego de la segunda dosis y 18% luego de la primera y segunda dosis. No presentó ninguna reacción adversa 47% (IC95 47% + 3,6). Se notificaron 659 reacciones adversas, 71% locales y 29% sistémicas. Entre las reacciones locales el dolor fue la más frecuente (55%) y entre las sistémicas el decaimiento (30%).Conclusiones: la prevalencia de reacciones adversas en esta población fue 53% (IC95 53% + 3,6). No se observó ninguna reacción adversa severa. Estos resultados coinciden con lo descrito en otras series.
Palabras clave: VACUNA ANTIMENINGOCOCICA BC - efectos adversos.
* Estudiantes del curso de posgrado de Pediatría.
† Estudiante del curso de posgrado de Pediatría.
‡ Pediatras tutores (Santa Lucía).
‡ Prof. Adjunto Clínica Pediátrica, Prof. Adjunto Farmacología y Terapéutica.
§ Prof. Agregada Clínica Pediátrica.
¶ Prof. Directora Clínica Pediátrica.
Correspondencia: Dra. Rosario Goyetche, Clínica Pediátrica "C".
]]> Dr. Gustavo Giachetto, Clínica Pediátrica "A", Hospital Pediátrico Centro Hospitalario Pereira Rossell, Br. Gral. Artigas 1550.Montevideo, Uruguay.
E-mail: rousi@adinet.com.uy
Recibido: 5/9/03.
Aceptado:12/3/04.
Introducción
La vacuna antimeningocócica de origen cubano VA-MENGOCC-BCR del Instituto Finlay está constituida por proteínas mayoritarias de la membrana externa del meningococo B y polisacárido capsular de meningococo C, purificados, conjugados y absorbidos en un gel de hidróxido de aluminio. Se trata de un conjugado no covalente donde la fuerza de asociación está en la estructura del proteoliposoma formado por proteínas, lipopolisacáridos y fosfolípidos. Esta asociación le confiere a la vacuna un carácter bivalente dado que estos dos elementos estimulan de manera independiente la protección contra la enfermedad(1-3).
La cepa de meningococo B utilizada en la elaboración de esta vacuna es la CU385, B: P1:15:L3,7,9; DNA secuencia subtipo P1.19.15. Dicha cepa circuló en Cuba durante la epidemia de 1976(3).
La vacuna se administra por vía intramuscular profunda en la región deltoidea; 0,5 ml en dos dosis con un intervalo de seis a ocho semanas(3).
]]> Esta vacuna ha sido administrada fundamentalmente en forma de campañas por decisión de los ministerios de Salud de distintos países, como medida de acción frente al incremento del número de casos de la enfermedad(1).En Uruguay, en los últimos años, se ha observado un cambio en la epidemiología de la enfermedad meningocócica, con descenso de los casos correspondientes al serogrupo C y predominio de los casos del serogrupo B. En diciembre de 2001 se realizó una campaña de vacunación masiva con VA-MENGOCC-BCR en una localidad de 16.000 habitantes (Santa Lucía, departamento de Canelones) donde se detectaron eventos que alertaron sobre la posibilidad de un brote epidémico por meningococo grupo B, con predominio de la cepa B: 4, 7:P1.15,19(4).
Esta fue la primera vacunación masiva con la vacuna cubana realizada en Uruguay. Esta vacuna es considerada inocua dado el tipo de componentes y su naturaleza purificada. Se describen reacciones adversas principalmente locales(5-8).
Este estudio se realizó con el objetivo de determinar la prevalencia y el tipo de reacciones adversas a la vacuna VA-MENGOCC-BCR en la población incluida en esta campaña.
Material y método
Se evaluaron en forma prospectiva los efectos adversos de la vacuna antimeningocócica BC de origen cubano, aplicada en dos dosis a intervalo de ocho semanas por personal especializado en inmunizaciones a una población de 5.366 niños y adolescentes de 2 a 19 años de edad de la ciudad de Santa Lucía.
Se tomó una muestra simple al azar por rango de muestreo de 744 niños. Para el cálculo del tamaño muestral se utilizó el programa Statcalc Epi Info 6, teniendo en cuenta una prevalencia esperada de reacciones adversas de 10%, un peor resultado aceptado de 8% y un intervalo de confianza de 95%.
El registro de las reacciones adversas luego de la primera y segunda dosis se realizó a través de encuesta personal o telefónica. La recolección de datos se realizó 30 días luego de cada dosis. La información fue obtenida por médicos posgrados de pediatría y pediatras previamente entrenados, en una ficha precodificada.
Se consideró reacción adversa toda manifestación local o sistémica, o ambas, relacionada temporalmente con la administración de la vacuna (hasta 21 días posvacunación); habiéndose descartado enfermedad intercurrente(9-11).
Las reacciones adversas fueron clasificadas como:
]]> 1. Locales: aquellas limitadas al sitio de aplicación de la vacuna.Dolor: se consideró cuando produjo dificultad para la movilización del brazo o requirió analgésicos.
a) Tumefacción e induración.
b) Eritema.
2. Sistémicas: aquellas no limitadas al sitio de aplicación.
a) Fiebre: temperatura axilar > 38ºC.
b) Somnolencia: tendencia no habitual al sueño o dificultad para despertarse, o ambas.
c) Decaimiento.
d) Irritabilidad y llanto: alteraciones de la conducta, llanto inconsolable por más de tres horas.
e) Cefaleas: fue considerada en niños mayores de 4 años y sólo cuando no se acompañó de fiebre.
]]> f) Erupción cutánea.g) Reacción anafiláctica.
h) Púrpura.
i) Síndrome hipotónico - hiporreactivo: disminución del tono muscular con trastorno de la conciencia una hora después de la vacunación.
Resultados
No se pudieron evaluar las reacciones adversas en 16 niños debido a cambios de dirección o teléfono, o ambos. Se incluyeron en el estudio 728 niños (98% de la muestra), 363 mujeres y 365 varones. La media de edad fue 10 años. La distribución de la población por edades fue: 2 a 3 años 11%, 4 a 11 años 51% y 12 a 19 años 38%.
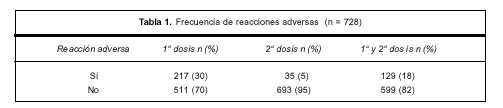
Fueron evaluados en forma telefónica 603 niños y en forma personal 125. No presentaron ninguna reacción adversa a la vacuna 345 niños (47%, IC95 47% + 3,6). Desarrollaron algún tipo de reacción adversa en las primeras 24 horas luego de la administración 383 niños (53%, IC95 53% + 3,6): 217 (30%) luego de la primera dosis, 35 (5%) luego de la segunda dosis y 129 (18%) luego de ambas dosis (tabla 1). En ningún caso las reacciones adversas se prolongaron más allá de 48 horas.
La distribución de las reacciones adversas por grupos etarios se muestra en la tabla 2. Los niños mayores de 3 años fueron los que presentaron más efectos adversos.
Se notificaron 659 reacciones adversas, 469 (71%, IC95 71% + 1,68) locales y 190 (29%, IC95 29% + 1,68) sistémicas. Entre las reacciones locales el dolor fue la más frecuente (55%) y entre las sistémicas, el decaimiento (30%) (tabla 3).
De las reacciones locales, 42% ocurrió luego de la primera dosis, 27% luego de la segunda y 31% luego de ambas. De las reacciones sistémicas, 46% ocurrió luego de la primera dosis, 2% luego de la segunda y 33% luego de ambas.
]]>
Discusión
Cuando una vacuna es lanzada al mercado ha pasado por distintas etapas de evaluación experimental en animales y seres humanos. Los estudios previos a su autorización y registro incluyen ensayos clínicos controlados randomizados que evalúan su eficacia. Estos estudios permiten, además, identificar efectos adversos comunes que ocurren en un período corto de tiempo luego de la vacunación. En general permiten conocer los efectos más frecuentes (>1%). Sin embargo, son insuficientes para identificar efectos adversos más raros y graves que pueden ocurrir más tardíamente(12).
Es necesario continuar con la farmacovigilancia del producto una vez comercializado para poder determinar la prevalencia de los efectos adversos en cada población y evaluar su efectividad.
La asociación causal entre la vacuna y los efectos adversos es difícil de determinar; no se dispone de tests específicos. La notificación espontánea de casos, el seguimiento de series de casos y los estudios de factores de riesgo constituyen la forma de conocer la seguridad de la vacuna y el riesgo de la población(12-15).
Este estudio constituye la primera evaluación de los efectos adversos de la vacuna VA-MENGOCC-BCR en Uruguay. En esta población la frecuencia de efectos adversos a la vacuna fue similar a la observada en otras series(5-8). La mayoría de las reacciones adversas registradas fueron locales. El dolor fue el efecto adverso más frecuente. No se observaron reacciones adversas sistémicas graves que contraindicaran la administración de la segunda dosis. A diferencia de otras series, en esta población no ocurrió ningún caso de anafilaxia, púrpura o síndrome hipotónico-hiporreactivo(7,8,10). Con excepción de la fiebre, el resto de los efectos sistémicos observados fueron muy inespecíficos y subjetivos.
La frecuencia de efectos adversos fue mayor luego de la primera dosis y en el grupo de 4 a 11 años (p< 0,05).
Estos resultados permiten concluir que en esta población la vacuna VA-MENGOCC-BCR presentó un adecuado perfil de seguridad, lo que no descarta la necesidad de continuar su farmacovigilancia.
Summary
]]> Background. The first massive vaccination campaign with VA-MENGOCC-BCR antimeningococcal vaccine in Uruguay was set up in December 2001. In Santa Lucía city (Canelones) 5 366 children and youths were vaccinated. The vaccine is thought to be harmless, main adverse reactions recorded are local.Objective. To determine the prevalence and types of adverse reactions associated to VA-MNGOCC-BCR antimeningococcal vaccines in this population.
Method. A sample of 744 children were randomly assigned to the study. Adverse reactions were recorded after the first and the second dosage by personal interview or by phone 30 days later than dosages.
Results. Among the 744 children, 728 were assessed (98%). Adverse reactions were seen in 53% (IC95 53% + 3,6): 30% after the first intake, 5% after the second and 18% between the first and the second dosage. Adverse reactions were not seen in 47% (IC95 47% + 3,6). Among the 659 recorded adverse reactions, 71% were local and 29% systemic. Pain was the most frequent local adverse reaction, fatigue was the most frequent systemic adverse reaction.
Conclusion. The prevalence of adverse reactions in this population was 53% (IC95 53% + 3,6). There were no severe adverse reactions. Results are coincident with other series.
Résumé
Introduction: en décembre 2001, on lance la première campagne vaccinale massive avec VA-MENGOCC-BCR en Uruguay. Dans la ville de Santa Lucía (Canelones) on a vacciné 5.366 enfants de 2 à 19 ans. Ce vaccin est considéré non nuisible; les effets adverses signalés sont locaux.
Objectifs: déterminer la prévalence et le type de réac-tions adverses au vaccin VA-MENGOCC-BCR dans cette population.
Méthode et matériel: on a pris un échantillon simple au hasard de 744 enfants. Le dépistage des réactions adverses après la première et la deuxième dose a été fait au moyen d'une enquête personnelle ou téléphonique 30 jours après chaque dose.
Résultats: on a évalué 728 enfants (98% de l'échanti-llon). 53% (IC95 53% + 3,6) a développé un type de réaction adverse: 30% après la 1è dose, 5% après la 2è et 18% après la 1è et la 2è dose. 47% n'a présenté aucune réaction adver-se (IC 95 47%+ 3,6). On a signalé 659 réctions adverses, 71% locales et 29% systémiques. Parmi les premières, la douleur a été la plus fréquente (55%) et parmi les systémi-ques l'affaiblissement (30%).
]]> Conclusions: la prévalence de réactions adverses dans cette population a été de 53% (IC95 53% +3,6). Aucune réaction adverse sévère n'a été observée. Ces résultats se correspondent à d'autres déjà décrits.Bibliografía
1. Almeyda González L, Rico Cordeiro O. Información general sobre la enfermedad meningocócica en Cuba. Vacuna para su prevención y alcance. Rev Hosp Niños Bs As 1994; 36(158/159): 234-41.
2. González Sierra G. Informe Instituto Finlay. La Habana: Instituto Finlay, 1993.
3. Martínez Torres E, Leguén Castillo F. La enfermedad meningocócica: un problema mundial que comienza a tener solución. Rev Cub Pediatr 1993; 65(1): 63-72.
4. Pírez MC, Picón T, Galazka J, Quian J, Gutiérrez S, Ferrari AM et al. Enfermedad meningocócica en Uruguay. Informe epidemiológico y recomendaciones, mayo 2002. Rev Med Urug 2002; 18(1): 83-8.
]]>5. Gaivironsky R, Polack N. Reacciones secundarias a la administración de la primera dosis de vacuna antimeningocóccica BC. Resultados de una encuesta sobre 2000 niños. Rev Hosp Niños Bs As 1994; 34: 255.
6. Díaz Legaspe A. Informe sobre el Programa de Vacunación Antimeningocóccica de la Provincia de Buenos Aires. Rev Hosp Niños Bs As 1994; 36(158/159): 257-9.
7. Debbag R, Rüttimann R, Stamboulian D. Evaluación de las reacciones adversas asociadas con la vacuna antimeningocóccica BC. Informe preliminar sobre 8.177 vacunados. Rev Hosp Niños Bs As 1994; 36(158/159):249-54.
8. De Cicco LT, Kataife F, Bernardez V, Talamoni H, Altuna D, Musante G, et al. Efectos adversos asociados a la administración de la vacuna antimeningocóccica BC. Arch Arg Pediatr 1995; 93: 245-53.
9. Karch FE, Lasagna L. Adverse drug reactions: a critical review. JAMA 1975; 234: 1236-41.
]]>10. Lepow ML, Perkins BA, Hughes PA, Poolman JT. Meningococcal Vaccines. In: Plotkin SA, Oreintein WA. Vaccines, 3ª ed. Philadelphia: Saunders, 1999.
11. Asociación Americana de Infectología. Asociación Española de Pediatría. Sociedad Latinoamericana de Pediatría. Vacunación contra el meningocco. In: Manual de Vacunas en Pediatría. 2ª ed. Méxocp: Latinoamericana, 2000: 165-77.
12. Esteban Calvo C, Francés Foz M, Frías Iniesta J. Farmacovigilancia. Medicine 1995; 6(91): 4037-44.
13. Uppsala Monitoring Centre, World Health Organiza-tion. Collaborating Centre for International Drug Monitoring. Vigilancia de la seguridad de los medicamentos. Guía para la instalación y puesta en funcionamiento de un Centro de Farmacovigilancia. Geneva: UMC, 2001.
14. Organización Panamericana de la Salud. Oficina Regional de la Organización Mundial de la Salud. División de Vacunas e Inmunización. Vacunación segura: Cómo enfrentar los eventos supuestamente atribuidos a la vacunación o inmunización. Washington: OPS, 2002.
]]>15. Halsey NA. The Science of Evaluation of Adverse Events Associated with Vaccination. Semin Pediatr Infect Dis 2002; 13(3): 205-14.
]]>