Introducción
La hepatitis autoinmune (HAI) es una enfermedad hepática crónica de naturaleza inflamatoria, generalmente con un curso progresivo, y que se caracteriza por una serie de rasgos inmunológicos, como la presencia de autoanticuerpos circulantes y la elevación de las globulinas plasmáticas.
La dificultad en el manejo de esta enfermedad radica en la gran variedad de formas de presentación, manifestaciones clínicas, hallazgos histológicos, fenotipos inmuno-genéticos y anomalías serológicas que presenta. Se caracteriza por cursar desde formas asintomáticas o crónicas insidiosas, hasta formas agudas graves e incluso fulminantes, o presentarse en fases avanzadas, debutando como cirrosis descompensada.
La efectividad del tratamiento inmunosupresor puede variar acorde al momento en que se lo inicie y a la forma presentación, siendo aquellas formas agudas y severas, con aumento de los niveles de bilirrubina, caída de la función biosintética y necrosis masiva/submasiva o cirrosis en la histología, las de más difícil manejo 1.
Las publicaciones acerca de pacientes con HAI severa son escasas, y la mayoría se basan en el análisis retrospectivo de pequeñas series de pacientes con resultados disímiles respecto a cuándo y cómo iniciar la terapia con corticoides, o a cuáles son las variables asociadas a una pobre respuesta a dicho tratamiento. 1-5) Este hecho pone de manifiesto la variabilidad que existe en el pronóstico, sino también en el abordaje clínico de estos pacientes.
El presente trabajo fue dirigido a contribuir en el manejo terapéutico y en la toma de decisiones en este grupo complejo de pacientes. Los objetivos son evaluar la tasa de respuesta al tratamiento corticoideo en pacientes con HAI severa, establecer variables asociadas a dicha respuesta en este grupo de pacientes y determinar la supervivencia global y libre de trasplante hepático (TH) en dicho escenario.
Metodología
Se realizó el análisis retrospectivo de pacientes con diagnóstico de HAI aguda evaluados consecutivamente en la Unidad de Hepatología del Hospital Universitario de la Fundación Favaloro (HUFF), entre enero del 2010 y julio del 2016.
b) Variables
Para descartar otras causas de enfermedad hepática concomitante se realizaron pruebas serológicas (virus hepatitis A, virus hepatitis B, virus hepatitis C, virus Epstein-Barr, citomegalovirus), estudios del metabolismo del hierro y del cobre, imagenología, e histología en aquellos pacientes biopsiados.
Los pacientes seleccionados para iniciar tratamiento médico recibieron dosis iniciales de Prednisona de 20-60 mg por día combinado con Azatioprina 50-100 mg/día, de acuerdo con las guías y recomendaciones publicadas para el manejo de esta entidad. 8-10
Los parámetros de laboratorio tales como bilirrubina total, ALT, globulinas, inmunoglobulina G, creatinina plasmática e INR fueron analizados al día 0 (ingreso), y a los 7, 30 y 90 días posteriores al inicio del tratamiento inmunosupresor. La albúmina plasmática, la colesterolemia, y la presencia de anticuerpos antinucleares (FAN), anticuerpos anti-mitocondriales (AMA), anticuerpos anti-músculo liso (ASMA), anticuerpos microsomales hígado y riñón (LKM1) y otros Anticuerpos (anticitosol hepático tipo 1 -LC1 y SLA LP) fueron solicitados únicamente en la fase pre-tratamiento.
Variables clínicas como la presencia de encefalopatía hepática (EH) y o de ascitis fueron analizadas con la misma sistemática que las variables de laboratorio.
El planteo de sospecha clínica de cirrosis se basó en la presencia de várices esofágicas en la endoscopía digestiva, hallazgos ecográficos compatibles (hígado disminuido de tamaño, circulación colateral, ascitis y/o esplenomegalia), y estigmas de enfermedad hepática avanzada en el examen físico.
Las biopsias hepáticas fueron obtenidas previamente al inicio del tratamiento y analizadas en conjunto por el Servicio de Anatomía Patológica y la Unidad de Hepatología del HUFF. El grado de necro-inflamación y el estadio de fibrosis fueron evaluados acorde a los criterios del GIHAI y al score de Ishak respectivamente (7.
La respuesta al tratamiento con corticoides se definió como completa, parcial o nula de acuerdo con variables clínicas, bioquímicas y parámetros de funcionalidad hepática: (8-10
-Remisión completa: normalización de AST/ALT, bilirrubina total y gamma-globulina luego de al menos 6 semanas de tratamiento, en ausencia de peoría en el lapso de 3 semanas a 3 meses post suspensión del mismo.
-Remisión parcial: pacientes que respondieron al tratamiento, pero que requirieron dosis bajas de corticoides para el mantenimiento de la respuesta.
-Falla al tratamiento: ausencia de respuesta a dosis máximas de corticoides y azatioprina por al menos 1 mes.
C) Análisis estadístico
El análisis de las variables clínicas, bioquímicas e histológicas fue realizado por pruebas no paramétricas (Chi-cuadrado y U Mann- Whitney). Fue considerado estadísticamente significativo un valor de p ≤0.05.
La descripción de las variables numéricas se realizó por la mediana y su rango intercuartil (p25-p75), mientras que las variables categóricas se expresaron en porcentajes.
La supervivencia actuarial global y libre de trasplante hepático o muerte fue realizada por Kaplan-Meyer, realizándose un subanálisis según MELD < 25 o ≥ 25.
Todos los datos fueron analizados con el software estadístico SPSS 17.0.
Resultados
Fueron incluidos 33 pacientes con una mediana de edad de 52 años (31.5-62), que cumplían los criterios diagnósticos modificados del GIHAI (≥ 6 puntos) (7.
El 97% de los casos (n=32) fueron mujeres. El 57% (n=19) fue catalogado como cirróticos en la valoración inicial, 10 presentaron EH (30%) y 15 ascitis (45%).
En cuanto al perfil inmunológico, el 39.4% (n= 13) presentaron ANA/FAN y ASMA positivos, 6.1% (n=2) anti-LC1 positivos, y 3% (n=1) anti-LKM1 positivos.
El valor de inmunoglobulina G fue 2662 (1802-3445) mg/dl y de gammaglobulina 2.6 (2-3.8) gr/dl.
Las variables bioquímicas al ingreso que presentaron una mediana elevada fueron la bilirrubina total (8.8 mg/dl), y el INR (1.72).
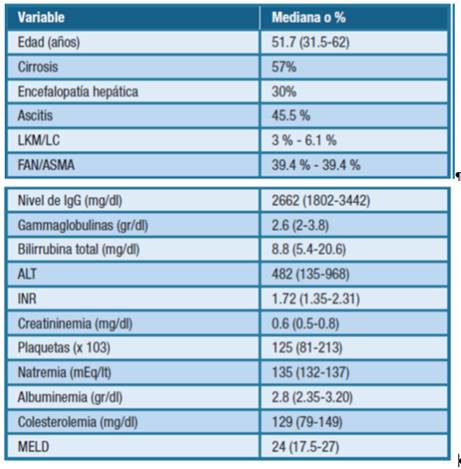
Respecto a otros parámetros, los resultados fueron los siguientes: creatininemia: 0.6 (0.5-0.8) mg/dl, recuento de plaquetas: 125000 (81000-213000), natremia: 135 (132-137) mEq/L, albuminemia: 2.8 (2.3-3.2) gr/dl, y colesterolemia: 129 (79-149) mg/dl. (Tabla 1).
Tabla 1: Descripción de la cohorte en lo que refiere a datos demográficos, clínicos y bioquímicos al momento del reclutamiento
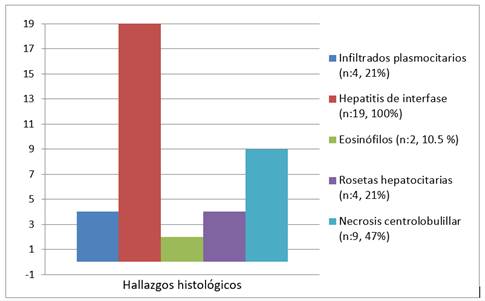
En lo que refiere a los hallazgos histológicos, en 19 pacientes se realizó biopsia hepática (57.6%), 13 por vía transyugular (68.4%), y 6 por vía percutánea (31.6%). La mediana del Score de Ishak fue de 9.5 (6.7-12), 21% (n=4) presentaron infiltrados plasmocitarios, 10.5% (n=2) presencia de eosinófilos, 100% (n=19) hepatitis de interfase, 21% (n=4) rosetas hepatocitarias, y 47.4% necrosis centrolobulillar (55% severa, 11.1% moderada, 33.3% leve). En un 26 % (n=5) de los casos los hallazgos fueron compatibles con necrosis masiva/submasiva. En cuanto al grado de fibrosis, 9 pacientes presentaron estadio F4 (42.3%), 5 F3 (26.3 %), 1 F2 (5.2%), 2 F1 (10.5%) y 1 F0 (5.2%). La valoración de la fibrosis fue dificultosa en algunos casos por la presencia de importante necrosis hepatocitaria (Gráfico 1y2).
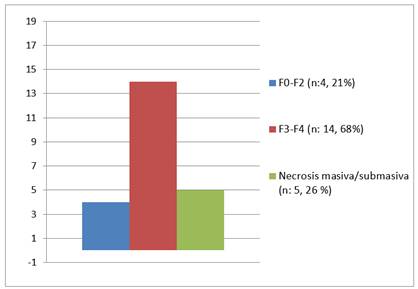
Gráfico 2: Estadio de fibrosis y necrosis masiva/submasiva en pacientes con biopsia pre-tratamiento (n=19).
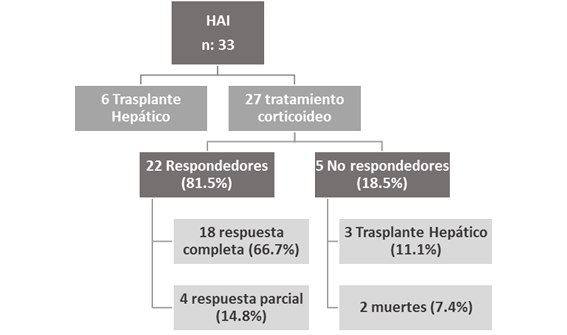
En lo que refiere al seguimiento de los pacientes, en 6 (18,2%) se realizó TH de inicio, en 27 (82%) se inició tratamiento con corticoides- Prednisona a 40 (20-60) mg/día, agregando posteriormente Azatioprina (50 mg/día). Siguiendo los criterios de respuesta, 18 pacientes (66.7%) tuvieron respuesta completa, 4 (14.8%) parcial, y 5 (18.5%) presentaron falla al tratamiento. De los 5 pacientes no respondedores, 60% (3/5) requirieron TH por deterioro de la función hepática, y 40% (2/5) fallecieron por desarrollo de infecciones bacterianas intercurrentes (peritonitis bacteriana espontánea y neumonia aguda comunitaria). Figura 1.
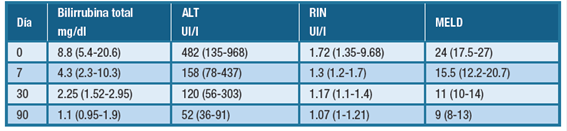
La Tabla 2 detalla la mediana (p25-p75) de las variables de laboratorio analizadas a lo largo del tratamiento en el grupo respondedor (n= 22) a los días 0, 7, 30 y 90 respectivamente.
Tabla 2: Variables de laboratorio analizadas a lo largo del tratamiento en el grupo de pacientes respondedores
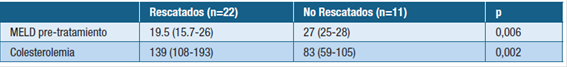
En cuanto a los predictores asociados al “no rescate” vs “rescate” del TH, se analizaron las diferentes variables de forma dinámica (n=33), 2 de las cuales fueron estadísticamente significativas: el MELD pre-tratamiento (27 vs 19.5, p= 0,006) y la colesterolemia basal (83 vs 139 mg/dl, p=0,002).
La ausencia de correlación entre la severidad histológica y el “no rescate” plantea que, a pesar de que presenten necrosis masiva/submasiva o cirrosis, es probable que el tratamiento corticoideo permita evitar la necesidad de TH en este grupo de pacientes.
En lo que refiere a variables asociadas a falla del tratamiento corticoideo vs respuesta al mismo, las que tuvieron significancia estadística fueron la colesterolemia basal (68 vs 139 mg/dl, p=0.004) y la presencia de EH (60 vs 18.2%, p=0.05).
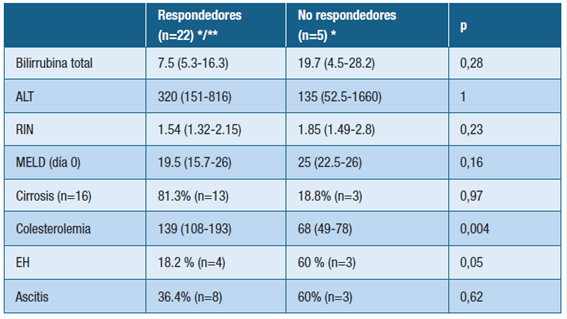
Respecto a la supervivencia de la cohorte analizada, luego de una mediana de 2 años de seguimiento (0.63-3.4), 22 (66.7%) permanecieron vivos bajo tratamiento, sin necesidad de TH (“rescatados del TH”), 9 (27.3%) fueron trasplantados (6 al inicio y 3 no respondedores). Fallecieron 3 (6%) pacientes (2 no respondedores y 1 post-TH) (“no rescatados del TH”) (Tablas 3y4).
Tabla 4: Variables asociadas a la “respuesta” vs “no respuesta” al tratamiento corticoideo (n=27). Referencias: (*) Valor de la Mediana (rango intercuartil, p25-p75). (**) Respondedores: Remisión Completa (n=18) + Remisión Parcial (n=4)
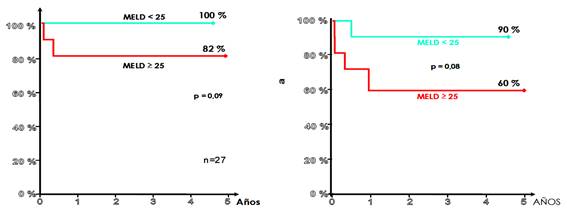
La supervivencia global y libre de TH o muerte a 5 años (n=33) fue de 90% y 62.5% respectivamente. La supervivencia libre de eventos en función del puntaje MELD (<25 vs. ≥ 25) fue de 85% y 41% (p= 0,001), mientras que la supervivencia global fue de 100% vs. 80% (p=0,09) (Gráfico 3).
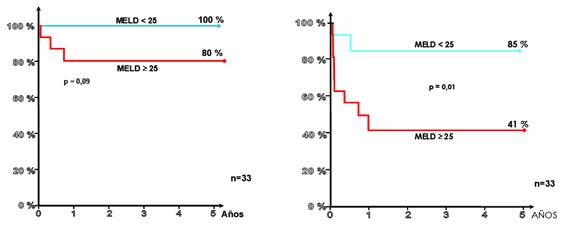
Gráfico 3: Supervivencia global y libre de TH o muerte a 5 años según MELD en la cohorte del estudio (n=33).
En el grupo tratado con corticoides (n=27) la supervivencia global y libre de TH o muerte a 5 años fue de 92% y 77.5% respectivamente. La supervivencia libre de eventos en función del puntaje MELD (<25 vs. ≥ 25) fue de 90% y 60% (p=0,08) respectivamente, y la supervivencia global de 100% vs. 82% (p=0,1) (Gráfico 4).
Discusión
Los pacientes con HAI severa constituyen un subgrupo difícil de tratar, y con mayores posibilidades de presentar falla al tratamiento corticoideo (3.
En este estudio los pacientes con HAI severa presentaron un estadio histológico avanzado (necrosis masiva/submasiva, cirrosis) y un mayor deterioro de la función de síntesis hepática (ictericia, MELD elevado).
En cuanto al score de MELD, el subgrupo que mostró menor respuesta al tratamiento y supervivencia fue aquel con score ≥ 25. Según Yeoman y col. (3 el MELD promedio de aquellos pacientes que fallaron a la terapia con corticoides, y que presentaron peor evolución fue de ≥ 26 (16-35). Por tanto, conocer este comportamiento es fundamental para seleccionar adecuadamente a los pacientes candidatos a tratar en un centro de referencia con posibilidades de brindar acceso a los cuidados de la hepatología crítica, incluyendo el trasplante hepático.
En el análisis de los grupos “rescatados” vs “no rescatados” del TH, las variables estadísticamente significativas asociadas con dicha respuesta fueron el score de MELD y la colesterolemia pre-tratamiento. Existen reportes que coinciden con el valor pronóstico del MELD (≥ 26 p= 0,02) al día 0 3. Este hallazgo abre la interrogante sobre cuál es la mejor conducta frente a este grupo de pacientes, en quienes se debe discutir si iniciar el tratamiento inmunosupresor, o avanzar hacia el trasplante hepático.
En los 27 pacientes (82%) que recibieron corticoides se identificaron variables asociadas a falla del tratamiento. El valor de colesterol plasmático y la presencia de encefalopatía hepática pre-tratamiento fueron predictores estadísticamente significativos de falla al tratamiento. La determinación del colesterol plasmático es una prueba bioquímica que valora el grado de función de síntesis hepática, por lo cual la hipocolesterolemia puede encontrarse tanto en la hepatitis aguda grave como en la cirrosis. Su limitación clínica radica en el hecho de que no es un marcador temprano de insuficiencia hepática, por lo que podría carecer de valor en la toma de decisiones terapéuticas iniciales. En el presente estudio la hipocolesterolemia podría explicarse por la alta prevalencia de cirrosis y necrosis masiva/submasiva en este grupo de pacientes. La encefalopatía hepática se presenta como complicación tanto en la insuficiencia hepática crónica como en la aguda, pudiendo ser un evento precoz. Esto le otorga más sensibilidad como marcador de severidad y predictor precoz de falla al tratamiento. En el estudio de Villamil y col. (1) los pacientes con EH grado 4 presentaron menor posibilidad de responder al tratamiento corticoideo. En el presente trabajo, la bilirrubina total aumentada (7.5 versus 19.7 mg/dl, p= 0,28), y el INR prolongado (1.54 versus 1.85, p= 0,23) fueron más frecuentes en aquellos no respondedores, sin una diferencia estadísticamente significativa.
En este estudio el valor de MELD fue un predictor de respuesta al tratamiento, ya que el total de los respondedores presentaba un puntaje < 25. En la publicación de Verma y col. 11) el total de los respondedores tuvo un score MELD inicial ≤ 28. Del total de pacientes tratados con corticoides (27), 18 (66.7%) presentaron remisión completa, y 4 (14.8%) respuesta parcial, conformando el total del grupo respondedor (22) 8-10 .
El 59.1% (13/22) de los pacientes respondedores presentaba cirrosis (por sospecha clínica o confirmación histológica) lo cual no fue determinante en la probabilidad de repuesta. Esto coincide con lo presentado por Yeoman y col. 3) quien no encontró hallazgos histológicos significativamente diferentes entre el grupo respondedor y no respondedor.
Realizando el análisis en función del MELD se concluyó que aquellos con un puntaje < 25 presentaron una supervivencia global del 100 % y libre de TH del 90%. En pacientes que iniciaron tratamiento con MELD ≥ 25 la supervivencia global bajó al 82% y libre de TH a un 60%. Con esta última observación se puede concluir que aún en el grupo de pacientes con HAI severa la tasa de supervivencia global es más que aceptable, lo que justificaría el intento de tratamiento con corticoides independientemente de la gravedad de la situación inicial, siempre considerando que frente a la falla de este existe la posibilidad de avanzar al TH.
Este último concepto es de especial importancia en muchos de los países de la región, ya que la accesibilidad al TH en escenarios de falla hepática aguda está condicionada por la baja disponibilidad de órganos en los plazos adecuados.
Debido a las excelentes tasas de supervivencias halladas en este estudio, el tratamiento con corticoides es una herramienta válida en la actualidad como primera línea terapéutica independientemente de la severidad de la enfermedad.
El 18% de los pacientes no iniciaron terapia con corticoides por presentar EH grado 4, necrosis masiva/submasiva en la biopsia hepática, o desarrollo de complicaciones infecciosas intercurrentes. Este constituye un grupo de pacientes de difícil manejo por la ausencia de estudios prospectivos multicéntricos que contribuyan en la toma de decisiones clínico-terapéuticas.
Conclusiones
La HAI de presentación aguda y severa, con aumento de la bilirrubina sérica (forma ictérica) representa un verdadero desafío médico. La decisión de iniciar el tratamiento corticoideo y el mejor momento para hacerlo es el punto de mayor discusión.
En el presente análisis los pacientes con HAI y MELD < 25 presentaron una sobrevida a 5 años libre de eventos (TH o muerte) del 90 %.
A pesar de la menor sobrevida libre de TH que presentó el grupo de mayor severidad (MELD ≥25), la tasa se mantuvo dentro de valores aceptables, cercana al 60%.
Esto último reafirma la necesidad de priorizar el tratamiento con corticoides independientemente del grado de enfermedad que presenten los pacientes con HAI al momento del debut, dado que en función de los resultados de este estudio presentan una alta probabilidad de ser rescatados del TH.