Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Medicina Interna
Print version ISSN 2393-6797On-line version ISSN 2393-6797
Rev. Urug. Med. Int. vol.1 no.2 Montevideo Aug. 2016
Trabajo original
Insuficiencia renal aguda en la cirrosis hepática: análisis de causas
Acute renal in liver cirrhosis: analysis of causes
Dra. Selene Correa
Internista. Nefróloga. Prof. Adjunto Clínica Médica
Dra. Carolina Ponce de León
Internista. Ex Residente de Medicina Interna
Dra. Mercedes Perendones
Internista. Prof. Agregado Clínica Médica
Recibido: 26/5/16 - Aceptado: 29/7/16
Departamento e Institución responsables: Clínica Médica 2. Prof. Dra. Mabel Goñi. Facultad de Medicina. Universidad de la República. Hospital Pasteur. Montevideo – Uruguay.
Correspondencia: Dra. Selene Correa. Dirección: Larravide s/n esq Cabrera. Hospital Pasteur, Montevideo-Uruguay. Correo electrónico: correaselene1@gmail.com
RESUMEN
Introducción: La insuficiencia renal aguda es una complicación frecuente en los pacientes cirróticos, existen varios estudios que señalan que el riesgo de insuficiencia renal aguda está significativamente aumentado en pacientes con hiperbilirrubinemia, hiponatremia y peritonitis bacteriana espontánea. La mayoría de los estudios se han centrado en la insuficiencia renal secundaria a la disfunción circulatoria que se denomina síndrome hepatorrenal; sin embargo que exisen otras causas, mucho más frecuentes en estos pacientes cuya posibilidad de prevención y corrección con tratamiento dirigido impone la pesquiza etiológica específica. Resultados: Durante el período analizado se registraron 18 episodios de insuficiencia renal aguda en 33 episodios de descompensación hepática crónica. La hipotensión por distintas causas y el uso de medios de contraste sin nefroprotección fueron los hechos más destacados. Discusión: la prevalencia de insuficiencia renal aguda fue superior a datos internacionales. Se analizan las distintas causas encontradas y su posible mecanismo etiopatogénico, así como medidas de prevención.
Palabras claves: Insuficiencia renal aguda. Cirrosis. Nefroprotección
ABSTRACT
Introduction: Acute renal failure is a frequent complication in cirrhotic patients, several studies indicating that the risk of acute renal failure is significantly increased in patients with hyperbilirubinemia, hyponatremia and spontaneous bacterial peritonitis. Most studies have focused on the renal failure secondary to circulatory dysfunction called hepatorenal syndrome; however, that exisen other causes, much more common in these patients whose possibility of prevention and treatment directed correction imposes specific etiologic. Results: During the period analyzed 18 episodes of acute renal failure occurred in 33 episodes of chronic liver decompensation. Hypotension various causes and the use of contrast media without nephroprotection were the highlights. Discussion: The prevalence of acute renal failure was higher than international data. Found the different causes and its pathogenic mechanism and prevention measures are analyzed.
Key words: Acute renal failure. Cirrhosis. Nephroprotection
Introducción
El deterioro de la función renal o insuficiencia renal aguda (IRA) es una complicación frecuente en los pacientes cirróticos (1, 2) ,pero existe poca información acerca de la incidencia, los factores predisponentes, la historia natural y el tratamiento de esta afección.
El diagnóstico de IRA es un factor predictor de mortalidad independiente en estos pacientes. (2,3) El deterioro de la función renal en la cirrosis es un fenómeno que progresa lentamente en la medida que el paciente avanza por las distintas etapas de la enfermedad (4), existen varios estudios que señalan que el riesgo de IRA está significativamente aumentado en pacientes con hiperbilirrubinemia, hiponatremia y PBE. (2)
Se han acuñado varias definiciones para el diagnostico de IRA. El Club Internacional de Ascitis propone la elevación de los niveles de creatinina sérica por encima de 1,5 mg/dl, que corresponde a una tasa de filtrado glomerular de aproximadamente 40 ml/ min (3,4) siendo la más aceptada en el ámbito de la hepatología.
Sin embargo, es bien sabido que dicho nivel sobreestima el filtrado glomerular (GFR) por una menor producción de creatinina, por una disminución de la masa muscular propia de estos pacientes. Por otra parte un nivel de creatinemia menor a 1,5 mg/dl no excluye necesariamente la disfunción renal.(5)
Así es como surge el concepto de "daño renal agudo" (DRA) en la propuesta del grupo de trabajo AKIN (Acute Kidney Injury Network) del 2007 que propone una nueva definición y clasificación en tres estadíos (1) descritos en la tabla 1. El daño renal agudo en la cirrosis se define como un aumento del nivel de creatinina sérica (CrS)>1,5 veces respecto al valor basal o como una elevación del nivel de CrS ≥0,3mg/dl en <48hs. (5- 8) Este criterio tiene la ventaja de la detección de la disfunción renal en fases precoces con abordaje oportuno, sabiendo que la mortalidad aumenta en estadíos más avanzados y también que pequeños incrementos en la creatininemia sérica se asocian de forma independiente con mayor mortalidad en los pacientes hopitalizados con cirrosis. (1, 5, 9)
Tabla 1. Estadíos de la Insuciencia renal en pacientes cirróticos según AKIN
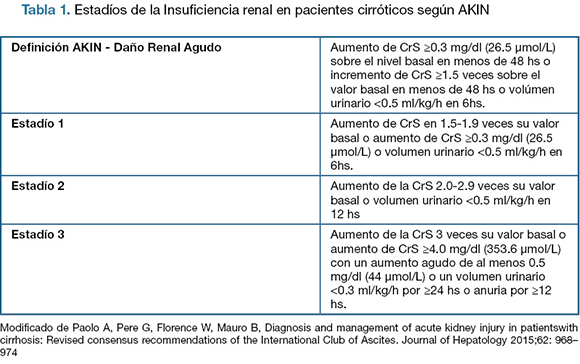
El valor de creatininemia 1,5 mg/dl sigue siendo un buen biomarcador aislado en cuanto a que predice riesgo de progreso a estadios más avanzados de la enfermedad renal (estadios 2 ó 3). (1)
La mayoría de los estudios se han centrado en la insuficiencia renal del paciente cirrótico secundaria a la disfunción circulatoria intrarrenal que se denomina síndrome hepatorrenal (SHR). (10, 11) Sabemos sin embargo que exisen otras causas de IRA mucho más frecuentes en estos pacientes cuya posibilidad de prevención y corrección con tratamiento dirigido impone la pesquiza etiológica específica dado la asociación pronóstica demostrada según la causa. (11) Adoptaremos una clasificación fisiopatológica para enumerarlas según describe la tabla 2.
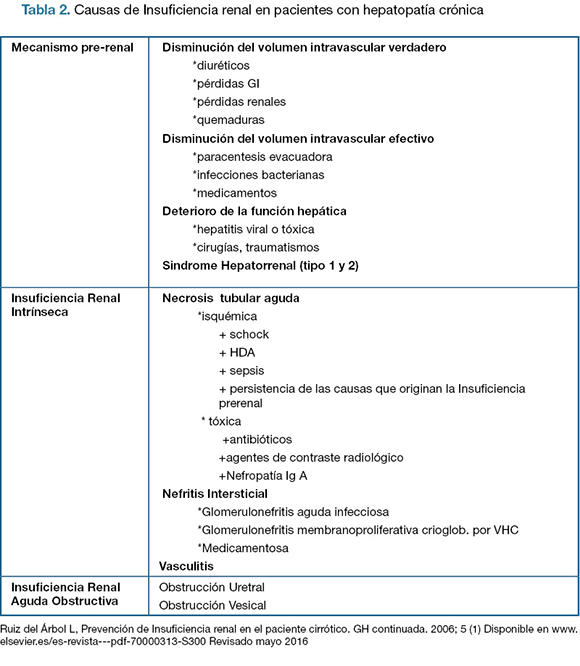
La IRA puede clasificarse en pre-renal, renal o intrínseca y pos-renal de acuerdo al mecanismo que la desencadena. La IRA pre-renal se caracteriza por hipoperfusión renal sin lesiones glomerulares ni tubulares. La hipoperfusión renal es responsable del 90% (6) de los casos de IRA y se debe a la deplección de volumen por hemorragias, pérdidas digestivas, paracentesis evacuadoras masivas o al uso de diuréticos. También puede deberse a mecanismos hemodinámicos por el uso de fármacos inhibidores de la enzima de conversión (IECA) o antiinflamatorios no esteroideos (AINE). El síndrome hepatorrenal se encuentra en este grupo, con la particularidad de no mejorar con la reposición de volumen. (12) La fisiopatología del SHR se basa en una intensa vasocontricción de la circulación arteriolar intrarrenal que conduce a una disminución del flujo sanguíneo renal y, en consecuencia del filtrado glomerular.
La IRA pre-renal puede evolucionar y determinar la necrosis tubular aguda (NTA) isquémica cuando la reducción del flujo de sangre lleva a la necrosis de las células tubulares renales.
En la insuficiencia renal intrínseca la causa está en el parénquima renal y es determinada por distintos mecanismos: necrosis tubular (isquémica o tóxica), glomerulonefritis o nefritis intersticial. (12) En la NTA por tóxicos destacamos entre otros la utilización de medios de contraste en los estudios de imagen, entidad denominada Nefropatía inducida por contraste (NIC). (13, 14)
La insuficiencia post-renal se debe a una obstrucción en la vía urinaria.
El análisis diagnóstico en función de la causa de IRA es fundamental para poder iniciar y dirigir el tratamiento así como por su valor pronóstico. (1, 5, 6)
El objetivo del presente trabajo es determinar la prevalencia, etiologias y pronóstico de los casos de IRA en pacietes con cirrosis internados.
Metodología
Se trata de un estudio retrospectivo, descriptivo de una población de pacientes con cirrosis hepática asistidos en policlínica que requirieron ingreso en cuidados moderados por descompensación de su afección hepática. Consideramos el período comprendido entre setiembre de 2012 – marzo de 2014.
Criterios de inclusión: edad mayor a 15 años, de ambos sexos, asistidos en la policlínica de hepatopatía.
Criterios de exclusion: pacientes con enfermedad renal crónica (ERC) en etapa de hemodiálisis
Criterios diagnósticos - definiciones
IRA: aumento del nivel de creatinina sérica >1.5 veces el valor basal o una elevación del nivel de creatinina sérica ≥0,3mg/dl en <48hs respecto al valor basal.
Se considero IRA pre-renal en aquellos casos en que se reconoció un elemento precipitante de los ya enunciados en la tabla 2 y que tras corrección del mismo los valores de creatinina sérica retornaron a los valores basales en 24 a 72 horas.
Se considero IRA parenquimatosa en aquellos casos en que no mejoraron al adoptar las medidas correctivas de los factores encontrados como responsables en los casos de IRA pre-renal o la IRA instalada tras el uso de farmacos o toxicos (contraste) así como aquella en que la etiologia se asume dentro de los factores parenquimatosos enunciados en la tabla 2.
Se consideró IRA pos-renal en aquellos casos en que mejora retornando a los valores basales una vez corregido o sorteado el obstáculo en el flujo urinario.
Hipotensión arterial se define por cifras de presión arterial (PA) menores o iguales a 90/60 mmHg. (15)
Hiponatremia se definió como la concentración de sodio sérico menor de 135 mEq/l.
Procedimiento: se identificaron los pacientes ingresados en el periodo de estudio a partir de la información de la policlínica de hepatologia. Se realizó la revisión de dichas historias utilizando para ello un formulario precodificado obteniéndose datos epidemiologicos, causas de descompensacion hepatica (ascitis, infecciones diferenciando PBE u otras, hemorragia digestiva alta (HDA), encefalopatia hepática), presencia de hipotensión arterial, análisis de tratamientos recibidos (enalapril, propranolol, furosemide, espironolactona), tóxicos (contraste), creatininemia al ingreso , cifras máximas durante la internación y al egreso y presencia de hiponatremia. Se analizó funcionalidad hepática a traves de los datos de albúmina considerando el promedio durante la internación, tiempo de protrombina considerando el promedio durante la internación y valores de bilirrubina total (BT) y bilirrubina directa (BD) en sangre al ingreso. Se registró la presencia de factores de riesgo cardiovascular (hipertension arterial (HTA), diabetes (DM) y tabaquismo) a los efectos de determinar la existencia de otras causas de enfermedad renal no vinculadas a la enfermedad hepática. Se registró finalmente dias de internación y mortalidad.
Analisis estadistico: las variables continuas se expresaron con la media y el desvío estándar correspondiente. Para analisis de variables continuas se utilizo chi cuadrado y para variables discretas el test de t, con nivel de significación alfa 5%.
Resultados
Durante el periodo analizado se registraron 28 pacientes internados. 5 de ellos tuvieron dos internaciones, por lo que se contabilizaron 33 episodios de descompensación hepática que motivó la internación y que fueron analizados. En los mismos se registraron 18 episodios de IRA.
En la tabla 3 se presentan las caracteristicas epidemiologicas de ambos grupos y en la tabla 4 se presentan los factores encontrados como potencialmente responsables entre ambos grupos.

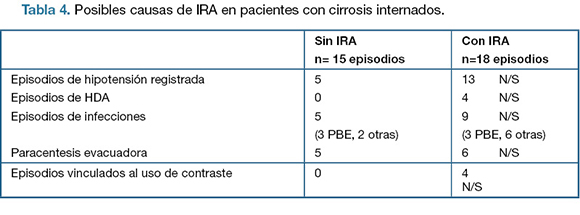
En 7 episodios de IRA se constató el uso de 3 ó 4 fármacos de los analizados. 6/7 tuvieron hipotesión arterial, mientras que del grupo sin IRA sólo en 2 episodios se registró consumo de 3 ó 4 fármacos presentando ambos casos hipotensión arterial.
En la tabla 5 se presentan los valores alcanzados de azoemia y creatininemia en ambos grupos.
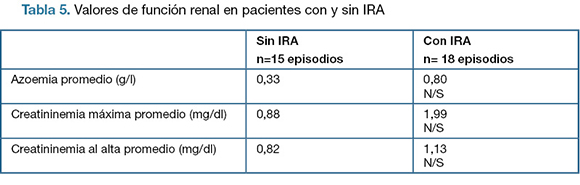
El grupo de pacientes con IRA presentó una natremia promedio de 131 mEq/l vs 122 mEq/l que presentó el grupo con IRA. Si bien se trata de un valor menor, no presenta diferencia estadísticamente significativa.
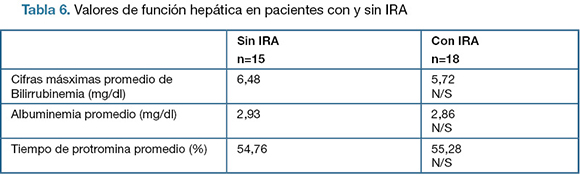
En la tabla 6 se presentan los criterios de funcionalidad hepática de ambos grupos; y por último en la tabla 7 se presentan días de internación y mortalidad.

Discusión
En nuestro estudio encontramos una prevalencia de IRA de 0,54 (18 episodios en 33 internaciones) que es mucho mayor a los datos internacionales ubicada en 23% (29 episodios en 127 internaciones) según lo reportado por Wu y col en un hospital de Hong Kong. (15) En un estudio realizado por Mathurin y col en el Servicio de Clínica Médica del Hospital de Santa Fe - Argentina la incidencia fue del 21,6% (35 episodios en 162 internaciones). (2)
Las diferencias en la incidencia es multicausal: a) los dos estudios internacionales citados se realizan en hospitales de segundo nivel de atención por lo cual es posible que los pacientes que requieran tratamiento sustitutivo de la función renal o ingreso a cuidados intensivos se deriven a hospitales de tercer nivel de atención, contribuyendo a un menor registro de episodios de IRA b) la definición utilizada por Mathurin y col (2) solo reconocían IRA con valores de creatininemia mayores a 1.5mg/dL y no incluían pacientes con variaciones de 0.3mg de creatininemia, si no se superaban los 1.5mg/dL de creatininemia durante la internación c) es conocido la importancia de los factores de riesgo cardiovasculares en el desarrollo de injuria renal (16), si bien en nuestra población no hubo diferencia estadísticamente significativa en la presencia de los mismos en el grupo con y sin IRA, en los dos estudios analizados, las poblaciones eran más jovenes que la nuestra y no fue consignada la presencia de factores de riesgo cardiovascular que podrían incidir en el desarrollo de IRA. (2, 15)
En cuanto a las causas de IRA, encontramos en nuestra serie varios mecanismos potencialmente responsables de la misma en cada paciente, siendo difícil explicar el factor predominante.
Hay muchos marcadores de laboratorio, de uso clínico que permiten diferenciar la IRA pre-renal de la parenquimatosa (FENA, índices U/P, etc); la lipocalina asociada a gelatinasa de los neutrófilos, un biomarcador urinario, se utilizaría para diagnosticar más precozmente la IRA parenquimatosa (5). Pero dado el impacto pronóstico del SHR lo verdaderamente importante sería contar con un marcador precoz para el diagnóstico del mismo.
La hiponatremia no se vincula como causa determinante de IRA; pero es reconocido como un factor presente en las etapas avanzadas de la enfermedad hepática crónica. En nuestro trabajo no encontramos diferencia estadísticamente significativa en su valor entre el grupo con y sin IRA, aunque destacamos la existencia de un valor promedio mucho menor en el grupo con IRA, lo que explicaría que hepatopatías más graves (con mayor hiponatremias) tienen más fallo renal.
La hipotensión arterial, única variable con significación estadística, que pudo constatarse en 13 pacientes con IRA podría deberse a insuficiencia hepática con vasodilatación de los lechos esplácnicos (17), al uso de fármacos hipotensores, a la hipovolemia aguda por sangrado digestivo o por diarreas copiosas, entre otras causas sospechables.
Siendo la hepatopatía una enfermedad con varias complicaciones (PBE, HDA, descompensación hepatocirculatoria) y tratamientos (paracentesis, diuréticos, beta bloqueantes) que implican redistribución de volúmen con modificaciones hemodinámicas, parece lógico que en la hipotensión confluyan los mecanismos de varias de las etiologías comentadas.
Algunas causas de IRA particularmente presentes en los pacientes cirróticos se han estudiado en mayor profundidad conociéndose su impacto y pronóstico en mayor detalle.
La presencia de procesos infecciosos está reconocida como uno de los factores precipitantes de IRA. Hay trabajos que sostienen que las infecciones bacterianas son la causa más común de insuficiencia renal en pacientes cirróticos. (5) Son varios los mecanismos patogénicos que lo explican: la exacerbación de la vasodilatación arterial sistémica propia de la hepatopatía, productos bacterianos, citoquinas y factores vasoactivos que surgen en el contexto de la infección-inflamación. (5)
Si bien en nuestro trabajo la presencia de ésta no fue estadísticamente significativa, debemos destacar que el grupo con IRA presentó más procesos infecciosos que el grupo sin IRA (9/18 vs 5/15 respectivamente).
Dentro de las infecciones bacterianas, la más estudiada como factor predictor e incluso independiente de IRA es la PBE (5,6) , que determina una mortalidad del 30% en el grupo de pacientes con IRA vs 7% sin IRA (18). Las causas son multifactoriales involucrándose alteraciones hemodinámicas, presencia de shock séptico hasta en el 10% de los paciente con PBE. (19) En nuestro trabajo no existieron diferencias significativas al analizar esta variable entre los pacientes que tuvieron o no IRA.
Las infecciones bacterianas no PBE, ocasionan daño renal por mecanismos similares a los ya descritos y requieren seguimiento para su detección precoz. En nuestro grupo de pacientes 2/15 sin IRA tuvieron procesos infecciosos no PBE vs 6/18 (FR 0,33) con IRA, aunque esta relación no fue estadisticamente significativa.
Otra eventualidad altamente prevalente en la enfermedad hepática avanzada es la necesidad de paracentesis evacudora siendo una maniobra que implica disfunción circulatoria en 60-70% de los casos. Esta complicación se reduce al 18% con la administración de albúmina i/v como otra medida de alta eficacia a considerar en la prevencion de IR de causa pre-renal (18) . No hubo diferencia significativa en el desarrollo de IRA al analizar la realización de paracentesis en ambos grupos, seguramente vinculado a la implementación protocolizada de la reposición con expansores o albumina tras la maniobra (20).
Asimismo los fármacos pueden determinar IRA pre renal por diferentes mecanismos como deshidratación e hipotensión (por ejemplo diuréticos) con hipoperfusión renal ante la reducción del volúmen circulante efectivo, alteraciones en la hemodinamia renal con inhibición de las prostaglandinas vasodilatadores como en el caso de los AINES o de la ruta de la angiotensina II como en el caso de los IECA. El mecanismo generador de IRA prerenal por IRA se vincula a la vasodilatación de la arteriola eferente del glomérulo renal, disminución de la presión de filtración y caída del filtrado glomerular (5, 18). Señalamos que en 7/18 (FR 0,38) episodios de IRA se administró la combinación de 3 o más fármacos en relación a solo 2/15 (FR 0,13) episodios sin IRA, lo cual pensamos puede haber contribuido en su génesis.
La perpetuación de algunos de los mecanismos prerenales pueden conducir a la NTA isquémica como causa de IRA parenquimatosa. Uno de los mejores ejemplos podría ser la IRA en el contexto de la HDA siendo una entidad con incidencia conocida de 8-11% según las series, asociado a irreversibilidad en 60% y mortalidad en 83%. (18) La HDA puede determinar IRA pre renal por hipovolemia e hipotensión en primera instancia, siendo además un conocido factor de riesgo para PBE en la evolución. (20,21) Reforzamos la idea de la interrelación de mecanismos patogénicos y la gravedad implícita a la hora de planificar correctamente los tratamientos así como las profilaxis.
Al igual que en otros estudios como el de Mathurin y col (2), nosotros tampoco encontramos una asociación entre HDA e IRA.
El uso de medios de contraste que determinan NTA causada por tóxicos, también llamada NIC responde a un mecanismo lesional multifactorial. Se caracteriza por un daño provocado por toxicidad directa del medio de contraste, cambios en la hemodinamia renal (18) y efectos deletéreos de la osmolaridad del producto administrado que determinan la elevación de la creatinina sérica evidente al 2° o 3° día posterior al estudio y la recuperación tras 5 a 7 días de tratamiento adecuado.(22,23) Algunos trabajos demuestran que los pacientes con ascitis son más vulnerables a la NIC. (20) En nuestro trabajo aunque no encontramos asociación estadística significativa, el uso de medios de contraste estuvo vinculado a 4/18 (FR 0,22) de los episodios de IRA, sin detectarse en los episodios sin IRA.
Destacamos que en ninguno de los casos se realizaron las medidas de nefroprevención recomendadas. (13, 14)
En cuanto a las características clínicas de la enfermedad hepática, en el estudio de Mathurin y col se demostró que el riesgo de IRA esta aumentado en los pacientes con hiperbilirrubimemia (2) , asumiendo que la misma contribuye a la nefrotoxicidad. (14)
En nuestro trabajo no logramos vincular la peoría de la funcionalidad hepática con el desarrollo de IRA al considerar las cifras de bilirrubina total, la tasa de protrombina y la albúmina.
En cuanto a los días de internación ambos grupos presentaron una media superior a la media de estadía hospitalaria.
Con respecto a la mortalidad fallecieron 2/16 pacientes del grupo con IRA y ninguno del grupo sin IRA, sin que hubiese asociación estadísticamente significativa.
Conclusiones
Concluímos que en los pacientes portadores de cirrosis hepática ingresados al sistema hospitalario la IRA es frecuente y responde a varias causas donde destacan las que determinan una caída de la perfusión renal o causas pre-renales.
La hipotensión es frecuente en estos pacientes que requieren varios tratamientos e intervenciones y tienen complicaciones inherentes a su enfermedad de base. La hipotensión fue más prevalente en el grupo con IRA.
No hubo diferencia estadísticamente significativa en nuestro trabajo, la utilización de medios de contraste se identificó únicamente en el grupo con IRA y es un factor ampliamente reconocido en la determinación de ésta, evitable con medidas de prevención estandarizadas.
No se registraron diferencias estadísticamente significativas en cuanto a la mortalidad y días de internación entre ambos grupos.
Es necesario continuar profundizando en esta temática con trabajos prospectivos que analicen esta población específica de pacientes que presentan particularidades características.
Agradecimientos
Al Prof. Agregado Dr. José Valiño y Dra. Luciana Spinelli por sus aportes durante el desarrollo del trabajo, a los médicos residentes Dra. Sofía De Betolaza y Dr. Javier Gaudiano por contribuir con la recolección de la información.
Bibliografía
1-Paolo A, Pere G, Florence W, Mauro B. Diagnosis and management of acute kidney injury in patientswith cirrhosis: Revised consensus recommendations of the International Club of Ascites. J Hepatol. 2015;62(4):968-74
2- Mathurin S, Jaimet C, Turletti C, Arosio A, González G, Kuzmicz G. Insuficiencia renal en pacientes con cirrosis y ascitis: incidencia, etiología y factores predictivos. Acta Gastroenterol Latinoam. 2008;38(2):116-25.
3-Arroyo V, Ginès P, Gerbes AL, Dudley FJ, Gentilini P, LaffiG, et al. Definition and diagnostic criteria of refractory ascites and hepatorrenal syndrome in cirrhosis. International Ascites Club.Hepatology 1996;23:164-176.
4- Wong F, Nadim MK, Kellum JA, Salerno F, Bellomo R, Gerbes A, et al. Working Party proposal for a revised classification system of renal dysfunction in patients with cirrhosis. Gut 2011; 60(5): 702-9
5-Graupera I, Cárdenas A. Enfoque diagnóstico de la Insuficiencia Renal en los Pacientes con Cirrosis. Clin liver dis. 2013;2: 3S-7S.
6-Thalheimer U, Burroughs A. To Close the stable door before the horse has bolted. J Hepatol. 2014, 60: 678-9
7-Tsien C, Rabie R, Wong F. Acute kidney injury in decompensated cirrhosis. Gut. 2013; 1 : 131- 138
8-Mehta RL, Kellum JA, Shah SV, Molitoris BA, Ronco C, Warnock DG, et al. Acute Kidney Injury Network. Acute Kidney Injury Network: report of an initiative to improve outcomes in acute kidney injury. Crit Care. 2007;11:R31
9- Scott RA, Austin AS, Kolhe NV, McIntyre CW, Selby NM. Gastroe Acute kidney injury is independently associated with death in patients with cirrhosis. Gastroenterologhy.2013;4: 191–197.
10-Salerno F, Gerbes A, Gines P, Wong F, Arroyo V. Diagnosis,prevention and treatment of hepatorrenal syndrome in cirrhosis. A consensus workshop of the international ascites club. Postgrad Med J. 2008; 84(998):662-70.
11-Schepke M, Appenrodt B, Heller J, Zielinski J, Sauerbruch T. Prognostic factors for patients with cirrhosis and kidney dysfunction in the era of MELD: results of a prospective study. Liver Int. 2006; 26: 834–839
12- Thadhari R, Pascual M, Bonventre J. Acute renal failure. N Engl J Med. 1996;334(22): 1448-60.
13-Silvariño R, Noboa Oscar. Prevención de la lesión renal en el perioperatorio de cirugía no cardíaca [en línea). Arch Med Int. 2011[acceso: 2016-02-01)1; 33: 59-64. Disponible en: http://www.scielo.edu.uy/pdf/ami/v33n3/v33n3a02.pdf
14-Uruguay. Ministerio de Salud Pública. Ordenanza Ministerial nº89 del 28 de febrero de 2014 (en línea). Montevideo: MSP; 2014 (acceso julio 2016).
Disponible en: http://www.msp.gub.uy/sites/default/files/archivos_adjuntos/Ord.%20Min.%20N%C2%BA%2089%20y%20Anexos.pdf
15- Wu CC, Yeung LK, Tsai WS, Tseng CF, Chu P, Huang TY, et al. Incidence and factors predictive of acute renal failure in pacients with advanced liver cirrhosis. Clin Nephrol. 2006;65:28-33.
16- Heras M, Fernández-Reyes M J, Guerrero M T, Sánchez R, Muñoz A, Molina Á, et al. Factores predictores de fracaso renal agudo en ancianos con enfermedad renal crónica (en línea ). Nefrología (Madr.) 2012 (acceso 2016 Mar. 09]; 32(6): 819-823. Disponible en: http://www.revistanefrologia.com/es-publicacion-nefrologia-articulo-factores-predictores-fracaso-renal-agudo-ancianos-con-enfermedad-renal-cronica-X0211699512002232
17- Martinez J, Albillos A. Tratamiento de la ascitis refractaria. Gastroenterol Hepatol. 2014; 37 (S2): 68-73.
18- Ruiz del Árbol L, Prevención de Insuficiencia renal en el paciente cirrótico(en línea]. Gastroenterol Hepatol Contin 2006 (acceso May 2016] ;5:241-5 Disponible en www.elsevier.es/es-revista---pdf-70000313-S300
19- Ruiz-del-Arbol L, Urman J, Fernández J, González M, Navasa M, Monescillo A, et al. Systemic, renal, and hepatic hemodynamic derangement in cirrhotic patients with spontaneous bacterial peritonitis. Hepatology 2003;38:1210-1218
20- Choi H, Kim Y, Kim SM, Shin J, Jang HR, Lee JE, et al Intravenous albumin for the prevention of contrast-induced nephropathy in patients with liver cirrhosis and chronic kidney disease undergoing contrast-enhanced CT. Kidney Res Clin Pract. 2012;31(2):106-11.
21- Hartleb M, Gutkowski K. Kidneys in chronic liver diseases. World J Gastroenterol. 2012;18(24):3035-49.
22- Aguirre M. Nefropatía por medio de contraste (en línea]. Acta Med Colombia. 2007 (acceso 2016 Mar 17); 32: 68-79.
23- Solomon R, Deray G. Consensus Panel for CIN. How to prevent contrast induced- nephropathy and manage risk patients: Practical recommendations. Kidney Int Suppl. 2006;(100):S51-3.














