Services on Demand
Journal
Article
Related links
Share
Revista Uruguaya de Medicina Interna
Print version ISSN 2393-6797On-line version ISSN 2393-6797
Rev. Urug. Med. Int. vol.1 no.2 Montevideo Aug. 2016
Artículo original
Enfermedad de hígado graso no alcohólico: abordaje clínico y genético.
Primer estudio nacional.
Disease nonalcoholic fatty liver disease: clinical and genetic approach.
First national study.
Lic. Carolina Beloso (*)
Grado 1. Departamento de Biodiversidad y Genética.
Dr. Marcos Pintos (+)
Médico Internista. Ex Asistente Clínica Médica
Dra. Mercedes Perendones (+)
Médico Internista. Profesor Agregado Clínica Médica
Dra. Adriana Mimbacas (*)
Profesor Adjunto de Investigación DT. Encargada del Grupo Genética Humana.
Recibido: 12/4/16 - Aceptado: 24/7/16
Departamento e Institución responsables: (*) Departamento de Biodiversidad y Genética. Instituto de Investigaciones Biológicas Clemente Estable. (+) Clínica Médica 2. Prof. Dra. Mabel Goñi. Hospital Pasteur. Facultad de Medicina. Universidad de la República. Montevideo – Uruguay.
Correspondencia: Lic.Carolina Beloso, Av Italia 3318, tel: 24861417-Fax:2487-5461correo electrónico: carobeloso@gmail.com
RESUMEN
Introducción: La enfermedad de hígado graso no alcohólico representa un grupo heterogéneo de afecciones hepáticas, caracterizadas por el depósito graso (triglicéridos) a nivel hepático vinculadas a la presencia del síndrome metabólico. Es una enfermedad compleja y multifactorial influenciada por el estilo de vida, factores nutricionales y genéticos. La variante -493G/T en el gen PMTT podría ser un marcador molecular útil en el estudio de la EHGNA. Objetivo: genotipificación del SNP -493G/T en el promotor del gen que produce la PMTT analizando si existe asociación de este SNP con la enfermedad. Resultados: Se analizaron 41 individuos con EHGNA (casos) y 42 individuos (controles). Se encontraron diferencias estadísticamente significativas en el índice de masa corporal (IMC) y algunas variables que corresponden al perfil lipídico y perfil hepático. No se encontró diferencia en la presencia de los genotipos G/G, G/T y T/T entre ambos grupos. Conclusiones: los hallazgos genéticos a nivel internacional son contradictorios y se relacionan a las diferentes conformaciones étnicas de las poblaciones y el grado de miscegenación.
Palabras claves: Enfermedad hígado graso no alcohólico. Genotipificación.
ABSTRACT
Introduction: The disease NAFLD represents a diverse group of liver disease, characterized by fatty deposits (triglycerides) in the liver associated with the presence of metabolic syndrome. It is a complex and multifactorial disease influenced by lifestyle, nutritional and genetic factors. The -493G / T variant in PMTT gene could be a molecular marker useful in the study of NAFLD. Objective: SNP genotyping -493G / T in the promoter of the gene that produces the PMTT analyzing whether there is an association of this SNP with the disease. Results: 41 individuals with NAFLD (cases) and 42 individuals (controls) were analyzed. Statistically significant differences in body mass index (BMI) and some variables corresponding lipid profile and liver profile found. No difference was found in the presence of genotypes G / G, G / T and T / T between the two groups. Conclusions: genetic findings internationally are contradictory and different ethnic conformations of populations and the degree of miscegenation relate.
Keywords: Disease NAFLD. Genotyping.
Introducción
La Enfermedad de Hígado Graso no Alcohólico (EHGNA) es una enfermedad metabólica caracterizada por una acumulación anormal de triglicéridos (TG) en el hígado sin consumo de alcohol en cantidades toxicas (1). Incluye un espectro de enfermedades que van desde la esteatosis simple (ES) que representa la infiltración grasa del hígado, esteatohepatitis no alcohólica (EHNA) que correspondiendo a la presencia de grasa con inflamación con distintos grados de fibrosis llegando incluso a cirrosis hepática (CH) (2). La ES es benigna, mientras que la EHNA puede conducir a CH con insuficiencia hepática y al carcinoma hepatocelular (3).
La EHGNA es una de las principales causas de enfermedad hepática crónica en todo el mundo y está directamente relacionada con el aumento de la prevalencia de la obesidad y la diabetes mellitus tipo 2 (DM2) en la población general (4).
En Uruguay no se conoce la prevalencia de esta enfermedad por lo cual debe tenerse en cuenta las comorbilidades asociadas. Los estudios de prevalencia de obesidad ENSO II, realizada en el año 2009, mostraron que el 54% de la población uruguaya tiene sobrepeso/obesidad y el 25.6% tiene una cintura mayor a 100 cm (5). La prevalencia de Diabetes es de un 8% (6).
Extrapolando en base a estás comorbilidades, se puede estimar que la prevalencia de la enfermedad en Uruguay sería elevada.
Los síntomas de la EHGNA varían considerablemente de persona a persona, siendo incluso una enfermedad asintomática en la mayoría de ellas. La elevación de la enzima hepática transaminasa Glutámico Pirúvica (TGP) es una de las principales alteraciones analíticas que se observan en la enfermedad.
El diagnóstico de EHGNA se confirma a través del hallazgo de un hígado hiperecogénico en ecografía o por intermedio de una tomografía computarizada (TC), confirmando la esteatosis. A través del funcional y enzimograma hepático se valora los elementos de actividad hepática que sirven como elemento de sospecha para la enfermedad.
La patogenia puede explicarse por el modelo propuesto llamado “two hits” (“dos impactos”) (7). En el que el “primer hit” consiste en una excesiva acumulación de grasas en el hígado debido, en la mayoría de los casos, a la insulino resistencia (IR) predisponiendo al hígado a una inflamación crónica, pero no es suficiente para causar EHNA (8). Como los factores de riesgo responsables del “segundo hit” fueron indicados el estrés oxidativo debido a especies reactivas del oxígeno (9), lipopolisacáridos derivados de la ingesta y mediadores solubles liberados tanto del sistema inmune como del tejido adiposo (10). Es en esta etapa en donde se desarrolla la EHNA que puede luego evolucionar a cirrosis.
Desde el punto de vista de la patogénesis la EHGNA se considera una enfermedad compleja y multifactorial influenciada por el estilo de vida, factores nutricionales y genéticos (11). La acumulación de TG en el hepatocito es considerado el mayor desencadenante patogénico en el desarrollo de la EHGNA (12).
Anomalías en el metabolismo de lípidos y lipoproteínas acompañadas de inflamación crónica son considerados los pasos centrales para el desarrollo de comorbilidades relacionadas con la obesidad, como son la EHGNA y las enfermedades cardiovasculares (13,14).
En los pacientes con EHGNA, durante el ayuno el hígado aumenta la producción de lipoproteínas de muy baja densidad (VLDLs) ricos en TG (15,16) al igual que frente al estado de hiperinsulinemia (17).
Desde el punto de vista genético, ciertas variaciones genéticas en el metabolismo lipídico pueden producir diferencias en la velocidad de acumulación de lípidos en los hepatocitos. El gen PMMT (proteína microsomal transportadora de triglicéridos) mapea en el cromosoma 4q23 y está compuesto por 17 intrones (18). La proteína codificada por este gen regula la incorporación de TG en las Apolipoproteinas B100 y es una enzima clave para el ensamblaje y secreción de VLDLs.(8,19)
Se sabe que la baja expresión hepática de la PMTT es inducida por polimorfismos genéticos en el gen PMTT y está relacionado con la patogénesis de la EHGNA (20,21). Bernard y cols en el año 2000 (22) detectaron que en el polimorfismo de un solo nucleótido (SNP) -493G/T en el promotor del gen PMTT, el alelo G disminuye la transcripción de dicho gen, tiende a incrementar la concentración intrahepática de TG provocando susceptibilidad a EHNA.
La información expuesta anteriormente más el hecho que la mayor ruta de eliminación de TG del hígado son la beta oxidación de ácidos grasos y la secreción de VLDLS (23), la variante -493G/T en el gen PMTT podría ser un marcador molecular útil en el estudio de la EHGNA.
El objetivo de este trabajo fue la genotipificación del SNP -493G/T en el promotor del gen que produce la PMTT analizando si existe asociación de este SNP con la enfermedad.
Materiales y Métodos
Población
Los pacientes (casos) fueron seleccionados en un periodo desde 2011 al 2013 por médicos de la Policlínica de Hepatopatía del Hospital Pasteur de Montevideo con diagnóstico de EHGNA confirmado a través de estudios imagenológicos (ecografía y/o TC). Fueron excluidos pacientes con consumo de alcohol en exceso, Hepatitis viral u otra causa de Hepatopatía.
Los controles fueron recolectados por los mismos médicos en las salas de internación del mismo hospital. Se descartó la presencia de la EHGNA mediante ecografía y cumplían con los mismos criterios de exclusión que los pacientes.
Todos los individuos firmaron el consentimiento escrito aprobado por el Comité de ética.
Procesamiento de muestras y Genotipificación
En el laboratorio del IIBCE se recibió la sangre de los pacientes y controles seleccionados. A partir de esa muestra se realizó extracción de ADN genómico mediante el método Fenol-cloroformo a partir de 5 ml de sangre periférica y se midió la pureza del mismo mediante el espectrofotómetro UV/visible (NanodropTM2000).
El diseño de primers y sondas específicas para la genotipificación del SNP -493G/T (rs1800591) del gen PMTTse realizó mediante la utilización del Software BeaconDesigner 7. Las secuencias diseñadas fueron: Primer F TTCACACATAAGGACAATCA, Primer R GGACATCTTTGATTTTTATGC, Sonda G/G HEX-TTGAAGTGATTGGTGGTGGTATGAATT-BHQ1 y SondaT/T FAM-TTGAAGTGATTGGTTGTGGTATGAATT-BHQ1.
Tanto los casos como los controles fueron genotipificados por duplicado mediante reacción en cadena de la polimerasa (PCR) en tiempo Real con el uso de sondas Taqman® y utilizando controles negativos en todos los experimentos. Se utilizó el equipo Rotor Gene 6000 con un software de análisis de las series 1.7 (CorbettResearch, Division de CorbettLifeScience). Se confirmó la amplificación del fragmento esperado mediante secuenciación (Macrogen, Corea) y se alinearon las secuencias mediante el programa Mega 5.05.
Análisis estadístico
El análisis de los resultados fue realizado mediante el software del Corbett 6000 y el paquete estadístico SPSS v.10.0 (SPSS Inc. Chicago). El análisis del polimorfismo fue realizado con la herramienta online SNPStats (http://bioinfo.iconcologia.net/snpstats/start.htm). El estadístico sigue una distribución chi-cuadrado con grados de libertad igual al número de parámetros adicionales en el modelo más complejo y el menor valor de criterio de información Akaike (AIC) y bayesiano (BIC). Se consideró en todos los casos una diferencia estadística significativa con p<0.05 y un intervalo de confianza (IC) del 95%.
Resultados
Se analizaron un total de 41 individuos (31 mujeres y 10 hombres) diagnosticados con EHGNA (casos) y 42 individuos (22 mujeres y 20 hombres) que no tienen la enfermedad (controles). En todos los individuos se realizó la extracción de ADN y se obtuvieron buenas concentraciones y pureza del mismo.
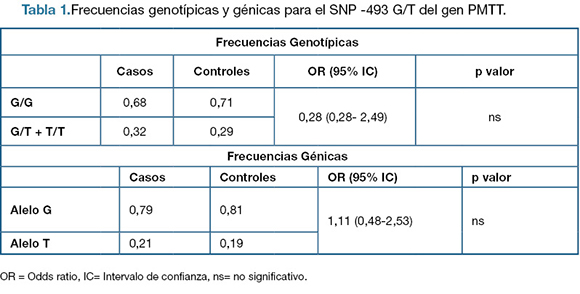
Se genotipificó mediante Real Time PCR con Sondas Taqmanlos controles y los casos y las frecuencias genotípicas obtenidas para el SNP -493G/T del gen PMTT se observa en la Figura 1.
Mediante el uso del programa SNPstat se seleccionó el mejor modelo de herencia para el SNP estudiado: modelo recesivo (G/G vs G/T+T/T), con un p valor= 0.71, AIC=107.5 y BIC= 112.1. La muestra de controles se encuentra en equilibrio Hardy-Weinberg, no así la muestra de casos (p=0.04). En la Tabla 1 se observan los resultados de las frecuencias genotípicas, según el modelo de herencia utilizado, y de las frecuencias alélicas encontradas en toda la población. El análisis mediante tablas de contingencia de 2 x 2 para la búsqueda de asociación entre el SNP y la población no mostró diferencias estadísticas significativas entre casos y controles.
Tabla 1.Frecuencias genotípicas y génicas para el SNP -493 G/T del gen PMTT.
Se realizó la comparación de las distintas variables paraclínicas en los casos y controles (Tabla 2).
Tabla 2. Características clínicas y bioquímicas de la población. Test de t de las variables analizadas en ambas poblaciones con sus medias y desvió estándar (X ± DS).
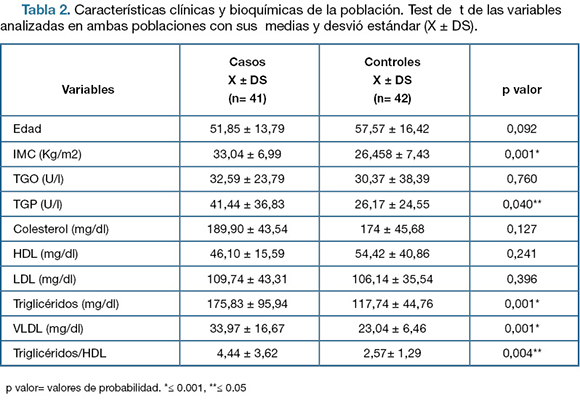
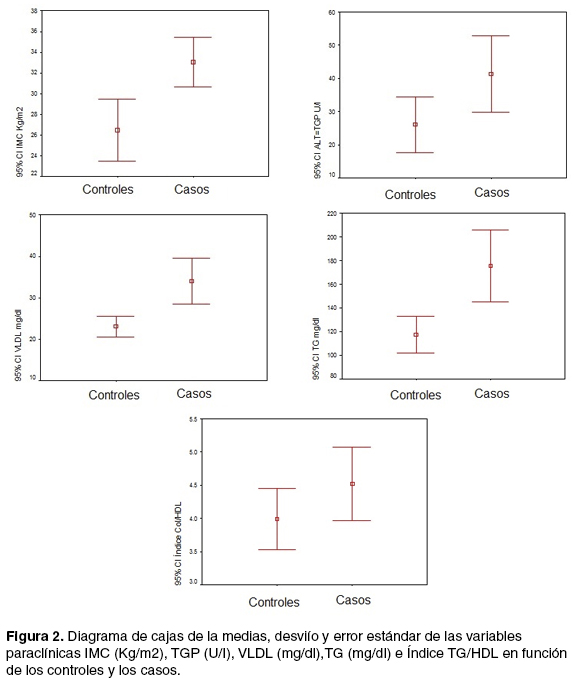
Se observaron diferencias estadísticamente significativas en el índice de masa corporal (IMC) y algunas variables que corresponden al perfil lipídico y perfil hepático (Tabla 2). Las variables con diferencias significativas se graficaron en diagramas de caja (Figura 2). No se encontraron diferencias al realizar el estudio por sexos por lo cual esta variable no está actuando como confusora.
Discusión y comentarios
La EHGNA es una enfermedad de origen multifactorial en la que contribuyen varios factores genéticos y ambientales. Variantes genéticas relacionadas principalmente con el metabolismo de lípidos, insulino resistencia y estrés oxidativo incrementan la susceptibilidad a la enfermedad.
En la bibliografía existente se postula que la EHGNA sería el componente hepático del síndrome metabólico y se encuentra asociada con la epidemia mundial de obesidad (4,24). En gran parte es por esto que resulta muy interesante su estudio.
En nuestro trabajo observamos que de los 41 pacientes diagnosticados con EHGNA, 31 son mujeres mientras que solo 10 son hombres. Con respecto a la diferente prevalencia en relación al sexo, en la bibliografía existen resultados contradictorios encontrándose quienes encuentran la enfermedad mayormente asociado en mujeres y otros en hombres (25,26).
Los datos generales de la población del Hospital Pasteur entre 2012-2013 (según datos epidemiológicos del Departamento de Registros Médicos), mostraron que se atendieron un 55% de hombres y un 45% de mujeres. Sin embargo, en lo que respecta a la población en estudio derivada a la Policlínica de Hepatopatías parecería no mantenerse dicha proporción. Esto podría explicarse por el hecho que, en la mayoría de los casos, es una enfermedad asintomática por lo cual no todos los pacientes son derivados a la policlínica de hepatopatías. A su vez en la bibliografía más allá de la asociación por sexo, existe una mayor prevalencia de EHGNA en mujeres posmenopáusicas (27). Esto último se aprecia en nuestra muestra de casos ya que, el promedio de edad de las mujeres fue de 55 años.
Tanto en la muestra con EHGNA como en la muestra sin la enfermedad se encontró aproximadamente el mismo porcentaje de genotipos G/G, G/T y T/T en ambas. Según el modelo de herencia que se utilizó (G/G vs G/T+T/T) no se encontró asociación estadísticamente significativa con la enfermedad (OR=0,28; IC 0,45-3,23; p=0,71). En la bibliografía existen muchos trabajos en las que se analiza este polimorfismoen poblaciones de diferentes etnias y donde se separa la población con EHGNA en esteatosis simple y estados avanzados de la misma (EHNA y cirrosis). Ejemplos de estos trabajos demuestran que pacientes con el genotipo G/G presentaban un estado más avanzado de la enfermedad (22,28).Sin embargo, Olivera et al.,en el año 2010 observaron que en una población de pacientes de Brasil, no se encontraron diferencias significativas en la frecuencia de los genotipos G/G y G/T cuándo clasificaron la población en EHNA vs esteatosis simple y entre pacientes con EHGNA y controles (29). Estas contradicciones encontradas en la bibliografía en relación a la asociación del polimorfismo estudiado con la enfermedad podría ser efecto de las diferentes conformaciones étnicas de las poblaciones y el grado de miscegenación.
La población uruguaya presenta un origen tríhibrido (europeo, africano, amerindio) con mayor proporción de origen caucásico pero con un alto grado de miscegenación (30) y un significante aporte amerindio de origen materno (31,32). Este podría ser uno de los factores que generan variabilidad en los resultados de genotipificación encontrados. La prevalencia de la EHGNA varía desde un 45% entre los hispanos, a un 24% en afroamericanos y un 33% en los caucásicos estadounidenses (33). Entre los asiáticos ocurre en un 25% (34). Recientemente, en un meta-análisis del SNP -493 G/T en el gen PMTT, se concluye que éste podría aumentar el riesgo de EHGNA tanto en poblaciones caucásicas como no caucásicas (35).
En nuestro trabajo no se encontró asociación con la enfermedad. Sin embargo, la población con EHGNA no se encuentra en equilibrio Hardy Weinberg. Esto estaría indicando una posible asociación entre el polimorfismo -493 G/T en el gen PMTT con la EHGNA pero que existen algunas variables o sesgos que podrían estar enmascarando este hecho. Pensamos que el número de individuos que se colectaron en el plazo establecido fue bajo lo que constituiría una de las limitantes de este estudio.
Por otro lado este polimorfismo se ha asociado a etapas más avanzadas de la enfermedad. En nuestra población no fue posible clasificar a todos los pacientes según esteatosis simple vs. estadios avanzados, para poder realizar estudios comparativos como los descriptos anteriormente. Este hecho se debió a que la técnica que se utiliza para clasificar las etapas de la enfermedad es la biopsia hepática y al ser una técnica invasiva solo fue utilizada exclusivamente en los pacientes en que se consideró estrictamente necesaria.
Desde el punto de vista clínico, en nuestro trabajo el IMC, TGP, VLDL, TG e Índice de IR son variables que mostraron diferencias estadísticamente significativas entre casos y controles. El IMC y la resistencia a la Insulina de los pacientes con EHGNA tienen una media mayor a los controles. Está ampliamente descripto en las publicaciones que estas variables son factores de riesgo para la EHGNA y para su progresión a estadios más avanzados (36,37). LaTGPes uno de los marcadores bioquímicos que se encuentra mayormente alterado en las personas con la enfermedad por lo cual comparando con nuestros controles, es interesante ver el claro aumento de esta enzima en la población enferma. Respecto al perfil lipídico de nuestros pacientes encontramos también una media superior de VLDLs y triglicéridos. Estos parámetros derivan de la presencia de insulino resistencia que existe en nuestra población lo que genera sobreproducción de VLDLs y niveles elevados de triglicéridos (15).
En suma, en nuestro trabajo se genotipificó una variante genética que a priori estaría relacionada con la enfermedad. La genotipificación se realizó con tecnología de punta como son las sondas Taqman que tienen una gran eficiencia y sensibilidad. Cuando analizamos los diferentes factores de riesgo vimos que algunos de ellos se presentaban con diferencia estadísticamente significativa entre casos y controles.
La creación de una base de ADN y de datos de una población con la EHGNA permitirá en un futuro seguir trabajando en el estudio de la enfermedad pudiéndose ampliar la cantidad de casos. Los nuevos estudios genéticos podrían estar enfocados al análisis de otras variantes génicas relacionadas con, por ejemplo, rutas vinculadas con la inflamación en particular la inducción de citocinas proinflamatorias como la interleucina 6.
Actualmente se estudian técnicas de imagen más modernas como la elastografía de transición (Fibroscan®); método no invasivo de detección de fibrosis, cuya aplicación aún se encuentra en la esfera de las investigaciones y los diseños de protocolos (38). Esta nueva tecnología ya se encuentra disponible en Uruguay y podría ser de gran ayuda en la detección de fibrosis hepática (39).
Bibliografía
1. Adams L a., Lymp JF, St. Sauver J, Sanderson SO, Lindor KD, Feldstein A, et al. The natural history of nonalcoholic fatty liver disease: A population-based cohort study. Gastroenterology. 2005;129:113–21.
2. Farrell GC, Larter CZ. Nonalcoholic fatty liver disease: from steatosis to cirrhosis. Hepatology. 2006;43(2 Suppl 1):S99–112.
3. Vanni E, Bugianesi E, Kotronen A, De Minicis S, Yki-Järvinen H, Svegliati-Baroni G. From the metabolic syndrome to NAFLD or vice versa? Dig Liver Dis. 2010;42:320–30.
4. López-Velázquez JA, Silva-Vidal K V, Ponciano-Rodríguez G, Chávez-Tapia NC, Arrese M, Uribe M, et al. The prevalence of nonalcoholic fatty liver disease in the Americas. Ann Hepatol. 2014;13:166–78.
5. Pisabarro R, Gutiérrez M, Bermúdez C, Prendez D, Recalde A, Chaftare Y, et al. Segunda Encuesta Nacional de Sobrepeso y Obesidad ( ENSO 2 ) adultos ( 18-65 años o más ). Rev Med Urug 2009; 25: 14-26.
6. Ferrero R, García MV. Encuesta de prevalencia de la diabetes en Uruguay. Arch Med Interna. 2005;27(1):7–12.
7. Day CP, James OF. Steatohepatitis: a tale of two “hits”? Gastroenterology. 1998;114(4):842–5.
8. Malaguarnera M, Di Rosa M, Nicoletti F, Malaguarnera L. Molecular mechanisms involved in NAFLD progression. J Mol Med (Berl). 2009;87(7):679–95.
9. Day CP. From fat to inflammation. Gastroenterology. 2006 Jan;130(1):207–10.
10. Lalor PF, Faint J, Aarbodem Y, Hubscher SG, Adams DH. The role of cytokines and chemokines in the development of steatohepatitis. Semin Liver Dis. 2007;27(2):173-93.
11. Ono M, Okamoto N, Saibara T. The latest idea in NAFLD/NASH pathogenesis. Clin J Gastroenterol. 2010;3(6):263–70.
12. Tacer KF, Rozman D. Nonalcoholic Fatty liver disease: focus on lipoprotein and lipid deregulation. J Lipids. 2011;
13. Schindhelm RK, Heine RJ, Diamant M. Prevalence of nonalcoholic fatty liver disease and its association with cardiovascular disease among type 2 diabetic patients. Diabetes Care. 2007;30(9):e94.
14. Loria P, Lonardo A, Bellentani S, Day CP, Marchesini G, Carulli N. Non-alcoholic fatty liver disease (NAFLD) and cardiovascular disease: an open question. Nutr Metab Cardiovasc Dis. 2007;17(9):684–98.
15. Adiels M, Taskinen MR, Packard C, Caslake MJ, Soro-Paavonen A, Westerbacka J, et al. Overproduction of large VLDL particles is driven by increased liver fat content in man. Diabetologia. 2006;49(4):755–65.
16. Fabbrini E, Mohammed BS, Magkos F, Korenblat KM, Patterson B, Klein S. Alterations in Adipose tissue and Hepatic lipid kinetics in obese men and women with nonalcoholic fatty liver disease. Gastroenterology. 2008;134(2):424–31.
17. Adiels M, Westerbacka J, Soro-Paavonen a, Häkkinen a M, Vehkavaara S, Caslake MJ, et al. Acute suppression of VLDL1 secretion rate by insulin is associated with hepatic fat content and insulin resistance. Diabetologia. 2007;50(11):2356–65.
18. Shoulders CC, Narcisi TM, Read J, Chester A, Brett DJ, Scott J, et al. The abetalipoproteinemia gene is a member of the vitellogenin family and encodes an alpha-helical domain. Nat Struct Biol. 1994;1(5):285–6.
19. De Alwis NMW, Day CP. Genes and nonalcoholic fatty liver disease. Curr Diab Rep. 2008;8(2):156–63.
20. Dowman JK, Tomlinson JW, Newsome PN. Pathogenesis of non-alcoholic fatty liver disease. QJM. 2010;103(2):71–83.
21. Siqueira ER, Oliveira CP, Correa-Giannella ML, Stefano JT, Cavaleiro AM, Fortes MA, et al. MTP -493G/T gene polymorphism is associated with steatosis in hepatitis C-infected patients. Braz J Med Biol Res. 2012;45(1):72-7
22. Bernard S, Touzet S, Personne I, Lapras V, Bondon PJ, Berthezène F, et al. Association between microsomal triglyceride transfer protein gene polymorphism and the biological features of liver steatosis in patients with Type II diabetes. Diabetologia. 2000;43(8):995–9.
23. Donnelly KL, Smith CI, Schwarzenberg SJ, Jessurun J, Boldt MD, Parks EJ. Sources of fatty acids stored in liver and secreted via lipoproteins in patients with nonalcoholic fatty liver disease. J Clin Invest. 2005;115(5):1343–51.
24. Dietrich P, Hellerbrand C. Non-alcoholic fatty liver disease, obesity and the metabolic syndrome. Best Pract Res Clin Gastroenterol. 2014;28(4):637-53.
25. Castro-martínez MG, Banderas-lares DZ, Ramírez-Martínez JC, Peña JE. Prevalencia de hígado graso no alcohólico en individuos con síndrome metabólico. Cir Cir 2012;80:128-133.
26. Loguercio C, De Simone T, D'Auria MV, de Sio I, Federico A, Tuccillo C, et al. Non-alcoholic fatty liver disease: a multicentre clinical study by the Italian Association for the Study of the Liver. Dig Liver Dis. 2004;36(6):398-405.
27. Carulli L, Lonardo A, Lombardini S, Marchesini G, Loria P. Gender, fatty liver and GGT. Hepatology. 2006 Jul;44(1):278–9.
28. Namikawa C, Shu-Ping Z, Vyselaar JR, Nozaki Y, Nemoto Y, Ono M, et al. Polymorphisms of microsomal triglyceride transfer protein gene and manganese superoxide dismutase gene in non-alcoholic steatohepatitis. J Hepatol. 2004;40(5):781–6.
29. Oliveira CP, Stefano JT, Cavaleiro AM, Zanella Fortes MA, Vieira SM, Rodrigues Lima VM, et al. Association of polymorphisms of glutamate-cystein ligase and microsomal triglyceride transfer protein genes in non-alcoholic fatty liver disease. J Gastroenterol Hepatol. 2010 Feb;25(2):357-61
30. Hidalgo PC, Bengochea M, Abilleira D, Cabrera A, Alvarez I. Genetic Admixture Estimate in the Uruguayan Population Based on the Loci LDLR , GYPA , HBGG , GC and D7S8. Int J Hum Genet. 2005;5(3):217–22.
31. Bonilla C, Bertoni B, González S, Cardoso H, Brum-Zorrilla N, Sans M. Substantial Native American female contribution to the population of Tacuarembó, Uruguay, reveals past episodes of sex-biased gene flow. Am J Hum Biol. 2004;16(3):289-97.
32. Gascue C, Mimbacas A, Sans M, Gallino JP, Bertoni B, Hidalgo P, et al. Frequencies of the four major Amerindian mtDNA haplogroups in the population of Montevideo, Uruguay. Hum Biol. 2005;77(6):873–8.
33. Browning JD, Szczepaniak LS, Dobbins R, Nuremberg P, Horton JD, Cohen JC, et al. Prevalence of hepatic steatosis in an urban population in the United States: Impact of ethnicity. Hepatology. 2004;40:1387–95.
34. Nomura H, Kashiwagi S, Hayashi J, Kajiyama W, Tani S, Goto M. Prevalence of fatty liver in a general population of Okinawa, Japan. Jpn J Med. 1988;27(2):142–9.
35. Zheng W, Wang L, Su X, Hu X-F. MTP -493G>T polymorphism and susceptibility to nonalcoholic fatty liver disease: a meta-analysis. DNA Cell Biol. 2014 Jun;33(6):361–9.
36. Vernon G, Baranova A, Younossi ZM. Systematic review: The epidemiology and natural history of non-alcoholic fatty liver disease and non-alcoholic steatohepatitis in adults. Aliment Pharmacol Ther. 2011;34:274–85.
37. Brea Hernando A, Puzo Foncillas J. Enfermedad Del Hígado Graso No Alcohólico Y Riesgo Cardiovascular. Clin e Investig en Arterioscler. 2010;22(6):259–71.
38. Díaz J, Pereira O, León A, Del Valle S, Hodelín R. Relación entre los hallazgos ecográficos, laparoscópicos e histológicos en pacientes con esteatosis hepática no alcohólica. MEDISAN. 2015;19(3):345–53.
39. Pintos M, Perendones M, Goñi M. Elastometría hepática de transición. Nueva técnica de diagnóstico en hepatología. Arch Med Interna. 2013;35(3):80–4.