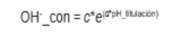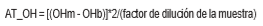Introducción
La acideztitulable se utiliza para estimar las magnitudesde encaladoensuelosácidos (Bailey, Stevens y Kilpatrick,1989; Bohn, McNeal y O’Connor, 1993; Casanova y Ferrando,2010). En Uruguay, la determinación de AT_pH = 7 seutiliza con fines taxonómicos, al ser un criterio de clasificaciónde los horizontes superficiales y para la identificacióndel Orden de suelos Desaturados Lixiviados (Altamirano etal., 1976).Al medir la acidez titulable a pH = 7 (AT_pH7) se determinala cantidad de acidez que el suelo es capaz de liberarcuando es llevado a ese valor de pH (Bohn, McNeal yO’Connor, 1993). Para su determinación, se agrega al suelouna solución tampón de pH = 7, lo cual genera que loscoloides del suelo liberen H+. Posteriormente se cuantificala acidez liberada mediante titulación con un álcali (Jackson,1976; Quaggio y van Raij, 2001; Camargo et al., 2009).Al ser el gasto de álcali durante la titulación proporcional a lacantidad de acidez, el valor de pH al que llega la mezclasuelo:acetato de calcio (pH_equilibrio) sería proporcional algasto de álcali. Es esperable que exista una relación linealentre intensidad y cantidad de acidez, en un rango de cincoa ocho unidades de pH (Curtin, Campbell y Messer, 1996).
El objetivo de este trabajo fue estimar la acidez titulable apartir del valor de pH_equilibrio, lo cual ahorraría tiempo ycosto de análisis al no tener que realizarse la titulación delas muestras. Se evaluó el impacto que tendría esta propuestaen la clasificación de los suelos acorde a su porcentajede saturación en bases.
Materiales y métodos
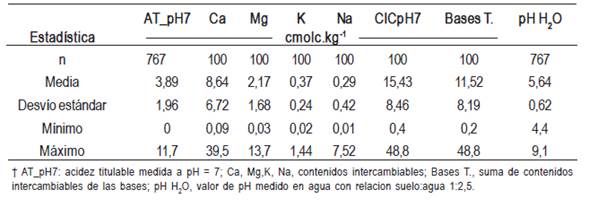
Se midió la acidez titulable a pH = 7 (AT_pH7) en 767muestras de horizontes A de diferentes suelos (Cuadro 1).Las muestras fueron secadas a 40 °C durante 48 horas ymolidas hasta pasar por malla de 2 mm.
A 5 g de suelo seco se le agregaron100 mL de acetatode calcio 1N buffereado a pH = 7, se agitó la mezcla durante10 minutos, se dejó reposar 16 horas y se filtró la extraccióncon papel Watman N°2. Se tomaron 40 mL del filtrado, semidió el pH_equlibrio, se tituló con NaOH 0,1 N hasta llegara pH = 7 y con el gasto de NaOH se calculó AT_pH7 (Camargoet al., 2009). En cada tanda de medición de AT_pH7(aproximadamente 40 muestras) se realizó la medición deun blanco, el cual consistió en una muestra sin suelo cuyovalor se descontó a cada muestra. Para las mediciones depH se utilizó electrodo con cuerpo de epoxy (ThermoSientific_9165NWP). La calibración del equipo se realizócon soluciones buffer de pH = 7 y pH = 4, acorde a loindicado por el fabricante, al comienzo de las mediciones ycada 15 muestras medidas.
Se ajustó un modelo de regresión para los valores deAT_pH7 en función de pH_equilibrio 1, con los valores delecturas de 160 muestras, denominado set de calibración. Alas muestras cuyo pH_equilibrio fuera superior al del acetatode calcio buffereado, previo a la titulación, se les asignó elvalor de pH_equlibrio del blanco. El modelo de regresiónobtenido se utilizó para estimar AT_pH7 (AT_eq) en un setde 607 muestras no utilizadas en la calibración, denominadoset de validación, cuyos valores de AT_pH7 también se midieron.
donde AT_pH7 son los meq.100 g-1 de acidez titulable apH = 7 en función de pH_equlibrio de las muestras ypH_equilibrio del blanco; b, c y a son coeficientes estimadospor mínimos cuadrados.
Se tituló el acetato de calcio desde pH = 7 hasta pH = 5(0,5 puntos de pH menor al pH_equilibrio más bajo observado)y se ajustó una función exponencial 2para explicarla relación entre la cantidad de álcali consumido (OH-_con)y el valor de pH alcanzado. Dicha relación se utilizó paraestimar la cantidad de equivalentes OH- consumidos porcada muestra (OHm) y blanco de cada tanda, a partir delrespectivo pH_equilibrio, mediante la ecuación 2.
donde OH-_con es la cantidad de equivalentes OH- neutralizadosen 100 mL de acetato de calcio al agregarle ácidoacético 1,9840 N para llegar a determinado valor de pH(pH_titulación).
La acidez titulable a pH = 7 (AT_OH) se estimó comola diferencia entre los OH consumidos por el extracto dela muestra (OHm) y los OH- consumidos por el blanco(OHb) 3
Se clasificaron 100 muestras seleccionadas al azardel set de validación, acorde a su saturación en bases apH = 7 (V7), en saturadas o desaturadas, según el valor V7fuera mayor o menor a 50 % respectivamente. La estimaciónV7 se basó en la suma de los cmolc.kg-1 de Ca, Mg, Nay K sobre la CIC estimada a pH = 7. Acorde al valor AT_pH7,AT_eq o AT_OH, se calcularon V7, V7_eq o V7_OH, respectivamente.
La exactitud de las estimaciones de AT_eq y AT_OH, seevaluó por regresión y comparación de medias apareadascon los valores AT_pH7, con el software InfoStat/P. Se consideraronlos valores AT_pH7 como correctos. La precisiónde las estimaciones AT_eq y AT_OH se evaluó a travésdel CV obtenido de cinco mediciones realizadas a cincomuestras. Se evaluó la concordancia entre la clasificaciónde suelos en saturados o desaturados por el índice de Kappa.
Resultados y discusión
Al ajustar la ecuación 1 con el set de calibración, losvalores de los coeficientes fueron: b = -21,47; c = 8,71;y a = 88,59; R2 = 0,94. Las diferencias entre AT_pH7 y laestimada a partir de la ecuación 1 para el set de calibracióntuvieron distribución normal (W = 0,98; p = 0,3469), por loque no hubo sesgo en la regresión ajustada. Al utilizar la función 1 para el set de validación, el ajuste obtenido fue satisfactorio (Cuadro 2). Hubo, sin embargo, sesgo en lasdiferencias entre AT_pH7 y AT_eq (W = 0,97; p < 0,001). Lamagnitud promedio de la diferencia (-0,50 cmolc.kg-1) difirióde cero (p < 0,001). Al estimar el valor de acidez titulable através del pH_equilibirio, subestimaríamos dicho valor. Podemosinferir que en las muestras aquí analizadas, la cantidade intensidad de la acidez mantuvieron una relación deproporción en el rango de acidez entre el pH_equilibrio y elpH = 7, lo cual concuerda con lo esperado acorde a Curtin,Campbell y Messer (1996). Gama et al. (2013) obtuvieronuna relación lineal de segundo orden y un valor de predicciónsimilar al aquí obtenido al relacionar el pH de equilibriode una solución de SMP con el valor de AT_pH7.
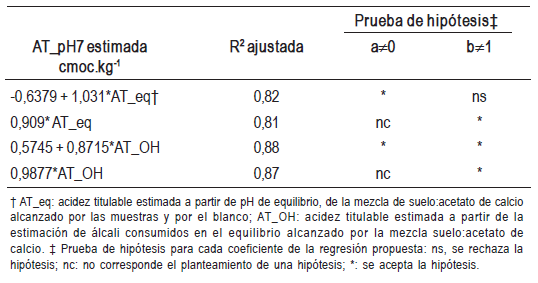
Cuadro 2: Ajuste de la estimación de acidez titulable a pH = 7 (ATpH7) a partir del pH deequilibrio de la mezcla suelo: acetato de calcio para el set de validación de 607 muestras.
La titulación del acetato de calcio permitió estimarlos coeficientes de la ecuación 2, los cuales fueron:c = 2437002,293; y d = -2,385. Se obtuvo un ajuste aceptableentre AT_pH7 y AT_OH, para el set de validación (Cuadro2). Las diferencias entre los valores, sin embargo, presentaronsesgos (W = 0,97; p < 0,001) y la magnitudpromedio de la misma (0,06 cmolc.kg-1) difirió de cero(p = 0,031). Al utilizar los valores AT_OH se estaría subestimandola acidez titulable, pero las diferencias serían demenor cuantía que al utilizar los valores AT_eq.
El valor de pH_equilibrio tuvo un CV promedio de 0,4 %al medir cinco repeticiones de una muestra; las estimacionesAT_eq y AT_OH, sin embargo, tuvieron coeficientespromedio de 13,9 y 18,8 % respectivamente, mientras elvalor de AT_pH7 tuvo un CV de 7,3 %. Aunque el valor depH_equlibrio es menos variable que la medición de AT_pH7,las estimaciones AT_eq y A_OH poseerían menor precisión.
Clasificación de las muestras acorde a su saturaciónen bases a CICpH7
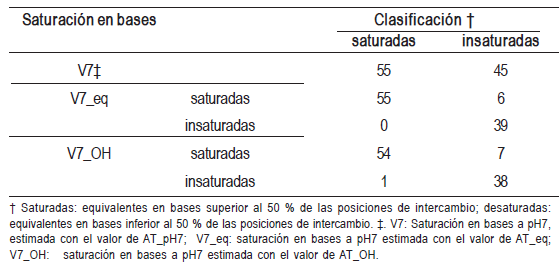
Al clasificar las muestras por V7_eq o V7_OH hubo pocasclasificaciones erróneas (Cuadro 3). El índice de concordanciade Kappa fue 0,877 y 0,836 para V7_eq y V7_OH,respectivamente. Ambos valores son considerados muybuenos acorde a Landis y Koch (1977).
Conclusiones
Al estimar la acidez titulable a pH = 7, a partir del valor depH al cual llega la solución de la mezcla suelo:acetato decalcio, hay diferencias estadísticamente significativas, peromuy bajas y no se introducen errores de consideración enla interpretación de resultados. Es posible, por lo tanto, utilizarestas estimaciones, con lo cual se puede estimar laacidez titulable a pH = 7 en menor tiempo y menores costos.