Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Agrociencia (Uruguay)
versión impresa ISSN 1510-0839versión On-line ISSN 2301-1548
Agrociencia Uruguay vol.19 no.1 Montevideo jun. 2015
Efecto de la temperatura de conservación en el contenido de carotenoides y vitamina C en frutos de pomelo rojo
Lado Joanna1,2 , Pascual Marta1, Zacarías Lorenzo1, Rodrigo María Jesús1
1 Instituto de Agroquímica y Tecnología de Alimentos CSIC. Av. Agustín Escardino 7, Paterna, Valencia 46980.
2 Instituto Nacional de Investigación Agropecuaria (INIA). Camino a la represa s/n, Salto, Uruguay.
Correo electrónico: jlado@inia.org.uy
Recibido: 26/9/14 Aceptado: 20/4/15
Resumen
Los carotenoides y la vitamina C son componentes importantes de la calidad nutricional y organoléptica en los frutos cítricos. Los frutos de pomelo rojo deben su coloración a la presencia de licopeno, un caroteno lineal de color rojo, tanto en la piel como en la pulpa, una característica muy inusual en los frutos cítricos. Esta propiedad le confiere a los frutos un interés especial dada la gran actividad antioxidante de este compuesto y sus posibles beneficios para la salud. La conservación refrigerada es una práctica habitual durante la postcosecha de los frutos cítricos. El objetivo de este estudio fue evaluar el efecto de la temperatura de conservación en el contenido de carotenoides y vitamina C en la piel y la pulpa de frutos de pomelo rojo Star Ruby (SR). Los resultados indican que los frutos almacenados hasta ocho semanas a 12 ºC alcanzan concentraciones de carotenoides totales en la piel tres a cuatro veces superiores a las de los frutos mantenidos a 2 ºC. La mayor temperatura de almacenamiento (12 ºC) potenció la acumulación de los carotenos lineales (fitoeno, fitoflueno y licopeno) y se observó una disminución de los carotenoides derivados del licopeno (β-caroteno y xantofilas). De forma similar, el contenido en vitamina C se incrementó ligeramente en la piel de los frutos conservados a 12 ºC. Sin embargo, en la pulpa no hubo cambios significativos en el contenido de carotenoides ni de vitamina C en función de la temperatura de almacenamiento.
Palabras clave: ÁCIDO ASCÓRBICO, CAROTENOIDES, FRUTOS CÍTRICOS, POSTCOSECHA, STAR RUBY
Summary
Effect of Storage Temperature on Carotenoid and Vitamin C Content in Red Grapefruit
Carotenoids and vitamin C are important attributes that contribute to the organoleptic and nutritional quality in citrus fruits. The fruits of red grapefruit owe their colouration to the presence of lycopene, a red linear carotene, both in the peel and the pulp, a very unusual feature in citrus fruits. This property confers relevant nutritional interest due to its powerful antioxidant activity and possible health benefits of the fruit. Postharvest refrigerated storage is a common practice in citrus fruits. In this study, we evaluated the effect of storage temperature on carotenoids and vitamin C content in the pulp and the peel of red Star Ruby (SR) grapefruit. Results indicate that the fruit stored up to eight weeks at 12 °C reach concentrations of total carotenoids in the peel three to four times higher than fruits kept at 2 °C. The higher storage temperature (12 ºC) favored the accumulation of linear carotenes (phytoene, phytofluene and lycopene) while decreased the level of carotenoids derived from lycopene (β-carotene and xanthophylls). Similarly, vitamin C content slightly increased in the peel of fruits stored at 12 ºC. However, no changes in carotenoid and vitamin C contents occurred in the pulp due to postharvest temperature.
Keywords: ASCORBIC ACID, CAROTENOIDS, CITRUS FRUITS, POSTHARVEST, STAR RUBY
Introducción
El pomelo rojo ‘Star Ruby’ (SR) (Citrus paradisi) es una variedad de pomelo de tamaño medio que se caracteriza por presentar tonalidades rosadas o rojas en la piel y pulpa de color rojo intenso (Gmitter, 1995). El color de los frutos cítricos es uno de los principales atributos de calidad comercial y es un factor determinante en la aceptación por los consumidores. La diversidad del color de la piel (flavedo) y la pulpa de los frutos de las diferentes especies y variedades cítricas se debe a las diferencias en el contenido y composición de carotenoides (Gross, 1987; Kato, 2012; Rodrigo et al., 2013). Desde el punto de vista químico, los carotenoides son isoprenoides C40, siendo una de sus características más importantes la presencia de numerosos dobles enlaces conjugados en la parte central de la molécula que actúa como cromóforo (Britton, 1995).
En general, la biosíntesis de carotenoides es más activa en la piel y, como consecuencia, se acumula una mayor cantidad de carotenoides que en la pulpa (Gross, 1987; Kato, 2012; Rodrigo et al., 2013). Los frutos de pomelo rojo deben su coloración principalmente a la acumulación de licopeno y, en menor proporción, a otros carotenoides anaranjados como el β-caroteno (Alquézar et al., 2013). Además, estos frutos también acumulan cantidades importantes de fitoeno y fitoflueno, que no afectan a la coloración. En general, los compuestos fitoeno, fitoflueno y licopeno representan entre el 60 y 90 % de los carotenoides totales en los frutos de pomelo rojo (Alquézar et al., 2013). La variedad SR puede alcanzar tonalidades rojas intensas (Gmitter, 1995; Rouseff et al., 1992) y diferentes trabajos han determinado que la concentración de carotenoides totales oscila entre 40-60 y 15-50 µg/g en la piel y la pulpa, respectivamente (Fanciullino et al., 2006; Xu et al., 2006; Alquézar et al., 2013). Además de la importancia de estos metabolitos en la calidad organoléptica de los frutos, también son relevantes en la calidad nutricional, ya que muchos de ellos presentan actividad provitamina A (principalmente, β-caroteno, α-caroteno y β-criptoxantina) y una elevada capacidad antioxidante, destacando entre estos el licopeno (Krinsky, 1989; Codoñer-Franch y Valls-Bellés, 2010; Aizawa et al., 2011).
El desarrollo de la coloración en los frutos cítricos es un proceso influenciado por diferentes factores endógenos y exógenos. Entre estos últimos destacan las condiciones ambientales, siendo la temperatura y la luz los más relevantes (Casas y Mallent, 1988; Mesejo et al., 2012; Lado et al., 2013; Rodrigo et al., 2013; Porras et al., 2014). En los frutos cítricos existe un efecto positivo de las bajas temperaturas nocturnas y de la amplitud térmica sobre la inducción de la coloración en el campo (Mesejo et al., 2012; Porras et al., 2014). Sin embargo, temperaturas más elevadas (12 ºC) durante el almacenamiento postcosecha han demostrado ser beneficiosas para aumentar la acumulación de carotenoides en naranjas (Carmona et al., 2012). En la variedad ‘Navelina’, en los frutos almacenados a 12 ºC durante un periodo prolongado (cinco a siete semanas), se observó una coloración más intensa en la piel y pulpa, debido a un incremento en la concentración de carotenoides, incluyendo la β-criptoxantina y el apocarotenoide β-citraurina, responsables de la intensa coloración de la piel (Carmona et al., 2012). Por otro lado, los mismos autores no detectaron cambios significativos a 2 ºC en la composición de los carotenoides ni en el color (Carmona et al., 2012). Sin embargo, en mandarinas satsuma o en el tangor Ortanique no se observaron cambios importantes en los niveles de estos compuestos con temperaturas de 5-8 ºC (Cohen et al., 1990; Matsumoto et al., 2009). De acuerdo con estos antecedentes, el efecto de la temperatura puede ser dependiente de la especie o incluso de la variedad.
Por otro lado, la vitamina C en forma de ácido ascórbico (AsA) y dehidroascórbico (DHA) es un compuesto hidrosoluble que se recomienda ingerir regularmente en la dieta. Los frutos cítricos son una de las principales fuentes de esta vitamina, tanto en fresco como en zumo (Cruz-Rus et al., 2012). Estudios realizados en tejidos de distintas variedades de frutos cítricos muestran que el contenido en AsA oscila entre 130-374 mg/100 g en la piel, mientras que en la pulpa estos valores son inferiores (20-70 mg/100 g) (Sinclair, 1984; Martí et al., 2009; Bermejo et al., 2011; Yang et al., 2011; Alós et al., 2014). Al igual que los carotenoides, la síntesis de vitamina C en las plantas es influenciada por factores exógenos, entre los que destacan la luz y la temperatura (Lee y Kader, 2000). Por otro lado, la temperatura de almacenamiento también puede influir en el contenido de vitamina C. Generalmente, en la mayoría de las frutas y hortalizas, las elevadas temperaturas y periodos prolongados de vida postcosecha disminuyen sus niveles (Adisa, 1986; Lee y Kader, 2000). En algunos cultivos sensibles al frío se producen pérdidas superiores de esta vitamina a bajas temperaturas (Lee y Kader, 2000). Sin embargo, en otros trabajos realizados con mandarinas almacenadas durante 75 días a 3,5 °C no se han encontrado variaciones en el contenido de vitamina C (Ladaniya, 2011). En el caso de zumos de pomelo rojo no se han detectado alteraciones importantes en el contenido de la misma luego de cuatro semanas a 9 ºC (Chebrolu et al., 2012). En general, el contenido en vitamina C desciende en los frutos cítricos durante el almacenamiento a elevadas temperaturas, sin embargo, las pérdidas respecto a otro tipo de vegetales son inferiores debido a que el AsA es más estable en las condiciones ácidas presentes en los cítricos (Nagy, 1980).
Debido al interés actual de las propiedades nutricionales de los alimentos y considerando los antecedentes expuestos, el objetivo del presente trabajo fue conocer el efecto de la temperatura de conservación sobre el contenido de carotenoides y vitamina C en la piel y la pulpa de frutos de pomelo Star Ruby, almacenados a 2 y 12 ºC durante tres y ocho semanas.
Materiales y métodos
Material vegetal y tratamientos postcosecha
Para la ejecución de este trabajo se utilizaron frutos de pomelo rojo (Citrus paradisi) de la variedad ‘Star Ruby’ (120 frutos), provenientes de una parcela comercial situada en la localidad de Llíria (Valencia, España). El estado de desarrollo o índice de madurez al momento de cosecha se correspondió con el color externo en base a la relación (a/b) de 0,21 y un valor interno de 1,36. Los frutos se dividieron en dos lotes de 30 frutos cada uno, los cuales fueron almacenados durante ocho semanas a 2 ºC (lote 1) y 12 ºC (lote 2). En el momento de la cosecha, y a las tres y ocho semanas de conservación, se evaluó el color de la piel y la pulpa de los frutos utilizando un colorímetro Minolta CR-330, cuantificando los valores de las coordenadas L a b (Hunter). En las mismas fechas se tomaron muestras de flavedo y pulpa, inmediatamente se congelaron y trituraron en nitrógeno líquido, y se llevaron a congelador de -80 ºC para su análisis posterior. El diseño experimental fue completamente aleatorizado con tres réplicas de 10 frutos por tratamiento. El análisis estadístico de los datos obtenidos se realizó mediante un análisis de varianza (ANOVA) y la diferencia entre tratamientos fue determinada mediante la prueba T (p < 0,05), utilizando el programa Infostat.
Extracción y cuantificación de carotenoides
El tamaño de muestra para las determinaciones en el laboratorio consistió en 0,5 g de flavedo y 1,5 g de pulpa siguiendo el procedimiento descrito por Rodrigo et al. (2003). Brevemente, los carotenoides y clorofilas se extrajeron con metanol, y posteriormente con una mezcla de Tris-HCl (pH 7) y cloroformo. Las diferentes fases orgánicas combinadas se llevaron a sequedad con rotavapor a 40 ºC. Posteriormente, los extractos se saponificaron y los carotenoides se extrajeron repetidamente con una mezcla de éter de petróleo/éter etílico en una relación de 9:1. El extracto de carotenoides totales concentrados se secó completamente con N2 y se mantuvo en atmósfera de N2 a -20 ºC hasta el momento del análisis. Todos los procesos se realizaron en ausencia de luz para evitar la degradación e isomerización de los carotenoides.
Separación, identificación y cuantificación de carotenoides por HPLC-PDA
El extracto obtenido se disolvió en metanol/acetona/cloroformo (3:2:5) y se inyectó una alícuota de 20 µL en un sistema de HPLC con bomba cuaternaria acoplada a un detector de diodos (PDA) (Waters). La separación de carotenoides se realizó utilizando una precolumna y columna YMC C30 (250 x 4,6 mm, 5,0 µm) en un gradiente ternario de metanol/agua/metil tert-butil eter, según las condiciones descritas por (Alquézar et al., 2008). La identificación de cada compuesto se llevó a cabo mediante comparación de los tiempos de retención y de los espectros de absorción con los indicados en la literatura o los estándares puros disponibles (Alquézar et al., 2008). Para su cuantificación se utilizaron curvas de calibración de fitoeno, fitoflueno, ζ-caroteno, luteína, α y β-caroteno, licopeno,β-criptoxantina, zeaxantina y 8-β-apocarotenal (Rodrigo et al., 2004; Alquézar et al., 2008). El contenido de carotenoides totales se obtuvo de la suma de los niveles individuales, siendo los resultados expresados en µg/g de peso fresco (PF).
Determinación de vitamina C: ácido ascórbico (AsA) y dehidroascórbico (DHA)
El contenido en AsA se cuantificó siguiendo el protocolo descrito por Alós et al. (2014). La extracción consistió en la homogeneización de 0,5 g de tejido (pulpa o flavedo) con 4 mL de ácido metafosfórico al 2 %, centrifugándose inmediatamente a 4500 rpm a 4 ºC durante 10 min. Para las muestras de flavedo se realizó una dilución 1:3 con el sobrenadante y ácido metafosfórico al 2 %, mientras que para las muestras de pulpa se tomó todo el volumen del sobrenadante. Este sobrenadante se filtró a través de un cartucho C18 (Sep Pak, Waters) y un filtro de 0,45 µm (25 mm de diámetro, Análisis Vínicos, España). A continuación se inyectaron 20 µL en un sistema HPLC Dionex con software Chromeleon (Dionex), equipado con una columna Ultrabase C18 (100 x 4,5 mm, 2,5 µm) y un detector de diodos (PDA). La fase móvil consistió en metanol: agua (pH 2,5) (15:85, v/v) a un flujo de 0,2 mL/min y la temperatura de la columna se fijó a 35 ºC. El área del pico cromatográfico correspondiente a AsA se cuantificó mediante una curva de calibración realizada con estándar de AsA (Sigma-Aldrich) disuelto en ácido metafosfórico al 2 % abarcando concentraciones entre 1 y 100 µg/mL. El resultado final se expresó en mg de AsA en 100 g de peso fresco (PF). Por otro lado, con el objetivo de reducir el DHA de la muestra para su posterior cuantificación como AsA se tomaron 250 µL del extracto al que se añadió 125 µL de 200 mM ditiotreitol (DTT), preparado en 400 mM Tris-HCl. Luego de 15 minutos de incubación con DTT, se interrumpió la reacción mediante la adición de 125 µL de ácido ortofosfórico 8,5 %, y se procedió a la cuantificación de AsA según lo descrito anteriormente.
Resultados y discusión
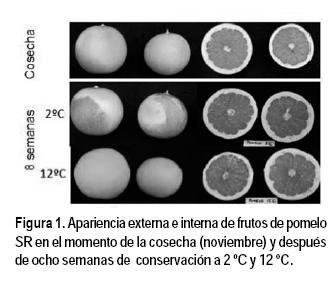
Con el objetivo de determinar la influencia de la temperatura de conservación en la acumulación de carotenoides y el contenido en AsA en frutos de pomelo rojo SR, se cosecharon frutos en el mes de noviembre y se almacenaron a 2 ºC y 12 ºC durante ocho semanas. La apariencia externa de los frutos utilizados en el presente estudio al inicio y al final del período de conservación se presenta en la Figura 1. Si bien en el momento de la cosecha la piel de los frutos presentó zonas verdes y coloreadas (naranja/amarillo), luego de ocho semanas a 12 ºC alcanzaron una coloración rojiza uniforme en toda la superficie del fruto. Los frutos almacenados a 2 ºC desarrollaron los síntomas característicos del daño por frío (Schirra 1992; Lafuente y Zacarías, 2006), que se localizaron generalmente en las zonas verdes de la piel. La coloración de la pulpa no presentó cambios significativos durante el almacenamiento tanto a 2 °C como a 12 ºC (Figura 1). Después de ocho semanas de conservación, el color de la piel, determinado como parámetro Hunter a/b, fue significativamente mayor en aquellos frutos mantenidos a 12 ºC, con valores de 0,40, en comparación a frutos almacenados a 2 ºC, con valores de 0,15 (Figura 2A), mientras que en la pulpa no se observaron diferencias importantes entre las dos temperaturas de conservación evaluadas, permaneciendo en valores constantes entre 1,2 y 1,5 (Figura 2B). El cambio de color de la piel de naranjas y mandarinas a temperaturas refrigeradas intermedias (10-12 ºC) se atribuye a una estimulación de la biosíntesis y acumulación de carotenoides (Carmona et al., 2012). Además, las temperaturas nocturnas alrededor de 10 ºC y diurnas de 20 ºC son las óptimas para inducir el cambio de color durante la maduración natural de los frutos cítricos (Wheaton y Stewart, 1973; Mesejo et al., 2012; Rodrigo et al., 2013; Porras et al., 2014). Los resultados de este trabajo concuerdan con los descritos por Chaudhary et al. (2014) en frutos de pomelo SR donde se recomienda el almacenamiento de los frutos a 11 ºC para evitar la aparición de daño por frío y el desarrollo de patógenos durante un periodo de almacenamiento de al menos ocho semanas.
La coloración de los frutos cítricos está determinada fundamentalmente por la concentración y composición de carotenoides que, además, varía a lo largo del desarrollo y maduración, y puede verse afectada durante la vida postcosecha de los frutos (Matsumoto et al., 2009; Carmona et al., 2012). En el presente trabajo el efecto de la temperatura de conservación sobre la concentración de carotenoides totales e individuales de piel y pulpa de pomelos Star Ruby mostró que en el flavedo la misma aumentó de tres a cuatro veces en los frutos almacenados a 12 ºC en relación a aquellos sometidos a 2 ºC y a los recién cosechados (Figura 3). Este efecto fue similar al obtenido en naranjas ‘Navelina’ y ‘Palmer Navel’ almacenadas a temperaturas similares (Carmona et al. 2012; Van Wyk et al., 2009). En mandarinas Satsuma también se ha reportado un aumento de carotenoides a mayores temperaturas de almacenamiento (Matsumoto et al., 2009), mientras que en mandarinas ‘Or’ almacenadas a temperaturas inferiores a 8 ºC, se produjo una reducción de la coloración (Tietel et al., 2012).
En cuanto a la composición y proporción relativa de los diferentes carotenoides individuales, la acumulación de carotenos lineales (fitoeno, fitoflueno y licopeno) aumentó en la piel de los frutos durante el almacenamiento a 12 ºC, representando un total de 92 µg/g PF (Figura 3). Por otro lado, los carotenoides derivados del licopeno (β-caroteno y xantofilas) disminuyeron a esta temperatura, lo que sugiere una reducción adicional de la capacidad enzimática de la licopeno β-ciclasa, responsable de la conversión de licopeno en β-caroteno en los frutos de pomelo SR a 12 ºC (Alquézar et al., 2009, 2013). De forma similar, en naranjas ‘Navelina’, el almacenamiento a 12 ºC también estimuló la acumulación de los carotenos lineales fitoeno y fitoflueno, aunque aumentó la concentración de xantofilas y sus derivados apocarotenoides coloreados (Carmona et al., 2012), en contraste con lo observado en pomelos. En los frutos SR almacenados a 2 ºC no se detectaron cambios significativos en el contenido y composición de carotenoides luego de tres y ocho semanas de almacenamiento, tal como se ha reportado en mandarinas ‘Satsuma’ almacenadas a 5 ºC (Matsumoto et al., 2009). Adicionalmente, en la piel de los frutos se detectó la presencia de otros carotenoides característicos de tejidos verdes, aunque en menor proporción, como el α-caroteno, la luteína y la violaxantina, cuya concentración fue, en general, menor en los frutos almacenados a 12 ºC respecto a los almacenados a 2 ºC (Figura 3). Por otra parte, en los pomelos mantenidos a 12 ºC también se detectaron trazas de α-caroteno y ζ-caroteno (datos no mostrados).
En síntesis, estos resultados sugieren que a 12 ºC ocurre una estimulación de la biosíntesis y acumulación de carotenos lineales hasta el licopeno y que el bloqueo en la conversión de licopeno en β-caroteno que existe en los pomelos rojos (Alquézar et al. 2009, 2013) se mantiene a 12 ºC, ya que a esta temperatura se acumulan los carotenoides anteriores de la ruta de biosíntesis (fitoeno, fitoflueno y licopeno) y disminuye la concentración de xantofilas, que se forman a partir del licopeno (Figura 3).
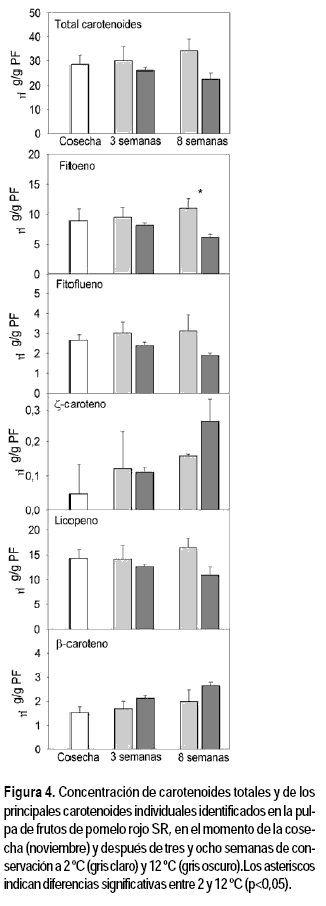
Los cambios en los carotenoides individuales observados en la pulpa no fueron relevantes comparados con los resultados obtenidos en al análisis de la piel. El contenido total no presentó diferencias entre los frutos recién cosechados y los almacenados a 2 ºC y 12 ºC y permaneció en 25-30 µg/g PF (Figura 4). En mandarinas ‘Satsuma’ también se ha descrito que los carotenoides totales en la pulpa no se modifican o pueden incluso reducirse durante el almacenamiento a 5 ºC (Matsumoto et al., 2009). Sin embargo, en naranjas ‘Navelina’ se ha descrito un claro aumento en la proporción de xantofilas en la pulpa (principalmente β-criptoxantina, violaxantina y anteraxantina), luego de cinco semanas de almacenamiento a 12 ºC comparado con el almacenamiento a 2 ºC (Carmona et al., 2012), sugiriendo que el efecto de la temperatura en la pulpa de los frutos cítricos puede ser dependiente de la especie y/o variedad. Entre los carotenoides individuales identificados se destacó una mayor concentración de licopeno (10 a 15 µg/g PF), seguido del fitoeno (5 a 10 µg/g PF). A su vez el fitoflueno y el β-caroteno se detectaron en cantidades destacables (Figura 4). Otros carotenoides minoritarios identificados en la pulpa fueron un isómero cis del licopeno y el ζ-caroteno.
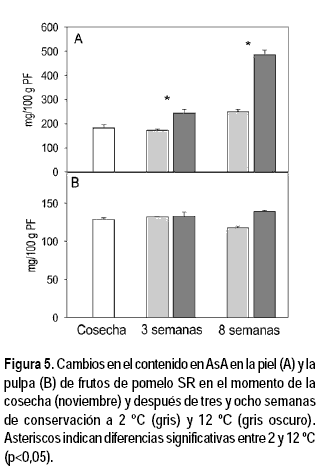
El contenido en AsA es un parámetro de calidad nutricional importante en los frutos cítricos, lo cual los ubica entre los diez primeros frutos con mayor aporte del mismo a la dieta (Cruz-Rus et al., 2012). Puesto que el DHA puede convertirse fácilmente en AsA en el organismo, es importante determinar la concentración de ambos para conocer la actividad de la vitamina C en frutas y hortalizas (Lee y Kader, 2000). En este estudio se obtuvieron niveles bajos de DHA (15-19 mg/100 g) en la piel de los frutos de pomelo SR. En cambio, no se detectó la presencia de DHA en la pulpa.
El almacenamiento a 12 ºC provocó un aumento de la acumulación de AsA en la piel (Figura 5A), mientras que no afectó el contenido de esta vitamina en la pulpa (Figura 5B). A 2 ºC el contenido de AsA permaneció prácticamente constante tanto en la piel como en la pulpa. Estos resultados son similares a los descritos en pomelos almacenados a temperatura ambiente o a 9 ºC, en los cuales no se registraron cambios en el contenido de AsA (Chebrolu et al., 2012). Es interesante mencionar que en la piel de los frutos la concentración en AsA fue mayor a 12 ºC que a 2 ºC, siendo estos últimos frutos los que manifestaron síntomas de daño por frío (Figura 1). La presencia de daño por frío se ha relacionado con una disminución acelerada del contenido de AsA, y este fenómeno se puede producir incluso antes de que se manifiesten los síntomas visibles del daño (Miller y Heilman, 1952). Izumi et al. (1984) estudiaron el efecto de diferentes temperaturas de almacenamiento sobre el contenido de AsA en distintos cultivos sensibles al frío y observaron que el contenido en AsA disminuyó únicamente en los frutos sometidos a la temperatura que produjo daño de frío, indicando una relación entre la sensibilidad o la manifestación de los daños por frío y el contenido de AsA.
En el caso de la pulpa, no se apreciaron diferencias en el contenido de AsA durante la conservación a 2 y 12 ºC (Figura 5B). Chaudhary et al. (2014) y Chebrolu et al. (2012) estudiaron la variación del contenido en AsA en zumo de pomelo rojo SR durante 16 semanas de almacenamiento a 2, 9 y 11 ºC. La concentración de AsA a las cuatro primeras semanas de almacenamiento no experimentó variaciones significativas en concordancia con nuestros resultados. Sin embargo, a las ocho semanas se produjo una leve disminución en los frutos almacenados a 12 ºC.
El efecto de la temperatura en el contenido de carotenoides y vitamina C fue claramente diferencial en los dos tejidos evaluados, con un aumento en ambos compuestos bioactivos a 12 ºC en el flavedo y sin cambios en la pulpa. Los resultados obtenidos en los frutos de pomelo rojo apoyan la hipótesis de que en los frutos cítricos numerosos procesos fisiológicos y metabólicos están regulados de forma independiente en la piel y la pulpa (Tadeo et al., 2008).
Conclusiones
La conservación prolongada de frutos de pomelo SR a 12 ºC aumentó el contenido de los carotenoides lineales fitoeno, fitoflueno y licopeno en la piel y, al mismo tiempo, disminuyó la concentración de xantofilas. Por otro lado, la conservación a 12 ºC incrementó, igualmente, el contenido en AsA en la piel de los pomelos. A 2 ºC se desarrollaron síntomas visibles de daño por frío en la piel de los frutos y no se detectaron cambios importantes en el contenido y la composición de carotenoides, así como en la concentración de AsA. La temperatura de almacenamiento no afectó el contenido de carotenoides ni de vitamina C en la pulpa de frutos de pomelo rojo.
Agradecimientos
Nuestro agradecimiento a Amparo Beneyto por su excelente ayuda técnica. Este trabajo ha sido financiado por los proyectos (AGL2009-11558 y AGL2012-34573) del Ministerio de Ciencia e Innovación, Economía y Competitividad. Al proyecto PROMETEOII/2014/027 (Generalitat Valenciana) (Generalitat Valenciana) y Fun-C-Food (CSD2007-0063C; Ministerio de Ciencia e Innovación). Joanna Lado es receptora de una beca JAE- Pre CSIC (Fondo Social Europeo). Los autores de este trabajo pertenecen a la Red CYTED IBERCAROT (ref. 112RT0445).
Bibliografía
Adisa VA. 1986. The influence of molds and some storage factors on the ascorbic acid content of orange and pineapple fruits. Food Chemistry, 22(2): 139 – 146.
Aizawa K, Iwasaki Y, Ouchi A, Inakuma T, Nagaoka S, Terao J, Mukai K. 2011. Development of singlet oxygen absorption capacity (SOAC) assay method. 2. Measurements of the SOAC values for carotenoids and food extracts. Journal of Agricultural and Food Chemistry, 59: 3717 – 3729.
Alós E, Rodrigo MJ, Zacarías L. 2014. Differential transcriptional regulation of L-ascorbic acid content in peel and pulp of citrus fruits during development and maturation. Planta, 239: 1113 – 1128.
Alquézar B, Rodrigo MJ, Lado J, Zacarías L. 2013. A comparative physiological and transcriptional study of carotenoid biosynthesis in white and red grapefruit (Citrus paradisi Macf.). Tree Genetics & Genomes, 9(5): 1257 – 1269.
Alquézar B, Zacarías L, Rodrigo MJ. 2009. Molecular and functional characterization of a novel chromoplast-specific lycopene beta-cyclase from Citrus and its relation to lycopene accumulation. Journal of Experimental Botany, 60: 1783 – 1797.
Alquézar B, Rodrigo MJ, Zacarías L. 2008. Regulation of carotenoid biosynthesis during fruit maturation in the red-fleshed orange mutant ‘Cara Cara’. Phytochemistry, 69: 1997 – 2007.
Bermejo A, Llosá MJ, Cano A. 2011. Analysis of bioactive compounds in seven citrus cultivars. Food Science and Technology International, 17(1): 55 - 62.
Britton G. 1995. Structure and properties of carotenoids in relation to function. FASEB Journal, 9: 1551 – 1558.
Carmona L, Zacarías L, Rodrigo MJ. 2012. Stimulation of coloration and carotenoid biosynthesis during postharvest storage of ‘Navelina’ orange fruit at 12 ºC. Postharvest Biology and Technology, 74: 108 – 117.
Casas A, Mallent D. 1988. El color de los frutos cítricos : I. Generalidades. II. Factores que influyen en el color. Influencia de la especie, de la variedad y de la temperatura. Revista de Agroquímica y Tecnología de Alimentos, 28(2): 184 – 201.
Chaudhary PR, Jayaprakasha GK, Porat R, Patil BS. 2014. Low temperature conditioning reduces chilling injury while maintaining quality and certain bioactive compounds of ‘Star Ruby’ grapefruit. Food Chemistry, 153: 243 – 249.
Chebrolu KK, Jayaprakasha GK, Jifon J, Patil BS. 2012. Production system and storage temperature influence grapefruit vitamin C, limonoids and carotenoids. Journal of Agricultural and Food Chemistry, 60: 7096 – 7103.
Codoñer-Franch P, Valls-Bellés V. 2010.Citrus as functional foods. Current Topics in Nutreceutical Research, 8(4): 173 - 184.
Cohen E, Shalom Y, Rosenberger I.1990. Post-harvest behaviour of ‘Ortanique’ (‘Topaz’) tangor citrus fruit during long-term storage at various temperatures. Scientia Horticulturae, 44: 235 – 240.
Cruz-Rus E, Amaya I, Valpuesta V. 2012. The challenge of increasing vitamin C content in plant foods. Biotechnology Journal, 7: 1110 – 1121.
Fanciullino AL, Dhuique Mayer C, Luro F, Casanova J, Morillon R, Ollitrault P. 2006. Carotenoid diversity in cultivated citrus is highly influenced by genetic factors. Journal of Agricultural and Food Chemistry, 54: 4397 – 4406.
Gmitter FJ. 1995. Origin, evolution and breeding of the grapefruit. En: Janick J. [Ed.], Plant Breeding Reviews. Florida : John Wiley & Sons. pp. 345 – 363.
Gross J. 1987. Pigments in fruits. En: Schweigert BS [Ed.] Food science and Technology : a Series of Monographs. London : Academic Press. pp. 303.
Izumi H, Tatsumi Y, Murata T.1984. Effect of storage temperature on changes of ascorbic acid content of cucumber, winter squash, sweet potato and potato. Nippon Shokuhin Kogyo Gakkaishi, 31: 47 – 49.
Kato M. 2012. Mechanism of Carotenoid Accumulation in Citrus Fruit. Journal of Japanese Society of Horticultural Science, 81: 219 – 233.
Krinsky NI. 1989. Antioxidant functions of carotenoids. Free Radical Biology & Medicine, 7: 617 – 635.
Ladaniya MS. 2011. Physico-chemical, respiratory and fungicide residue changes in wax coated mandarin fruit stored at chilling temperature with intermittent warming. Journal of Food Science and Technology, 48: 150 – 158.
Lado J, Rodrigo MJ, Zacarias L. 2013. Influencia de la luz en la coloración y maduración de los frutos cítricos. Levante Agrícola, (Especial Postcosecha): 179 – 185.
Lafuente MT, Zacarías L. 2006. Postharvest physiological disorders in citrus fruit. Stewart Postharvest Review, 1: 2.
Lee S, Kader AA. 2000. Preharvest and postharvest factors influencing vitamin C content of horticultural crops. Postharvest Biology and Technology, 20(3): 207 – 220.
Martí N, Mena P, Cánovas JA, Micol V, Saura D. 2009 Vitamin C and the role of citrus juices as functional food. Natural Products Communcations, 4: 677 - 700.
Matsumoto H, Ikoma Y, Kato M, Nakajima N, Hasegawa Y. 2009. Effect of postharvest temperature and ethylene on carotenoid accumulation in the flavedo and juice sacs of Satsuma mandarin (Citrus unshiu Marc.) fruit. Journal of Agricultural and Food Chemistry, 57: 4724 – 4732.
Mesejo C, Gambetta G, Gravina A, Martinez-Fuentes A, Reig C, Agusti M. 2012. Relationship between soil temperature and fruit colour development of ‘Clemenpons’ Clementine mandarin (Citrus clementina Hort ex.Tan). Journal of the Science of Food and Agriculture, 92: 520 – 525.
Miller EV, Heilman AS. 1952. Ascorbic acid and physiological breakdown in the fruits of the pineapple (Ananas comosus L. Merr.). Science, 116(3019): 505 – 506.
Nagy S. 1980. Vitamin C contents of citrus fruit and their products : a review. Journal of Agricultural and Food Chemistry, 28(1): 8 – 18.
Porras I, Brotons JM, Conesa A, Manera FJ. 2014. Influence of temperature and net radiation on the natural degreening process of grapefruit (Citrus paradisi Macf.) cultivars Rio Red and Star Ruby. Scientia Horticulturae, 173: 45 – 53.
Rodrigo MJ, Alquézar B, Alós E, Lado J, Zacarías L. 2013. Biochemical bases and molecular regulation of pigmentation in the peel of Citrus fruit. Scientia Horticulturae, 163: 46 – 62.
Rodrigo MJ, Marcos JF, Zacarías L. 2004. Biochemical and molecular analysis of carotenoid biosynthesis in flavedo of orange (Citrus sinensis L.) during fruit development and maturation. Journal of Agricultural and Food Chemistry, 52: 6724 – 6731.
Rodrigo MJ, Marcos J, Alférez F, Mallent D, Zacarías L. 2003. Characterization of Pinalate, a novel Citrus sinensis mutant with a fruit-specific alteration that results in yellow pigmentation and decreased ABA content. Journal of Experimental Botany, 54: 727 – 738.
Rouseff RL, Sadler GD, Putnam TJ, Davis JE. 1992. Determination of â-carotene and other hydrocarbon carotenoids in red grapefruit cultivars. Journal of Agricultural and Food Chemistry, 40: 47 – 51.
Schirra M. 1992. Behaviour of ’Star Ruby’ grapefruits under chilling and non-chilling storage temperature. Postharvest Biology and Technology, 2: 315 – 327.
Sinclair WB. 1984. Ascorbic acid (Vitamin C) in lemons and other citrus fruits. En: Sinclair WB. [Ed.]. The Biochemistry and Physiology of the Lemon. Oakland : University of California Publications. pp.157 – 183.
Tadeo FR, Cercos M, Flores MC, Iglesias DJ, Naranjo MA, Ri G, Morillon L, Ollitrault P, Talón M. 2008. Molecular physiology of development and quality of Citrus. Advances in Botanical Research, 47: 147 – 223.
Tietel Z, Lewinsohn E, Fallik E, Porat R. 2012. Importance of storage temperatures in maintaining flavor and quality of mandarins. Postharvest Biology and Technology, 64: 175 – 182.
Van Wyk AA, Huysamer M, Barry GH. 2009. Extended low-temperature shipping adversely affects rind colour of ‘Palmer Navel’ sweet orange (Citrus sinensis) due to carotenoid degradation but can partially be mitigated by optimizing post-shipping holding temperature. Postharvest Biology and Technology, 53: 109 – 116.
Wheaton TA, Stewart I. 1973. Optimum temperature and ethylene concentrations for post harvest development of carotenoids pigments in Citrus. Journal of the American Society for Horticultural Science, 98: 337 – 340.
Xu CJ, Fraser PD, Wang WJ, Bramley PM. 2006. Differences in the carotenoid content of ordinary citrus and lycopene-accumulating mutants. Journal of Agricultural and Food Chemistry, 54(15): 5474 – 5481.
Yang XY, Xie JX, Wang FF, Zhong J, Liu YZ, Li G-H, Peng SA. 2011. Comparison of ascorbate metabolism in fruits of two citrus species with obvious difference in ascorbate content in pulp. Journal of Plant Physiology, 168: 2196 - 2205.