Introducción
Dos cambios importantes han mejorado los resultados en la cirugía de coordinación:
1. La introducción de la cirugía mínimamente invasiva (CMI) o cirugía video asistida, que revolucionó la cirugía abdominal, disminuyendo significativamente el impacto de la cirugía mayor, sus complicaciones y acelerando la recuperación. El interés por las técnicas de CMI, fue impulsado por el deseo de mejorar los resultados, especialmente la recuperación postquirúrgica. Sin embargo hay un límite entre la técnica quirúrgica y los factores perioperatorios que retrasan la recuperación. Estos factores múltiples y complejos, incluyen respuesta al estrés quirúrgico, dolor, náuseas y vómitos postoperatorios, movilidad limitada, sobrecarga de líquidos, fatiga y uso de sondas (incluso en ausencia de complicaciones quirúrgicas).
2. El otro cambio importante para mejorar los resultados perioperatorios, fueron los planes coordinados de atención multidisciplinaria, que incorporaron intervenciones basadas en evidencias a lo largo de todo el proceso, conocidos como Recuperación mejorada luego de la cirugía, o por su terminología en inglés: Enhanced Recovery After Surgery (ERAS), o el programa basado en el ERAS de Brasil denominado ACERTO (ACEleração da Recuperação TOtal pós-operatória).
ERAS representan un cambio paradigmático de la atención tradicional, integrando múltiples elementos individuales de la atención perioperatoria, así como el compromiso de los pacientes y cuidadores para comprender mejor el proceso de recuperación. Al aprovechar los logros alcanzados por las técnicas de CMI con la vía ERAS, el objetivo fue mejorar aún más la recuperación, disminuir las complicaciones y la variabilidad en la práctica, lo que a su vez se reflejaría en una internación más corta y con menos costos asistenciales.
En su página web la ERAS Society se presenta de la siguiente manera1:
El desafío inmediato para la mejora de la calidad de la atención quirúrgica no es el descubrimiento de nuevos conocimientos, sino más bien la forma de integrar lo que ya sabemos.
ERAS es una vía de atención perioperatoria multimodal cuyo objetivo es atenuar la pérdida de la capacidad funcional y mejorar la recuperación en el período perioperatorio.
ERAS representa un cambio de paradigma en el manejo perioperatorio de dos maneras. En primer lugar, se vuelve a examinar las prácticas tradicionales, sustituyéndolos con las mejores prácticas basadas en la evidencia. En segundo lugar, es amplia en su alcance, que abarca todas las áreas del paciente a través del proceso quirúrgico. De esta manera, se reduce la morbilidad y se mejora de manera significativa la recuperación, reduciendo el estrés quirúrgico con control óptimo del dolor, movilización y realimentación precoz. Como consecuencia, se reducen la internación y los costos hospitalarios.
Es así que nos encontramos frente a un proceso de cambio, que hasta hace pocos años se basaba en hábitos y experiencias adquiridas, más que en hechos demostrados científicamente. Los conocimientos de los médicos referentes, se transmitían de generación en generación; en muchos casos sin un sustento científico que los avalara. El postoperatorio se basaba en esperar la recuperación de las funciones fisiológicas modificadas por la agresión quirúrgica y farmacológica, en base a la reserva orgánica, con una mínima intervención en todo el proceso perioperatorio.
Si bien es cierto que no existe mucha bibliografía sobre Vías de Recuperación Mejorada en niños, ya que hay quienes sostienen que esto es debido a notables diferencias con los adultos lo que no justificaría su instrumentación, estamos convencidos que muchos niños se verían beneficiados si se instrumentaran estos protocolos. Motivados por este nuevo paradigma de la Cirugía moderna es que realizamos esta revisión monográfica esbozando algunas propuestas.
Objetivo
La presente revisión bibliográfica tiene como objetivo resumir la información existente sobre este tema, fundamentalmente desde el enfoque del paciente pediátrico, e identificar los aspectos relevantes con el fin de determinar la posibilidad y viabilidad de su implementación en la Clínica Quirúrgica Pediátrica del Centro Hospitalario Pereria Rossell, así como su eventual proyección a otros servicios quirúrgicos de dicho Centro.
Búsqueda bibliográfica
Se realizó la búsqueda bibliográfica en servidores como Pubmed y LILACS, entre los años 2000 y 2017, en español e inglés, sin límite de edad, para palabras claves como ERAS, Fast track y Enhancement Recovery After Surgery. A su vez, se realizaron búsquedas bibliográficas limitadas a la población pediátrica, para cada uno de los puntos que establecen los protocolos ERAS, que se desarrollan a continuación.
Protocolo ERAS
Se clasifica en función del período perioperatorio.
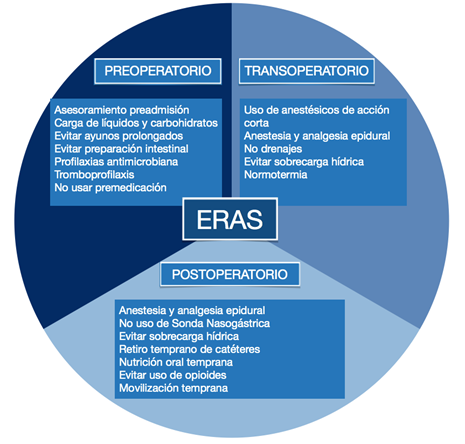
Los siguientes son los elementos claves para abordar e incluir en el desarrollo de vías de recuperación mejoradas. Este enfoque es aplicable a través de una variedad de procedimientos, pero la expresión de cada elemento puede diferir entre los procedimientos y las instituciones. Figura 1.
3) Abordaje postoperatorio
― Analgesia multimodal, ahorradora de opioides.
― Profilaxis íleo postoperatorio.
― Examinar el uso de drenajes, tubos, catéteres y monitoreo.
― Nutrición temprana.
― Deambulación temprana.
― Mapas de atención diaria.
― Criterios de alta predefinidos.
― Plan de rehabilitación.
Los criterios de alta hospitalaria son fundamentalmente los siguientes: tolerancia a la dieta sólida, analgesia oral eficaz y una correcta movilización del paciente.
Estamos convencidos que este concepto es hacia dónde apunta el futuro de la cirugía pediátrica, por lo cual es importante acompañarlo desde el inicio.
Historia
A finales del siglo pasado comienzan a surgir nuevas pautas de manejo sobre el ayuno preoperatorio. Se les puede considerar originales e innovadoras, ya que se deja de lado el paradigma del ayuno total para hacerlo selectivo por tipo de alimento. Comienza entonces una profunda toma de conciencia sobre el efecto metabólico de la dieta y su incidencia en el período intraoperatorio y la calidad de la recuperación postoperatoria.
ERAS tiene sus orígenes a partir de la década de los 90, cuando distintos grupos de investigadores presentaron diferentes medidas para mejorar la evolución postoperatoria de los pacientes adultos intervenidos de cirugía colorrectal de coordinación. En Dinamarca, el Dr. H. Kehlet propone una combinación de técnicas con el objetivo de reducir la respuesta al estrés quirúrgico, optimizar la recuperación y reducir los días de internación. El incluía anestesia peridural, movilización y realimentación postoperatoria precoz. Los pacientes sometidos a cirugía abierta de colon, tuvieron una recuperación precoz de la función intestinal, disminución de la respuesta al estrés, y mejora de la función física con reducción de la estadía hospitalaria2.
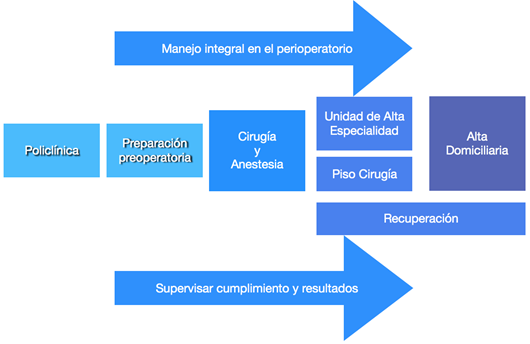
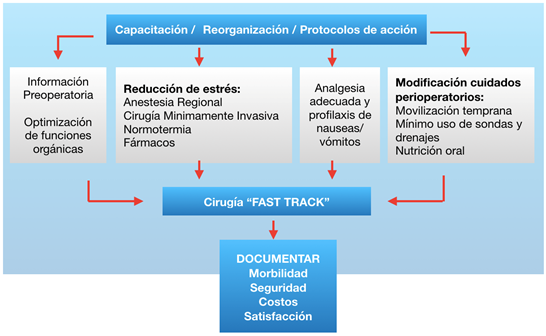
Surgen programas de rehabilitación multimodal, llamados Fast-Track, con el objetivo de atenuar la pérdida de la capacidad funcional y mejorar la recuperación. En base a estos principios, medidas tradicionales en la práctica anestésico-quirúrgica, como el ayuno preoperatorio prolongado, la preparación mecánica del colon y el uso de sonda nasogástrica de rutina, ya no se recomendaron. Se demostró que prácticas como la analgesia intravenosa para control del dolor, en especial con opioides, el retraso en el inicio de la alimentación hasta la aparición del peristaltismo evaluado de manera subjetiva y el reposo en cama son factores de riesgo, que favorecen el aumento de los días de internación y los costos de atención3. (Figura 2)
La aplicación de estos programas redujo la morbilidad y mejoraron de manera significativa la recuperación, actuando sobre el estrés quirúrgico mediante el control óptimo del dolor, movilización y realimentación precoz4.
En el año 2001, se constituyó el ERAS Study Group, integrado por diferentes unidades de cirugía procedentes de cinco países (Escocia, Suecia, Dinamarca, Noruega y Holanda). Este grupo realizó un consenso que denominaron el proyecto ERAS, caracterizado por un programa de rehabilitación multimodal para pacientes intervenidos de cirugía de coordinación. Este protocolo incluye una combinación de estrategias preoperatorias, intraoperatorias y postoperatorias basadas en la evidencia científica5. Finalmente en el año 2010 se funda la ERAS Society.
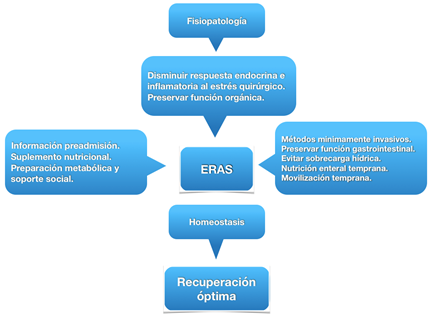
La filosofía principal del protocolo ERAS es reducir el estrés metabólico causado por el trauma quirúrgico y al mismo tiempo apoyar la recuperación temprana del paciente. Esta actuación sobre factores implicados en la respuesta biológica a la agresión impacta en las complicaciones postoperatorias (Figura 3).
Si bien esta práctica se comienza en adultos para cirugía colorectal, luego se expande a otras áreas de la cirugía general (sistema digestivo alto, bariátrica, duodenopancreatectomías, etc), así como a otras especialidades (ginecología, urología y traumatología).
En los últimos años, la Cirugía Pediátrica se ha interesado en esta nueva modalidad, aunque la bibliografía en este sentido es escasa. El artículo de Schinnick y cols. Enhancing recovery in pediatric surgery: a review of the literature6; realiza una revisión, en la cual destacan que solo cinco artículos, cumplen al menos con cuatro de las recomendaciones propuestas por ERAS Society.
Fundamentos de programas ERAS
A pesar de continuos avances, los principales procedimientos quirúrgicos en adultos, siguen presentando secuelas indeseables: dolor, complicaciones cardiopulmonares, infecciosas, tromboembólicas, disfunción cerebral, náuseas y parálisis gastrointestinal, fatiga y convalecencia prolongada. Claramente pueden estar relacionadas con la calidad anestésica y quirúrgica, pero también pueden ocurrir independientemente de esas variables.
Una característica común compartida por todos los pacientes quirúrgicos son los cambios generalizados en la función de sus órganos, la llamada respuesta de estrés quirúrgico7. Se cree que estos cambios funcionales, están mediados por los cambios metabólicos endocrinos inducidos por traumas y la activación de varios sistemas biológicos como la cascada de citoquinas, complemento, metabolitos del ácido araquidónico, óxido nítrico, radicales libres de oxígeno, etc. Aunque estas respuestas han evolucionado presumiblemente para conferir una ventaja para la supervivencia, pueden, si se amplifican y prolongan, contribuir a la erosión de la masa celular corporal y la capacidad de reserva fisiológica.
La pregunta clave en la comprensión de la patogénesis de la morbilidad postoperatoria, está por lo tanto relacionada con el papel fisiopatológico de los diversos componentes de la respuesta al estrés quirúrgico y si una modificación de tales respuestas puede mejorar el resultado.
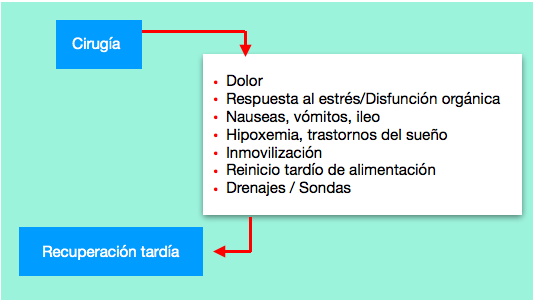
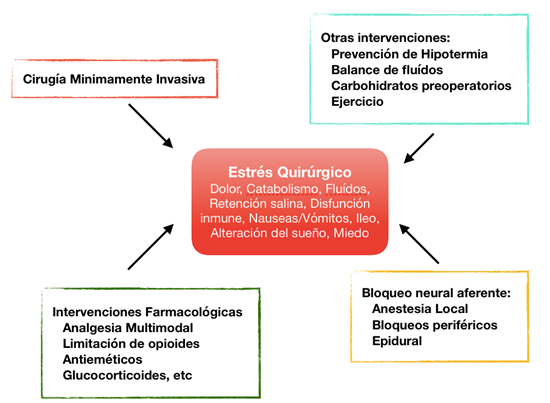
Los obstáculos que demoran la recuperación incluyen: disfunción preoperatoria de órganos, estrés quirúrgico y catabolismo, dolor, náuseas y vómitos postoperatorios, íleo, exceso de líquidos, ayunos prolongados, inmovilización y tradiciones o cultura quirúrgica (Figura 4).
Para muchos cirujanos que se formaron en los últimos 25 años, la CMI fue la respuesta a la mejora en la recuperación. Sin embargo, muchas otras intervenciones tienen el potencial de retrasar o acelerar la misma, a través de su impacto en la respuesta al estrés quirúrgico. Estos incluyen bloqueo neural aferente, intervenciones farmacológicas, control de líquidos y temperatura, nutrición y ejercicio8. Existe abundante evidencia para orientar las mejores prácticas en la atención perioperatoria; aunque el problema no es la falta de pruebas o de directrices, sino cómo puede organizarse la atención, para lograr la obtención de esa evidencia en la práctica y mejorar los resultados. Para avanzar, debemos introducir nuevas intervenciones que resulten beneficiosas y también dejar de hacer otras no beneficiosas e incluso perjudiciales (Figura 5).
Vías de recuperación mejorada
Una vía de recuperación mejorada (VRM) es un consenso integrado, basado en evidencia, multimodal, sobre la atención perioperatoria que reorganiza la atención alrededor de la cirugía. Representa un cambio de paradigma de un sistema centrado en el clínico, a un sistema centrado en el paciente, que integra cada paso a lo largo de la trayectoria perioperatoria en una vía única. Debe abordar la preparación del paciente, el manejo intraoperatorio, postoperatorio y la auditoría. Este último enfoque ayuda a introducir pruebas en práctica y los resultados se traducen en menor morbilidad, menor internación, menor variabilidad entre los profesionales, y menor uso de los recursos9.
Este enfoque es un cambio filosófico de la gestión tradicional en varios aspectos importantes. En primer lugar, proporciona un enfoque coherente de la atención perioperatoria, para todos los pacientes sometidos a un procedimiento particular, independientemente del clínico. Esto normaliza los procesos y disminuye la variabilidad no deseada entre los profesionales, facilitando la toma de decisiones para los enfermeros y para los residentes. Esto requiere que los miembros del equipo lleguen a un consenso durante la creación de las VRM, creando algoritmos de tratamiento.
Los pacientes avanzarán a lo largo de una trayectoria predeterminada, sin necesidad de que se escriba la dieta diaria, manejo del dolor, catéter, la movilización, fluidos y controles. Los pacientes informados de las metas diarias en el período preoperatorio están más comprometidos con su propio cuidado. Esta vía, está orientada a acelerar la recuperación de los pacientes sin complicaciones, que son la mayoría. En lugar de mantener a todos los pacientes en ayunas porque la minoría de pacientes no tolerará la ingesta oral temprana, permite que más pacientes se beneficien de la nutrición temprana. Por supuesto, el equipo debe seguir supervisando e intervenir para los pacientes que desarrollan complicaciones (Figura 6).
Es importante que el programa trate problemas comunes o complicaciones que puedan ocurrir. El desarrollo y la implementación de un enfoque VRM es mejor logrado por un equipo multidisciplinario que incluye cirujanos, anestesiólogos, nurses, enfermeras involucradas en todas las fases de la atención, nutricionistas, fisioterapeutas y administradores. Crear materiales de educación para el paciente y familiares ―metas diarias, conjuntos de órdenes estándar, hojas de flujo de enfermería y criterios de egreso vinculados a metas con una fecha límite de alta―; y capacitación de todo el personal. El equipo debe auditar los procesos seleccionados y revisar el programa según sea necesario.
Una revisión sistemática a partir de 2.014 identificó 38 ensayos aleatorios en cirugía colorrectal, genitourinario, osteoarticular, torácica y sistema digestivo superior. La revisión concluyó que el uso de un VRM se asoció con una internación hospitalaria reducida, sin aumento en las readmisiones. Los VRM también se asociaron con una reducción del 30% de las complicaciones a los 30 días, sin riesgo aumentado de complicaciones mayores o muerte. El efecto fue similar en las diferentes disciplinas y al comparar la cirugía laparoscópica versus colorectal abierta. A la fecha, son cada vez más los estudios que apoyan estos beneficios. Esto se relaciona no solo con una mejor organización de la atención, sino también a menos complicaciones “generales” y más rápido retorno de la función intestinal10.
ERAS en pediatría
Pocos estudios han explorado su éxito en pediatría. Un argumento potencial contra las vías estandarizadas en los pacientes quirúrgicos pediátricos, es que los resultados son abrumadoramente buenos, en relación con los adultos, por lo cual limitan el beneficio potencial de los algoritmos de atención, que demandan mucho tiempo y organización. Para el mismo procedimiento, los resultados postoperatorios, como la mortalidad, la morbilidad mayor o incluso la duración de internación, varían sustancialmente entre niños y adultos. Aunque la mortalidad perioperatoria es menor en los niños, la evidencia sugiere que algunos procedimientos de cirugía pediátrica tienen muchos resultados comunes, de los observados en adultos11. En particular, los procedimientos colorrectales pediátricos presentan una incidencia dispar de infección del sitio quirúrgico (ISQ) en relación con otros procedimientos quirúrgicos en los niños12. La alta tasa de infección en los procedimientos colorectales pediátricos, hacen de esta subespecialidad un grupo atractivo para los ensayos de VRM en niños. El objetivo es que estos niños tengan una recuperación acelerada del intestino, disminución de la tasa de infección y aumento de la satisfacción del paciente y la familia. En esta línea de trabajo, se encuentra trabajando el Dr P. Mattei del Children´s Hospital of Philadelfia, que ha publicado en su libro Fundamentals of Pediatric Surgery, un capitulo especifico del tema13.
La educación perioperatoria tendrá que ser modificada para los distintos grupos etarios, con el fin de que los niños participen en su cuidado.
El desarrollo de la vía ERAS no consiste en crear nuevas hipótesis para una mejor atención, sino más bien en la organización de la mejor evidencia científica disponible, en un paquete implementable que ayude a estandarizar la atención a través de una práctica, institución o sociedad profesional.
Hay un gran grado de variabilidad dentro de la atención pediátrica del paciente quirúrgico, incluyendo las preferencias de la práctica individual. Un reciente análisis norteamericano a nivel nacional, de datos administrativos, demostró variación de la prescripción de antibióticos perioperatorios tanto del cirujano, como institucional y que la mitad del tiempo no se cumplía con guías nacionales14).
Slusher et al.15 demostraron que la normalización del tratamiento de la apendicitis aguda disminuyó las necesidades de antibióticos y redujo las readmisiones sin cambiar la duración de la internación o la incidencia de abscesos.
La aplicación directa de los protocolos ERAS en los niños ha sido limitada, principalmente por la falta de pruebas para la extrapolación a una población pediátrica. El único metanálisis realizado en los programas ERAS utilizados en niños, encontró solo cinco estudios que implementaron específicamente protocolos de recuperación perioperatoria, que incluyeron al menos cuatro componentes de la ERAS Society. Incluso el más completo, sólo incluyó 6 de las 20 intervenciones recomendadas.
Cada paciente pediátrico es único, pero los que presentan un adecuado desarrollo del lenguaje, podrían ofrecer una vía de recuperación similar a la utilizada por los adultos. Los pacientes adolescentes pueden de hecho recuperarse más rápidamente que los adultos; sin embargo, los mecanismos de afrontamiento, las habilidades de comunicación y las prioridades entre los dos grupos son muy diferentes.
Comienzan a aparecer datos que apoyan el uso de componentes ERAS individuales en los niños. Uno de los principales elementos ERAS, es la analgesia multimodal intraoperatoria y postoperatoria. En nuestro centro hospitalario se apoya el uso de técnicas de anestesia regional, como complemento de la anestesia general y el manejo del dolor postoperatorio. En cuanto a la atención postoperatoria, la alimentación enteral temprana ha demostrado que no tiene ningún efecto negativo en los reingresos postoperatorios, por ejemplo para las piloromiotomías16.
Uno de los estudios más prometedores hasta la fecha, de West et al.17, comparó pacientes pediátricos con enfermedad inflamatoria intestinal versus controles de adultos. Ambos grupos se sometieron al mismo procedimiento, pero los pacientes adultos se recuperaron más rápidamente bajo los principios ERAS. Los pacientes pediátricos promediaron un adicional de 3 días en el hospital y 3 días sin una dieta sólida, mientras que no hubo ninguna diferencia en los reingresos o en la morbilidad.
El artículo de H. Short y cols.18, en el cual por un proceso Delphi modificado y un panel de expertos multidisciplinarios, evaluó la propiedad de usar protocolos de recuperación mejorada a nivel pediátrico, concluye que 19 de sus items son de uso adecuado para adolescentes sometidos a cirugía intestinal de coordinación. Es así que los mismos autores publican sus primeras experiencias19.
Respuesta metabólica al traumatismo quirúrgico
El paciente quirúrgico está expuesto a agresiones propias de la edad, de la cirugía, de la anestesia, periodos de ayuno y alteraciones biológicas propias de la enfermedad. Si la magnitud de la agresión es suficiente, la respuesta local se rebasa y los estímulos desencadenan una respuesta, de sistemas regulados por mediadores químicos, la cual se conoce como SRIS ―síndrome de respuesta inflamatoria sistémica―, caracterizada por la liberación descontrolada de mediadores.
La respuesta orgánica es proporcional a la magnitud de las lesiones; de modo que una incisión pequeña y limpia sólo lesiona las células que están a lo largo de la herida y causa inflamación mínima, en tanto que una quemadura extensa y profunda es una lesión mayor que causa daños extensos en los tejidos y se expresa una respuesta inflamatoria exagerada20.
Esta respuesta se caracteriza por la activación inmediata del sistema nervioso y del sistema endocrino; participando los mediadores de los sistemas inmunológico y vascular.
Los estímulos pueden ser tanto de orígen local (lesión de tejidos), como sistémicos (temor o ansiedad, ayuno, hipotermia, estados de hipoxemia, efectos anestésicos, fármacos, sustancias tóxicas, pérdida de volumen circulante por hemorragia o deshidratación, alteraciones del pH sanguíneo, desequilibrios hidroelectrolíticos, desequilibrios metabólicos).
Las vías aferentes de información, pueden transmitirse por vía nerviosa (sistema simpático y por el vago en las cirugías abdominales) o vía humoral (mediadores de la inflamación).
El cerebro integra y procesa las señales nerviosas y humorales que recibe, generando una respuesta neuroendocrina, la cual se expresa a través de dos ejes dominantes: el eje simpático suprarrenal y el eje hipotálamo-hipófisis-suprarrenal que convergen en sus efectos.
Síndrome de respuesta inflamatoria sistémica (SIRS)
Se atribuye a una reacción inflamatoria masiva y daño endotelial generalizado que se supone mediado por moléculas proinflamatorias o reactantes de fase aguda.
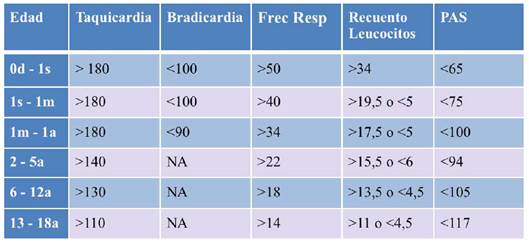
La definición de consenso para SRIS en niños se muestra en la Figura 7 y las diferencias de la definición de adultos en negrita. Aunque las recomendaciones básicas de Bone et al. para la definición de SRIS son aplicables a la niños, taquicardia y taquipnea son síntomas comunes de presentación de muchos procesos de la enfermedad pediátrica. Por lo tanto, la diferencia principal en la definición entre adultos y niños es que el diagnóstico de SRIS pediátrica, requiere que la temperatura o las anomalías de leucocitos estén presentes (es decir, no debe ser diagnosticado si exhibe solamente aumento de frecuencia cardíaca y respiratoria). Además, los valores numéricos de cada criterio deben modificarse para tener en cuenta la diferente fisiología de los niños (Tabla 1). Finalmente, la bradicardia puede ser un signo de SRIS en el grupo de edad recién nacido, pero no en los niños mayores (en los que se trata de un evento casi terminal).
Tabla 1: Sindrome de Respuesta Inflamatoria Sistémica

Fuente: extraída de Goldstein B et al: International sepsis consensus conference: Definitions for sepsis and organ dysfunction in pediatrics. Pediatr Crit Care Med 2005;6:2-8. NA-No Aplica
Existen múltiples artículos que analizan SRIS en niños como por ejemplo, evolución en apendicitis21, cirugía intestinal22, etc., qué demuestran que los niños con SIRS, tienen más probabilidades de presentar complicaciones postoperatorias.
La respuesta de estrés quirúrgico y desarrollo de resistencia insulínica
Dentro de los cambios fisiológicos de la respuesta metabólica a la cirugía, está el desarrollo de la resistencia a la insulina. Existe una correlación entre los altos valores circulantes de la Proteína C Reactiva (PCR), marcador de respuesta inflamatoria y una pobre sensibilidad a la insulina preoperatoria.
La resistencia a la insulina puede definirse como una condición en la que una concentración normal de insulina produce una respuesta biológica subnormal. La hiperglucemia y la descomposición proteica representan las dos principales consecuencias metabólicas del estrés quirúrgico.
Se han identificado condiciones preoperatorias tales como cáncer, obesidad mórbida y síndrome metabólico, y elementos perioperatorios tales como ayuno y hambre, dolor, reposo en cama y fatiga, contribuyendo al establecimiento del estado de resistencia a la insulina postoperatorio. La modulación de la respuesta al estrés resultaría en la normalización de la acción de la insulina y los principales componentes del metabolismo, preservando los depósitos de proteínas.
Reducción del estrés quirúrgico
La reducción del estrés durante un procedimiento quirúrgico electivo, no sólo proporciona una base racional para el aumento de la recuperación, sino que también disminuye el riesgo de disfunciones y complicaciones orgánicas. Por lo tanto, el principal objetivo para el futuro es proporcionar una "operación libre de estrés y dolor". Los factores que modifican y/o reducen la respuesta al estrés y disfunciones orgánicas son múltiples23 y por lo tanto requieren un enfoque planificado y coordinado. Figura 5
Educación preoperatoria y optimización médica
Información
La educación preoperatoria del niño y su famila, es un elemento esencial en un programa de recuperación mejorada24. Se ha asociado con menores niveles de ansiedad, menor dolor postoperatorio y menor hospitalización. Deberemos adaptar la información a cada etapa de desarrollo del niño. Esta debe proporcionarse mediante directrices claras por escrito, incluyendo las metas específicas para cada día del postoperatorio, la duración prevista de la internación, los criterios de alta ―determinada por la evolución del niño y por lo tanto impredecible― y la manera de continuar su recuperación tras esta.
El alta para una cirugía, es variable según la aparición o no de complicaciones. Sin embargo, las familias deben tener una idea de lo que se espera que sea una duración media de la internación.
Se ha visto que es mejor informar por un tiempo corto de estadía, que para una prolongada. Por ejemplo, en el Children´s Hospital of Philadelfia muchos pacientes están listos para el alta en el día 2 ó 3 postoperatorio, luego de una ileocecectomía laparoscópica por enfermedad de Crohn, por lo cual esos son los días que se les informa25.
Hoy en día muchos centros de referencia, cuentan con información multimedia de las diversas patologías, para que las familias tengan una aproximación y puedan comprender a qué situación se están enfrentando.
Se puede mejorar la comunicación entre los profesionales de la salud y los pacientes. Creemos que es de fundamental importancia sugerir que los clínicos disminuyan la velocidad de su lenguaje, usar un lenguaje sencillo, no médico, mostrar dibujos, limitar la cantidad de información y crear un ambiente libre de vergüenza.
Los materiales impresos, son herramientas esenciales de educación preoperatoria. Una guía para pacientes específica del procedimiento, aumenta la consistencia de los mensajes recibidos a lo largo del período perioperatorio. Las listas de objetivos diarios crean expectativas realistas sobre cosas como nutrición postoperatoria, movilización y duración de la internación. Estos mensajes reducen la ansiedad y permiten a los pacientes desempeñar un papel activo en su propia recuperación.
El enfoque multidisciplinario, para desarrollar materiales de educación permitirá, que la información sea menos fragmentada. Por ejemplo, en cirugía colorrectal, la enfermera de ostomas debe ser parte del equipo, reuniéndose con futuros pacientes antes de la cirugía.
Muchos pacientes recurren a Internet para obtener información sobre la salud y no todos los sitios web son confiables. Con la universalización que presenta el Plan Ceibal, podría utilizarse este medio, como vía de información para las cirugías mas frecuentes.
Psicoprofilaxis quirúrgica
En nuestro medio, existe instituciones en la que se realiza psicoprofilaxis quirúrgica de forma rutinaria (Dirección Nacional de Sanidad Policial, BPS ― DEMEQUI ― CRENADECER). En el Centro Hospitalario Pereira Rossell, se está en vías de retomar esta práctica.
Optimización médica y prehabilitación
Este es un punto que en la población pediátrica, por suerte no presenta mayores inconvenientes, ya que a esta edad la mayoría de nuestros pacientes están libres de contaminantes, como puede tratarse del tabaquismo, abuso de alcohol, drogas y las enfermedades crónicas que estos provocan. Por supuesto que a mayor edad, podrán presentar una mayor exposición, hecho a tener en cuenta en los adolescentes. Los niños con enfermedades crónicas, a modo de ejemplo pacientes cardiopulmonares, diabéticos, podrán si encontrar cierto beneficio a este nivel.
Manejo de anticoagulación
Se deberá de evaluar factores de riesgo como obesidad, malformaciones vasculares, tipo de cirugía, internación con reposo absoluto en CTI, trauma, inmovilización, etc., sabiendo que es poco frecuente su uso.
Manejo de la glucosa
La incidencia de diabetes mellitus tipo 1 y tipo 2 en los niños está aumentando en todo el mundo. Los pacientes con diabetes corren mayor riesgo de morbilidad y mortalidad postoperatoria. Cuando sea factible, los niños con diabetes no deben someterse a una cirugía electiva hasta que estén metabólicamente estables. La cirugía debería programarse como el primer caso en la mañana, evitando el ayuno prolongado y que el tratamiento se ajuste con mayor facilidad26.
Preparación intestinal
La preparación intestinal se utiliza para vaciar parte del tubo digestivo antes de una cirugía. La razón principal por la que se prescribe antes, es proporcionar un intestino completamente limpio para minimizar el riesgo de derrame fecal intraoperatorio, disminuir el volumen del intestino para una mejor manipulación, o para facilitar la posibilidad de palpar pequeñas masas intraluminales.
La preparación ideal, debería de ser de bajo volumen a ingerir, agradable en gusto, barata, que logre vaciar toda la materia fecal y sin efectos adversos (alterar histológicamente la mucosa, alteraciones hidroelectrolíticas, etc.). Las posibilidades no invasivas de preparación son una dieta líquida oral o una dieta mínima en residuos, combinada con laxantes, dan resultados subóptimos y deben iniciarse días antes de la intervención planificada.
Las preparaciones más comúnmente recetadas son el polietilenglicol (PEG) y el fosfato sódico (preparación mecánica). Un enema, puede lograr una preparación intestinal del colon descendente y recto.
En adultos, la evidencia es suficiente para concluir que la limpieza intestinal se puede omitir con seguridad y no induce una menor tasa de complicaciones en la cirugía del colon. No hay evidencia estadísticamente significativa de que los pacientes se beneficien de la preparación intestinal. Por lo tanto, para resecciones del lado derecho no se requiere ninguna acción. Para las resecciones a la izquierda, muchos cirujanos prescriben un enema el día anterior o el día de la cirugía.
Artículos pediátricos
Los datos son mucho más limitados. Aunque se ha demostrado que es seguro utilizar polietilenglicol y electrolitos, en niños y bebés, su uso sigue siendo bastante difícil. La mala aceptación, la dificultad con el cumplimiento y la tolerancia, y la incapacidad para que los niños comprendan la necesidad de la preparación hacen que la administración sea difícil, y a menudo hacen necesario el uso de sondas nasogástricas para su administración. Son pocos los estudios que analizan este punto.
Leys (2005)27) busca comprobar si la omisión de la preparación mecánica colónica (PMC) en la población pediátrica aumentaría la tasa de complicaciones postoperatorias infecciosas o anastomóticas, y concluye que no hay diferencias significativas. Observó una reducción estadísticamente significativa en el tiempo de la primera deposición y una tendencia a la reducción de la duración de estadía en el grupo que no recibió PMC.
Breckler y Rescorla (2010)28, estudian la infección de las heridas luego del cierre de colostomías, en pacientes con antibióticos vía oral, intravenosos y/o PMC. Observaron que en un pequeño número de pacientes que no habían realizado PMC, no presentaron infecciones de la herida quirúrgica.
En 2012 Serrurier29, organiza un trabajo retrospectivo multicéntrico, donde llega a la conclusión que la PMC se asoció con un mayor riesgo de infección de la herida, no protegió sobre otras complicaciones, y se asoció con mayor duración de la internación (corroborando los estudios de adultos) y sugiere que la preparación intestinal se puede omitir con seguridad en muchos niños que se someten a cirugía del colon, lo que reduce el costo y la incomodidad. Tabla 2.
Tabla 2: Riesgos en la PMC
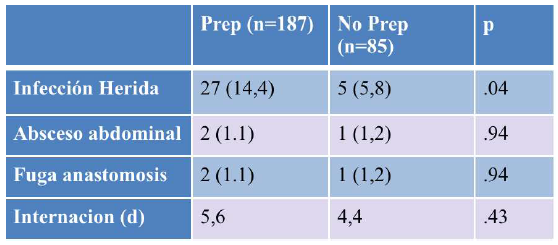
Fuente: Traducida y extraída de Serrurier K, et al. A multicenter evaluation of the role of mechanical bowel preparation in pediatric colostomy takedown. J Pediatra Surg 2012;47:190-193
Un estudio prospectivo randomizado, publicado en la Journal of Pediatric Gastroenterology 201530, concluye que no hay diferencias estadísticamente significativas en las complicaciones (fuga anastomótica, absceso intraabdominal, infección de la herida), entre un grupo que recibió PMC y otro que no.
En la misma línea, en Setiembre 201631, Shah publica un estudio prospectivo aleatorizado, que demostró que no hubo diferencias estadísticamente significativas, en las tasas globales de complicaciones o tasas de infección de la herida, abscesos intraabdominales, fuga anastomótica, sepsis, obstrucción intestinal o complicaciones extraabdominales al comparar el uso de PMC vs ninguna preparación intestinal (líquidos claros el día previo) en pacientes sometidos a resección intestinal electiva o cierre de ostomía. Estos hallazgos apoyan la necesidad de estudios más grandes, potencialmente multiinstitucionales, que investiguen líquidos claros solos, como una alternativa adecuada a las preparaciones intestinales preoperatorias en la población de pacientes pediátricos.
El último trabajo publicado32, utiliza el “Pedatric Health Information System", nucleando 1.581 pacientes de grandes hospitales de Estados Unidos y los divide en tres grupos (Sin PMC, Con PMC, Con PMC + antibióticos orales), llegando a la conclusión de que no existe un beneficio claro para la PMC e incluso que la adición de antibióticos orales podría de hecho aumentar las complicaciones quirúrgicas.
En conclusión, la limpieza mecánica exhaustiva del intestino se ha considerado durante mucho tiempo como esencial antes de las operaciones colorrectales. Se creía que un intestino vacío disminuiría el riesgo de fuga anastomótica y complicaciones sépticas. Sin embargo, durante la última década varios estudios han concluido uniformemente que no hay ventaja de la preparación intestinal antes de las resecciones colónicas, encontrando tasas iguales o menores de fuga anastomótica y complicaciones sépticas en pacientes sin preparación intestinal. Esta conduce a alteraciones de la pared intestinal y a cambios inflamatorios y la misma, puede omitirse con seguridad en las resecciones colónicas de coordinación.
Ayuno preoperatorio y tratamiento de carbohidratos
El ayuno preoperatorio, es una rutina que busca asegurar un estómago vacío en el momento de la inducción anestésica, con el fin de reducir el riesgo de regurgitación del ácido gástrico, el cual puede causar neumonítis química. Basado en estudios de vaciado gástrico, las pautas actuales para la cirugía de coordinación, recomiendan que, los alimentos sólidos no deben ingerirse antes de 6 h de la inducción anestésica y la ingesta de líquidos claros puede recomendarse a la mayoría de los pacientes hasta 2 h antes. Sin embargo, esta guía es probablemente uno de las más subutilizadas. La razón de esto es probable que sea histórica, pero también puede relacionarse con la renuencia de los médicos a cambiar los hábitos tradicionales y la facilidad de adherirse a una regla que es simple y bien conocida que data de los años 60; “Ayuno desde medianoche hasta el momento de la cirugía”.
En 2011, luego de un exhaustivo análisis de la evidencia científica, la Sociedad Europea de Anestesiología desarrolla las guías de ayuno preoperatorio para adultos y niños. Sin embargo, a pesar de ser aceptadas mundialmente y de los beneficios que representan para los pacientes, aún en la actualidad no existe un apego en su totalidad por parte de los anestesiólogos.
Impacto del ayuno en el perioperatorio
Un mal manejo de los períodos de ayuno en el perioperatorio puede asociarse con efectos deletéreos. Estudios actuales demuestran que el ayuno prolongado no significa un estómago vacío, sino que éste se encuentra ocupado de alto contenido ácido. Además, el ayuno aplicado de manera incorrecta provoca alteraciones metabólicas (insulino resistencia), hidroelectrolíticas (deshidratacion e hipovolemia) y una importante sensación de malestar. La deprivación de líquidos previo a una cirugía facilita la presencia de hipotensión durante la inducción, deshidratación, hipoglucemia y una intensa sensación de sed y hambre que inducen a la irritabilidad, especialmente en niños.
Soop y col.33 demostraron que es importante ingerir azúcar con los líquidos claros para evitar la resistencia a la insulina. No solo se logran beneficios metabólicos, sino también se aumenta la sensación de bienestar del por la ausencia de hambre y sed.
Guías de ayuno preoperatorio
El trabajo pionero en este sentido es canadiense, dirigido por el Dr. R Maltby34, quién demostró que la ingesta de 150 ml de líquidos de agua 2 h antes de la cirugía (en lugar de ayunar durante la noche), determinó un menor volumen de líquidos gástricos al momento de la cirugía.
El grupo europeo ERAS, publicó en 2005 un consenso respecto a cuidados perioperatorios, presentando varios cambios de las formas tradicionalistas de cuidados, basadas en estudios controlados y aleatorizados y en metaanálisis. Las modificaciones más relevantes fueron adaptadas al proyecto Aceleracao da Recuperacao Total Pós-Operatória (ACERTO) en Brasil35. Tras su implantación los pacientes pasaron de ayunar una media de 16 h preoperatoriamente a 4 h, no describiéndose ningún caso de aspiración(Tabla 3) .
Tabla 3: Guías de ayuno preoperatorio en pediatría
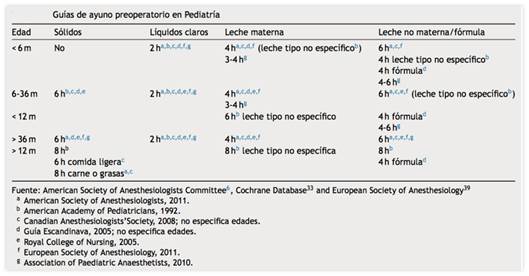
Fuente: extraído de A.C. López Muñoz, N. Busto Aguirreurreta. Guías de ayuno preoperatorio: actualización. Rev Esp Anestesiol Reanim. 2015;62(3):145-156
Una reciente revisión de Cochrane, Ayuno prequirúrgico para la prevención de complicaciones perioperatorias en niños36, buscaba evaluar el efecto de los diferentes regímenes de ayuno (duración, tipo y volumen de ingesta permitida) y la repercusión sobre las complicaciones perioperatorias y el bienestar del paciente (aspiración, regurgitación, morbilidad relacionada, sed, hambre, dolor, comodidad, comportamiento, náuseas y vómitos). Incluyó cuarenta y tres ensayos controlados aleatorizadas (de 23 ensayos, 2.350 niños), y concluye que no existen pruebas de que los niños a los que no se les permiten líquidos orales durante más de 6 horas, se benefician en cuanto al volumen gástrico intraoperatorio y el pH, sobre los niños a los que se permite una cantidad ilimitada de líquido hasta 2 horas antes. Además estos últimos, tienen una experiencia prequirúrgica más cómoda en cuanto a la sed y el hambre. Estas pruebas se aplican sólo a los niños, que se consideran en riesgo normal de aspiración/regurgitación durante la anestesia.
Las pautas de Febrero 2016 de la Cátedra de Anestesia y Reanimación de la UdelaR37, son acorde a estas recomendaciones.
A pesar de la disponibilidad de guías, un reciente trabajo publicado en la Journal of Pediatric Surgery38, concluye que las pautas preoperatorias pediátricas que recomiendan tiempos de ayuno más liberales, no están siendo seguidas. Los tiempos preoperatorios de “nada por boca”, fueron mayores que los recomendados en el 70% de los pacientes estudiados.
Carbohidratos preoperatorios
El objetivo principal, es cambiar el estado de ayuno nocturno a un estado de alimentación, a través de la presencia de la insulina, a los niveles observados después de una comida normal (5-6 veces los niveles basales de ayuno); los hidratos de carbono administrados, deben asegurar que las reservas de glucógeno estén llenas. Al mismo tiempo, era necesaria una bebida que se vaciara lo suficientemente rápido para cumplir con las guías de ayuno modernas. Esto se logró mediante la utilización de una bebida con carbohidratos complejos, hipoosmolar (importante para vaciado gástrico rápido). La bebida que se desarrolló y probó, contiene 12,5% de carbohidratos y tiene una osmolalidad de aproximadamente 265 mosm/kg. Se demostró que se vaciaba del estómago en 90 minutos, sólo ligeramente más lento que una cantidad similar de agua, evocando la respuesta de insulina deseada.
Varios estudios demostraron que tanto la glucosa intravenosa, como los carbohidratos orales, podrían reducir la resistencia a la insulina en un 50% aproximadamente al día siguiente a la cirugía. En los pacientes quirúrgicos de coordinación, el grado de resistencia a la insulina está relacionado con la magnitud de la operación.
Características de bebida con carbohidratos
Hay pocas bebidas comerciales disponibles para este propósito específico. No todas las bebidas con carbohidratos serán útiles, y algunos pueden incluso ser potencialmente peligrosos en la cirugía.
Hay varias bebidas que predeciblemente no estarán logrando estos efectos. Por ejemplo, las bebidas deportivas contienen una concentración de carbohidratos de alrededor del 6%. Estas están diseñadas para dar fluidos, sales y algunos carbohidratos sin provocar una marcada liberación de insulina. Muchos suplementos nutricionales, producirán una elevación suficiente de la insulina, pero no pasaran el estómago lo suficientemente rápido como para ser seguros. El jugo de manzana y otros jugos (sin pulpa) se utilizan. Aunque es probable que muchos de ellos puedan servir al propósito, no se han probado específicamente.
La utilización de forma más frecuente, de la ecografía preoperatoria, para valoración del volumen gástrico39, determinando la seguridad de la ingesta 2 h previo a la cirugía, de líquidos con carbohidratos. También se está evaluando la posibilidad de tomar líquidos, hasta el momento de ser llamado para ir a block quirúrgico40.
Papel del anestesiólogo
Aunque ha habido avances importantes en tecnología quirúrgica y técnicas de anestesia, la tasa relativamente alta de complicaciones postoperatorias continúa teniendo un impacto importante.
Preparar al paciente para la cirugía
La anemia, el mal estado nutricional y un control glicémico deficiente tienen un mayor impacto en la tasa de infección postoperatoria, la función inmune y la cicatrización de los tejidos. Se ha demostrado que la ansiedad preoperatoria, la angustia emocional y la depresión se asocian con mayores tasas de complicaciones, mayor dolor postoperatorio, trastornos cognitivos y convalecencia más lenta.
El papel de la clínica preoperatoria es identificar a los pacientes que presentan un riesgo quirúrgico y anestésico, e intentar optimizarlos desde el punto de vista físico, metabólico, nutricional y mental. Tiene sentido que el anestesiólogo, al ser experto en disciplinas quirúrgicas y médicas, lidere el programa preoperatorio, en conjunto con pediatras, hematólogos, enfermeras, fisioterapeutas, nutricionistas y psicólogos.
Llegar a la Cirugía en Estado de Alimentación
A pesar de la recomendación de la ingesta de líquidos claros hasta 2 h antes de la cirugía, la práctica clínica en muchos hospitales sigue el viejo dogma de mantener al paciente ayunando desde la medianoche.
Elección de fármacos anestésicos
La elección de fármacos anestésicos se basa en el entendimiento de que la respuesta fisiológica y metabólica a la cirugía tiene que ser minimizada y la prolongación del efecto de los fármacos anestésicos en la recuperación debe evitarse. Con esto en mente, deben evitarse ansiolíticos de acción prolongada y se deben usar agentes anestésicos de acción corta. El índice biespectral (BIS), es una tecnología donde a partir de un electroencefalograma continuo, se monitoriza la profundidad anestésica. Permite administrar la dosis adecuada de fármacos para mantener el nivel anestésico deseado, evitando la sobredosificación y por tanto reduciendo los efectos adversos de los mismos. Se pueden usar fármacos anestésicos adyuvantes tales como ketamina, dexmedetomidina, lidocaína y dexametasona para sus efectos ahorradores de opioides. Se aconseja fuertemente la profilaxis de náuseas y vómitos (dexametasona, droperidol, odansetrón).
Papel de la anestesia regional
La anestesia regional tiene amplios beneficios, pero requiere de experiencia técnica. Su uso en neonatos, lactantes y niños continúa aumentando, tanto como anestesia única o en combinación con anestesia general, para proporcionar analgesia intraoperatoria e inicial postoperatoria. El dolor no tratado tiene varios efectos deletéreos, desencadenando estrés quirúrgico con consecuencias autonómicas, hormonales, metabólicas, inmunológicas/inflamatorias y neurocomportamentales. El alivio efectivo del dolor puede desempeñar un papel importante en el resultado quirúrgico. Los lactantes y los recién nacidos tienen un riesgo ligeramente mayor de complicación, y estos grupos de edad deben seguir siendo dominio de los profesionales experimentados.
La anestesia regional generalmente se realiza en combinación con anestesia general en niños. Existen varias ventajas para esta práctica, ya que la profundidad anestésica puede reducirse, disminuyendo potencialmente las complicaciones del acto anestésico. Los sistemas de órganos inmaduros (cardiovascular, nervioso central y respiratorio) son sensibles a los efectos depresivos de los anestésicos. Todos los agentes anestésicos inhalados producen una disminución de la mecánica cardiorrespiratoria y del control ventilatorio central, particularmente en neonatos, lactantes y niños pequeños.
La anestesia regional se ha utilizado como un agente único para prematuros sometidos a reparación de hernia inguinal, evitando complicaciones asociadas con la anestesia general (apnea, hipoxemia y bradicardia).
Además, en estos últimos años, la neurotoxicidad o el impacto que los agentes anestésicos generales tienen sobre el cerebro en desarrollo, está estimulando un gran interés. Estudios recientes41 han sugerido que los anestésicos (agonistas del receptor NMDA, antagonistas del receptor GABA) pueden inducir la muerte celular neuronal en el cerebro en desarrollo inmaduro.
Mantener la homeostasis durante la cirugía
La hipotermia, la sobrecarga de fluidos, la hiperglicemia, las respuestas cardiovasculares exageradas como la taquicardia, la hipertensión, la hipotensión, las arritmias y los trastornos respiratorios como la hipercapnia, la resistencia a las vías respiratorias y la hipoxia deben ser evitadas durante la cirugía. Todos estos elementos representan factores estresantes importantes que pueden dar cambios metabólicos y tener un impacto en el resultado postoperatorio.
Analgesia multimodal para facilitar la recuperación
En vista de la naturaleza multifactorial y complejidad de las vías de dolor, la analgesia debe lograrse con diferentes clases de medicamentos que actúan en múltiples sitios. Las estrategias analgésicas multimodales no sólo tienen como objetivo mejorar el control postoperatorio del dolor, sino también atenuar la disfunción multiorgánica inducida por el dolor no aliviado y también reducir los efectos secundarios de los opioides, como náuseas, vómitos e íleo, facilitando así la reanudación temprana de la vía oral y movilización.
Hipotermia
Los pacientes pediátricos son particularmente susceptibles al desarrollo de hipotermia (temperatura central <36° C) en la sala de operaciones debido a que tienen una proporción reducida de peso/superficie, aumento de la pérdida de calor en la cabeza y reservas limitadas de grasa subcutánea en comparación con adultos. Además, los fármacos anestésicos, deprimen las capacidades termorreguladoras de los recién nacidos y lactantes.
Causas de la hipotermia perioperatoria
Los pacientes frecuentemente se enfrían cuando llegan al block quirúrgico (BQ), ya que usan una ropa delgada y la anestesia general altera nuestras respuestas termorregulatorias. La inducción de la anestesia causa vasodilatación periférica directa y disminuye el umbral de los escalofríos y la vasoconstricción de 2-3° C, dando como resultado una vasodilatación y una distribución del calor del núcleo a la periferia, que disminuirá la temperatura central de 1-1,5° C después de 1 h de anestesia.
Tander et al.42) han demostrado que el tipo de cirugía y la temperatura BQ son los principales factores para la disminución de la temperatura central en recién nacidos y lactantes. En los recién nacidos, las temperaturas centrales son menos estables, independientemente de la temperatura y el tipo de cirugía. En una temperatura ambiental alta, los lactantes pueden estabilizar su temperatura central mejor que los neonatos. La mayor disminución de la temperatura central, se produce en los recién nacidos sometidos a cirugía mayor y con una temperatura baja de la sala (<23° C). La cirugía mayor aumentó la probabilidad de disminución de la temperatura central en 2,66 veces y la temperatura BQ <23° C por 1,96 veces.
Consecuencias adversas de la hipotermia perioperatoria
Incluso la hipotermia perioperatoria leve (34-36° C) se ha demostrado que se asocian con resultados adversos. La hipotermia leve triplica el riesgo de ISQ, al afectar directamente la inmunidad y causando vasoconstricción, lo que disminuye el suministro de oxígeno a la herida. También aumenta significativamente la pérdida de sangre y el riesgo relativo de transfusión en aproximadamente un 20% por cada 1° C de caída en la temperatura central, que es sustancial y clínicamente significativa. Altera también la función plaquetaria, así como la función de las enzimas en la cascada de la coagulación, prolonga la duración de la acción de los anestésicos y los bloqueadores neuromusculares que pueden resultar en una recuperación tardía. La hipotermia, puede persistir durante varias horas y se suele recordar como uno de los peores aspectos de su experiencia perioperatoria. Esta molestia también es estresante para los pacientes y eleva la presión arterial, la frecuencia cardíaca y los niveles de catecolaminas plasmáticas.
Nauseas y vómitos postoperatorios
Las náuseas y vómitos postoperatorios (NVPO) son complicaciones comunes y desagradables de la anestesia y la cirugía. Se estima que la tasa de incidencia total de NVPO para todos los pacientes quirúrgicos, adultos y pediátricos, es del 25%, mientras que la tasa de NVPO en pacientes de alto riesgo puede llegar a un porcentaje mayor.
Una mejora significativa reciente hacia un control eficaz de las NVPO, ha sido determinada por la identificación del paciente en riesgo utilizando factores predictivos; la modificación de la técnica anestésica para mantener el riesgo lo más bajo posible y la administración de antieméticos racionalmente, teniendo en cuenta su grado de eficacia, su riesgo y sus posibles efectos aditivos.
Identificación de pacientes de alto riesgo
A nivel pediátrico, no es posible aplicar las tablas pensadas para adultos y los datos a este nivel son escasos. Sin embargo, en un estudio observacional multicéntrico prospectivo llevado a cabo en Francia (2007/8)43, con 2.392 pacientes, estableció cinco factores de riesgo independientes y los utilizó para crear un nuevo score predictivo pediátrico, que va de 0 a 6 puntos. Los factores de riesgo considerados son: edad, predisposición de náuseas y vómitos, duración de anestesia mayor a 45 minutos, cirugías de riesgo y uso de opioides. Con este puntaje, los niños con una puntuación de 0-1 punto tienen un riesgo bajo, 2-3 un riesgo moderado, y 4 o más tienen un riesgo alto (Tabla 4).
Tabla 4: factores de riesgo

Fuente: Adaptado de Bourdaud N, Devys JM, et col. Development and validation of a risk score to predict the probability of postoperative vomiting in pediatric patients: the VPOP score. Pediatr Anesth 24 (2014) 945-95
El tratamiento profiláctico con antieméticos es clave en la prevención de NVPO. La combinación de distintos fármacos, con mecanismos de acción sinérgicos, presenta mejores resultados.
Se ha demostrado que el uso de propofol como parte de anestesia total intravenosa (TIVA), disminuye la incidencia de NVPO temprana, en aproximadamente el 25%. Una revisión sistemática44 de 58 estudios ha demostrado que la TIVA también es útil para la prevención de NVPO después del alta.
Los métodos de reducción del riesgo deben utilizarse para todos los pacientes, evitando el óxido nitroso y reduciendo la necesidad de opioides intraoperatorios y postoperatorios mediante el uso de técnicas regionales y neuroaxiales. Además, el tratamiento profiláctico con ondansetrón y dexametasona debe utilizarse en aquellos pacientes con factores de riesgo.
Manejo de líquidos
El objetivo en el manejo de líquidos y electrolitos, es el mantenimiento de un equilibrio de fluidos “cero”, junto con una ganancia o pérdida de peso mínima.
Para lograr resultados postoperatorios óptimos, los programas quirúrgicos deben implementar vías de equilibrio de fluidos, utilizando un aumento de peso mínimo como indicador de calidad. Sin embargo, no es raro ver a los pacientes quirúrgicos sépticos ganar litros en el agua corporal total en las primeras 48 h después de la reanimación con cristaloides. Como el cuerpo es incapaz de excretar el exceso de sal con facilidad, puede tardar hasta 3 semanas para perder este exceso de líquido acumulado. Aunque la sobrecarga de sal y agua, a veces puede ser una consecuencia inevitable de la reanimación de enfermos críticos, este escenario es frecuentemente e innecesariamente encontrado después de la cirugía, retrasando así la recuperación, aumentando las complicaciones y prolongando la internación.
El manejo perioperatorio de fluidos en pacientes quirúrgicos pediátricos, no ha sido ajeno a esta corriente45. Holliday y Segar46 en 1957 presentaron por primera vez un método práctico para prescribir líquidos intravenosos basándose en los requerimientos metabólicos estimados para pacientes en reposo en cama. Sin embargo, tanto el volumen como la composición, deben ser adaptados según el estado del paciente, el tipo de operación y los eventos esperados en el período perioperatorio. El agua corporal total de un recién nacido es de 75-80% y disminuye gradualmente a medida que la grasa y el músculo aumentan con la edad al nivel de adultos de aproximadamente el 60%. El fluido extracelular representa el 45% del peso corporal en neonatos a término y el 30% a la edad de 1 año, en comparación con el 20% en adultos. Se requiere un manejo meticuloso del líquido en pacientes pediátricos ya que el margen de error es extremadamente limitado.
Optimización del estado de hidratación preoperatoria
El asesoramiento y la preparación preoperatorios, son un componente clave de los protocolos de VRM. Es importante que los pacientes sean alentados y tengan la oportunidad de mantener la ingesta oral de líquidos (idealmente bebidas que contienen carbohidratos) hasta 2 h antes de la operación, para evitar la depleción de líquidos. Del mismo modo, la preparación mecánica intestinal lleva a pérdidas de sal y agua, y no parece disminuir el riesgo de infección. Si se usan, los pacientes deben recibir terapia líquida intravenosa suplementaria para reemplazar las pérdidas gastrointestinales y asegurar el equilibrio de fluidos cero. La inducción de la anestesia en pacientes con un déficit de fluido, reduce aún más el volumen circulatorio efectivo al disminuir el tono simpático.
Terapia intraoperatoria dirigida
La terapia dirigida, tiene como objetivo principal guiar la reposición y la terapia vasopresora/inotrópica, utilizando mediciones del gasto cardíaco u otros parámetros similares, para mejorar el volumen sistólico, el índice cardiaco y la perfusión esplácnica. Se pueden utilizar varios dispositivos como el Doppler transesofágico, el análisis del pulso arterial y las técnicas de termodilución transpulmonar para monitorizar y dirigir la reposición.
Fluidoterapia postoperatoria óptima
En el contexto de un protocolo VRM, el fracaso en lograr y mantener un equilibrio nulo, tiene efectos deletéreos potenciales sobre la respiración (aumento de la neumonía), gastrointestinales (íleo prolongado, edema esplácnico, presiones de ruptura anastomóticas menores y aumento de la fuga), la movilidad del paciente (reducida por edema periférico) y el bienestar (aumento de náuseas). Por el contrario, pueden producirse efectos perjudiciales de la subhidratación perioperatoria, lo que resulta en una disminución del retorno venoso, el gasto cardíaco, la disminución de la perfusión tisular y el suministro de oxígeno. Además, la subhidratación aumenta la viscosidad de la sangre y la viscosidad pulmonar, dando como resultado formación de tapones mucosos y atelectasias.
El medio óptimo para suministrar fluidos después de la cirugía es a través de la vía oral, lo que junto con el comienzo temprano de la nutrición oral, facilita el retorno precoz de la función intestinal y permite la interrupción temprana del aporte intravenoso, ayudando a la movilidad y una recuperación más rápida. Revisiones sistemáticas han establecido la seguridad de la nutrición oral temprana, la cual reduce la morbilidad postoperatoria sin aumentar el riesgo de fuga anastomótica47 y en pediatría se están siguiendo las mismas tendencias48).
Lo previamente expuesto, resulta evidente en un trabajo doble ciego aleatorizado en niños49, a los cuales se realizó una cirugía del hemiabdomen inferior, menor de una hora de duración, en el cual diferencian dos grupos en base a su aporte de líquidos intraoperatorio (10 vs 30 ml/kg/h). El grupo al cual se administró 30 ml/kg/h, presentaron menor índice de vómitos postoperatorios y menor sensación de sed.
Recomendaciones del Proyecto Brasileño ACERTO para la población pediátrica
―Cirugía del día: Retirar vías venosas después del procedimiento.
―Evitar fluidoterapia de mantenimiento con líquidos hipotónicos por el riesgo de hiponatremia50)(51
―La administración de fluidos debe ser detallada y exhaustiva52.
―En recién nacidos una pequeña pérdida puede conducir a la deshidratación y por lo tanto a la hipovolemia.
―El ayuno prolongado puede causar hipoglucemia e incluso pérdidas en el mantenimiento del gasto cardíaco durante la cirugía.
―En la cirugía coordinada intestinal, el mal manejo de fluidos puede causar edema en el postoperatorio con riesgo de disfunción intestinal y prolongar el íleo postoperatorio.
Analgesia
La incisión quirúrgica y la manipulación de los tejidos conducen a la lesión celular y la activación de respuestas inflamatorias humorales y mediadas por células. Una variedad de mediadores químicos intracelulares se liberan de los tejidos lesionados, y luego activan los nociceptores sensitivos periféricos (hiperalgesia primaria). Estas sustancias proinflamatorias, sensibilizan los nociceptores también en los receptores de tejidos adyacentes no lesionados (hiperalgesia secundaria). La repetida y prolongada estimulación de los nociceptores periféricos en la zona y en los tejidos adyacentes, conduce a una mayor activación de las neuronas a nivel de la médula espinal (sensibilización central). El dolor agudo quirúrgico puede ser por tanto somático, visceral o neuropático dependiendo del tipo de cirugía y el abordaje quirúrgico53.
Estos mecanismos fisiopatológicos pueden orientarse por parte de un enfoque multimodal para minimizar el impacto de estos procesos biológicos. Un componente clave de una recuperación mejorada incluye por lo tanto estrategias analgésicas para prevenir la disfunción multiorgánica, inducida por el dolor no aliviado y en última instancia facilitar una pronta recuperación.
Los tratamientos analgésicos son más eficaces si se administran antes de la incisión quirúrgica (analgesia preventiva). Sin embargo, el papel de las estrategias preventivas tales como la administración de analgésicos preoperatorios como acetaminofeno, inhibidores de COX-2, antagonistas de NMDA, y/o gabapentinoides sigue siendo poco clara, especialmente en el contexto de un programa de recuperación mejorada.
Componentes de la estrategia multimodal
Existen varias opciones para la elaboración de la estrategia del manejo del dolor multimodal54. El objetivo principal es reducir al mínimo o evitar los opioides sistémicos, que siguen siendo una piedra angular en el tratamiento farmacológico del dolor agudo postoperatorio. Cuando consideramos la fisiopatología del origen del dolor, parece intuitivo que los opioides administrados por sí solos no son suficientes para controlar los múltiples aspectos del dolor postoperatorio. Los opiáceos sistémicos bloquean la nocicepción actuando a nivel central y periférico. Tienen efectos secundarios indeseables, tales como la inducción de íleo, náuseas y vómitos. Estos efectos secundarios, perjudican de manera significativa la recuperación de pacientes sometidos a cirugía gastrointestinal, ya que retrasan la recuperación de la función digestiva e impiden la alimentación precoz. Por lo tanto, es fundamental utilizar formas alternativas de control del dolor con opioides55.
Hay una variedad de medicamentos no opioides, que están incluidos en un enfoque multimodal. Los anti-inflamatorios no esteroideos (AINE), inhibidores ciclooxigenasas-2 (COX-2), y los esteroides sistémicos atenúan el componente inflamatorio de dolor quirúrgico. Los anestésicos locales sistémicos, también han demostrado tener propiedades analgésicas mediante la reducción de la liberación excesiva de mediadores inflamatorios y atenuando la regulación al alza de las células inflamatorias. Los agentes anti-NMDA, como la ketamina y el magnesio atenúan la sensibilización central mediante la menor activación de la médula espinal. Los gabapentinoides, reducen la liberación de importantes neurotransmisores excitatorios que participan en la nocicepción, especialmente en el desarrollo del dolor neuropático. Los Alpha-2 agonista como la clonidina y dexmedetomidina, modulan la transmisión de estímulos nocivos, mediante la activación de receptores α2 presinápticos y postsinápticos de la médula espinal. Los anestésicos locales bloquean la transmisión neural, y por lo tanto evitan la transmisión de estímulos nocivos desde la periferia hacia el sistema nervioso central56. Finalmente, los antagonistas de receptores µ, tales como alvimopan, se pueden utilizar en conjunto con medicamentos narcóticos para limitar los efectos secundarios gastrointestinales.
Entre otros elementos de la analgesia multimodal contamos con la analgesia epidural torácica, analgesia espinal, infusión intravenosa de lidocaína, infusión continua de heridas con anestésico local, bloqueos abdominales (bloqueo del plano transverso-abdominal (TAP) y bloqueo de vaina del recto), medicamentos como los AINE, acetaminofeno y antagonista de receptor opioide de acción periférica (Alvimopan).
En definitiva, se recomienda un abordaje analgésico multimodal que incluya técnicas de analgesia regional cuando se indique, analgésicos no opioides regulares y opioides, para proporcionar una analgesia óptima, minimizar los efectos secundarios de los opioides y facilitar la recuperación quirúrgica.
Infección del sitio quirúrgico
Las ISQ están entre las infecciones más evitables y son una carga importante para los sistemas de salud. Su prevención es compleja y requiere de la implementación de una serie de medidas antes, durante y después de la cirugía.
Las ISQ son una complicación frecuente y son un factor de riesgo de reingreso durante el primer mes luego del alta hospitalaria57. Además de la morbilidad que le provoca al paciente, implica una mayor utilización de los recursos sanitarios (días de internación, consultas, material blanco para curación, medicación, etc.).
Los elementos centrales a considerar son:
―Readministración de antibióticos.
―Preparación de la piel.
―Baño de clorhexidina preoperatoria.
―Control perioperatorio de la glucosa.
―Las directrices de la Sociedad ERAS indican que la preparación mecánica del intestino no debe usarse rutinariamente para la cirugía del colon.
―Oxigenación en el perioperatorio.
―Mantener euvolemia.
―Prevención de la hipotermia.
―Protectores de heridas y laparoscopía.
A nivel pediátrico, la actual evidencia deriva casi exclusivamente de la población adulta, y los datos de resultados clínicos de alta calidad, para guiar la práctica clínica en los niños, son muy necesarios. Hasta que se dispongan de más datos, las recomendaciones que se ofrecen deben utilizarse como directrices. Existen trabajos norteamericanos a nivel pediátrico que analizan las tasas de infecciones institucionales, nacionales58, y otros como la revisión de Shawn J. Rangel y col.59, cuyo objetivo fue proporcionar un resumen completo de todas las pruebas disponibles para la prevención de complicaciones infecciosas después de los procedimientos colorrectales en niños.
En Lancet Infectious Diseases, Renko y col.60 evaluaron la eficacia del material de sutura impregnado con un agente antiséptico (triclosán) en comparación con el material de sutura convencional. Realizaron un ensayo doble ciego, aleatorizado controlado, de un solo centro de niños, obteniendo 1.633 niños operados de diversos procedimientos en 4 años. Los autores concluyeron que las suturas que contienen triclosan reducen eficazmente la incidencia de infecciones del sitio quirúrgico y que estos resultados son consistentes con ensayos previos y metaanálisis en adultos61.
A finales del 2016, la World Health Organization realiza una publicación basados en una revisión bibliográfica, de 29 recomendaciones para la prevención de la ISQ62)(63.
Nutrición temprana
Se ha creído durante mucho tiempo, sin sustento científico, que el cese de la ingesta oral durante al menos 4-5 días en el postoperatorio de una anastomosis intestinal tenía un papel protector de la misma, lo cual no ha sido probado. Sin embargo, al día de hoy son ampliamente aceptados los beneficios de la alimentación oral precoz tales como la mejora inmunológica, la disminución de la infección quirúrgica, disminución de la atrofia de las vellosidades intestinales y muchos efectos psicológicos positivos64. También puede mejorar la respuesta metabólica a la cirugía reduciendo la resistencia a la insulina, la pérdida de fuerza muscular y el balance de nitrógeno negativo.
En los proyectos de VRM a los pacientes se les permite una dieta líquida clara (agua, jugo, jugos enriquecidos en proteínas) tan pronto como estén despiertos y pueden avanzar a una dieta baja en residuos en el primer día postoperatorio con un suplemento de bebida proteica en cada comida. Algunos programas reordenan el ambiente de la sala para que los pacientes coman en una mesa de comedor común en lugar de ser inmovilizados y aislados en sus propias camas, lo cual fomenta la movilización precoz.
El ayuno prolongado en los niños es más problemático que en los adultos. El ayuno de más de 2-3 días requeriría usar nutrición parenteral total, que tiene sus propios problemas, costos y complicaciones.
Un estudio publicado en la African Journal of Paediatric Surgery65, es uno de los pocos estudios realizados sobre este tema y concluye que es segura la alimentación temprana. Estudios similares66)(67 mostraron que la alimentación oral temprana después de una anastomosis gastrointestinal de coordinación es bien tolerada, ayuda la resolución temprana del íleo, disminuye la infección de la herida y disminuye los días de internación. Otro estudio realizado en 64 niños menores de 12 años sometidos a resección intestinal y anastomosis, mostró que el inicio de la alimentación antes de las 72 h y después de 5-7 días no tiene ninguna diferencia en las complicaciones68. En un meta-análisis y una revisión sistemática de 11 estudios, incluidos 837 pacientes, se encontró que el ayuno largo de los pacientes después de la cirugía gastrointestinal de coordinación no es útil y el inicio de la alimentación temprana es más beneficioso69. Un estudio que se realizó en México, determina la seguridad y la eficacia de la alimentación enteral temprana después de las anastomosis intestinales electivas distales (ileon-colon) en niños70.
También se está valorando la alimentación precoz, en otras situaciones clínicas, como en las gastrosquisis71y la colocación de tubos de gastrosomia72.
En pediatría, además, ha sido motivo de investigación por varios años la realimentación postoperatoria luego de la piloromiotomía extramucosa de Fredet-Ramstedt y se ha demostrado que la alimentación enteral temprana, no tiene efectos negativos73. En un estudio en recién nacidos, que requirieron cirugía abdominal por anomalías congénitas, se vio que los que se alimentaban precozmente realizaban su primer defecación 24 hs antes en promedio, la alimentación por SNG era menos prolongada, retomaban la vía oral completa antes, no presentaban infección de la herida y tenían una estadía hospitalaria menor74.
El proyecto brasileño ACERTO propone que, volúmenes pequeños de la dieta después de la operación son capaces de:
―Estimular el tracto gastrointestinal.
―Producir peristalsis propulsivas.
―Estimular el tracto gastrointestinal y reducir el período de íleo postoperatorio.
―Disminuir los días de internación.
―Promover la reducción catabólica en respuesta al estrés.
―Mejorar el sistema inmunológico y el trofismo intestinal.
―Proporcionar una mejor cicatrización de las heridas y mejorar la cicatrización de las anastomosis.
―Disminuir la tasa de infección postoperatoria y diversos efectos psicológicos beneficiosos.
Movilización temprana
Los pacientes que se levantan precozmente de la cama después de una cirugía mayor, tienden a recuperarse más rápidamente y tienen menos complicaciones. Hay que alentarlos a levantarse de la cama y caminar al baño el mismo día de la cirugía o, si no pueden hacerlo con seguridad, no más allá de la mañana siguiente. La movilización temprana es un paso importante en la aceleración de la recuperación postoperatoria y es un componente clave de los programas de recuperación mejorada. El dolor, los drenajes y las vías reducen la posibilidad de deambulación.
Ileo postoperatorio
El íleo postoperatorio (IPO) es un cese transitorio de la actividad intestinal. Podría decirse que es la complicación más frecuente después de la cirugía digestiva. Vather et al.75 realizaron una revisión sistemática que incluye la IPO como variable principal. El hallazgo más importante de la revisión fue que las definiciones eran extremadamente variables y, a veces contradictorias. Las definiciones sugeridas por el autor fueron:
1. El íleo postoperatorio es el intervalo de la cirugía hasta la expulsión de gases o heces y que se tolere una dieta oral. Se espera que estas dos condiciones deban cumplirse antes del día postoperatorio.
2. Prolongado (patológico); si dos de los siguientes criterios se cumplen en el 4 día postoperatorio, sin previa resolución del íleo:
(1) náuseas o vómitos;
(2) intolerancia a los alimentos;
(3) ausencia de gases;
(4) la distensión abdominal;
(5) la confirmación radiológica.
El tratamiento perioperatorio tiene un impacto importante en el IPO. El manejo de fluidos perioperatoria sirve como ejemplo. La administración de un exceso de líquidos por vía intravenosa perioperatoria, especialmente solución salina, tiene un profundo efecto patológico en la fisiología intestinal. Características fisiopatológicas comunes, incluyen el edema intestinal, la acidosis y la presión abdominal, resultando en problemas en la curación de heridas, complicaciones anastomóticas, e IPO.
Prevención del íleo postoperatorio
1. Alimentación oral temprana.
2. Manejo de fluidos.
3. Consideraciones quirúrgicas: La incidencia y la duración del IPO parece estar en proporción con el grado de traumatismo quirúrgico.
4. Consideraciones anestésicas: drogas anestésicas perioperatorias, técnicas analgésicas, y el momento y la cantidad de líquidos intravenosos.
5. Analgesia ahorradora de opioides.
6. Otras intervenciones. La goma de mascar estimula la respuesta cefálica-vagal y es una forma de simulacro de alimentación.
Manejo de sondas y drenajes
Las sondas nasogástricas son algunos de los procedimientos más molestos que infligimos a los pacientes. También pueden resultar así los drenajes, que de dudosa utilidad en muchos casos, tienen el efecto contraproducente de “atar el paciente a la cama”.
A nivel pediátrico Sandler76 y Davila-Perez77, llegaron a las conclusiones que su uso rutinario no reduce el riesgo de íleo o aspiración y tampoco representaban ningún beneficio clínico relevante. Además, contribuye en el retraso de la ingesta de alimentos por vía oral y prolongar el tiempo de internación.
Recientemente, un estudio prospectivo78, que busca determinar el uso de SNG en niños que requirieron cirugía digestiva, concluye que su uso rutinario luego de cirugía de coordinación es innecesario. Además destaca que el grupo sin SNG, se alimentó precozmente y presentaron tiempos de internación menores, con cifras estadísticamente significativas. En contraposición, el grupo con SNG, presentó síntomas como dolor de garganta y nauseas, ausente en el grupo sin SNG.
Las recomendaciones del Protocolo brasileño ACERTO en relación al uso de SNG, van en el mismo sentido, sugiriendo su uso de forma individualizada, preventivo y por tiempo limitado, en pacientes con alto riesgo de dilatación gástrica o íleo prolongado.
Por tanto se pueden llegar a las siguientes conclusiones:
― La descompresión gástrica rutinaria en niños sometidos a resecciones intestinales electivas no está indicada.
― La descompresión gástrica rutinaria puede ser perjudicial en la población pediátrica.
― Varios ensayos controlados aleatorizados han demostrado que el uso rutinario de la sonda nasogástrica debe interrumpirse.
― La descompresión nasogástrica debe utilizarse sólo en pacientes sintomáticos.
Los drenajes causan inflamación, evidenciado por el ascenso de citoquinas en el líquido drenado a los 7 días. Además en un alto porcentaje se colonizan con bacterias, por lo que pueden provocar inflamación e infección, lo que podría conducir a una formación de abscesos. Pueden moverse del sitio colocado, no obteniendo la información deseada. Pueden taparse al cubrirse con material con fibrina, coágulos o epiplón.
En definitiva, los drenajes pueden ser útiles en casos complicados o donde el riesgo de sangrado o fuga es alto y en particular donde el riesgo es elevado, como en la pancreatectomía. De lo contrario, no se recomienda el drenaje abdominal de rutina.
Sondas vesicales
La producción urinaria se ha utilizado para evaluar el volumen intravascular y la necesidad y la cantidad de líquido de reanimación. Sin embargo, la producción de orina, particularmente durante la cirugía laparoscópica, no es un buen monitor del volumen intravascular. Varias herramientas de medición hemodinámica no invasiva, incluyendo el doppler esofágico y los dispositivos de pulso arterial, están disponibles para guiar más fiablemente la reposición de líquidos.
El riesgo de infección del tracto urinario aumenta con la duración del cateterismo. Los catéteres hacen que sea más difícil para el paciente deambular y hacen innecesario que se levante con el fin de orinar.
Implementación de un programa de recuperación mejorada
Cada vez es más claro que cuando se aplican protocolos perioperatorios sistemáticos y basados en la evidencia, se puede hacer que los pacientes se sientan más cómodos y mejoren su recuperación. El cuidado del paciente también debe ser racionalizado y los pacientes no deben ser sometidos a la incomodidad y la indignidad de los procedimientos innecesarios, los rituales sin valor y las terapias que no están apoyados por la evidencia científica.
Debe existir una base científica sólida para cada paso específico del protocolo de recuperación mejorada, así como para el programa en su conjunto, que agrupa varios conceptos dentro de una única vía clínica integral. Pero no se pretende que sean estrictos, sino que también es importante que sea flexible y cuidadosamente diseñado para satisfacer las necesidades de cada paciente.
Resulta evidente por la cantidad de artículos que han surgido en el último año, respecto a la aplicación de programas ERAS en pediatría, el interés de los cirujanos pediátricos en este tema.
Se han utilizado con seguridad los programas de recuperación mejorada, en pacientes con apendicitis, hipospadias, cirugía torácica, pieloplastias, funduplicaturas, anastomosis digestivas, nefrectomias, etc.79. El tema común es que cada componente debe ser apoyado por la evidencia científica.
¿Donde se podría aplicar en el CHPR?
Basados en lo expuesto previamente, consideramos que para comenzar un programa de estas características, sería adecuado comenzar en sectores donde ya estén equipos formados. Los programas ERAS, tuvieron sus inicios a fines de la década de los 90, en relación a la cirugía colorectal en adultos y de ahí se han extendido a otras áreas de la cirugía general y a otras especialidades, como urología, traumatología y ginecología fundamentalmente.
En nuestro centro hospitalario, contamos con posibles sectores para comenzar, que desde nuestro punto de vista podrían ser:
―La policlínica de coloproctología.
―La policlínica de cirugia torácica.
―El Centro Hemato - Oncológico.
―En la Clínica Quirúrgica Pediátrica, seleccionando una patología frecuente, como es la apendicitis aguda.
La corta historia y el éxito de los protocolos de recuperación me jorados deberían ser una clara lección de que los métodos empíricos, las prácticas supersticiosas y la práctica tradicional pueden estar equivocados y, a pesar de nuestra habilidad técnica, atención al detalle y buenas intenciones, puede provocar sufrimiento y daño real a nuestros pacientes por adherirse obstinadamente a métodos tradicionales no probados. Es mucho mejor, para nuestros pacientes, que veamos la enseñanza tradicional y la sabiduría convencional con escepticismo, mantengamos una mente abierta e insistamos en que cada acción que tomemos en el cuidado de nuestros pacientes, sea justificada y basada en principios científicos sólidos.