Introducción y antecedentes
Muchos de los Desórdenes Potencialmente Malignos (DPM) presentes en la mucosa bucal, suelen manifestarse clínicamente con lesiones blancas1. Dentro de ellos, la leucoplasia y una variante muy agresiva llamada leucoplasia verrugosa proliferativa (LVP), o mejor llamada “leucoplasia proliferativa multifocal”(LPM)2, es la que tiene mayor tasa de transformación maligna. La LPM es una entidad descripta por Hansen et al3 en 1985 y cuyos criterios de diagnóstico han sido optimizados por muchos autores hasta la actualidad 4-5. La Organización Mundial de la Salud (OMS), definió la LPM como una variedad agresiva de leucoplasia caracterizada por una alta tasa de recurrencia y transformación maliga6.
La LPM se presenta inicialmente como una lesión blanca pudiendo corresponderse a mancha o placa queratótica, la cual gradualmente comienza a adquirir un carácter proliferativo abarcando diferentes áreas de la mucosa bucal volviéndose multifocal, con un crecimiento difuso e incontrolable. Las lesiones puede comenzar a tomar volumen adquiriendo aspectos verrugosos y transformarse en Carcinomas Verrugosos o Carcinomas de Células Escamosas 7.
Las lesiones de LPM son usualmente rebeldes a las terapéuticas, incluyendo modalidades como escisión láser, cirugía convencional, radiación y quimioterapia. Sin embargo, el seguimiento estricto de los pacientes, el control y las biopsias tempranas son la mejor herramienta para evitar la transformación carcinomatosa5. El objetivo de este trabajo es reportar un caso clínico de una paciente con lesiones de LPM y su estricto seguimiento clínico durante un período de tres años (estado actual).
Descripción
En marzo de 2017, concurrió una paciente de sexo femenino de 75 años derivada por un Cirujano de Cabeza y Cuello a la Cátedra de Estomatología “A” de la Facultad de Odontología de la Universidad Nacional de Córdoba, Argentina por la presencia de lesiones blancas en borde de lengua, sin síntomas asociados.
La paciente, edéntula total, presentó como antecedentes personales patológicos artrosis e hipertensión y sin otros antecedentes personales ni heredofamiliares de relevancia para el caso. No se reportaron hábitos asociados como consumo de tabaco, alcohol y drogas. Su dieta era rica en vegetales y frutas y consumo diario de un litro de mate cuya temperatura no superaba los 75°.
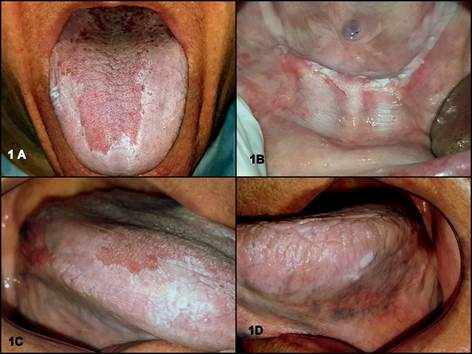
Durante la inspección intraoral se observó una extensa lesión blanca de 5 años de evolución, que no se desprendía al raspado localizada en sector anterior del reborde alveolar inferior, cara dorsal y ventral, bordes y punta de lengua comprometiendo de la misma manera mucosa yugal de ambos lados. Las lesiones se presentaron por sectores como verdaderas placas queratóticas con tendencia a hacerse verrugosas, como puede observarse en la Fig. 1.
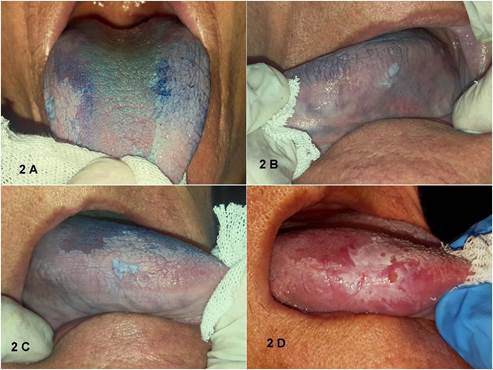
Se solicitaron análisis de laboratorio prequirúrgicos, y se decidió realizar biopsias incisionales seriadas de las áreas más representativas guiadas con Azul de Toluidina (Figura 2). Cabe destacar que este pigmento no penetra fácilmente a los estratos profundos del epitelio, por lo que su utilización quedaría limitada a lesiones verrugosas o hiperqueratóticas. Sin embargo, siempre resulta una herramienta de complemento para la selección del área representativa previa a las maniobras quirúrgicas. Además, se obtuvieron células mediante frotis o escobillado, para luego de ser depositadas en un medio de transporte específico, realizar la prueba de Reacción de Polimerasa en Cadena (PCR) para detección de Virus Papiloma Humano (VPH) y su posterior genotipificación.
La anatomía patológica de los especímenes biopsiados mostró imágenes similares, demostrando un epitelio hiperplásico, acantósico con hiperqueratosis superficial, hipergranulosis y presencia de algunas alteraciones celulares afectando el estrato basal compatible con una displasia leve. Las manifestaciones clínico-patológicas pueden ser encuadradas dentro de los criterios de diagnóstico de Leucoplasia Proliferativa Multifocal. El resultado de PCR-VPH fue negativo, por lo tanto, se descartó la presencia de ADN viral en las lesiones.
Dada la multifocalidad y las extensas áreas que abarcaban las lesiones, se procedió a implementar un protocolo de follow-up. Dicho protocolo fue consensuado con la paciente y sus familiares, estipulando visitas mensuales el primer semestre de seguimiento, bimensuales el segundo semestre, trimestrales el segundo año de seguimiento y luego según la evolución del cuadro clínico se pactó espaciar visitas o acortar los espacios inter-consultas. Inicialmente, se prescribió un tratamiento antimicótico local, eliminación de cualquier elemento traumatizante de las prótesis completas que portaba la paciente y educación sobre las técnicas de higiene. Se insistió en importancia del control periódico.
Posteriormente se procedió a la calibración de residentes de Medicina Oral del servicio en el seguimiento del caso para estandarizar los criterios de follow-up y seguir una metodología estricta de trabajo en las visitas de control: examen general estomatológico, fotografía de todas las áreas de la mucosa bucal afectadas o no, tinción vital con azul de toluidina y decisión de toma biopsia (en el caso de presencia de áreas verrugosas no advertidas en el último control, presencia de lesiones nodulares con aumento de consistencia, presencia de áreas de rápido crecimiento desde el último control y presencia de áreas eritroplásicas que no mejoren frente a la eliminación del trauma o infección micótica o que no estén asociadas a estas condiciones) (Fig.3).
La paciente se mantuvo estable durante tres años. Se requirió de la realización de una nueva toma de biopsia por presentar una lesión que cumplía con los criterios de indicación antes mencionados, con diagnóstico histopatológico de hiperqueratosis con displasia leve, similar a las observadas inicialmente.
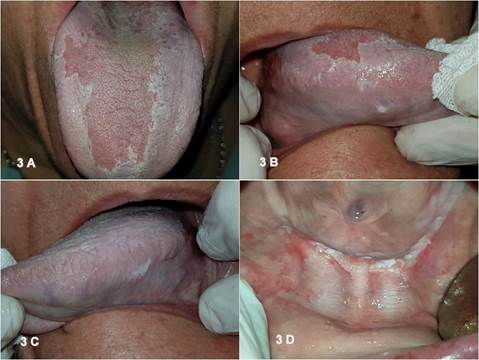
Fig. 3: Fotos obtenidas a los 8 meses de la primer visita con una notoria estabilidad de la lesiones
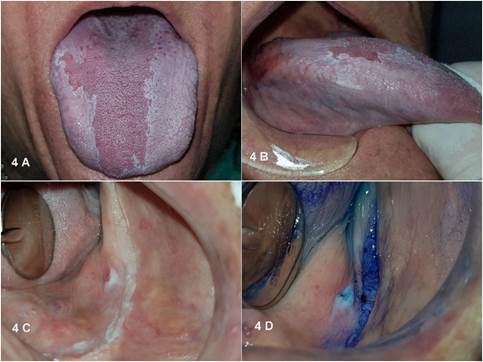
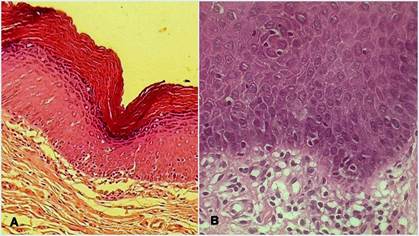
La paciente fue adherente a los controles durante el primer año, sin embargo, no siguió en forma rigurosa durante los años subsiguientes por presentar dificultades en la movilización asociadas a su artrosis. Hasta el momento de la realización de este texto, no se observaron focos de transformación carcinomatosa. La fig. 4 evidencia el último control y la fig. 5 muestra la histopatología de la primer biopsia de borde de lengua.
Discusión
La LPM es una de las patologías que generó y genera más debate en torno a su nomenclatura, naturaleza y tratamiento. A lo largo de las últimas décadas se han propuesto diferentes criterios de diagnóstico de la enfermedad. En muchos casos, puede comenzar como una leucoplasia única homogénea8 que prolifera transformándose en una entidad multicéntrica, con o sin cambios malignos al momento del diagnóstico. Uno de los criterios diagnósticos más utilizados son los propuestos por Cerero-Lapiedra y cols propuestos en 20114. La paciente presentada en nuestro caso era una mujer de 70 años de edad, sin factores de riesgo asociados como el tabaco y alcohol. Clínicamente se trataba de una placa blanca de más de 3 cm, con existencia de áreas verrugosas que se encontraba comprometiendo más de dos sitios diferentes de la cavidad oral: cara dorsal y ventral, bordes y punta de lingual, mucosa yugal y reborde alveolar inferior, denotando que durante su evolución, las lesiones se diseminaron. Todas estas son características que coinciden con casos similares de LPM reportados en la literatura a lo largo de los años y reúne todos los criterios mayores y menores de Leucoplasia Proliferativa Multifocal propuestos por Cerero-Lapiedra et al en 2011.
Como parte del manejo clínico y seguimiento, se recomienda la documentación mediante fotografías en cada visita, registrando las lesiones y también áreas de mucosa clínicamente sana. Las biopsias estarán indicadas en casos de encontrar clínicamente áreas rojas, nodulares o verrugosas o zonas de induración. En casos de informarse displasia, las lesiones deberán ser eliminadas quirúrgicamente y los patólogos deberán siempre reportar los márgenes de las LPM, aún en ausencia de displasias5. Esta paciente realizó un seguimiento estricto durante los primeros años, llevando un pormenorizado control clínico de las lesiones, así como también el chequeo permanente del estado de las prótesis para evitar irritación mecánica crónica y sobreinfección micótica.
Aún no se ha establecido la patogénesis de la enfermedad9. Debido al aspecto clínico verrugoso de las lesiones asociadas a LPM, se relacionó la infección por VPH, encontrando en la literatura diferentes tasas de infección por VPH en LPM10. Además, se han encontrado aberraciones en genes reguladores del ciclo celular, con deleciones, pérdida de heterocigosidad, y mutaciones en algunas de estas lesiones11. En nuestro caso, la PCR para diagnóstico molecular de VPH fue negativa y no se pudo vincular la patología a hábitos de la paciente ni otros factores externos (como por ejemplo la residencia en zonas de alto consumo de agua contaminada con arsénico frecuente en nuestro país), asociados a la presencia de leucoplasia bucal.
Es de destacar que algunos autores han propuesto que algunas LPM podrían tener en sus inicios formas clínicas similares a las reportadas en liquen plano bucal (LPB) y lesiones liquenoides12. La frecuencia de LPM en pacientes mujeres, no fumadoras, y con lesiones multifocales usualmente mayores a 50 años y la similitud de este escenario clínico con el LPB, puede ser uno de los puntos que vinculen ambas patologías13. En este caso las características de la paciente concuerdan con lo referido anteriormente. Además, existen detalles clínicos que llevaron a presumir la evolución a LPM de un cuadro asociado a LPB previo. En la lesión de dorso lingual, se observó más hacia la punta una zona francamente queratótica con un patrón que forma estrías similares a las descriptas en LPB. Sin embargo, no hubo biopsias de la mucosa bucal anteriores a la primer consulta de la paciente y por lo tanto el diagnóstico de LPB no pudo realizarse inicialmente. También algunos autores han propuesto hallazgos clínicos similares al presentado en este caso donde pueden coexistir lesiones de LPM con zonas liquenoides5,14,15. En algunos casos reportados de LPM, se observó un infiltrado linfocitario de interfase yuxtaepitelial similar al de LPB16-17, lo que generó algunas controversias acerca de la verdadera naturaleza de la LPM. El infiltrado yuxtaepitelial en banda presente en muchas lesiones blancas, no sería exclusivo de patologías como LPB o liquenoides, siendo un hallazgo histológico inespecífico presente en lesiones displásicas, alérgicas, asociadas a irritación mecánica14.
La LPM no solamente se caracteriza por su alta tasa de recurrencia post quirúrgica, sino por su alta tasa de transformación carcinomatosa, siendo el DPM con mayor potencialidad de convertirse en un carcinoma. Las tasas de transformación van del 60 al 100%, siendo la gíngiva y el paladar las dos zonas de mayor frecuencia de transformación8,9,16,18,19. En nuestro caso las lesiones estaban mayoritariamente en el reborde desdentado, lengua, mucosa yugal y labial y ausencia de lesiones palatinas. También se pudo observar cómo una vez eliminada quirúrgicamente las lesiones en las biopsias incisionales, rápidamente la mucosa cicatrizó con una patrón queratinizante. Los protocolos de seguimiento estrictos y la adhesión de la paciente a los mismos, permitió seguir un cuidadoso examen en la evolución de la lesión realizando biopsias tempranas en el caso de observar cambios significativos. Debido a que es una entidad refractaria a las terapias actualmente aplicadas, el acompañamiento del paciente en el tiempo es fundamental.
Finalmente, se protocolizaron los seguimientos de follow up de los pacientes con LPM, incluyendo este caso. Los controles incluyeron: revisión sistemática de toda la mucosa bucal mediante visión y palpación, control protético funcional en estática y dinámica, salud periodontal (en el presente caso no se necesitó ya que era una paciente edéntula) y posible sobreinfección micótica. Se evalúa la presencia de lesiones nuevas o aumento de las lesiones observadas en el último control. En estos pacientes, existe un minucioso control de historias clínicas y material fotográfico de mucosa enferma y mucosa sana a fin de establecer si la patología se encuentra en franca evolución o si lleva momentos de remisión del patrón proliferativo. Una vez evaluados todos estos aspectos, se procede a la tinción vital con azul de toluidina de zonas de lesión y zonas de mucosa sana por ser considerados pacientes de alto riesgo de desarrollo de carcinomas, destacando específicamente bordes de lengua y piso de boca. Posteriormente se procede a la observación de los resultados de la tinción, complementándose con la palpación de las lesiones. En base al análisis de todas estas variables controladas durante el follow up, se decide a la realización de biopsias incisionales en el caso de encontrar alguna lesión sospechosa como se aclaró anteriormente.
Conclusión
La LPM es una enfermedad de la mucosa bucal que tiene el mayor índice de transformación carcinomatosa. El éxito de tratamiento en estos pacientes es evitar dicha transformación, y en casos tan extendidos como el aquí presentado donde la extirpación total de la lesión es imposible, el exhaustivo follow up constituye la medida preventivo-terapéutica más importante.
En estos casos, los esfuerzos deben ir dirigidos a crear condiciones para que el paciente y su entorno genere empatía con el Servicio de Medicina Bucal donde está siendo atendido, para lograr una adherencia al seguimiento. Las biopsias tempranas frente a cambios clínicos de alerta son el primer paso para evitar la transformación carcinomatosa de la LPM.











 texto en
texto en