Introducción
La Organización Mundial de la Salud y Ellis y Auclair describieron al adenocarcinoma de células basales (ICD-O Code 8147/3, International Classification of Diseases for Oncology) como una neoplasia epitelial citológica e histomorfológicamente muy similar al adenoma de células basales, pero con crecimiento infiltrante y una baja incidencia de metástasis 1-3).
Antecedentes
Algunos autores consideran que este tumor surge a partir de un adenoma de células basales mientras que otros sostienen que se origina de novo. En un 80% se localiza en parótida, 9% en submandibular y 11% en glándulas salivales menores. Es un tumor poco común, más frecuente en adultos entre la 4º y 9º décadas de la vida siendo muy raro en los niños. La tumefacción suele ser su único síntoma pero a veces produce dolor y en ocasiones no se diagnostica hasta pasados 10 años. Se lo ha categorizado en cuatro tipos en base a su patrón histológico de crecimiento: sólido, membranoso, trabecular y tubular 4-6. Debido a su baja incidencia y a la escasa información bibliográfica, resulta a menudo difícil diagnosticar un adenocarcinoma de células basales 7.
El objetivo del presente estudio fue presentar un caso de adenocarcinoma de células basales de lóbulo profundo de parótida en una mujer de 52 años e identificar características morfológicas e inmunohistoquímicas que contribuyan a su diagnóstico.
Este trabajo es parte del proyecto “La matriz extracelular y el componente mioepitelial de los tumores epiteliales de glándulas salivales humanas: estudio estructural, histoquímico, inmunohistoquímico y lectinhistoquímico, autorizado por el Comité de Etica del Hospital Nacional de Clínicas. Facultad de Ciencias Médicas. Universidad Nacional de Córdoba. Argentina (Registro 188/14).
Caso clínico
Paciente mujer de 52 años, que en noviembre de 2002 consultó con el odontólogo y un servicio de otorrinolaringología por dolor en la región izquierda de la mandíbula, sin llegarse a un diagnóstico. En diciembre de 2002 realizó una nueva consulta, donde se encontró una masa nodular en la rama ascendente izquierda de la mandíbula, con aumento del dolor a la palpación. Se le diagnosticó neuralgia del trigémino descartando la importancia de la lesión nodular; se indicó fisioterapia en la región cervical. Sin embargo, el dolor continuó en aumento por lo que en diciembre de 2003 se le realizó una punción biopsia de una adenopatía donde se informó la presencia de un proceso inflamatorio.
En enero de 2004 se realizó una interconsulta con un cirujano de cabeza y cuello quien solicitó una TAC de cuello donde se evidenció una imagen compatible con lesión tumoral. En febrero del mismo año se extirpó un tumor de lóbulo profundo de parótida izquierda con buena evolución postquirúrgica.
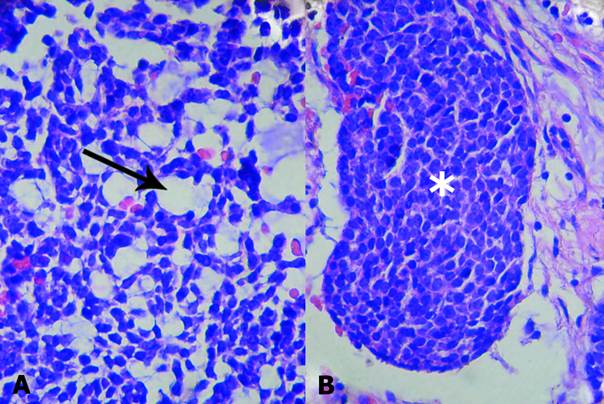
Informe anátomo-patológico: A la macroscopía se observó una masa encapsulada ligeramente lobulada, de 5x 1,7x 1,2cm de color gris violáceo con zonas firmes al corte. En el examen microscópico de los cortes coloreados con H/E se observó una cápsula fibrosa que rodeaba a las células basaloides con citoplasma eosinofílico pálido y núcleos redondeados u ovales organizadas en láminas y nidos de forma y tamaño variables, separados por bandas de estroma conectivo. No se encontraron áreas de necrosis tumoral, atipias celulares ni figuras mitóticas.
El patrón histológico de crecimiento era de tipo sólido y tubular. El patrón sólido presentó nidos y cordones de células basaloides contiguas que en la periferia de estas estructuras formaban una capa celular organizada en empalizada.
En el patrón tubular se destacaban islotes celulares basaloides que contenían seudoquistes o luces prominentes revestidos por células cuboideas (Fig. 1A y B).
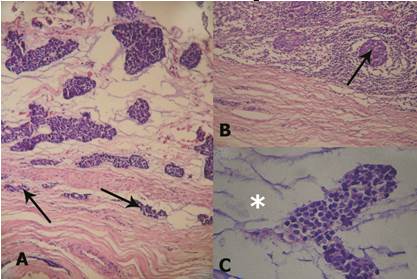
El diagnóstico de adenocarcinoma de células basales tipo mixto se hizo sobre la base de sus patrones histológicos (sólido y tubular) y su carácter maligno, con un crecimiento agresivo con infiltración de la cápsula tumoral y la grasa periparotídea, invasión perineural y metástasis de un nodo linfoide regional (Fig. 2A, B y C).
Posteriormente se observó el compromiso del seno maxilar con metástasis ósea.
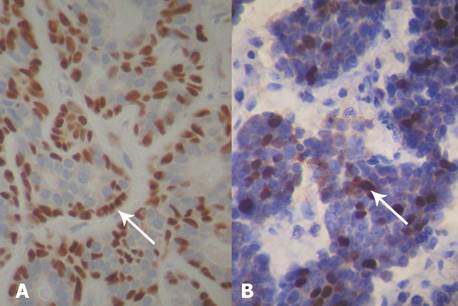
Se realizaron marcaciones inmunohistoquímicas para investigar la diferenciación de las células basaloides en células epiteliales (CK 19) y mioepiteliales (p63 y alfa actina de músculo liso) (Fig. 3A). Con el marcador para Ki-67 se estudió la capacidad proliferante del tumor. Se dio sólo puntuación positiva si existía más de un 10% de células marcadas 8, obteniéndose un 25% de células positivas. (Fig. 3B).
Los resultados se muestran en la Tabla 1.
Tabla 1: Análisis inmunohistoquímico del adenocarcinoma de células basales
| Marcador | Célula marcada | Reacción * |
|---|---|---|
| Ki- 67 (marcador pronóstico de proliferación celular) | Células epiteliales (núcleos) | Fuerte |
| p63 (diferenciación miógena) | Células mioepiteliales (núcleos) | Fuerte |
| Alfa-AML (diferenciación miógena) | Células mioepiteliales (citoplasma) | Moderada |
| CK19 (diferenciación epitelial) | Células epiteliales (citoplasma) | Fuerte |
Alfa-AML: alfa-actina de músculo liso. CK19: citoqueratina 19
* Se realizó la evaluación cualitativa de la marcación según la intensidad de coloración.
Los resultados obtenidos en el estudio histopatológico determinaron que la paciente fuese derivada para su tratamiento oncológico, con indicación de radioterapia postoperatoria durante seis semanas, la que comenzó en marzo de 2004. El plan de tratamiento incluyó la irradiación de la parótida más la región cervical izquierdas a una dosis total de 60Gy, con una dosis diaria de 2 Gy. Presentó como complicaciones mucositis, disfagia y micosis, que, al recibir su tratamiento específico, mejoraron al finalizar la radioterapia.
En setiembre de 2004 se observó en una ortopantomografía un quiste en la rama horizontal izquierda de la mandíbula y una imagen vegetante en seno piriforme homolateral. Se le realizó la cirugía y la biopsia resultó negativa para malignidad.
Posteriormente, en marzo de 2005, comenzó con dolor en el paladar duro y la región izquierda del maxilar. Se indicó TAC donde se observó una lesión a nivel del piso del maxilar. Se hizo la cirugía y se diagnosticó metástasis en el piso del seno maxilar. Se decidió un nuevo plan de radioterapia con complicaciones de mucositis y disfagia.
La paciente empeoró su estado general y presentó un cuadro de deshidratación y somnolencia. No se pudo completar el esquema de radioterapia; se continuó con los cuidados paliativos hasta su fallecimiento dos meses después.
Discusión
Los tumores basaloides primarios de las glándulas salivales son lesiones caracterizadas por un predominio de células epiteliales “basaloides” con núcleos redondos u ovoides rodeados por un citoplasma delgado. La denominación células epiteliales basaloides surgió de las observaciones con técnicas histológicas de rutina que no permiten distinguir si hay células mioepiteliales o epiteliales ductales o basales. En estos casos la marcación inmunohistoquímica es una herramienta útil para detectar ambos tipos celulares, ya que mejora la precisión del diagnóstico. El panel de inmunohistoquímica utilizado en el caso descrito (p63, alfa-actina de músculo liso y CK19) fue importante para el diagnóstico de las células “basaloides”de este carcinoma 9-10.
El grupo tumoral heterogéneo de células epiteliales basaloides incluye a tumores benignos como el adenoma pleomorfo, y el adenoma de células basales y malignos como el carcinoma adenoide quístico, el carcinoma indiferenciado de células pequeñas y al adenocarcinoma de células basales 10-11.
El adenocarcinoma de células basales afecta principalmente a la glándula parótida (más del 90%) y es histológicamente similar al adenoma de células basales. Sin embargo, manifiesta un crecimiento infiltrante y una baja incidencia de metástasis 1-2,12.
Se lo considera generalmente como un carcinoma de bajo grado de malignidad, localmente destructivo y con recurrencias frecuentes. El período de recurrencia varía de 6 meses a dos años y solo ocasionalmente produce metástasis a distancia 12-13.
En este caso la evolución fue atípica, presentó una metástasis ósea en forma temprana, a menos de un año de finalizado su tratamiento derivó en el deterioro del estado general de la paciente y su fallecimiento. Esto puede explicarse por el diagnóstico tardío de la lesión, con metástasis en nodo linfoide; y factores histológicos de mal pronóstico como son la invasión capsular, perineural y de la grasa periglandular.
No existe predilección por género y el 80% de los tumores ocurre después de los 50 años con un promedio de 60 años 14. El caso presentado por nosotros corresponde a una mujer de 52 años.
Sus patrones histomorfólogicos se describen como sólido, membranoso, tubular o trabecular. El patrón sólido es el más frecuente, caracterizado por nidos celulares sólidos de forma y tamaño diferentes. Un estroma colágeno, constituido por bandas de diferente grosor, separa estos nidos que corresponden al patrón histológico más frecuente y con mayor riesgo de producir metástasis. En el patrón membranoso se observan abundantes depósitos de una membrana basal hialinizada fuertemente eosinofílica. El patrón de crecimiento es tubular cuando entre las células epiteliales basaloides se forman espacios luminales mientras que en el crecimiento trabecular las células epiteliales basaloides se disponen en bandas celulares interconectadas 15.
En nuestro estudio el tumor se localizó en la glándula parótida con un patrón de crecimiento mixto ya que las células epiteliales basaloides se disponían en áreas sólidas y tubulares.
En relación a la prevalencia de esta neoplasia en América Latina en las bases de datos consultadas sólo encontramos datos en dos investigaciones, de Ruiz-Godoy y Rivera y col y de Ito y col 16-17.
En el año 1996 Ruiz-Godoy Rivera y col realizaron un estudio clinicopatológico de seis casos de adenocarcinoma de células basales analizados en el Instituto Nacional de Cancerología de México 16.
Ito y col examinaron los archivos del Departamento de Patología del Instituto del Cáncer de Londrina (estado de Paraná, Brasil) correspondientes al período 1972-2001 y analizaron un total de 496 casos de tumores de glándulas salivales mayores y menores. Estos investigadores encontraron sólo tres casos de adenocarcinoma de células basales 17.
Histológicamente, el principal diagnóstico diferencial se realiza con el adenoma de células basales; pero también se incluyen en el mismo la variante sólida del carcinoma adenoide quístico, el carcinoma basaloide escamoso y el carcinoma de células basales cutáneo con invasión profunda 12,15.
Wilson y Robins afirman que la invasión local de los tejidos blandos circundantes y de la glándula son los mejores marcadores para diferenciar el adenoma de células basales del adenocarcinoma de células basales. También consideran de interés complementar el reconocimiento de estos tumores sobre las bases de la invasión con los marcadores de proliferación como Ki-67 y marcadores de apoptosis 18.
En un trabajo previo obtuvimos una marcación Ki-67 negativa en el adenoma de células basales, a diferencia del adenocarcinoma de células basales, donde observamos un índice de proliferación superior al 25%, lo que explica además la evolución desfavorable de esta paciente 10.
Saluja et al, también sostienen que el diagnóstico definitivo de malignidad se establece por la naturaleza invasiva de la neoplasia en los tejidos circundantes 19.
Por otro lado, Jung et al informaron que el adenoma de células basales con invasión capsular también puede ser considerado un tumor infiltrante, lo que lleva a cuestionar la categoría del adenocarcinoma de células basales. En su investigación estos autores describen que ambos tumores no presentan diferencias morfológicas, frecuentemente desarrollan un patrón de crecimiento cribiforme o sólido y son de mayor tamaño que el adenoma de células basales sin invasión capsular. Sin embargo, consideran que la estructura cribiforme del adenocarcinoma de células basales puede corresponder a un diagnóstico equivocado de carcinoma adenoide quístico. Por otra parte, la variante sólida del carcinoma adenoide quístico presenta células con marcada atipia nuclear y frecuentes mitosis 7.
Si bien las metástasis regionales y a distancia no son comunes, en el caso presentado se produjo una metástasis en un nodo linfoide regional y además en el piso de seno maxilar, metástasis que llevó a la muerte de la paciente 12.
En general no existe un consenso en cuanto a su tratamiento ya que algunos recomiendan la escisión local y otros la parotidectomía total, aún en casos de adenoma de células basales tipo membranoso, como mencionan Zhan et al 12.
Para el tratamiento primario del tumor, cuando se origina en las glándulas salivales menores, algunos autores consideran que la escisión quirúrgica debe ser amplia para asegurar su completa remoción 20.
Además, no hay acuerdo sobre el papel de la radioterapia. Sin embargo, se recomienda radioterapia postoperatoria en caso de cirugías con márgenes quirúrgicos positivos o escisión quirúrgica de tumores recurrentes 21-22.
Conclusiones
Coexisten células epiteliales y mioepiteliales en el adenocarcinoma de células basales de las glándulas salivales, identificadas por medio de marcaciones inmunohistoquímicas.
Es de fundamental importancia obtener cortes histológicos de la interfase del tumor con la glándula normal o con la grasa circundante para evaluar la invasión tumoral.
La invasión capsular, perineural y del tejido adiposo periparotídeo, la inmunomarcación Ki-67 positiva con un índice proliferativo de 25% y la metástasis en un nodo linfoide regional y en el seno maxilar son factores de mal pronóstico los que, asociados al diagnóstico tardío, explican la evolución desfavorable de la paciente.
Si bien se trata de un tumor con agresividad local y baja incidencia de metástasis, es de crucial importancia el diagnóstico precoz y la atención oncológica temprana, que dan una mayor posibilidad de curación de estos pacientes.











 text in
text in