MODALIDAD DE TRABAJO DEL TALLER DE PERI-IMPLANTITIS.
La misma se dividió en 3 etapas:1) Desarrollo de temáticas guía, selección y envío de artículos, 2) Recepción, evaluación y devolución de artículos y 3) Taller propiamente dicho.
PRIMERA ETAPA: dio inicio en febrero de 2014, donde se formularon 5 preguntas guía con el objetivo de ordenar la discusión del taller. Ellas fueron: Diagnóstico, Epidemiología, Factores de riesgo, Antecedentes Periodontales y Terapéutica de la Peri-Implantitis. Se realizó una búsqueda bibliográfica de artículos en PUBMED, EMBASE, LILACS y COCHRANE, en el lapso comprendido del año 2000 a la fecha, tanto en inglés como en portugués, siendo utilizados los siguientes descriptores: peri-implantitis, peri implant disease, perimplantitis, risk factor, epidemiology, incidence, prevalecence, treatment, therapeutics, combinado con operadores booleanos. En su mayoría, los artículos recuperados consistieron en estudios retrospectivos, transversales, revisiones sistemáticas, consensos, escasos meta-análisis y estudios prospectivos. Fueron descartados reportes de casos así como revisiones de autor. Por parte de los responsables del taller se seleccionaron los artículos más relevantes, dejando de lado los consensos y se enviaron vía email a los participantes del taller.
SEGUNDA ETAPA: consistió en la recepción y análisis de artículos seleccionados por los participantes del taller. Los que cumplían con los criterios de inclusión, fueron redistribuidos entre los talleristas. La actividad del taller se desarrolló de 8:30 a 12:30hs dedicándole un tiempo aproximado de 45 minutos a cada una de las preguntas guía propuestas. Luego de la discusión, el evaluador realizó un resumen y análisis de los artículos seleccionados destacando además si las conclusiones extraídas guardaban relación con la evidencia resultante de la bibliografía considerada.
Directores del taller: Dres. Judith Esquenazi y Diego Sales. Secretario: Dr. Martín Minvielle. Evaluador: Dr. Ernesto Andrade.
Participantes del taller: Dres.: Adriana Ramos, Carolina Verolo, Jorge Cabrera, Luis Arroyo, Magdalena Mayol, María José Quintana, Ricardo Kaufmann, Verónica Foglino, Virginia Papone, Michel Bittencourt, Carolina Aldaya, Alessia Molinari, Sebastián Pérez.
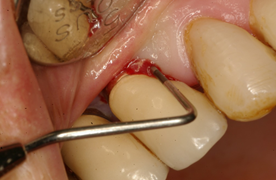
Pregunta Nº 1- ¿Cómo diagnosticamos: Mucositis y Peri-implantitis? El término Peri-implantitis fue introducido por Mombelli en 19871 y luego modificado en el 1er Taller Europeo de Periodoncia para describir una enfermedad inflamatoria que conduce a la pérdida ósea alrededor de los implantes2. Las enfermedades peri-implantarias incluyen además: la Mucositis, descripta como una lesión inflamatoria en la mucosa que rodea al implante, sin pérdida ósea concomitante3. La literatura presenta discrepancias en cuanto a los parámetros clínicos que se deben considerar (Fig. 1).
El tejido conectivo adyacente al implante presenta abundantes fibras colágenas, es relativamente acelular y avascular, presentando características histológicas semejantes al tejido cicatricial. La disposición de las fibras colágenas es paralela al eje implantar, dando por resultado una conexión más lábil y una progresión de la enfermedad más rápida para perimplantitis comparado con la enfermedad periodontal4.
Clasificación de Peri-implantitis5
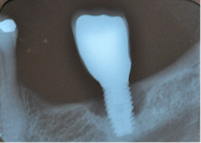
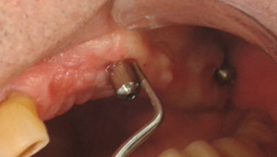
Temprana: Profundidad de sondaje >4 mm, con sangrado y/o supuración en >2 sitios del implante y pérdida ósea < 25% del largo del implante (Fig. 2)
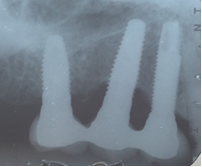
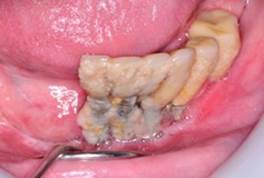
Moderada: Profundidad de sondaje >6 mm, con sangrado y/o supuración en >2 sitios del implante, y pérdida ósea entre 25% - 50% del largo del implante (Fig. 3).
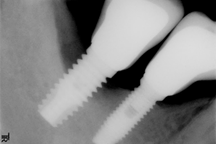
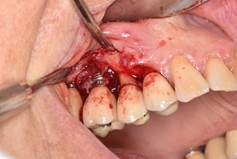
Avanzada: Profundidad de sondaje >8 mm, con sangrado y/o supuración en >2 sitios del implante, y pérdida ósea > 50% del largo del implante (Fig. 4).
Como en toda patología, el correcto diagnóstico es fundamental para establecer un adecuado tratamiento. Los parámetros a tener en cuenta son: el Sangrado al Sondaje y/o Supuración (SS) (Fig. 5) y Profundidad al Sondaje (Fig. 6) aumentada con respecto al examen inicial y control radiográfico. Otros métodos de diagnóstico aportan poca información, son más costosos y complejos de realizar.
La presencia de SS en una exploración delicada, con una presión no mayor a 0.25N es un parámetro muy útil para el diagnóstico tanto de la mucositis como de la peri-implantitis. Numerosos estudios han encontrado una relación directa entre el SS y la pérdida de inserción alrededor del implante. Un estudio prospectivo cuyo objetivo fue monitorear las condiciones de la mucosa peri-implantar durante la terapia periodontal de apoyo, reveló que el sangrado en un mismo sitio, en más de la mitad de las visitas de mantenimiento, durante un período de 2 años se relaciona con el progreso de la enfermedad6.
Diversos estudios han mostrado que un aumento en la Profundidad de Sondaje se traduce en pérdida de inserción y pérdida ósea1,7,8,9. Hay coincidencia en que la presión ejercida no debe superar los 0.25 N, ya que esto permite la recuperación total de los tejidos sin secuelas a los 5 días10, mientras que presiones mayores pueden penetrar los tejidos y llegar a la proximidad de la cresta ósea. En el 6to EUROPERIO (2008) se puso énfasis en que el perfil de emergencia y el contorno de la reconstrucción pueden dificultar la maniobra de sondaje en todo el perímetro, por lo que se sugiere que al menos una superficie (Mesial, Distal, Vestibular o Lingual) debe ser explorada11. Serino y col. en 201312, realizaron un estudio clínico en 119 implantes, donde se revela que sólo en el 37% de los sitios examinados la profundidad al sondaje fue la misma con y sin la rehabilitación instalada; mientras que en el 39% la diferencia fue de 1 mm y en 15% fue de 2 mm, lo que evidencia la dificultad en el correcto sondaje luego de instalada la rehabilitación. Por otro lado, en el 66 % de los implantes, la pérdida ósea fue similar en todo el perímetro, mientras que en los restantes casos fue diferente, siendo vestibular la superficie más afectada4.
Control Radiográfico. Hubo coincidencia entre todos los autores sobre la importancia del control radiográfico de los implantes en el tiempo. La discrepancia fundamental se centra en la oportunidad de obtener la radiografía inicial: al momento de la colocación del implante, cuando se instala la rehabilitación o posterior al remodelado óseo. Este taller encontró mayor evidencia científica, así como coincidencia entre los autores, que sugieren el control radiográfico inicial, luego del remodelado óseo post rehabilitación11,13,14.
Pregunta Nº 2. Epidemiología ¿Cuál es su prevalencia actual? La Epidemiologia representa el estudio de la distribución de las distintas enfermedades en las poblaciones. Se nutre de medidas como la prevalencia e incidencia, a la vez que intenta dilucidar la etiología y los factores de riesgo que participan en el proceso salud-enfermedad. Zitzman & Berglundh concluyeron que la prevalencia de peri-implantitis oscila entre un 28% - 56% de los individuos (12%- 40% de los implantes). Por otro lado, la mucositis peri-implantaria está presente en aproximadamente el 80% de los sujetos y 50% de los implantes3,11. Recientemente, un meta-análisis a partir de 9 artículos publicados hasta el año 2012 con 6283 implantes en 1497 pacientes evidenció que un 9,6% de los implantes presenta peri-implantitis, mientras que considerando al individuo como unidad experimental la cifra alcanza el 18,8%15. Hasta el año 2002, solo el 40-60% de los artículos recuperados aportó datos de sobre “nuevos casos de peri-implantitis”; a su vez, la falta de homogeneidad en los parámetros clínicos y para-clínicos utilizados para el registro de la enfermedad impidió extraer resultados concluyentes sobre la incidencia de la patología considerada16. El estudio de la Enfermedad Periimplantar (Mucositits y Periimplantitis) desde la óptica de la epidemiologia debe tomar en consideración los siguientes aspectos:
la mayoría de los estudios utilizaron muestras para conveniencia del investigador (pudiendo ser tendenciosas) y no seleccionadas por azar (no aleatorias), lo que impide la generalización de los resultados a las poblaciones (validez externa)45;
se observa inexistencia de datos iniciales (ej.: radiografías) que permitan valorar la pérdida ósea y estimar así la evolución;
desde una perspectiva epidemiológica, es inapropiado extraer datos de prevalencia de peri-implantitis solo a partir de un elemento o variable aislada (por ej.: sangrado al sondaje)46;
falta de unanimidad en la definición de peri-implantitis y en los umbrales de cada variable utilizada (sangrado y profundidad al sondaje) utilizada, lo que dificulta la comparación entre los estudios(23, 46)
la inclusión de fumadores y personas con periodontitis modifica la prevalencia de enfermedad, y no siempre estas sub-poblaciones están adecuadamente registradas y consideradas dentro de los estudios;
la utilización del “implante” en vez del “sujeto” como elemento utilizado para cuantificar la enfermedad (unidad experimental de análisis), no representa cabalmente la frecuencia de la enfermedad ya que puede subestimar la patología existente;
la mayor parte de los estudios publicados hasta el momento registran los casos de peri-implantitis con 5 años posterior a la carga del implante; sin embargo algunos autores consideran insuficiente este lapso de tiempo para el desarrollo de dicha enfermedad, siendo mencionados hasta 10 años16
existen carencias en la información que se presenta en los artículos publicados ya que hay datos o información que no son reportados47.
Pregunta Nº 3. ¿Cuáles son sus factores de riesgo? Para identificar un factor de riesgo verdadero son necesarios estudios prospectivos que permitan un seguimiento claro de una población específica y establezcan una relación temporal entre un factor de exposición y la enfermedad. Se han reportado muy pocos estudios con estas características y los datos disponibles generalmente surgen a partir de estudios transversales y series de casos que permiten así identificar indicadores de riesgo17,18.
¿Qué condiciones generales, locales e individuales pueden favorecer la aparición de peri-implantitis? El taller concluyó que los indicadores de riesgo asociados con mayor evidencia son:
Tabaquismo: un meta-análisis que compara fumadores con no fumadores, identifica al tabaquismo como un indicador de riesgo significativo para la pérdida ósea marginal, comparado con no fumadores. Esto debería ser considerado en la información proporcionada al paciente previo al tratamiento, así como en la etapa de mantenimiento donde es posible detectar en forma temprana cambios negativos en los tejidos peri-implantario17,19. El hábito de fumar tiene efectos deletéreos a largo plazo sobre la respuesta inflamatoria e inmunitaria, así como, sobre la cicatrización, con menor producción de colágeno, disfunción de fibroblastos, reducción de la circulación periférica y función de neutrófilos y macrófagos comprometida20.
Higiene oral deficiente: La acumulación del biofilm dental, resultado de una higiene oral deficiente, conduce a enfermedad peri-implantaria11. La asociación entre la cantidad de biofilm y la peri-implantitis, parece ser dosis dependiente ya que los sujetos con valores elevados de biofilm tienen más posibilidad de presentar peor condición peri-implantaria21) (Fig. 7).
Historia de enfermedad periodontal (es analizada más adelante ya que fue considerada como una pregunta aparte).
Por otro lado los indicadores con menor riego son:
Diabetes: ha sido asociada a Xerostomía, Caries y Enfermedad Periodontal. Se considera que la susceptibilidad aumentada a la Enfermedad Periodontal se debe a una influencia negativa de la hiperglicemia en los mecanismos inflamatorios e inmunitarios del hospedero, resultando en una respuesta desregulada, cicatrización alterada y afecciones en la microvasculatura. La heterogeneidad de los datos disponibles impide por ejemplo la realización de meta-análisis22. Un estudio transversal en 212 sujetos, con 578 implantes, incluyó 29 diabéticos. Los resultados de este estudio, muestran que el control metabólico inadecuado en diabéticos aumenta el riesgo de desarrollar peri-implantitis. Se diagnosticó peri-implantitis en el 24,13% de los diabéticos, mientras que en los no diabéticos fue significativamente menor 6,56%21.
Sobrecarga oclusal: los reportes son controversiales, ya que no hay unanimidad en la definición de sobrecarga oclusal. Los implantes se consideran más lábiles que los dientes al enfrentarse a fuerzas no axiales, por la falta de ligamento periodontal23. El stress excesivo puede ocasionar micro fracturas y eventual pérdida ósea. Una revisión sistemática reciente24 sugirió que la sobrecarga oclusal está asociada positivamente con la reabsorción ósea marginal periimplantaria. Sin embargo el biofilm sigue siendo el factor causal clave. Se necesitan más investigaciones con una definición precisa de sobre carga oclusal23.
Alcoholismo: Un estudio prospectivo de 3 años, evaluó la posible relación entre la pérdida ósea periimplantaria marginal, el consumo de tabaco y alcohol. El análisis multivariado mostro que la pérdida ósea estaba relacionada significativamente con el consumo de >10grs diarios de alcohol25.
Cemento residual: en un estudio prospectivo se incluyeron 39 pacientes portadores de 42 implantes, rehabilitados con coronas unitarias cementadas, con peri-implantitis. 12 de ellos tenían además 20 implantes rehabilitados bajo las mismas circunstancias, pero sin peri implantitis (este segundo grupo de implantes se utilizó como control). Para explorar el área subgingival se utilizó un endoscopio dental (Dental View, Irvine, CA). Como resultado se encontró cemento residual en 34 de los 42 implantes test y en ninguno de los controles, siendo removido mediante diferentes técnicas (quirúrgicas y no quirúrgicas). Luego de 30 días, se observó resolución de los signos de enfermedad peri implantaría en 25 de los 33 implantes del grupo experimental. Por lo tanto, el exceso de cemento y su incompleta remoción en la superficie subgingival del implante determina un medio susceptible para la colonización bacteriana y el desarrollo una respuesta inflamatoria26.
Superficie del implante: al momento actual no hay evidencia de que las características superficiales del implante puedan tener influencia significativa en la iniciacion de la peri-implantitis27.
Ausencia de encía queratinizada: La deficiencia de mucosa queratinizada alrededor de los implantes, parece estar relacionada a parámetros clínicos de inflamación y a la acumulación de biolfim. Sin embargo, en base a la evidencia disponible actualmente, la cantidad de mucosa queratinizada en relación al desarrollo de la peri implantitis permanece controversial28,29.
Pregunta Nº 4. Antecedentes Periodontales y la enfermedad peri-implantar. Desde hace algunos años, surge en la literatura un número creciente de trabajos, que tienen como objetivo analizar las relaciones entre la implantología y la periodoncia. La implantologia nacida para la rehabilitación de pacientes totalmente edéntulos, posteriormente también se ocupó de pacientes parcialmente dentados. El fracaso tardío de los implantes, parece estar principalmente correlacionado con el tipo de flora bacteriana peri-implantaria y las condiciones del huésped30. El biofilm asociado a los implantes con peri-implantitis, es semejante al que habita en los pacientes con enfermedad periodontal avanzada1,31 existiendo estudios que evidencian patógenos periodontales colonizando la superficie de los implantes32,33. Especies como Porphyromonas Gingivalis, Prevotella Intermedia y Aggregatibacter Actinomycemcomitans recolectadas a partir de bolsas periodontales avanzadas (asociadas con signos de inflamación) pueden traslocarse a sitios peri-implantarios34,35. La presencia de un biofilm de particular virulencia, se vincula con la aparición de peri-implantitis, dependiendo de la susceptibilidad del hospedero y la presencia de factores de riesgo (mencionados anteriormente). Considerando lo anteriormente mencionado, nos cabe preguntar, si la susceptibilidad a la periodontitis, aumenta la susceptibilidad a la peri-implantitis, incluso en pacientes que fueron tratados por paradenciopatias. Karoussis36 fue pionero en considerar la posibilidad de que personas con historia de enfermedad periodontal sean más propensos a desarrollar peri-implantitis, comparando, con individuos sin historia de enfermedad periodontal.
El análisis de la literatura destaca la existencia de dos categorías de estudios: a) los que investigan el éxito de la terapia implantar en el paciente con historia de enfermedad periodontal sin comparación con los pacientes que no la padecieron y b) los que ofrecen una comparación directa entre pacientes con historia de enfermedad periodontal destructiva y aquellos sin antecedentes de la misma. Varias revisiones sistemáticas37,38,39,40,41,41,43, así como un estudio prospectivo con 10 años en promedio de seguimiento muestran que las personas con historia de enfermedad periodontal tienen más probabilidades de desarrollar peri-implantitis que sin antecedentes de ella44.
Pregunta Nº 5. ¿Cuáles son las técnicas terapéuticas de la peri-implantitis y cuál es su previsibilidad? Las terapias propuestas para el manejo de la periimplantitis están basadas en la evidencia disponible del tratamiento de la enfermedad periodontal, por lo que los pasos básicos para su resolución son: control de la infección, terapia no quirúrgica y quirúrgica y terapia de apoyo. Para facilitar la oseointegración, la mayoría de los fabricantes de implantes presentan en el mercado superficies moderadamente rugosas para aumentar la superficie de contacto lo que representaría una desventaja si el implante queda expuesto al medio bucal. La rugosidad de la superficie y su composición química, al igual que el diseño de implantes roscados, tienen un impacto significativo en la acumulación de Biofilm Oral48. El diseño de la prótesis puede dificultar la correcta limpieza mecánica y el tratamiento de los implantes infectados, por lo que la corrección de la restauración es fundamental para el acceso de los elementos de higiene del paciente49.
Basados en los conceptos mencionados anteriormente, numerosos estudios proponiendo diferentes tratamientos como desbridamiento mecánico, uso de antisépticos, antibióticos locales y sistémicos tanto como acceso quirúrgico y realización de procedimientos regenerativos han sido empleados con resultados diversos. Los intentos por comparar la información disponible en la literatura que permitan extraer conclusiones robustas han fallado por inexsitencia de datos y por no completar los criterios estrictos de un estudio controlado aleatorizado. La ausencia de un verdadero grupo control, el no disponer de un número significativo de pacientes con características clínicas comparables, además de razones éticas, marcan la dificultad de realizar ensayos controlados aleatorizados50. Una revisión sistemática en la cual se incluyeron 9 ensayos clínicos controlados aleatorizados, donde se intentó identificar el tratamiento más efectivo concluyó que no había evidencia confiable que sugiriera qué tratamiento era superior51. Se recomienda comenzar con terapia no quirúrgica. Esto permite evaluar la respuesta tisular inicial así como el cumplimiento del paciente con las medidas de autocuidado, lo que determinara en gran medida el éxito de las opciones terapéuticas propuestas. Estudios donde diversas modalidades de tratamientos no quirúrgicos fueron comparados (desbridamiento mecánico con curetas de titanio y pulido con copas de goma vs. desbridamiento mecánico con dispositivos ultrasónicos y pulido con copas de goma con administración de antimicrobianos) se analizaron a partir de variables como el sangrado al sondaje, profundidad al sondaje y los depósitos de biofilm. En su evaluación al mes, tres y seis meses no se hallaron resultados clínicamente relevantes que demostraran superioridad entre los tratamientos propuestos52. Por otra parte, la utilización de dispositivos de laser (Er:YAG)53) y la aplicación de glicina en polvo a presión limitada54 al ser testeadas con el desbridamiento mecánico no evidenciaron diferencias ni clínica ni estadísticamente significativas. Sin embargo, la terapia no quirúrgica por sí sola es insuficiente en la mayoría de los casos de periimplantitis52. El biofilm y los depósitos calcificados deben ser removidos para permitir la cicatrización y reducir el riesgo de progresión de la enfermedad. El protocolo quirúrgico que implica un acceso quirúrgico, desbridamiento, descontaminación de la superficie, irrigación con suero fisiológico y el uso de antibióticos sistémicos ha sido evaluado, con resultados positivos mantenidos por 12 meses55. Por otro lado estudios realizados por Romeo en 2007, mencionan técnicas en las que se practica la implantoplastia, es decir el pulido de la superficie del implante con piedras de diamante, gomas y pastas siliconadas, reposicionando el colgajo apicalmente56.
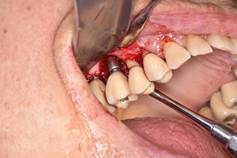
En resumen, de lo expuesto en el taller de periimplantitis del primer congreso de Implantología de la Facultad de Odontología de la Universidad de la República Oriental del Uruguay se concluye que: 1) el tratamiento quirúrgico debe siempre ser precedido por el tratamiento no quirúrgico basado en el desbridamiento mecánico y la utilización de antisépticos como la clorhexidina al 0,12% con una espera de 3 meses antes de comenzar con el tratamiento quirúrgico (Figs. 8, 9).
2) El tratamiento quirúrgico que consiste en: a) la apertura de un colgajo mucoperióstico con la eliminación del tejido de granulación; b) El tratamiento de la superficie del implante ya sea con gasa con suero, gasa con clorhexidina al 0,2%, gasa con H2O2 al 3%, antibiótico local sobre la superficie del implante, spray de bicarbonato de sodio o glicina, Er: YAG laser, curetaje mecánico o implantoplastia; c) técnicas regenerativas o resectivas; d) antibiótico administrado por vía sistémica (Amoxicilina 500mg y Metronidazol 500mg por 7 días); e) aplicación de clorhexidina al 0,12% hasta retomar la higiene mecánica; f) terapia de Apoyo de 3 a 6 meses.
Las técnicas de tratamiento de superficie nombradas han sido analizadas en numerosos estudios clínicos y no se ha comprobado aun la superioridad de alguna de ellas. Por otro lado, en la mayoría de los casos las secuelas estéticas son evidentes, comprometiendo el éxito del tratamiento implanto-protésico. Pese a que resultados a corto plazo fueron reportados en varios estudios, falta de resolución de la enfermedad, recurrencia de la misma y pérdida de implantes a pesar del tratamiento fueron también reportados. Hoy en día no tenemos certezas del éxito del tratamiento de la Peri Implantitis a mediano y largo plazo. Son entonces necesarios estudios prospectivos más extensos en el tiempo que uniformicen criterios como definición, severidad de la enfermedad, heterogeneidad del diseño, tiempo del seguimiento y criterios de inclusión o exclusión.
En cuanto al mantenimiento debe existir un control exhaustivo de biofilm y re motivación. En el examen clínico de los tejidos peri-implantares se debe sondear para controlar su profundidad buscando sangrado o supuración al sondaje. La remoción de la prótesis con este fin puede ser necesaria. Se debe incluir además el análisis oclusal, pesquisando facetas de desgaste o falta de estructura. Se debe complementar con aplicaciones de antisépticos57.











 texto en
texto en