Introducción
La producción animal se ve afectada por las enfermedades parasitarias. En el caso de la parasitosis por Rhipicephalus microplus, además de las mermas productivas que genera y los costos por su control, transmite enfermedades que aumentan las pérdidas y costos de producción (Schillhorn van Veen, 1997). Otro problema asociado son los residuos de acaricidas en productos de origen animal. Su mal manejo pone en riesgo la inocuidad alimentaria y los mercados comerciales para Uruguay (CONAHSA, 2016).
Esta situación se vuelve más compleja con la aparición de resistencia a los acaricidas. Esta se puede describir como la disminución en la susceptibilidad de una población de parásitos a un determinado acaricida cuando este es usado de la forma y a la dosis recomendada (FAO, 2004). La desarrollan los parásitos como respuesta a ser expuestos a condiciones ambientales desafiantes y de forma continua en el tiempo (Conway y Comins, 1979). La utilización de acaricidas reiteradamente y con una alta frecuencia ha llevado al desarrollo acelerado de resistencia (Cuore, 2016).
La resistencia a los acaricidas tiene una distribución internacional observándose en Australia, África, América central y América del Sur (Alonso-Díaz et al., 2006). En Uruguay la problemática de la resistencia de R. microplus a los acaricidas habilitados ha ido incrementándose con los años. El primer antecedente de resistencia fue en 1950 a los arsenicales (citado por Cardozo y Franchi, 1994), al que le siguieron los organofosforados en 1978 (Nari et al., 1982; Petraccia et al., 1983), los piretroides sintéticos en 1994 (Cardozo y Franchi, 1994), las mezclas de piretroides y fosforados en 1994 (Cardozo y Franchi, 1994), el fipronil en 2006 (Cuore et al., 2007), el amitraz en 2009 (Cuore et al., 2012) y las lactonas macrocíclicas en 2010 (Castro-Janer et al., 2012). Se considera que en determinadas oportunidades el mal uso de los acaricidas utilizados en Uruguay para el control de R. microplus, pudo haber acelerado el proceso de desarrollo de resistencia, lo cual fue observado en otros países (Alonso-Díaz et al., 2006; Cuore 2006;). Hasta la fecha, el fluazurón es el único principio activo habilitado sin registros de resistencia en Uruguay (Cuore et al., 2017). La situación de la resistencia se ha vuelto más difícil debido a la aparición de poblaciones multirresistentes en 2009 (Cuore y col, 2012, 2017). Observando esta perspectiva de resistencia claramente desfavorable y mientras no se cuente con una nueva herramienta química o biológica, se puede poner en riesgo en algunos predios la factibilidad técnica en el control de la garrapata R. microplus.
Conocer el perfil de resistencia de una población de R. microplus a los acaricidas es importante para realizar un correcto plan sanitario de control o erradicación de esta parasitosis. Para esto se utilizan las pruebas in vitro que son menos costosas que las técnicas in vivo, son prácticas e incluso son recomendadas para realizar pruebas a poblaciones de campo (Amaral, 1993). El Test de Paquete de Larvas (TPL) (Stone y Haydock, 1962) es una técnica in vitro que permite conocer el perfil de resistencia de R. microplus a todos los grupos químicos de acaricidas habilitados en Uruguay; piretroides, fosforados, amidinas, fenilpirazoles, lactonas macrocíclicas; menos a los inhibidores del crecimiento como Fluazurón (FAO, 2004; Cuore y col, 2017).
Debido a que la situación en el país en torno a esta parasitosis se adecuó la reglamentación existente en 2008 con la aprobación de la ley N° 18.268 de lucha contra la garrapata R. microplus y las enfermedades que esta trasmite. Dentro de las herramientas que plantea esta ley una de ellas refiere a la zonificación del territorio del país, reglamentada por la Autoridad Sanitaria, estableciéndose una zona libre (una superficie geográfica donde no se constata el parásito) y otra de control (una superficie geográfica donde la garrapata R. microplus se encuentra presente) y la CODESA determina las medidas que se deberán tomar para disminuir la presencia de este parásito y de las enfermedades que este trasmite, llevado a cabo por la Autoridad Sanitaria . Una de las medidas a tomar en predios considerados de riesgo es realizar un correcto y eficiente plan sanitario para el control de esta parasitosis. Este plan debería comenzar por conocer el perfil de resistencia de cada población de R. microplus, utilizando un test diagnóstico como el TPL.
El objetivo de este trabajo fue describir los perfiles de susceptibilidad de 47 poblaciones de R. microplus procedentes de establecimientos del norte del país para cinco grupos químicos de acaricidas habilitados en Uruguay utilizando el TPL y analizarlos junto a datos de cada predio obtenidos por medio de un cuestionario.
Materiales y métodos
Entre enero de 2017 y mayo de 2018 se analizaron 47 poblaciones de garrapatas R. microplus, en estadio de teleoginas, plenamente ingurgitadas, provenientes de 47 predios ubicados en departamentos del norte del país: Paysandú, Salto, Artigas, Rivera, Cerro Largo y Tacuarembó. Cada población de garrapatas se obtuvo de un predio diferente. El muestreo aplicado fue no probabilístico ya que los predios se ofrecieron de manera voluntaria. En el momento del muestreo se les realizó un cuestionario al propietario del predio o encargado consultándolo acerca del ingreso de animales al establecimiento ya sea de predios linderos, compras u otras formas posibles de ingreso de animales al establecimiento. Se les preguntó por el número de tratamientos garrapaticidas realizados por año, acerca de cuáles principios activos se habían utilizado históricamente en el predio y si tenían sospechas de resistencia a algún principio activo. Las garrapatas se extrajeron manualmente revisando la totalidad de bovinos de cada establecimiento. En caso de haber utilizado algún acaricida previamente al muestreo, la colecta se realizaba posteriormente a haber transcurrido su tiempo de poder residual. Las garrapatas se trasladaron al laboratorio en el transcurso de 1 a 3 días durante los cuales permanecieron en una caja de cartón que en su interior contenía papel secante humedecido y estaba sellada con cinta adhesiva y se le realizaron orificios de hasta 3mm en la parte superior de la caja. Una vez en el laboratorio se incubaron en las siguientes condiciones: 27°C, 85-90 % HR, 12 horas luz durante 14 días. Cumplido este período de tiempo su ovipostura se colocó en tubos de ensayo de 1,5 cm de diámetro. A estos tubos de ensayo previamente se les colocó 2 ml de agua destilada seguido de algodón colocado a presión en el fondo del tubo con una varilla de acero de aproximadamente 8mm de diámetro hasta que la superficie del tapón de algodón quedara seca. Se monitorearon los huevos hasta detectar su eclosión. Cuando las larvas tenían entre 14 a 21 días de eclosionadas se les realizó el TPL en el departamento de parasitología de la DILAVE Montevideo.
Para el TPL se utilizó una solución de tricloroethileno (analytical standard, n° 46267, Sigma-Aldrich, St. Louis, USA) y aceite de oliva (analytical standard, Supelco, SIGMA-Aldrich, St. Louis, USA) en una relación 2:1, donde se disolvieron los estándares analíticos de los principios activos para los que se evaluó la resistencia de las poblaciones analizadas; cipermetrina (grado técnico, 93.2 %, cedida por laboratorio Microsules, Montevideo, Uruguay), ethión (analytical standard, Sigma - Aldrich, 45477, Saint Louis, USA) , amitraz (amitraz comercial 12,5 %, Acarex), fipronil (analytical standard, Sigma - Aldrich, 46451, Saint Louis, USA), ivermectina (ivermectin, Sigma - Aldrich, I8898, Saint Louis, USA) y flumetrina (reference satandard, Bayer, T31100, Monheim, Alemania). Las concentraciones que se utilizaron para las diluciones fueron las correspondientes a las concentraciones discriminatorias para la cepa susceptible (Mozo), con la cual se pusieron a punto las técnicas en Uruguay (Cuore y Solari, 2013).
Tabla 1: Concentraciones discriminatorias de los 5 principios activos analizados para la cepa Mozo (Susceptible).
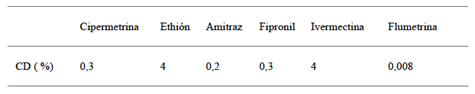
Con cada una de estas soluciones se impregnaron papeles filtro (papel filtro hoja 50x50 cm, equiv. Whatman 1, DIU código: 20 67968) rectangulares de 7,5 x 8,5 cm identificados con el principio activo correspondiente a la dilución con la que se impregnaron y la fecha de impregnación. Para esto se utilizaron 0,67mL de solución por papel distribuyendo la solución de forma homogénea con una pipeta multicanal (F1-Clip Tip, Thermo Fisher) usando nueve tips. Para lograr una mayor homogeneidad se realizaron seis descargas en paralelo, para llegar a los 0,67mL totales, simétricamente a un lado y otro de la línea media del papel (teniendo como referencia su lado de 7,5cm). Para el amitraz se realizó el mismo procedimiento, pero utilizando papel de nylon (2320, Cerex Advanced Fabrics, Pensacola, FL). Los papeles, una vez humedecidos, fueron colgados con un clip bull dog, para prevenir que estuviesen en contacto con cualquier superficie, dentro de una campana de extracción de gases a evaporar durante 24 horas. Transcurrido este plazo se los almacenó en freezer (-30 °C), envueltos en papel aluminio, correctamente identificados.
Para testear las poblaciones de los distintos establecimientos muestreados se colocaron aproximadamente 100 larvas sobre cada papel. Posteriormente se lo dobló a la mitad, por el largo de 8,5 cm, cerrándolo en los costados y el borde superior con clips bull dog, formando así los paquetes de larvas. Para cada dilución se realizaron dos réplicas por población de garrapatas testeadas. Estos paquetes se llevaron a incubar a 27°C, 85-90 % HR, 12 horas luz durante 24 horas. Transcurridas las 24 horas se abrieron los sobres y se contabilizó la cantidad de larvas vivas y muertas por sobre. Si las larvas estaban todas muertas se consideró que las mismas eran susceptibles a ese principio activo y si se encontraban larvas vivas se asumía como resistente. Luego se calculó el porcentaje de mortalidad de cada sobre.
Criterio para el análisis de resultados:
Ecuación 1
Porcentaje de mortalidad=(larvas muertas/larvas vivas+larvas muertas)*100
Cuando en las larvas utilizadas como control la mortalidad fue mayor a 5 % los resultados se corrigieron por la fórmula de Abbot
Ecuación 2
Porcentaje mortalidad corregida=(porcentaje mortalidad del grupo tratado=porcenaje mortalidad del grupo control)/(100-porcentaje mortalidad del grupo control)*100
Cuando esta superó el 10 % se descartaron los resultados.
La mortalidad media se calculó con el promedio de las mortalidades calculadas para ambas replicas realizadas por dilución para cada población. Por último, se realizó el cálculo del porcentaje de resistencia a partir de la mortalidad media (Miller et al., 2007; Stone y Haydock, 1962).
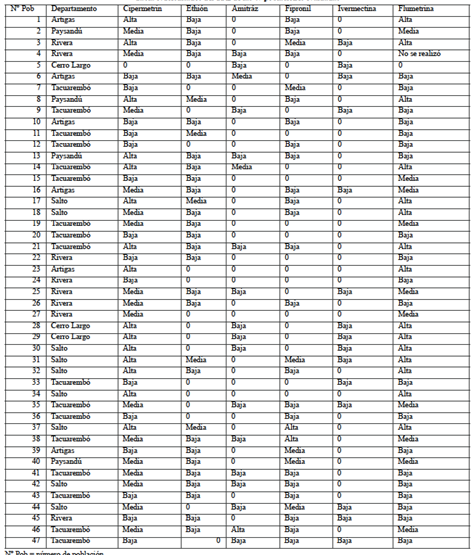
Se consideró que las poblaciones presentan un grado de resistencia bajo cuando el porcentaje de resistencia es menor a 20 %, un grado de resistencia media cuando se encuentra entre 20 % y 50 % y un grado de resistencia alta cuando es mayor a 50 % (14).
Los datos se analizaron mediante una estadística descriptiva.
Resultados
Los resultados obtenidos por medio del cuestionario se presentan en las tablas 2, 3 y 4.
Tabla 2: Resultados de la encuesta de la población 1 a la 18.
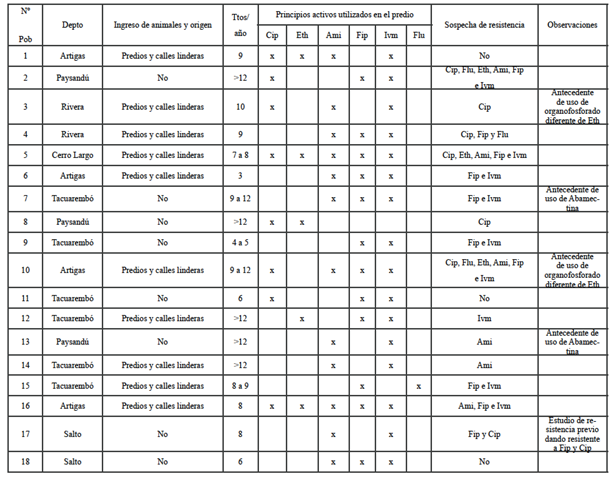
Pob= número de población, Depto=Departamento donde se encuentra el establecimiento,Ttos/Año=tratamiento que se realiza por año en el establecimiento, Cip=Cipermetrína,Flu=Flumetrina, Eth=Ethión,Ami=Amitraz, Fip=Fipronil,Ivm=Ivermectina.
Tabla 3: Resultados de la encuesta de la población 19 a la 36.
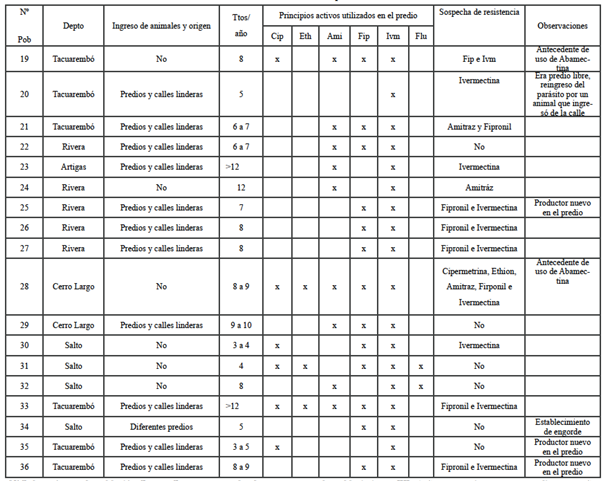
NºPob=número de población, Depto=Departamento donde se encuentra el establecimiento, Ttos/año=tratamientos que se realizan por año en el establecimiento, Cip=Cipermetrina, Flu=Flumetrina, Eth=Ethión, Ami=Amitraz, Fip=Fipronil, Ivm=Ivermectina. Tabla 4. Resultados de la encuesta de la población 37 a la 47.
Tabla 4: Resultados de la encuesta dela población 37 a la 47
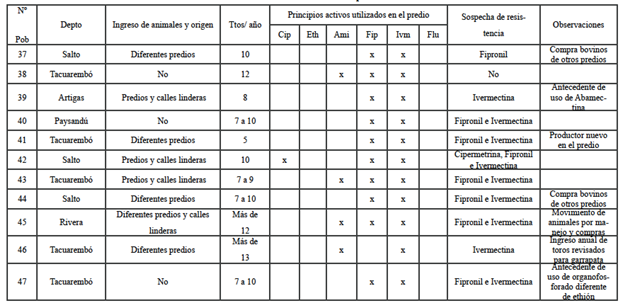
NºPob=número de población, Depto=Departamento donde se encuentra el establecimiento,Ttos/año=tratamientos que se realizan por año en el establecimiento, Cip=Cipermetrína, Flu=Flumetrina, Eth=Ethión, Ami=Amitraz, Fip=Fipronil, Ivm=Ivermectina.
Por medio del TPL se determinaron los perfiles de resistencia de las 47 poblaciones de R. microplus muestreadas observando que presentaron diferentes perfiles de resistencia como se presenta en la tabla 5.
Se destaca de la tabla 6 que los principios activos correspondientes al grupo químico de los piretroides, la cipermetrina y la flumetrina, fueron para los que se observó un mayor número de poblaciones resistentes, así como un mayor número de poblaciones con grado alto y medio de resistencia. La ivermectina por el contrario fue el principio activo para el cual se observó el menor número de poblaciones con resistencia siendo esta baja.
Tabla 6: Resultados agrupados por grupo químico y principio activo de la prueba de resistencia de las 47 poblaciones analizadas.
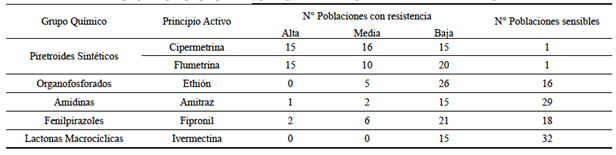
De las 47 poblaciones analizadas por TPL, 17 presentaron resistencia simultánea a tres grupos químicos, 15 resistencia simultánea a cuatro grupos químicos, 11 resistencia a dos grupos químicos y cuatro resistencia a un grupo químico. Ninguna población presentó resistencia simultánea a los cinco grupos químicos.
En la Tabla 7 se puede observar que determinadas poblaciones presentaron resistencia a principios activos cuyo uso no estaba registrado en el establecimiento de origen. Solo dos poblaciones (4,3 % de todas las poblaciones analizadas) tenían antecedentes de uso de todos los principios activos a los que se les detectó resistencia.
Tabla 7: Total de poblaciones resistentes a los diferentes principios activos analizados y discriminadas según si habían hecho uso o no del principio activo para el que fueron diagnosticadas resistentes.
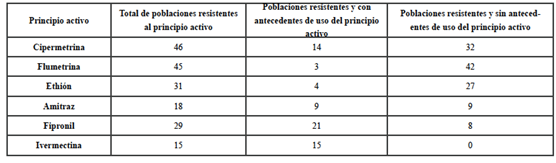
De los 45 establecimientos cuyas poblaciones fueron diagnosticadas resistentes a principios activos que no habían sido utilizados, 29 (64,4 % de las 45) informaron que tenían ingreso de animales con garrapata. Este ingreso se daba a través de alambrados desde predios linderos o desde caminos rurales en 24 predios (82,8 % de los 29 establecimientos que informaron de ingreso de animales), por compra de animales en cinco predios (17,2 % de los 29 establecimientos que informaron de ingreso de animales) y por traslado de ganado entre establecimientos de un mismo productor en dos predios (6,9 % de los 29 establecimientos que informaron de ingreso de animales). Se destaca el predio correspondiente a la población 45 que tiene registrado ingreso de animales por las tres causas. También el predio correspondiente a la población 20 que era un predio libre de garrapatas y debido al ingreso de un animal, desde un camino rural, ingresó R. microplus resistente a piretroides y ethion.
Por otro lado, cuatro de estos 45 establecimientos (8,9 % de los 45 establecimientos cuyas poblaciones fueron diagnosticadas resistentes a principios activos que no habían sido utilizados) correspondían a productores nuevos en el predio, que habían ingresado ganado recientemente al establecimiento y desconocían los antecedentes relacionados a R. microplus.
De las 45 poblaciones que presentaron resistencia a cipermetrina y flumetrina de forma simultánea se destaca que para 29 de estas (64,6 %) no se había hecho uso de piretroides en sus establecimientos de origen. De las 16 que tenían antecedentes de haber hecho uso de piretroides solo uno (6,25 %) había hecho uso de ambos principios activos evaluados, las otras 15 aunque demostraron ser resistentes a ambos principios activos tenían antecedentes de uso de uno solo de los piretroides evaluados (cipermetrina o flumetrina).
En tres de los 17 establecimientos (17,6 %) cuyas poblaciones de R. microplus presentaron resistencia al ethion, sin haber hecho uso de este, habían utilizado otros organofosforados anteriormente.
Se destaca que para todas las poblaciones a las que se les detectó resistencia a ivermectina, se hizo uso de esta en sus predios de origen (de donde fueron muestreadas).
En cuanto a las sospechas de resistencia no todos los establecimientos presentaban sospecha de resistencia. De los establecimientos que presentaron sospecha de resistencia no todas lograron confirmarse mediante TPL como se puede observar en la tabla 8.
Tabla 8: Poblaciones agrupadas según confirmación de sospecha de resistencia por principio activo.
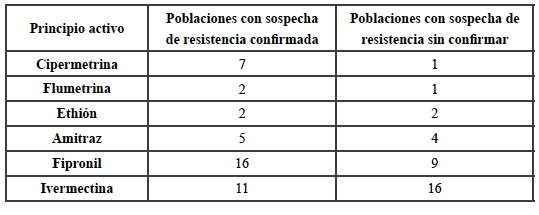
En relación a la información obtenida del número de tratamientos garrapaticidas realizados por año, se observó que ocho establecimientos realizaban de cero a cinco tratamientos por año, 30 predios realizaban de seis a 12 y nueve predios realizaban más de 12.
Discusión
Puede observarse que se presenta una situación compleja en torno a la resistencia evaluada en las 47 poblaciones analizadas, ya que existen grados variables de resistencia para los diferentes grupos químicos. Todas las poblaciones analizadas presentaron algún grado de resistencia al menos a uno de los grupos químicos analizados y hubo varias poblaciones que presentaron multirresistenica. Esto puede deberse a que desde hace más de 50 años que se comenzaron a usar acaricidas, comenzando por los organofosforados a fines de la década del 50. Desde entonces los mismos han evolucionado, se han creado moléculas nuevas las cuales se han ido usando con el correr del tiempo, generando resistencia en las distintas poblaciones según el uso que se les fue dando a las mismas, teniendo en cuenta frecuencia y modo de uso (Cuore, 2016). Por otro lado, es importante tener en cuenta que los establecimientos que se utilizaron para este trabajo fueron de productores que se ofrecieron de forma voluntaria, probablemente porque habían detectado dificultades en el manejo de esta parasitosis, posiblemente debida a sospechas de resistencia a algún acaricida.
La cipermetrina y la flumetrina presentaron una distribución similar en cuanto al número de poblaciones resistentes y el grado de resistencia que estas presentan. Ambos principios activos pertenecen al mismo grupo químico, los piretroides, lo cual puede explicar esta situación como un caso de resistencia cruzada. La resistencia cruzada se da debido a que dos principios activos presentan un mecanismo de resistencia similar, por lo cual la generación de resistencia a uno de ellos lleva a la resistencia del otro (Roush, 1993). Esto también podría explicar los resultados obtenidos en cuanto a antecedentes de uso de cipermetrina y flumetrina y los correspondientes resultados de resistencia. Ya que hubo 15 poblaciones que fueron resistentes a ambos principios activos pero que en sus predios de origen solo se había utilizado uno de ellos. También tanto la cipermetrina como la flumetrina, fueron los principios activos que presentaron más poblaciones con un grado de resistencia alto y una única población susceptible. Todo indicaría que hay una resistencia generalizada a este grupo químico que puede explicarse por la resistencia cruzada pero también porque los mismos fueron utilizados ampliamente para el control de la garrapata R. microplus. Este grupo químico tuvo un gran uso desde su surgimiento, liderando el mercado principalmente debido a razones comerciales, hasta que comenzaron a surgir los primeros problemas e resistencia (Cardozo, 2007), dándose el primer diagnóstico oficial de resistencia a los piretroides en 1994 (Cardozo y Franchi, 1994). También hay que considerar que los piretroides se utilizan para el control de otras parasitosis como la mosca de los cuernos (Haematobia irritans) pudiendo afectar de esta manera la susceptibilidad de las garrapatas a estos químicos (Nari, 2011). También son utilizados para el control de plagas en la agricultura, y este uso podría tener un efecto indirecto en R. microplus (Inglesfield, 1989; del Puerto y col, 2014; Pazos, 2008).
En otro caso que podría tratarse de resistencia cruzada sería en el caso de ethion, ya que si bien se observó resistencia a este principio activo en poblaciones donde no se había hecho uso del mismo en sus predios de origen, en tres casos se habían utilizado otros organofosforados históricamente.
Por otro lado, se observa que hubo varias poblaciones que presentaron resistencia a grupos químicos que nunca han sido utilizados en el establecimiento de donde fueron muestreadas. Hay que tener en cuenta que existen productores que han ingresado ganado a los establecimientos desconociendo los antecedentes en cuanto al uso de acaricidas. Otro factor a considerar son los movimientos de animales, principalmente ingreso de animales desde la calle, predios linderos u otros establecimientos. Muchas veces estos animales ingresan con garrapatas de otro origen que incluso presentan resistencia a acaricidas que no se han utilizado en el establecimiento de destino. Esto lleva a una modificación en el perfil de resistencia de la población actual basado en que la capacidad de resistencia se transmite genéticamente a la descendencia (Alonso-Díaz y col, 2006). Hubo un claro ejemplo de esto que fue un establecimiento de engorde al cual ingresaron animales de distintos establecimientos con garrapata, con distintos perfiles de resistencia a los diferentes grupos químicos. De esta manera se están generando cambios continuamente en la genética de la población de garrapatas que se mantiene en el establecimiento 21 explicando porqué es que puede haber poblaciones que presenten perfiles de resistencia a determinados acaricidas a los que nunca antes habían sido enfrentadas. Un caso extremo fue un establecimiento que era un predio libre de garrapata y debido al ingreso de un animal con R. microplus resistente a piretroides y ethion, desde un camino vecinal, ingresó esta parasitosis al establecimiento e incluso con una agravante, la resistencia.
En cuanto a los resultados obtenidos para ivermectina, se puede observar que se obtuvo un bajo número de poblaciones resistentes a este principio activo siendo la resistencia diagnosticada como baja. Debemos tener en cuenta que la técnica utilizada para estudiar este acaricida no es la más sensible (Castro-Janer et al., 2012), sin embargo, nos permite determinar poblaciones con un grado avanzado de resistencia.
Algunos productores manifestaron sospecha de resistencia, la cual no fue confirmada. Esto puede deberse al mal cálculo de dosis o concentración del acaricida para el tratamiento de los animales (Nari et al., 2003; Smith et al., 1999). También puede explicarse por el desconocimiento de que factores climáticos como la irradiación solar, las lluvias inmediatamente posteriores al tratamiento (Cuore et al., 2008) y las altas temperaturas (que pueden descomponer el producto) (FAO, 1996) podrían estar llevando a una subdosificación de los animales tratados. También el desconocimiento del modo de uso del producto y de su acción, pueden llevar a falsas sospechas de resistencia (Cuore, 2006). A modo de ejemplo, en ocasiones se espera observar un efecto de volteo utilizando productos que no lo tienen. Para aquellos acaricidas de acción sistémica es importante resaltar que su efecto puede variar ampliamente entre animales según su peso, condición corporal y estado fisiológico (Schmid et al., 1994) así como entre formulaciones (Cuore, 2016). Todos estos factores, que pueden generar una sospecha de resistencia cuando no la hay, fortalecen la necesidad de realizar pruebas de resistencia a las garrapatas y así conocer el perfil de resistencia de la población a tratar y poder diseñar un correcto programa de control o erradicación de este parásito.
Un dato importante es el número de tratamientos al año utilizados por los productores; 30 trataban de seis a 12 veces al año y nueve más de 12 veces. La frecuencia de tratamientos es uno de los principales factores para el desarrollo de resistencia (Denholm y Rowland, 1992; Nari y col, 2003). En Uruguay para el control de la garrapata utilizando el tratamiento generacional se recomiendan cinco o seis tratamientos por año (Cuore et al., 2009); por lo tanto, hay un número excesivo de tratamientos en los establecimientos estudiados. Esto puede ser debido a la presencia de resistencia y, consecuentemente, menor eficacia de los acaricidas o al desconocimiento de la correcta forma de uso y actuación de los acaricidas. Para esto es recomendable realizar pruebas de resistencia a las garrapatas para determinar las drogas a ser utilizadas y aplicar el tratamiento generacional (Cuore et al., 2009) de acuerdo a los resultados de las pruebas de resistencia.
Resultados informados por el Departamento de Parasitología de la DILAVE Montevideo y presentados en el 9 de Marzo del 2020 (CONAHSA, 2020) pueden observarse en la tabla 9 junto con los obtenidos por este estudio.
Tabla 9: Porcentaje de resistencia obtenido por la DILAVE y en el presente estudio para los diferentes grupos químicos.
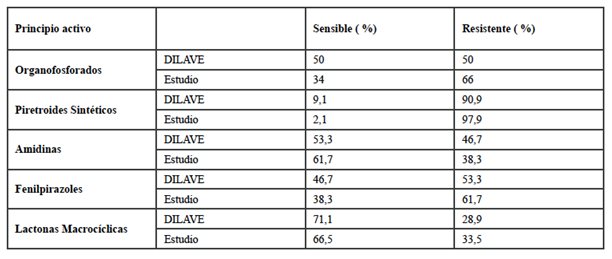
Los resultados observados de la DILAVE en esta son para 242 poblaciones analizadas en período de 2015 a 2019. El análisis de estos resultados por el Departamento de Parasitología de la DILAVE indica que el 16,1 % de las 242 poblaciones analizadas fueron resistentes a un grupo químico (comunicación personal), mientras que en este estudio se observó que estas correspondían al 8,5 % de las poblaciones analizadas. El 24,8 % de las poblaciones analizadas por la DILAVE demostró tener resistencia a dos grupos químicos de forma simultánea (comunicación personal), mientras que para este estudio fueron el 23,4 %. El 26 % de las poblaciones analizadas por la DILAVE tuvieron resistencia a tres grupos químicos de forma simultánea (comunicación personal), mientras que en este estudio fue el 36,2 %, así como el 21,1 % de las poblaciones analizadas por la DILAVE fueron resistentes a cuatro grupos químicos de forma simultánea (comunicación personal), mientras que en este estudio fueron el 31,9 % de las poblaciones. En este estudio no se observaron poblaciones que fueran ni susceptibles ni resistentes a todos grupos químicos analizados de forma simultánea. Sin embargo, de las 242 poblaciones analizadas por la DILAVE Montevideo el 5,4 % fueron totalmente susceptibles, así como el 6,6 % fueron resistentes a los cinco grupos químicos (comunicación personal). Todas estas diferencias observadas pueden deberse a que la cantidad de poblaciones muestreadas son diferentes (242 DILAVE, 47 en este estudio) así como los períodos durante los cuales se obtuvieron las muestras (2015 a 2019 DILAVE, 2017 a 2018 este estudio). A su vez hay que destacar que los muestreos en ambos casos fueron no probabilísticos ya que las muestras se obtienen de forma voluntaria. De cualquier manera, en ambos casos la información muestra que el grupo químico que presentó mayores poblaciones con resistencia fue el de los piretroides y el que presentó menores poblaciones con resistencia fue el de las lactonas macrocíclicas.
En Brasil también se ha diagnosticado resistencia a estos 5 grupos químicos. Puntualmente Lovis et al. (2013) analizan 17 poblaciones muestreadas de cinco estados de Brasil; São Paulo (7), Rio Grande do Sul (4), Mato Grosso do Sul (4), Paraná (1) y Espírito Santo (1). En este trabajo determinan que el 94 % de las poblaciones (16) fueron resistentes a piretroides. Para organofosforados testean dos principios activos diferentes observando un 82 % de las poblaciones (14) resistentes a cumafos y un 65 % (11) resistentes al clorpirifos, observándose cinco poblaciones resistentes a ambos organofosforados simultáneamente. Describe también que el 88 % de las poblaciones (15) fueron resistentes a las amidinas. El 65 % (11) fueron resistentes a fenilpirazoles, donde todas ellas fueron resistentes al fipronil y ocho fueron resistentes al piriprol. Solo el 5,9 % de las poblaciones (1) fue resistente a lactonas macrocíclicas.
En otro trabajo, Klafkle et al. (2017) analizan 104 poblaciones de Brasil encontrando que 98,08 % era resistente a piretroides, el 76,92 % a amidinas, el 60,58 % a organofosforados, 53,85 % a fenilpirazoles y el 60,58 % a lactonas macrocíclicas.
Los datos presentados por Lovis et al. (2013) como los informados en el presente estudio muestran que el menor porcentaje de poblaciones resistentes fue observado para lactonas macrocíclicas, lo cual puede deberse al tipo de test utilizado como se explica anteriormente.
Se destacan los piretroides por ser el grupo químico que presenta en los tres estudios (Klafkle et al., 2017; Lovis et al., 2013 y el presente estudio) el grupo químico con mayor número de poblaciones resistentes. Incluso en el trabajo de Klafkle et al. (2017), como en el presente trabajo, es el grupo químico que presenta mayor número de poblaciones con niveles altos de resistencia (58,65 %). Estos estudios reflejan una clara situación regional compleja en torno a la resistencia y en particular relacionada a los piretroides.
Conclusiones
Se puede concluir que existe una situación compleja de resistencia a los acaricidas, para los establecimientos cuyas poblaciones fueron analizadas. Esta se podría vincular al modo, frecuencia y tiempo de uso de estos acaricidas. Un factor que está influyendo directamente en esto es el ingreso de animales desde orígenes donde esta parasitosis está presente y agravada debido a la resistencia.
Existen diversos factores que pueden llevar a falsas sospechas de resistencia. Por lo tanto, es prioridad hacer un buen uso de los acaricidas conociendo sus características.
Es así que se observa una situación en torno a la resistencia compleja que exige el más correcto de los manejos para ser controlada, haciendo uso de las diferentes herramientas de las que disponemos como por ejemplo las pruebas de resistencia.