Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Archivos de Medicina Interna
versión impresa ISSN 0250-3816versión On-line ISSN 1688-423X
Arch. Med Int vol.37 no. 1 Montevideo mar. 2015
Artículo original
Trasplante autólogo de progenitores hematopoyéticos en pacientes con Linfoma no Hodgkin agresivo. Experiencia de un centro.
Autologous transplant of Haematopoietic Stem Cells in Patients with Aggressive Non Hodgkin Lymphoma. Experience of a center.
Dra. Carolina Oliver
Hematóloga. Unidad de Hematología. Hospital Británico. Montevideo.
Dr. Sebastián Galeano
Hematólogo. Unidad de Hematología. Hospital Británico. Montevideo.
Dra. Silvia Pierri
Hematóloga. Unidad de Hematología. Hospital Británico. Montevideo.
Dra. Ada Caneiro
Hematóloga. Unidad de Hematología. Hospital Británico. Montevideo.
Dra. Laura Bello
Hematóloga. Unidad de Hematología. Hospital Británico. Montevideo.
Dra. Eloísa Riva
Hematóloga. Unidad de Hematología. Hospital Británico. Montevideo.
Dra. Regis Gai
Hematóloga. Unidad de Hematología. Hospital Británico. Montevideo.
Dr. Andrew Miller
Hematólogo.Unidad de Hematología. Hospital Británico. Montevideo
Dr. Pablo Muxi
Jefe de la Unidad de Hematología. Hospital Británico. Montevideo.
Recibido: 16/10/14 - Aceptado: 27/02/15
Trabajo de la Unidad de Hematología del Hospital Británico de Montevideo.
Correspondencia: Correspondencia: Dra. Ana Carolina Oliver Solimano,
Dirección: Libertad 2489/ 203.
E- mail: carolinaoliver@gmail.com
Resumen: Arch Med Interna 37(1): 01-06
Introducción: El Trasplante Autólogo de Progenitores Hematopoyéticos forma parte del tratamiento de pacientes con Linfoma No Hodgkin (LNH) agresivos en respuesta parcial y recaída. Objetivos: evaluar las respuestas y sobrevida en los pacientes con LNH agresivos trasplantados en Hospital Británico. Material y Métodos: estudio retrospectivo de pacientes con LNH agresivos que se trasplantaron entre el 1/01/1995 y el 1/07/2013. Total 65 pacientes. Resultados: el 95% logró una Remisión Completa post Auto-TPH y el 5% una Remisión Parcial. Con una mediana de seguimiento de 74 meses (5-219), la mediana de SG no se ha alcanzado. La media estimada es de 145 meses (122-169) con una SG a 5 años de 71% y a 10 años es de 60%. La mediana de SLE no se ha alcanzado, a 5 años es de 60% y a 10 años es de 58%. Conclusiones: el trasplante Autólogo de Progenitores Hematopoyéticos es una herramienta terapéutica útil. Los resultados de nuestro grupo son comparables a los reportados por grupos internacionales con una baja mortalidad relacionada al procedimiento.
Palabras clave: Trasplante Autólogo de Progenitores Hematopoyéticos, Linfoma No Hodgkin.
ABSTRACT: Arch Med Interna 37(1): 01-06
Introduction: Autologous Hematopoietic Stem Cell Transplantation is part of the treatment of patients with aggressive lymphomas in partial response or relapsed. Objectives: To evaluate the responses and survival in aggressive NHL patients transplanted in Hospital Británico. Material and Methods: Retrospective study of patients with aggressive NHL that were transplanted into... between 01/01/1995 and 07/01/2013. Total 65 patients. Results: 95% achieved a complete remission after Auto-SCT and 5% partial remission. With a median follow up of 74 months (5-219), the median OS has not been reached. The estimated mean is 145 months (122-169) with a 5-year OS of 71% and 60% at 10 years. The median DFS has not been reached, at 5 years is 60 % and at 10 years is 58 %. Conclusions: Autologous Hematopoietic Stem Cell Transplantation is a useful therapeutic tool. The results of our group are comparable to those reported by international groups with low procedure-related mortality.
Keywords: Autologous Stem Cell Trasnplantation, Non Hodgkin Lymphoma.
INTRODUCCIÓN
El Trasplante Autólogo de Progenitores Hematopoyéticos (Auto-TPH) forma parte del tratamiento de pacientes con Linfoma No Hodgkin (LNH) agresivos en respuesta parcial a primera línea de tratamiento y recaída. El LNH Difuso de Grandes Células B (DGCB) es el linfoma agresivo más frecuente. Desde la introducción del anticuerpo monoclonal Rituximab a la Quimioterapia (QT) tipo CHOP, se mejoraron las Respuestas Completas (RC), Sobrevida Global (SG) y Sobrevida Libre de Eventos (SLEv) en este grupo de pacientes tanto en jóvenes como en adultos mayores.(1-2) A pesar de esto, aún hay pacientes que solamente logran una Remisión Parcial (RP) y el 30-40% recaen luego del tratamiento, para los que el Auto-TPH es una herramienta de tratamiento útil(3). Desde la publicación del Parma Study Group en 1995 el Auto-TPH luego de QT de segunda línea se ha convertido en el estándar de tratamiento de los Linfomas agresivos quimiosensibles en recaída.(4)
El objetivo de este estudio es evaluar las respuestas, SG, SLEv y Sobrevida Libre de Enfermedad (SLE) en los pacientes con LNH agresivos trasplantados en Hospital Británico.
MATERIALES Y MÉTODOS
Se realizó un estudio retrospectivo por medio de revisión de historias clínicas de los pacientes con LNH agresivos que se trasplantaron en Hospital Británico. entre el 1 de enero de 1995 y el 1 de julio de 2013. Se incluyeron el total de pacientes que fueron 65. A tres de ellos se les realizó un segundo Auto-TPH posteriormente. El análisis se realizará en base a los 65 pacientes al 1° trasplante.
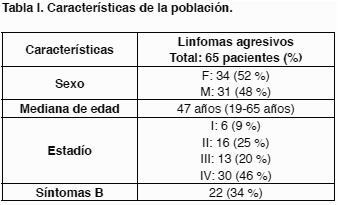
Características de la población
Se definieron como linfomas agresivos a las entidades correspondientes según la época en que debutaron, es por ello que incluimos pacientes que son seleccionados a través de 3 sistemas de clasificación diferente: según la Organización Mundial de la Salud (OMS) LNH DGCB y Folicular G3; según la Working Formulation Linfoma de Alto Grado; y según la clasificación de Lukes y Kiel Linfoma Difuso Centrocítico Centroblástico. En la Tabla I se presentan las características de la población. La mediana de planes de QT utilizada fue de 2 (1-3). El número de planes de QT utilizados fue: 1 en 29 pacientes (45 %), 2 en 28 (43 %) y 3 en 8 (12 %). Veinticuatro pacientes utilizaron estos planes asociados a Rituximab (37 %), 10 (15 %) recibieron radioterapia (RT) pre Auto-TPH y 19 (29 %) post trasplante.
Características de los pacientes al Auto-TPH
Estado de la enfermedad al momento del trasplante: 1° RC 28 pacientes (43 %), 2° RC 9 pacientes (14 %), 1° RP 19 pacientes (29 %), 2° RP 7 pacientes (11 %) y progresión 2 pacientes (3 %). La mediana de tiempo entre el debut y el trasplante fue de 12 meses (3-72 meses).
Stem Cells hematopoyéticas
La fuente de stem cells utilizadas varió dependiendo del año del trasplante. Los pacientes trasplantados en 1995 recibieron Médula ósea (MO), entre 1996 y Julio de 2000 recibieron MO y Stem Cells Periféricas (SCP) en conjunto y desde esa fecha se utilizan SCP solamente. En todos los casos la movilización de SCP se realizó con factores estimulantes de colonias de granulocitos (G-CSF). Se utilizó para la aféresis un procesador Cobe Spectra. Todos los productos fueron criopreservados en nitrógeno líquido a -198°C. Se dispone del recuento de CD 34 de 19 pacientes, la mediana de CD 34 fue de 3,8 x 106/kg (0,72-15,9). Disponemos del recuento de mononucleares de 64 pacientes siendo la mediana de 9,3 x 108/kg (1,18-36,3).
Condicionamiento pretrasplante y procedimiento
Los planes de condicionamiento pre trasplante fueron: en 48 % BEAC (Carmustina, Etopósido, Citarabina, Ciclofosfaminda), en 41 % BEAM (Carmustina, Etopósido, Citarabina, Melfalán), en 5 % BEAM-R (asociado a Rituximab), en 3 % un plan con Cisplatino, Doxorrubicina, Etopósido, Citarabina y en 3 % Cisplatino, Etopósido, Citarabina. En todos los pacientes se realizó aislamiento en habitación con cámara de flujo laminar con aire filtrado con filtros HEPA. Se hizo profilaxis de Pn. jiroveci con trimetroprín-sulfametoxazol y de infección viral por herpes virus con aciclovir. Durante el período de neutropenia se utilizó profilaxis con antifúngicos y antibacterianos. Se realizaron factores de crecimiento granulocitarios según pauta local.
Definiciones del estudio
Las respuestas se definen según criterios publicados por Cheson dependiendo del año del Auto-TPH y de disponibilidad o no de PET.(5,6) La SG se define como el tiempo en meses desde el trasplante a muerte. La SLEv se define como el tiempo en meses desde el trasplante a la recaída, progresión o muerte. La recaída fue evaluada en pacientes en RC al Auto-TPH o que lograron la RC post trasplante. La mortalidad relacionada al trasplante se determinó como la mortalidad que sucede en los primeros 100 días post trasplante.
Métodos estadísticos
Las comparaciones entre grupos se realizaron con el test de Chi-cuadrado, el test exacto de Fisher y el test de Student. Las curvas de sobrevida fueron calculadas de acuerdo al método de Kaplan-Meier y comparadas con el test Log Rank. La significación estadística se define como p < 0,05.
RESULTADOS
Entre el 1 de enero de 1995 y el 1 de julio de 2013 se realizaron 68 trasplantes autólogos en 65 pacientes con LNH agresivos B. La mortalidad relacionada al trasplante fue de 0 %. La recuperación de neutrófilos post trasplante se dio con una mediana de 10 días (5-18), la mediana de días de recuperación plaquetaria fue de 14 (7-38). La mediana de número de volúmenes de glóbulos rojos utilizados fue de 4 (0-16) y de número de transfusiones plaquetarias 3 (0-19). La mediana de días al alta fue de 17 (11-41).

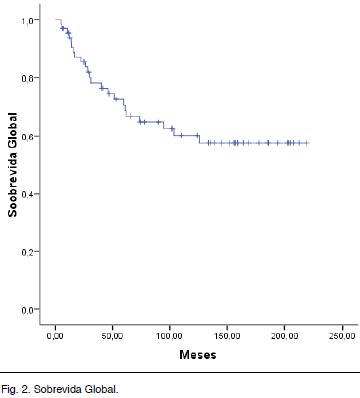
Con una mediana de seguimiento de 74 meses (5-219 meses), la mediana de SG no se ha alcanzado. La media estimada es de 145 meses (122-169 meses) con una SG a 5 años de 71 % y a 10 años es de 60 % (Figura 2).
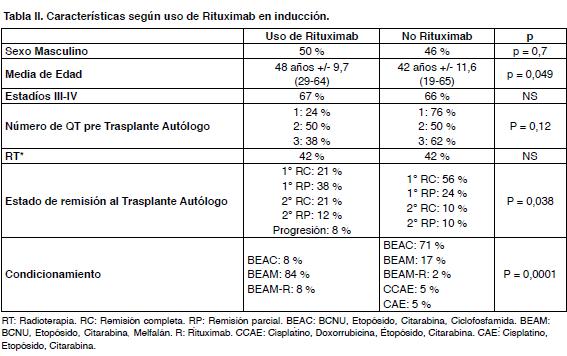
En la Tabla II se muestran los grupos que recibieron o no Rituximab en los planes de inducción y las diferencias entre ellos.
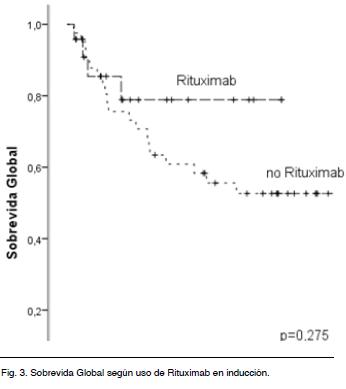
La SG a 5 y 10 años en los pacientes que recibieron Rituximab en los planes de inducción es de 79 % en ambos años y comparando con los que no lo incluyeron es de 68 % y 56 %. No existe diferencia estadísticamente significativa (Log Rank: p = 0,275) (Figura 3).
Del total, 22 pacientes recayeron (34 %). La mediana del tiempo a la recaída post Auto-TPH fue de 22,6 meses (2,16-108).
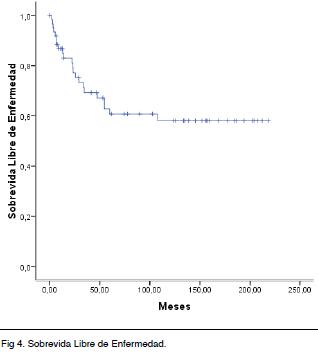
La mediana de SLEv no se ha alcanzado, a 5 años es de 60 % y a 10 años es de 58 % (Figura 4).
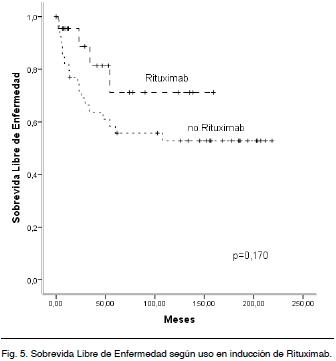
En los que recibieron Rituximab en la inducción la SLEv a 5 años es de 71 % y en los que no 55 % sin diferencia estadísticamente significativa (Log Rank p = 0,170) (Figura 5).
Los 3 pacientes que permanecieron en RP post Auto-TPH progresaron. Dos fallecieron a causa de progresión en 6 y 11 meses, el 3° paciente fue perdido de seguimiento. La mediana de SLEv no se ha alcanzado, a 5 años es de 57 % y a 10 años de 49 %.
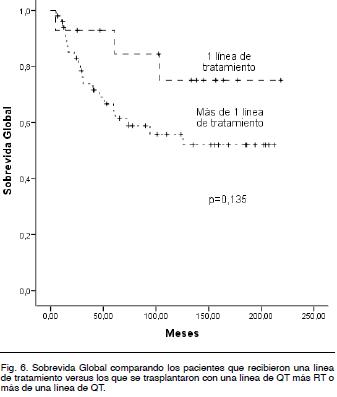
Los pacientes que se trasplantaron en 1° RC con una sola línea de quimioterapia previa y sin recibir RT ni previo ni posteriormente al Auto-TPH tuvieron una SG a 5 años de 93 %, a 8 años de 84 % y a 10 años de 75 %. Los que se trasplantaron con una línea de QT más RT o más de una línea de QT tuvieron una SG a 5 años de 64 % y a 10 años de 56 % (Log Rank p = 0,135) (Figura 6). La SLEv a 5 años en los que se trasplantaron con una línea de QT más RT o más de una línea de QT es de 55%.
De los 65 pacientes 37 están vivos, 23 muertos y 5 perdidos de seguimiento. Las causas de muerte fueron: en 16 recaída o progresión de la enfermedad, en 6 segundas neoplasias y en uno una miocardiopatía dilatada. Las segundas neoplasias fueron: 3 Síndromes Mielodisplásicos, 1 Neoplasia Digestiva, 1 Leucemia Prolinfocítica T y 1 Leucemia Aguda Mieloblástica M5 de la clasificación FAB.
DISCUSIÓN y comentarios
En este trabajo presentamos los datos de los pacientes con LNH agresivos que se trasplantaron en el Hospital Británico. entre 1995 y 2013. El objetivo principal es analizar los resultados de respuesta y sobrevida a largo plazo con el uso de altas dosis de QT y Auto-TPH en esta población.
Si bien ha habido mejoras en los últimos años en el tratamiento de los LNH DGCB con el agregado de Rituximab, existe un grupo de pacientes que recaerán. En menores de 60 años con aaIPI de 0 se estima que la recaída luego de 1ª línea es de 10 %(7), con aaIPI 1 de 20-30 %(8) y con 2-3 de 25-35 %.(9) En pacientes entre 60 y 70 años las tasas de recaída post R-CHOP son del 40 %, por lo que aún hoy existe un gran número de pacientes con LNH DGCB que requerirán tratamiento de 2ª línea y Auto-TPH de consolidación. El trabajo PARMA es la base para el planteo de Auto-TPH en estos pacientes. Este estudio comparó Auto-TPH más radioterapia (RT) de campo involucrado con QT de salvataje en pacientes con LNH < 60 años quimiosensibles. Con una mediana de seguimiento de 63 meses, la SLEv a 5 años en el grupo de trasplante fue de 46 % comparado con 12 % con QT solamente (p = 0,001), y la SG a 5 años fue 53 % comparada con 32 % entre grupo trasplante QT (p = 0,038)(4). Existe un número amplio de planes de 2ª línea que pueden utilizarse previo a Auto-TPH, los resultados más importantes son los expuestos en el trabajo CORAL donde se comparó R-ICE (Rituximab, Ifosfamida, Etopósido, Carboplatino) versus R-DHAP (Rituximab, Dexametasona, Citarabina, Cisplatino) seguido de Auto-TPH. La RG fue de 63 % con 38 % de RC sin diferencias en ambos grupos previo al Auto-TPH, llegando a 73 % de RC y 13 % de RP post trasplante. De este estudio surgieron que los factores que provocan una peor respuesta son: enfermedad refractaria o recaída < 12 meses, aaIPI > 1 y exposición a Rituximab previa en los recaídos en < 12 meses post 1ª línea.(10-11)
En nuestro trabajo se mejoraron las tasas de RG y RC post Auto-TPH al igual que en el trabajo Parma y CORAL. El Auto-TPH en esta población logró un cambio en las tasas de RC post trasplante, de 57 a 95 % con una diferencia estadísticamente significativa.
Es un hecho a destacar que en la literatura internacional los resultados son diferentes según se trate de consolidación post 1ª línea de tratamiento, recaída, respuesta parcial post 1ª línea o refractario.(4,12-14) La SG a 3 años en los que logran una RC post 2ª línea de tratamiento es de 55 %, en recaída quimiosensible 40 % y en quimioresistencia 28 % según el trabajo de Vose J et al.(14) Según estos y otros trabajos, el Auto-TPH queda reservado para los pacientes con recaídas quimiosensibles(4,10,11,13). Desde hace unos años se está explorando la posibilidad de mejorar las respuestas con la 1° línea de tratamiento. Una estrategia que se ha probado es el uso de Auto-TPH como consolidación post 1ª línea de tratamiento, los resultados son variables pero se ve una tendencia a mejor SG en los pacientes con IPI de mal pronóstico. Los resultados del grupo SWOG en IPI de alto riesgo muestran una SG a 2 años de 82 % con Auto-TPH versus 64 % con QT sola y los del grupo Francés una SG a 8 años de 64 % versus 49 % respectivamente(15-16). El meta-análisis publicado por Greb en 2007 de los estudios randomizados con Auto-TPH en 1ª línea no demostró beneficios concluyentes en términos de SLEv y SG, por lo que el Auto-TPH como consolidación en 1° línea se considera actualmente en el contexto de ensayos clínicos.(17) En Uruguay hasta hace unos años se realizaba consolidación post 1° línea de tratamiento a pacientes jóvenes, estrategia que ha cambiado con los resultados de estos estudios y actualmente se reserva para pacientes en remisión parcial o recaída quimiosensible.
La SG en el total de la población trasplantada en el Hospital Británico. a 5 años es de 71 % y la SLEv es de 57 %, resultados superiores a los publicados por el grupo PARMA (53 % y 46 % respectivamente).(4) Pero si nos centramos en la población de pacientes comparable a la de dicho estudio, o sea, aquellos refractarios o recaídos, tenemos 51 pacientes con una SG a 5 años de 64 % y una SLEv de 55 %. En esta población, los pacientes que se trasplantaron con una línea de tratamiento tuvieron una tendencia a mejores resultados: SG a 8 años de 84 % versus los reportados por el grupo SWOG o francés (64 %), planteamos que esta diferencia se debe principalmente a que esta población incluye pacientes de todos los grupos de riesgo IPI y en la de los trabajos internacionales solamente se incluyen pacientes de alto riesgo, por lo que incluyen una población de peor pronóstico.
Si bien el estándar de tratamiento en pacientes en recaída quimiosensible es el Auto-TPH, los trabajos que lo proponen son previos a la introducción del Rituximab. Se han realizado algunos trabajos que evalúan el rol del Auto-TPH en pacientes con uso previo de Rituximab como el estudio publicado por Smith en 2011 y el de Mounier en 2012. El primero muestra una mediana de SG de 67 meses para los que utilizaron Rituximab versus 44 meses para los que no (p = 0,3). El segundo muestra que la SLE post trasplante es mayor que la alcanzada previo al trasplante aún en los pacientes que habían recibido Rituximab (10 meses versus no alcanzada, p = 0,001).(12,18) Estos resultados sugieren que el Auto-TPH puede ser igualmente efectivo en pacientes que han recibido Rituximab en inducción como los que no, por lo que aún en la era de los anticuerpos monoclonales se lo sigue considerando estándar de tratamiento.(12,18)
En nuestra población los grupos de pacientes que usaron Rituximab en alguna de las QT de inducción y los que no, no son comparables ya que el grupo que recibió Rituximab es de mayor edad, y ambos difieren en la situación pre trasplante y los condicionamientos. Los condicionamientos diferentes están en relación al período en que se trasplantaron, desde el año 2001 se realiza principalmente BEAM(BCNU, Etopósido, Citarabina, Melfalán). Si bien son grupos no comparables por lo antes mencionado, se ve una tendencia a mejores resultados en los que utilizaron Rituximab en términos de SG y SLE.
CONCLUSIONES
El trasplante Autólogo de Progenitores Hematopoyéticos es una técnica que se realiza en Uruguay desde 1985. Es una herramienta terapéutica útil en el tratamiento de los linfomas agresivos recaídos y continúa siendo estándar de tratamiento aún en la era de los anticuerpos monoclonales para este subgrupo de pacientes. Los resultados de nuestro grupo son comparables a los reportados por grupos internacionales con una baja mortalidad relacionada al procedimiento.
BIBLIOGRAFÍA
1. Pfreundschuh M, Ho A, Cavallin-Stahl E, Wolf M, Pettengell R, Vasova I, et al. Prognostic significance of maximum tumour (bulk) diameter in young patients with good-prognosis diffuse large-B-cell lymphoma treated with CHOP-like chemotherapy with or without rituximab: an exploratory analysis of the MabThera International Trial Group [en línea]. Lancet Oncol. 2008;9(5):435-44. [acceso 20/12/2013]. Disponible en: http://www.thelancet.com/pdfs/journals/lanonc/PIIS1470-2045(08)70078-0.pdf .
2. Coiffier B, Lepage E, Briere J, Herbretch R, Tilly H, Bouabdallah R, et al. Chop Plus Rituximab Vs. CHOP alone in elderly patients with Diffuse LArge B-Celll Lymphoma. N Engl J Med. 2002;346:235 242.
3. Gisselbrecht C. Is there any role for transplantation in the rituximab era for diffuse large B-cell lymphoma? [en línea] Hematology Am. Soc. Hematol. Educ. Program. 2012;2012:410-6. [acceso 20/12/2013] Disponible en: http://asheducationbook.hematologylibrary.org/content/2012/1/410.full.pdf+html .
4. Philip T, Guglielmi C, Hagenbeek A, Somers R, Van Der Lelie H, Bron D, et al. Autologous Bone Marrow Transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive Non-Hodgkin’s Lymphoma. N Engl J Med. 1995;333:1540-1545.
5. Cheson BD, Pfistner B, Juweid ME, Gascoyne R, Specht L, Horning S, et al. Revised response criteria for malignant lymphoma [en línea]. J. Clin. Oncol. 2007;25(5):579-86. [acceso 21/12/2013]. Disponible en: http://jco.ascopubs.org/content/25/5/579.full.pdf+html .
6. Cheson BBD, Horning SJ, Coiffier B, Shipp M, Fisher R, Connors J, et al. Report of an International Workshop to Standardize Response Criteria for Non-Hodgkin ’ s Lymphomas.NCI Sponsored International Working Group. J Clin Oncol. 1999 Apr;17(4):1244.
7. Pfreundschuh M, Kuhnt E, Trümper L, Osterborg A, Trneny M, Shepherd L, et al. CHOP-like chemotherapy with or without rituximab in young patients with good-prognosis diffuse large-B-cell lymphoma: 6-year results of an open-label randomised study of the MabThera International Trial (MInT) Group [en línea]. Lancet Oncol. 2011;12(11):1013-22. [acceso 14/07/ 2014]. Disponible en: http://www.thelancet.com/pdfs/journals/lanonc/PIIS1470-2045(11)70235-2.pdf .
8. Récher C, Coiffier B, Haioun C, Molina T. ACVBP plus rituximab versus standard CHOP plus rituximab for the treatment of diffuse large B-cell lymphoma (LNH03-2B): an open-label randomised phase 3 trial [en línea]. Lancet. 2011; 378(9806):1858–67. [acceso 14/07/ 2014].Disponible en: http://www.thelancet.com/pdfs/journals/lancet/PIIS0140-6736(11)61040-4.pdf .
9. Tarella C, Zanni M, Di Nicola M, Patti C, Calvi R, Pescarollo A, et al. Prolonged survival in poor-risk diffuse large B-cell lymphoma following front-line treatment with rituximab-supplemented, early-intensified chemotherapy with multiple autologous hematopoietic stem cell support: a multicenter study by GITIL (Gruppo Italiano Terapie Innovative nei Linfomi) [en línea]. Leukemia. 2007;21(8):1802–11. [acceso 14/07/ 2014]. Disponible en: http://www.nature.com/leu/journal/v21/n8/pdf/2404781a.pdf .
10. Hagberg H, Gisselbrecht C. Randomised phase III study of R-ICE versus R-DHAP in relapsed patients with CD20 diffuse large B-cell lymphoma (DLBCL) followed by high-dose therapy and a second randomisation to maintenance treatment with rituximab or not: an update of the CORAL study [en línea] Ann Oncol. 2006;17 Suppl 4:iv31-2. [acceso 13/01/2014] http://annonc.oxfordjournals.org/content/17/suppl_4/iv31.long .
11. Gisselbrecht C, Glass B, Mounier N, Singh Gill D, Linch D, Trneny M, et al. Salvage regimens with autologous transplantation for relapsed large B-cell lymphoma in the rituximab era [en línea]. J. Clin. Oncol. 2010;28(27):4184-90. [acceso 11/01/2014]. Disponible en: http://jco.ascopubs.org/content/28/27/4184.full.pdf+html .
12. Mounier N, Canals C, Gisselbrecht C, Cornelissen J, Foa R, Conde E, et al. High-dose therapy and autologous stem cell transplantation in first relapse for diffuse large B cell lymphoma in the rituximab era: an analysis based on data from the European Blood and Marrow Transplantation Registry[en línea]. Biol. Blood Marrow Transplant. 2012;18(5):788-93. [acceso 26/12/2013]. Disponible en: http://www.bbmt.org/article/S1083-8791(11)00413-7/pdf .
13. Vose BJM, Zhang M, Rowlings PA, Lazarus H, Bolwell B, Freytes C, et al. Autologous Transplantation for Diffuse Aggressive Non-Hodgkin's Lymphoma in Patients Never Achieving Remission : A Report from the Autologous Blood and Marrow Transplant Registry. 2001;2(January 15):406-413.
14. Vose JM, Rizzo DJ, Tao-Wu J, Armitage J, Bashey A, Burns L, et al. Autologous transplantation for diffuse aggressive non-Hodgkin lymphoma in first relapse or second remission [en línea]. Biol. Blood Marrow Transplant. 2004;10(2):116-27. [acceso: 18/12/2013]. Disponible en: http://www.bbmt.org/article/S1083-8791%2803%2900370-7/pdf.
15. Stiff P, Unger J, Cook J, Constine L, Couban S, Shea T, et al. Randomized phase III U.S./Canadian intergroup trial (SWOG S9704) comparing CHOP ± R for eight cycles to CHOP ± R for six cycles followed by autotransplant for patients with high-intermediate (H-Int) or high IPI grade diffuse aggressive non-Hodgkin lymphom. J. Clin. Oncol. 2011;29(15-suppl):8001.
16. Haioun C, Lepage E, Gisselbrecht C, Salles G, Coiffier B, Brice P, et al. Survival Benefit of High-Dose Therapy in Poor-Risk Aggressive Non-Hodgkin’s Lymphoma: Final Analysis of the. J Clin Oncol. 2000;18(16):3025-3030.
17. Greb A, Bohlius J, Trelle S, Schiefe D, De Souza C, Gisselbrecht C, et al. High-dose chemotherapy with autologous stem cell support in first-line treatment of aggressive non-Hodgkin lymphoma - results of a comprehensive meta-analysis [en línea]. Cancer Treat. Rev. 2007;33(4):338-46 [acceso 14/07/2014]. Disponible en: http://www.cancertreatmentreviews.com/article/S0305-7372(07)00030-8/ppt .
18. Smith SD, Bolwell BJ, Rybicki L, Kang T, Dean R, Advani A, et al. Comparison of outcomes after auto-SCT for patients with relapsed diffuse large B-cell lymphoma according to previous therapy with rituximab [en línea]. Bone Marrow Transplant. 2011;46(2):262-6. [acceso 20/12/2013] Disponible en: http://www.nature.com/bmt/journal/v46/n2/pdf/bmt201095a.pdf .