Services on Demand
Journal
Article
Related links
Share
Archivos de Medicina Interna
Print version ISSN 0250-3816On-line version ISSN 1688-423X
Arch. Med Int vol.33 no.3 Montevideo Dec. 2011
Actualización
Las encefalitis herpéticas. Encefalitis producidas por la familia herpes.
Herpetic Encephalitis. Encephalitis produced by the Herpes family.
Dr. Ronald Salamano
Dra. Sara Lewin
SUMEN: Arch Med Interna 2011 - XXXIII(3):49-58
La familia herpesviridae presenta seis virus neurotropos (herpes virus simple tipo 1 y 2, el varicela-zóster, citomegalovirus, herpes virus humano tipo 6 y el Epstein-Barr) que son conocidos por su capacidad de producir encefalitis en niños y adultos. La encefalitis producida por el herpes virus simple tipo 1 es la mejor conocida, el resto guarda una serie de incógnitas relativas a sus manifestaciones clínicas, diagnósticas y terapéuticas no bien dilucidadas hasta el momento. La aplicación de técnicas de biología molecular aplicadas al LCR han permitido una expansión del conocimiento en la materia. La actual revisión pretende una puesta al día en la materia desde la literatura consultada y el pequeño aporte de nuestra experiencia, resaltando las similitudes y diferencias entre estas encefalitis.
Palabras clave: Encefalitis, familia herpes, Reacción en Cadena de Polimerasa (PCR)
Summary: Arch Med Interna 2011 - XXXIII(3):49-58
The herpes viridae family includes six neurotropic viruses (Types 1 and 2 Herpes simplex, Varicella-zoster, Cytomegalovirus, Type 6 Human Herpes virus and Epstein-Barr virus) well known for their ability to cause encephalitis in children and adults. The encephalitis produced by Type 1 Herpes simplex is the best known; the rest offer a number of relatively unknown factors in terms of their clinical, diagnostic and therapeutic manifestations that have not been clarified yet. Molecular biology techniques applied to the CSF have expanded our knowledge in that regard. The paper gives an updated overview of the matter, based on a literature review and a modest contribution presenting our experience, and highlighting the differences and similarities between these encephalitis.
Keywords: Encephalitis, herpes family, Polymerase Chain Reaction (PCR).
INTRODUCCIÓN
Los virus de la familia herpesviridae, en particular el herpes simple tipo 1 y 2 (HSV 1 y HSV 2), citomegalovirus (CMV), Epstein-Barr (EB), varicela-zóster (VZ), y el herpes virus humano tipo 6 (HHV 6) son responsables de numerosas infecciones del Sistema Nervioso Central (SNC) tanto en niños como adultos (1).
Una de sus principales características es la de provocar encefalitis. Dichas encefalitis son bien conocidas en el caso del HVS 1 desde largo tiempo atrás, en el caso del CMV se han observado sobretodo en relación a cuadros de inmunodepresión (VIH, transplantados de órganos sólidos, medicaciones inmunosupresoras, etc.).
El VZ es también conocido desde tiempo atrás por su impacto en el parénquima encefálico en el paciente inmunocompetente añoso o en niños y jóvenes, y recientemente se han abierto nuevas fronteras en el conocimiento de la relación existente entre este virus y el SNC; son menos conocidos y delineados, los cuadros encefalíticos consecutivos al HHV 6 y especialmente al EB (1).
Cualquiera de ellos puede producir daño por replicación viral en el tejido encefálico o puede provocar una respuesta inmunomediada que determina una Encefalomielitis Aguda Diseminada (EMAD) que se solapa a la infección viral o se da en diferido (2).
Esta actualización se centrará en lo que ocurre en pacientes adultos, excluyendo los fenómenos de EMAD.
Los virus de la familia herpes tienen una serie de características comunes que permitirán luego interpretar la patología que ocasionan, son DNA virus, luego de la primoinfección establecen latencia en el tejido cerebral (HHV 6) o en ganglios de pares craneanos (especialmente el V par para el HSV 1) y ganglios raquideos (HVS 2, VZ), reactivándose en situaciones puntuales o generales de inmunosupresión.
La palabra herpes deriva del griego, las lesiones cutáneas que provocan el HSV 1 y 2 se adjudican en su descripción a Herodotus (3,4).
Las técnicas de biología molecular aplicadas en general al LCR, técnicas de Reacción de Cadena de Polimerasa (PCR –Polymerase Chain Reaction en inglés–) han permitido dar un salto cualitativo en el diagnóstico de estas afecciones.
Las técnicas de cultivo viral han sido relegadas a centros específicos con fines de investigación y la detección de Ac y Ag en LCR suelen ser tardías para tomar decisiones terapéuticas, aunque permiten un diagnóstico en retrospectiva de la afección (5).
Asimismo las técnicas de PCR permiten que además de un diagnóstico positivo podamos en algunas encefalitis (HSV 1) monitorear la eficacia del tratamiento.
Las técnicas de PCR pueden dar falsos positivos, sobretodo cuando existe contaminación laboratorial ambiental, así como falsos negativos, como sucede en caso de sangre contaminante en las muestras, (derivados pirrolicos del núcleo hem de los eritrocitos) que inhiben la TAQ polimerasa, las proteinas aumentadas en el LCR no inhiben de por sí la reacción en esta técnica. Otros falsos positivos derivan de la replicación de fragmentos genómicos o infecciones latentes que no gravitan en el cuadro clínico del paciente (HHV 6) (5).
Sin embargo, en aproximadamente 50-70% de los casos de encefalitis virales no se puede identificar el virus a pesar de la incorporación de la técnica de PCR (6).
La utilización de la biopsia cerebral no ha desaparecido del espectro de las herramientas diagnósticas, sigue teniendo un papel relevante en aquellos casos PCR negativos en LCR donde la evolución clínica no es satisfactoria y existe convicción clínica y paraclínica de estar delante de una encefalitis o de otra afección tratable. En caso de ser necesaria y de ser posible, se prefiere la biopsia a cielo abierto a la esterotáxica, en ese caso la biopsia debe ser analizada por un experimentado neuropatologo utilizando técnicas de histopatología con inmunomarcación e inmunofluorescencia, PCR aplicado al material biópsico, microscopía electrónica y cultivo de la pieza en cuestión (7).
Hoy las técnicas de RM (especialmente cuando se aplica espectroscopia), SPECT o PET nos aproximan a discernir entre fenómeno inflamatorio-infeccioso o tumor y nos ofrecen diferentes patrones según las secuencias utilizadas que orientan la etiología del proceso (compromiso temporal en HSV 1, compromiso ependimario en CMV, compromiso encefalo-vasculítico en el VZ) (8).
ENCEFALITIS HERPÉTICA (EH) POR HSV-1 Y 2 EN EL ADULTO
Introducción histórica
Ya en el año 1922 Levaditi sospecha la implicancia del HSV viral en algunas encefalitis necrotizantes aguda. Smith y cols. en 1941 aislan el virus de la sustancia cerebral y Zarafonetis y cols. en 1944 junto a Whitman y cols. en 1946 confirman la observación de Smith, este mismo autor demuestra en 1977 la eficacia relativa del Adenosín-Arabinósido (Vidarabina) en el tratamiento de la EH (9).
Sköldenberg y cols. en 1984 (10) informan acerca de la superioridad del aciclovir en relación a la vidarabina en el tratamiento de la EH. Whitley en 1986 confirma esta observación (11).
Epidemiología
La EH es la causa más común de encefalitis viral aguda no epidémica. En niños mayores a seis meses y adultos, su incidencia se estima en 1 caso/250.000 h/año, ocurre sin predilección estacional y afecta a ambos sexos por igual.
Existe una distribución etárea bimodal, con un tercio de casos que ocurren en menores de menos 20 años y los 2/3 restantes en mayores de 50. El pico de mayor incidencia se ubica entre los 60-65 años (40% de los casos).
En ausencia de terapéutica, se estima que fallecen 70% de los afectados, quienes sobreviven quedan con secuelas que impiden un reintegro normal a la vida diaria. Apenas 3% de estos pacientes pueden volver a tener una vida normal. Por ello es imperativo que ante la sospecha clínica se comienze el tratamiento antiviral.
Mutaciones que involucran los genes que codifican receptores toll-like 3 y el factor 3 asociado al receptor de necrosis tumoral han sido asociados con casos familiares y de niños de EH. Tambien lo han sido medicaciones inmunomoduladoras tales como el inhibidor de factor de necrosis tumoral alfa y pacientes sometidos a fingolimod en la Esclerosis Múltiple (12).
La existencia de la EH por HSV 1 es típica del paciente no inmunocomprometido, mientras que la que es producida por el HSV 2 es característica del neonato y mas raramente del adulto inmunocomprometido (12).
Anatomía patológica
Se trata de una encefalitis necrotizante y hemorrágica que afecta a todas las células del parénquima: neuronas, astrocitos, oligodendrocitos. Las piezas de necropsia muestran necrosis, hemorragia, edema, cambios de coloración, etc., tanto en la sustancia blanca como en la gris, especialmente en el lóbulo temporal y cara orbitaria del lóbulo frontal, la microscopía óptica detecta infiltrados linfocitarios perivasculares con infiltración microglial y muchos macrófagos en las áreas comprometidas.
En las zonas de necrosis se encuentran hematíes y polimorfonucleares extravasados, es posible reconocer en la mitad de los casos cuerpos de Cowdry tipo A (inclusiones eosinófilas intranucleares en neuronas y células gliales). La microscopía electrónica nos permite reconocer los viriones a nivel intracelular (3,7).
Fisiopatología
La seroprevalencia para HSV 1 es de 80-90% en los adultos, independientemente de la región geográfica estudiada, mientras que el HSV 2 se ubica en 20% (12). Las reactivaciones pueden ser sintomáticas (recurrencia), disparadas por traumas mínimos, luz solar, inmunosupresión, irradiación por rayos X, etc., o asintomáticas, contribuyendo de manera sostenida a la trasmisión inadvertida de ambos virus. En la cavidad oral la reactivación asintomática del HSV 1 excede la recurrencia clínica y la siembra del HSV 2 puede ocurrir en más de los 2/3 de los individuos seropositivos.
Sólo 25% de pacientes con EH tienen úlceras bucales y vesiculas en labios, narinas, previo a su enfermedad, dicha incidencia es similar a la existente en la población normal. Tal como se mencionó la enfermedad tiene una distribución etárea bimodal, es posible que esta distribución refleje que la EH por debajo de 20 años sea consecuencia de primoinfección y que por encima de 50 años sea consecuencia de la reactivación viral (13).
En pacientes inmunocompetentes 90% de los casos son consecuencia del HSV 1, mientras que el 10% restante corresponden a HSV 2.
El HSV 1 y 2 son ADN virus de doble hélice. No es posible distinguir uno de otro mediante la microscopía electrónica, tienen una homología de 70% en su genoma y son antigenicamente distinguibles (14).
La infección primaria se produce en la mucosa oronasofaríngea, allí pueden desarrollarse vesículas-úlceras o ser la infección asintomática, lo cierto es que por vía retrograda axonal el virus alcanza directamente el parénquima encefálico por vía del nervio olfatorio produciendo la EH directamente tras la primoinfección o puede, de la misma manera, pero a través del V par, alcanzar el nervio trigémino y establecer latencia en dicho ganglio. Allí puede ser encontrado en todos aquellos que han hecho la seroconversión para este virus. Su reactivación produce nuevamente migración en un sentido distal provocando la sintomatología descrita en labios, narinas, mucosa bucal, etc.
En tal sentido existen experiencias neuroquirúrgicas que documentan la frecuente aparición de vesículas herpéticas en la boca o labios luego de intervenciones sobre el ganglio trigeminal (3,5).
El camino por el cual el virus produce EH no es muy claro, muchos sostienen la hipótesis de destino final errado a través de la migración hacia las ramas trigeminales en contacto con las meninges que cubren el lóbulo temporal y frontal en caso de reactivación. Dicha reactivación es producto de hechos puntuales (tales como exposición solar, traumatismos, etc., como se mencionó) que sospechamos permiten un escape inmunitario y la migración del virus al parénquima encefálico.
El ADN del HSV 1 puede ser amplificado usando PCR en diferentes topografías encefálicas en pacientes asintomáticos positivos (tronco cerebral, bulbo olfatorio, áreas límbicas, no así en el cerebelo y en otras regiones del cerebro). Permanece en la incertidumbre saber si este genoma refleja la presencia de un HSV 1 que tenga capacidad para reactivarse y provocar encefalitis (3,5).
El HSV 2 produce sobretodo herpes genital, con el virus que establece latencia en los ganglios raquídeos sacros, mediante sexo oral, la cepa puede producir infección bucal y puede reactivarse provocando herpes facial (12).
Manifestaciones clínicas
Las manifestaciones clínicas van a estar determinadas por un cuadro febril (alta temperatura en general) precedido o no de un cuadro pseudogripal, que afecta al paciente en su conciencia, provocando un cuadro confusional o deterioro en el nivel de vigilia que puede oscilar entre la obnubilación y el coma. Aparecen elementos focales neurológicos deficitarios, dependiendo estos del lóbulo y hemisferio afectado (afasia, hemiparesia, heminegligencia, etc.) y frecuentemente crisis epilépticas parciales o parciales secundariamente generalizadas acompañado de elementos de hipertensión endocraneana (cefaleas, vómitos, edema de papila). El cuadro suele ser agudo, con un acmé en el desarrollo de los síntomas y signos de pocos días, son infrecuentes los cuadros recidivantes y a los que se puede adjudicar cronicidad (3,15). Ochenta por ciento de los casos responde a este perfil evolutivo, que no puede ser distinguido de otras encefalitis agudas (NIAID Collaborative Antiviral Study Group –estudio CASG–) (12). Sin embargo, las técnicas de PCR aplicadas al LCR nos muestran que existen formas evolutivas benignas, o encefalitis de tronco, cuya responsabilidad depende del HSV 1 (16-25% de los casos) .
Las manifestaciones del HSV 2 pueden tener el mismo carácter que el HSV 1, aunque tienen una tendencia a ser formas clínicas más leves y atípicas. De preferencia se ven en pacientes inmunocomprometidos, aunque aun en esta circunstancia suelen ser raras. La epidemiología de las EH por HSV 1 en los pacientes inmunocompetentes es similar a la que ocurre en los inmunocomprometidos, aunque en estos es esperable que, cuando ocurran, sean formas también menos definidas (12).
En estas circunstancias clínicas el diagnóstico diferencial antes de realizar imagen son las colecciones supuradas intracraneanas (abscesos, empiemas), tromboflebitis infecciosa, endocarditis bacteriana con émbolo séptico cerebral, etc. (7).
La TAC y RM podrán distinguir entre estos procesos, sin embargo, en etapa temprana a veces existen dificultades con ambas técnicas para discernir entre cerebritis presupurativa o encefalitis vírica.
Exámenes complementarios
La TAC puede ser normal en los primeros días o dar una imagen sugestiva de cerebritis, isquemia cerebral, incluso con aumento de densidad en la cerebral media por la congestión local existente, también nos permitirá ver si existe hemorragia asociada.
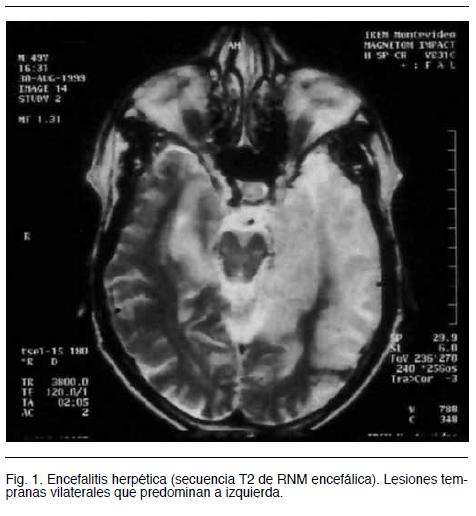
La RM en secuencia FLAIR muestra anomalías temporales en 90% de los adultos con EH a las 48 hs. del inicio de los síntomas, también son útiles la secuencia de difusión y la utilización de gadolinio, en general la lesión es bilateral predominando en alguno de los hemisferios. Muy raramente la RM es normal (menos de 10% tienen imagen normal con PCR +). En su plenitud las imágenes de RM muestran las lesiones en la parte medial del lóbulo temporal o en toda su extensión, cara orbito-frontal del lóbulo frontal y suelen ser bilaterales y asimétricas, raramente se pueden ver alteraciones en ganglios basales, tronco cerebral y cerebelo ( figura 1 y 2)
Estas imágenes en contexto clínico son altamente sugestivas del diagnóstico y cobra valor la bilateralidad, pero con predominio en un hemisferio. Otras enfermedades pueden tener una imagen similar, aunque algunas de ellas suelen respetar cierta simetría: encefalitis por HHV 6, encefalopatía mitocondrial (MELAS), encefalitis límbica paraneoplásica, síndrome de Ac anticanales de potasio, neurosífilis, etc. (5,16).
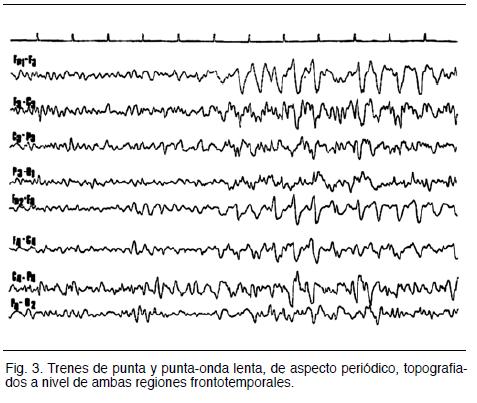
La electroencefalografía es una herramienta diagnóstica importante; no existen de hecho EEG normales. La EEG muestra elementos de enlentecimiento que suelen ser focales, luego aparecen complejos trifásicos característicos con dominancia temporal (figura3). Algunos pacientes desarrollan descargas epileptiformes periódicas lateralizadas (PLEDs) a un ritmo de 1-5 Hz, que se originan en el lóbulo temporal, que son altamente sugerentes de EH, aunque no patognomónicos. Su ausencia no invalida el diagnóstico; pueden estar ausentes al inicio, y la resolución de estas anomalías no se correlaciona bien con la clínica (8,17).
El estudio del LCR mediante citoquímico del LCR muestra una pleocitosis linfomonocitaria de 10 a 500 células, aunque en forma precoz puede mostrar un predominio polimorfonuclear que luego vira a linfomonocitario, hematíes crenados algunas veces, proteínas ligeramente elevadas, glucorraquia normal o ligeramente descendida y Pandy de + a ++. Menos de 8% de pacientes con EH probada con biopsia o PCR + en LCR tienen un citoquímico normal (se ve sobre todo en inmunodeprimidos). El LCR raramente contiene virus que puedan crecer en cultivos (8).
La detección de Ac no se recomienda para el diagnóstico agudo de la EH. Puede servir en retrospectiva para el diagnóstico tardío cuando la PCR se ha negativizado. La relación de 20:1 o menor en Ac en suero/Ac en LCR es diagnóstica de encefalitis reciente por HVS 1. Y, de hecho, la terapéutica antiviral debe ser discontinuada si el PCR es negativo a las 72 horas de haber comenzado la enfermedad en pacientes que tienen baja probabilidad de EH (imagen normal, citoquímico normal, vigilia normal, EEG normal) (5).
La PCR puede ser considerada al final del tratamiento para monitorear la respuesta al tratamiento. En caso de tratamiento exitoso, ésta debe ser negativa.
La introducción de esta técnica, tal como se mencionó, ha conducido a la identificación de formas leves o atípicas: encefalitis de tronco, mielitis, encefalitis multifocales o difusas sin compromiso temporal, etc. (20% de los casos).
Pueden existir falsos negativos, especialmente cuando el test se realiza antes de las 72 horas del debut de los síntomas, luego de 5-7 días de tratamiento antiviral y cuando existen inhibidores de esta reacción en LCR (componentes porfirínico de eritrocitos lisados).
La duración de la detectabilidad del ADN en el LCR luego del tratamiento de la EH no se conoce con exactitud. En un estudio retrospectivo (19), 4 de 19 pacientes (21%) permanecieron + luego de dos semanas de tratamiento. No está claro si la persistencia de una PCR + indica resistencia del virus que continúa su replicación o se trata de fragmentos de ADN de virus no viables. Lo último se apoya por la existencia de PCR + de cerebros de pacientes que han tenido una EH y se curaron.
De todas formas existe consenso que la PCR negativa al final del tratamiento suele ser un indicador de correcto tratamiento.
Hasta pocos años atrás se consideraba que una carga viral mayor a 100 copias/ml era un indicador de mal pronóstico clínico, sin embargo este estudio ha sido contravenido por otro que no otorga valor predictivo a la carga viral en el inicio del tratamiento (18).
La PCR pierde sensibilidad en casos de que el aciclovir se inicie antes que se haga la PL.
La biopsia cerebral se reserva para aquellos casos en que el PCR es negativo y existe convicción de encefalitis (u de otra enfermedad que simule una EH), y donde no existe respuesta al tratamiento con aciclovir. En esos casos se prefiere una biopsia a cielo abierto, dado que la biopsia esterotáxica no siempre retira material relevante. En la pieza biopsica se aplican técnicas de PCR, cultivo viral, técnicas de inmunomarcación e inmunoperoxidasas, así como microscopía electrónica (7).
Tratamiento
El tratamiento debe ser lo más precoz posible, el pronóstico vital y funcional depende en gran medida de ello. Se orienta a brindar el antivírico específico que es el aciclovir a razón de 10-15 mg/kg/8 hs. dadas en forma iv en infusión de 100 cc de fisiológico que se administra en una hora por 14-21 días. La dosis debe ajustarse según la función renal y debe establecerse un control estricto sobre dicha función debido a la potencialidad tóxica que tiene este antiviral. Se debe establecer un tratamiento antiepiléptico parenteral con fenitoina, valproato de sodio o levetiracetam. Y en caso de hipertensión endocraneana utilizar agentes osmolares, corticoides y eventualmente hiperventilación.
No es infrecuente que exista como complicación un Síndrome de Secreción Inadecuada de ADH (20).
Aproximadamente la mitad de los pacientes que sobreviven tienen un deterioro neurológico al cabo de seis meses de seguimiento.
Por tal motivo se está llevando a cabo un estudio donde luego de la terapéutica parenteral con aciclovir, se da valaciclovir oral por 90 días con la intención de verificar mayor mejoría que el end point de los 14-21 días, especialmente en parámetros neuropsicológicos (20). El valaciclovir tiene una buena biodisponibilidad y pueden acumularse adecuados niveles de la droga en el SNC. Se trata de una prodroga que es convertida por esterasas en aciclovir por el metabolismo hepático (21,22).
Los mecanismos de resistencia al aciclovir incluyen deficiencias en la timidin quinasa viral, mutaciones de esta y mutaciones de la ADN polimerasa. Se han descripto EH en inmunocomprometidos asociados con una cepa mutante resistente al aciclovir. No está claro si estas cepas pueden provocar EH en inmunocompetentes (20).
Cinco a diez por ciento de pacientes pueden reactivar síntomas encefalíticos luego del tratamiento antiviral. No está clara si la causa de esto es producto de una reactivación del virus, una respuesta inmunomediada o ambas (20).
Sin embargo el tratamiento precoz con Aciclovir en caso de sospecha de EH por la clínica y estudio de LCR, sigue teniendo fallos. Citando a Raschilas y cols., sólo 29% de estos pacientes recibieron aciclovir en puertas de urgencia, el 71% restante recibieron el antiviral luego de su ingreso, luego de una media de 16 horas de internación. Asi mismo se comprobó que existía una demora de 2 +/- 2,7 días entre la consulta hospitalaria y la instauración del tratamiento y que el tratamiento tuvo una demora de 5,5 +/- 2,9 días desde el inicio de los síntomas (23).
El tratamiento con corticoides ha sido objeto de controversia, aunque en general a nivel de expertos la recomendación es utilizarlos. La información obtenida de las investigaciones animales y de las observaciones clínicas retrospectivas indican que los pacientes pueden esperar un mejor pronóstico funcional si son tratados con dexametasona, aunque no existe hasta el momento evidencia suficiente para recomendar el uso de este medicamento en caso de EH.
En tal sentido se viene desarrollando un estudio multicentrico, multinacional (alemán, austriaco, holandés), randomizado, doble ciego y controlado con placebo (estudio GACHE) (24) que comenzó el reclutamiento en el año 2007 que ofrecerá resultados definitivos en el año 2013. El diseño del estudio compara pacientes con EH tratados con aciclovir + dexametasona versus aciclovir + placebo.
Pronóstico
A pesar de los avances reseñados, la mortalidad sigue siendo alta (20-30%) y sigue habiendo pacientes con secuelas invalidantes (menos de 20% son capaces de reintegrarse al trabajo). El mejor pronóstico lo tienen aquellos pacientes menores de 30 años con diagnóstico y tratamiento precoz y con un Glasgow de 6 o menos en la primera consulta.
Las cifras de mortalidad y discapacidad siguen siendo inaceptablemente altas, según Raschilas y cols. (23), en un estudio retrospectivo de 93 pacientes adultos, sólo 14% tuvieron una recuperación plena, 23% sobrevivieron con leve discapacidad, 63% con discapacidad moderada, 20% con discapacidad severa y 15% fallecieron. Estos datos son peores que los reportados por Whitley y Skoldenberg en sus trabajos fundamentales (donde 38-56% de los pacientes tratados se recuperaron sin déficit o con déficit leve).
ENCEFALITIS POR VARICELA-ZÓSTER
El virus VZ comparte la característica de latencia que es común a toda la familia herpes, luego de la primoinfección que se produce en la infancia (varicela) se establece en ganglios craneales, ganglios raquídeos y ganglios autonómicos.
El VZ se replica casi en exclusividad en células y tejidos humanos, un factor que restringe considerablemente la capacidad de estudiar sus propiedades biológicas y patogénicas. Las razones precisas del tropismo que se limita a los seres humanos y primates del VZ no están dilucidadas claramente pero probablemente se vinculen a receptores superficiales en las células para el anclaje de proteinas virales. A modo de ejemplo, la enzima que degrada la insulina recientemente se demostró que es un receptor que media entre la infección por VZ y la diseminación célula a célula.
Las complicaciones neurológicas pueden ser consecuencia de la infección primaria o de la reactivación del virus, produciendo una amplia gama de enfermedades: herpes zoster, neuralgia postherpética, vasculopatía, mielopatía, necrosis retiniana, cerebelitis y zoster sin herpes.
De todas formas las complicaciones producidas por la varicela y aquellas asociadas al herpes zóster son raras. Aquellas vinculadas con la varicela suceden en 1-3 casos/10.000 h. En adultos se asocia con frecuencia a situaciones de inmunodepresión.
La patofisiología del daño que produce el VZ corresponde a su acción vasculítica que compromete pequeños y medianos vasos arteriales cerebrales, y reacciones inmunomediadas con lesiones inflamatorias-desmielinizantes.
Justamente estos son los fenómenos que ocasionan las llamadas encefalitis por VZ. Los fenómenos vasculíticos pueden ocurrir un tiempo variable luego de la reactivación cutánea o no estar precedida por esta lo que hace mas difícil su diagnóstico.
En relación al diagnóstico licuoral, el citoquímico sigue los lineamientos de una reacción inflamatoria indistinguible de otras infecciones virales, la PCR es +, pero se limita a los primeros días de la neuroinfección, luego se negativiza. Se han detectado falsos positivos (Zóster no complicado), la detección de Ac antiIg M quizás sea la técnica más precisa y que se prolonga más en el tiempo, la sola detección de Ac antiIg G es controvertida, pues puede estar señalando la latencia exclusivamente del virus a nivel ganglionar.
La ataxia aguda cerebelosa es la complicación más común de la infección por varicela. El comienzo es agudo, tipicamente dentro de la semana del desarrollo del rash, pero puede ocurrir algunos dias antes hasta tres semanas después. Las opiniones están divididas en cuanto a si la lesión es inmunomediada o por agresión directa viral. La enfermedad dura en general 2-4 semanas pero puede ser menor en su duración o de meses de evolución, en general existe completa recuperación. Comienza con un síndrome vermiano que rápidamente se hace bihemisférico, puede haber irritabilidad, cefalea, vómitos, y temblor. Podemos hallar en el examen voz escandida, nistagmus, hipotonía y rigidez de nuca. Muchos pacientes no tienen anormalidades en la RM, otros muestran un aumento de señal en la corteza y eventualmente se tiñe débilmente con gadolinio (Figuras 4 y 5). El LCR puede ser normal o ligeramente inflamatorio.
La presentación clínica de las vasculitis por VZ pueden tener una presentación como ataque cerebrovascular (ACV), pueden cursar con cefaleas y fiebre. Aunque existen expresiones mas bizarras. Tambien se han descripto aneurismas y hemorragias. Muchas veces es la propia imagenología que muestra infartos hemorrágicos con aspecto inflamatorio quien pone en la pista al clínico.
La TC cerebral y la RM muestran imágenes de pequeño vaso (lesiones de aspecto numular, mas evidentes en pacientes inmunodeprimidos) o de vaso mediano con aspecto hemorrágico tal como se mencionó. La arteriografía muestra estenosis segmentarias u oclusiones y eventualmente aneurismas micóticos.
La vasculopatía unifocal relacionada al VZ (arteritis granulomatosa de gran vaso) es una variante que se describe en pacientes añosos inmunocompetentes, aunque no es exclusiva de estos tramos etáreos. La anatomía patológica revela células gigantes multinucleadas en la arterias, Ag para VZ, inclusiones tipo A de Cowdry y partículas de herpes virus en la microscopía electrónica.
El cuadro se relaciona con un herpes trigeminal y, como hemos descrito, la complicación neurológica puede manifestarse en forma variable en el tiempo. Esta es monofásica y autolimitada, pero también pueden verse formas remitentes o progresivas. También puede verse oclusión de las arterias retinianas ipsilaterales. Si el rash ocurre en el cuello o detrás de la oreja, puede haber infarto del tronco cerebral o compromiso de la circulación posterior.
Desde el punto de vista clínico, puede tener un debut súbito aunque, tal como se mencionó, puede simular un cuadro de proceso expansivo febril, incluidas crisis epilépticas.
El LCR a menudo, pero no siempre, presenta una pleocitosis mononuclear y bandas oligoclonales, la PCR no siempre es positiva, existe el convencimiento de que la positividad de esta reacción se limita a días, tal como se mencionó. La detección de Ac Ig M tiene valor de neuroinfección aguda, mientras que los Ac Ig G con PCR negativa, muestran el carácter crónico de la infección. Ambos test deben realizarse y sólo cuando ambos son negativos podemos excluir al VZ como responsable de la encefalitis. Dado que las vasculopatías por VZ pueden ocurrir sin rush, todas las vasculopatías de causa desconocida deben ser evaluadas para VZ.
Se exige un rápido diagnóstico dado que las vasculopatías por VZ pueden determinar alta mortalidad (25% de los casos) y el aciclovir puede curar el proceso.
La vasculopatía multifocal de pequeño vaso ocurre sobretodo en pacientes inmunodeprimidos, especialmente VIH +, transplantes de órganos sólidos o historia de neoplasia concomitante, puede no estar acompañada de rash o haber tenido VZ semanas o meses previos a la presentación del cuadro neurológico. El LCR muestra un perfil inflamatorio inespecífico. La RM muestra múltiples infartos pequeños que pueden ser hemorrágicos en la corteza y en sustancia blanca profunda. Las lesiones pueden ser isquémicas o desmielinizantes. Su presentación clínica es diversa (cefaleas, fiebre, alteraciones de conciencia, crisis epilépticas y fenómenos focales).
Otras complicaciones en inmunodeprimidos son las ventriculitis e infartos cerebrales secundarios a vasculitis leptomeningeas.
A pesar de la controversia sobre si tratar o no la ataxia aguda cerebelosa se prescribe aciclovir a 10 mg/ kg/8 hs./7 días en niños, en caso de paciente inmunocomprometido se extiende a 14-21 días. El mismo tratamiento se ensaya en las vasculitis y se adjunta prednisona a razón de 60-80 mg diarios durante 3-5 días (12,25,26).
ENCEFALITIS POR CMV
Diferentes estudios reportan que altos porcentajes de la población adulta tienen serología positiva para CMV, sin embargo, no desarrollan la enfermedad o bien sufrieron un cuadro similar al de la mononucleosis.
En pacientes inmunocomprometidos puede haber una reactivación viral y producir patología: encefalitis, retinitis y polirradiculomieloneuropatía (PRMN) aguda.
La experiencia desarrollada por CMV en el SNC se remite a pacientes VIH +, en estadío SIDA con severa disminución de su población linfocitaria y tambien en transplantados.
La encefalitis en estas circunstancias, aparece cuando la población de linfocitos T con receptores CD4 es menor a 100, se trata sobretodo de una ventriculoencefalitis necrotizante, y en menor medida pueden dar lesiones de aspecto redondeado en anillo que se ponen de relieve con gadolinio en la RM.
Esta complicación aparecía con una frecuencia baja en la época pretratamiento combinado antirretroviral (5-6%), sin embargo un tercio de las necropsias practicadas en pacientes con SIDA demostraban la presencia del virus en el parénquima nervioso. La clínica es algo proteiforme, se trata de un deterioro cognitivo-comportamental rápidamente progresivo (que lo diferencia de la demencia asociada al VIH), con elementos confusionales, fiebre, compromiso de pares craneanos y eventualmente signos focales. El cuadro se desarrolla en días o pocas semanas. Puede asociarse o ser antecedido de retinitis hemorrágica, polirradiculomieloneuropatía, adrenalitis, neumonitis, etc., lo que permite sospechar la etiología del cuadro.
La imagen, especialmente la RM muestra un realce ventricular característico con gadolinio e hipointensidad ventricular simétrica. Con menor frecuencia las imágenes en anillo descritas.
El LCR puede ser normal, aunque algunos muestran al igual que la PRMN, pleocitosis polimorfonuclear con descenso de la glucosa y proteinas elevadas, el estudio de PCR en LCR es el diagnóstico de elección, tiene una sensibilidad de 80% y una especificidad de 90%, su detección implica infección activa por CMV.
En los últimos años diversos autores han llamado la atención sobre formas encefaliticas provocadas por el CMV en pacientes inmunocompetentes. Se pueden perfilar dos grandes formas de presentación en dichos pacientes, a: por un lado un cuadro agudo con cefaleas, fiebre y síndrome meníngeo, con una evolución autolimitada (días o semanas) y benigna. Muy pocos tienen desenlace fatal. Por otro lado hay formas subagudas y crónicas con manifestaciones que evolucionan incluso con intermitencias, estas formas pueden acompañarse de elementos focales donde algunos pacientes mantienen secuelas neurológicas en el tiempo.
El tratamiento se basa en la administración de ganciclovir o foscarnet.
La evolución en los inmunocomprometidos es errática (12,27,28).
ENCEFALITIS POR HHV 6
La seroprevalencia en diferentes lugares del mundo se aproxima a 80% de la población adulta. Se trasmite por la saliva y no se descarta la trasmisión vertical y sexual.
Aunque en general el HHV 6 es asintomático, se lo ha asociado con el exantema súbito, las convulsiones febriles de la infancia (y eventualmente con las esclerosis mesial temporal), encefalitis en niños e inmunocomprometidos y puede jugar algún rol en la Esclerosis Múltiple, Guillain-Barré y la EMAD. Dado que el HHV 6 está presente en el encéfalo de personas sanas, su rol etiológico en ciertas entidades es incierto. Además, la detección de una PCR + en LCR no garantiza su rol etiológico en la enfermedad neurológica.
El HHV 6 puede causar complicaciones en transplantados de médula ósea, hígado y pacientes inmunocompetentes de todas las edades.
Existen dos cepas, la A y la B, la cepa A es la que tiene preferencia por el SNC. La infección primaria generalmente ocurre en la infancia, donde se radica a nivel renal y cerebral, quedando quiescente. Prácticamente 90% de los niños es seropositivo a la edad de 12 años.
En un estudio, 7% de encefalitis de etiología desconocida en la población general se asoció con la infección del HHV 6 del SNC. Se reportan en la literatura pocos casos en inmunocompetentes, en donde puede producir encefalitis de curso fulminante o subagudo. En los inmunodeprimidos (SIDA, transplantados) sigue un modelo de leucoencefalopatía, o encefalitis límbica (compromiso simétrico de cara interna de lóbulos temporales: pérdida de memoria, insomnio, actividad crítica temporal, etc.).
La TC craneal puede ser normal en un principio, pero luego revela afectación en el cortex y GB. La RM muestra areas de desmielinización a nivel de la sustancia blanca y tálamo.
La PCR + en LCR es sugestiva de encefalitis por HHV 6 pero no definitiva, pues el ADN del virus puede ser detectado en pacientes sin enfermedad neurológica. La detección de Ig M especifica tiene mayor especificidad.
La biopsia cerebral se necesita para la confirmación del diagnóstico en casos conflictivos de HHV 6.
En los pacientes con SIDA es esperable una alta prevalencia de HHV 6, pero esto no ocurre en la realidad. El HHV 6 fue detectado por inmunohistoquímica en 4 de 6 adultos con SIDA que tenían áreas de desmielinización en el momento de fallecer.
El tratamiento es con Ganciclovir o Foscarnet. Tambien pueden combinarse.
Luego de transplantes medulares, el HHV 6 se reactiva en 38-95% de pacientes documentado esto por cultivo viral o PCR. Hasta el momento la enfermedad que se asocia mas a esta circunstancia es la fiebre y el rash que suceden a las 2-4 semanas del transplante.
La encefalitis asociada al HHV 6 se ha reportado en pacientes inmunocompetentes e inmunodeprimidos en forma aislada o serie de casos de pocos pacientes. Entre los inmunocompetentes se ha visto que desarrollaron cefalea, fiebre y alteraciones mentales
Tambien se han detectado signos focales. Los pacientes tienen en general pleocitosis moderada con elevación de proteinas. Los estudios imagenológicos o fueron normales o mostraron alteraciones no específicas.
Los reportes de encefalitis se han visto sobre todo en transplantados medulares o de stem cells, Los casos descriptos en transplante de órganos sólidos han sido menos.
Los estudios de imagen van desde anormalidades en la sustancia blanca a edema del lóbulo temporal y sistema límbico. Recientemente se describieron 5 pacientes con patrón de encefalitis límbica, tuvieron insomnio, y deterioro de la memoria a corto plazo así como crisis temporales. El LCR mostró sobretodo una discreta elevación de proteinas. Todos los pacientes tuvieron tumefacción en el hipocampo en forma bilateral o unilateral en T2, con hipermetabolismo en el PET. En la necropsia se identificó la variante B.
Basado en lo anterior, debemos decir que no es claro que exista un síndrome clínico definido en la encefalitis por HHV 6. A su vez, los reportes se apoyan en la PCR para este virus, que como ya vimos puede ser positiva en sujetos sanos. La distinción entre la presencia ocasional de ADN vinculado al HHV 6 y la enfermedad sigue sin aclararse.
El diagnóstico descansa en el aislamiento del virus acompañado de la seroconversión.
La respuesta Ig M es corta y tiene reacción cruzada con el HHV 7. Y es muy difícil distinguir entre el A y el B.
Tratamiento: dado que el patrón de inhibición viral se asemeja al CMV, se utiliza ganciclovir y foscarnet. La inhibición con el aciclovir es pobre. El cidofovir parece ser la droga de elección seguida por ganciclovir y foscarnet (12,29,30).
ENCEFALITIS POR EPSTEIN-BARR
La mayoría de la población es seropositiva a los 30 años, habiendo cursado la infección en forma sintomática (mononucleosis infecciosa) o asintomática.
Las complicaciones neurológicas asociadas al EB, son raras (0,5%) y se ven sobre todo durante o inmediatamente luego de la mononucleosis infecciosa, la causa suele ser inmunomediada (cerebelitis, EMAD), aunque no se descarta acción directa viral. En caso de agresión directa existe PCR +, pero la exacta sensibilidad de la PCR no puede ser determinada, dada la rareza de la encefalitis por este virus.
Además, dado que el EB se encuentra en las células mononucleares periféricas sanguíneas y la sangre puede contaminar el LCR, es posible detectar falsos positivos.
La aplicación más útil es en la sospecha de linfomas o linfomatosis meníngeas diseminadas (más raro) en pacientes inmunodeprimidos, donde la PCR tiene una alta sensibilidad y especificidad. La negatividad no excluye el diagnóstico de linfoma.
En el estudio prospectivo del Colaborative Antiviral Study Group, donde se evaluaban aquellos casos que tenían signos focales como requisito de entrada, sólo 2% de los casos fueron asignados al EB (8 casos de 432).
El tratamiento es de soporte y sintomático (anticonvulsivantes), los corticoides pueden llegar a ser útiles en caso de HIC y casos inmunomediados. El aciclovir inhibe el EB in vitro, pero no tiene efectividad in vivo (12,32).
NUESTRA EXPERIENCIA
Nuestra experiencia sistematizada en la materia se condensa en la publicación “Meningitis y Encefalitis Víricas. Relevamiento mediante técnicas de Reacción en Cadena de Polimerasa aplicadas al LCR de los grupos herpes, enterovirus y arbovirus como principales agentes etiológicos. A propósito de 59 casos (32).
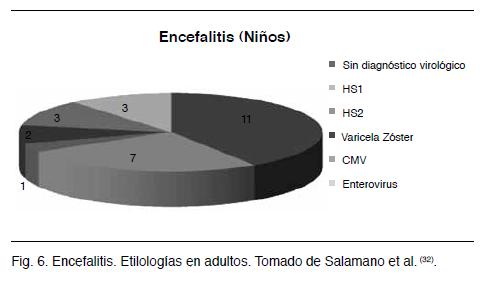
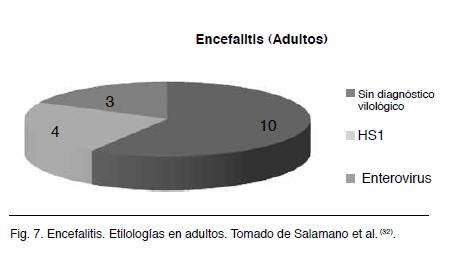
En este trabajo se detectaron 44 pacientes con clínica y paraclínica sugestivas de encefalitis viral; 21 de estos casos no tuvieron diagnóstico etiológico viral por PCR; 27 casos fueron encefalitis en niños mayores a seis meses y 17 en adultos; 17 tuvieron diagnóstico virológico vinculado a virus de la familia herpes: 11 por HSV 1, 3 por CMV, 2 por VZ y 1 por HSV 2. Es de destacar que los hallazgos de CMV, VZ y HSV 2 fueron en niños. Ninguno de los pacientes tenía circunstancias de inmunodepresión (Figuras 6 y 7).
Desde fines del año 2010 se viene desarrollando un trabajo conjunto de la Universidad de la República y del Ministerio de Salud Pública sobre Vigilancia Epidemiológica en Meningitis y Encefalitis Virales que permitirá identificar los virus circulantes en nuestro país responsables de estas entidades en adultos y niños. El reconocimiento se hará mediante técnicas de PCR aplicadas al LCR y cubrirá todo el país (33).
CONCLUSIONES
Las encefalitis herpéticas comparten una serie de aspectos en común que hacen necesario su conocimiento por parte del clínico. Son encefalitis esporádicas. Suelen ser consecuencia de primoinfecciones, y especialmente de reactivaciones, dada su tendencia a provocar latencia en el ser humano. No son frecuentes, pero tienen la posibilidad de ser tratadas con antivirales con resultados diversos. Algunas son preponderantemente del paciente inmunocompetente (la encefalitis por HSV 1 sobre todo), otras se pueden ver en el paciente inmunocompetente e inmunodeprimido (virus VZ) y otras son casi exclusivas del paciente inmunodeprimido (CMV). Tanto la encefalitis por HSV 2, como la producida por HHV 6 y EB, son sumamente raras y se desconocen muchos aspectos de ellas (Tabla 1).
Todas ellas comparten el hecho de que pueden provocar encefalitis por respuesta inmunomediada (EMAD). Se destaca el carácter vasculítico que provoca la encefalitis por VZ.
La configuración imagenológica es bastante típica en la EH por HVS 1 (compromiso temporal y frontal bilateral preponderante en un hemisferio) y puede ser sugestiva en las encefalitis por VZ (imágenes de infarto hemorrágico e imágenes monedas profundas).
La técnica de PCR en LCR suele ser una herramienta útil para distinguir entre las encefalitis por replicación viral directa y las inmunomediadas, a excepción de de la encefalitis por HHV 6, probablemente por EB y algunos casos de VZ. Sin embargo la sensibilidad y especificidad de esta técnica está exclusivamente validada en la EH por HSV 1.
La respuesta a los antivirales, especialmente el aciclovir en la encefalitis por HSV 1 y 2 es de alta eficacia, pero aún existe una mortalidad elevada (15-20%) y alta prevalencia de secuelas entre quienes la padecen.
Hoy, ante toda sospecha de Encefalitis Viral esporádica, se preconiza comenzar desde un inicio con aciclovir iv. La encefalitis por VZ también puede tener una buena respuesta ante el tratamiento con aciclovir. El resto de las encefalitis tienen una respuesta errática ante el tratamiento antiviral.
El uso de corticoides sigue estando en el terreno de lo controversial, aunque la opinión de expertos y pequeña serie de casos aboga por su utilización en los primeros días de la encefalitis. Actualmente se viene desarrollando un trabajo prospectivo (GACHE) para sostener o no la terapéutica con corticoides desde el punto de vista de la evidencia.
BIBLIOGRAFÍA
1. Whitley R, in Herpesvirus Infection of the Central Nervous System. Herpes2004; 11( Suppl 2): 47 A.
2. Oehninger C, Encefalomielis aguda diseminada y sus variantes. En Neuroinfecciones en el adulto y en el niño. Salamano R, Scavone C, Wajskopf S, Savio E.Montevideo:Arena;2008.p. 115-121.
3. Baringer JR, Herpex Simplex Infections of the Nervous Systen. In Current Issues in Clinical Neurovirology: Pathogenesis, Diagnosis and Treatment in Neurological Clinics. 2008; 26(3): 657-674.
4. Mueller NH, Gilden DH, Cohrs RJ, Mahalingam R, Nagel MA. Varicella Zoster Virus Infection. Diagnosis and Treatment in Neurological Clinics. 2008;26( 3): 675-698
5. Boivin G. Diagnosis of Herpesvirus Infections of the Central Nervous System. In Herpes 2004;11(Suppl 2):48A-56A.
6. Studhal M, Bergstrom T, Hagberg L. Acute viral encephalitis in adults. A prospective study. Scand J Infect Dis 1998; 30: 215-220
7. Salamano R, Encefalitis Herpética del Adulto. En Neuroinfecciones en el adulto y en el niño. Salamano R, Scavone C, Wajskopf S, Savio E.Montevideo:Arena;2008.p. 81-84.
8. Chaudhuri A, Kennedy PGE, Diagnosis and treatment of viral encephalitis. Postgrad Med J, 2002; 78; 575-583. Downloaded from pmj.bmj.com on 28 December; 2008.
9. Presles O. Encéphalites Aiguës Virales. Stratégie diagnostique et thérapeutique. Basilea :Karger . 1982 ; p. 103-109
10. Skoldenberg B, Forsgren M, Alestig K, Bergstrom T, Burman L, Dahlqvist E et al. Acyclovir versus vidarabine in herpes simplex encephalitis. Randomised multicentre study in consecutive Swedish patients. Lancet 1984; 2: 707-711.
11. Whitley RJ, Alford CA, Hirsch MS, Schooley RT, Luby JP, Aoki FY et al.Vidarabine versus acyclovir therapy in herpes simplex encephalitis. N Engl J Med 1986; 314: 144-149.
12. Tyler KL, Acute Viral Encephalitis. AAN, 63rd Annual Meeting, April 9-16, 2011. Hawaii.
13. Kennedy PGE, Chaudhuri A. Herpes Simplex Encephalitis J Neurol Neurosurg Pshychiatry 2002; 73: 237-238.
14. Steiner I, Kennedy PGE, Pachner AR. The neurotropic herpes virus: herpes simplex and varicella-zoster. Vol 6 November 20071015-1028. Disponible en : http://www.thelancet.com/journals/laneur/article/PIIS1474-4422(07)70267-3/fulltext
15. Salamano R, Ormaechea R, Perna A, Lorenzo J, Dansilio S, Ketzoian C, Spagnuolo E. Encefalitis Herpética a propósito de un caso clínico (importancia del diagnóstico y tratamiento precoz) Rev Med Uruguay 1999; 15: 66-70.
16. Kennedy PGE. Viral Encephalitis: Causes, differential diagnosis, and management. J Neurol Neurosurg Psychiatry 2004; 75 (Suppl I): i10- i15.
17. Tyler KL. Herpes Simplex Virus Infections of the Central Nervous System: Encephalitis and Meningitis, including Mollaret. In Herpes 2004; 11( Suppl 2): 57A-64A.
18. Schloss L, Falk K, Skoog E et al. Monitoring of herpes simplex virus DNA types 1 and 2 viral load in cerebrospinal fluid by real-time PCR in patients with herpes simplex encephalitis. J Med Virol 2009;81: 1432-1437
19. Lakeman FD, Whitley RJ. National Institute of Allergy and Infections Diseases Collaborative Antiviral Study Group. Diagnosis of herpes simplex encephalitis. Application of polymerase chain reaction to cerebrospinal fluid from brain-biopsied patients and correlation with disease. J Infect Dis 1995; 171: 857-63
20. Domingues RB. Treatment of Viral Encephalitis. Central Nervous System in Medicinal Chemistry 2009; 9: 56-62
21. De Clercq E, Field HJ. Antiviral prodrugs, the development of successful prodrug strategies for antiviral chemoteraphy. Br J Pharmacol, 2006, 147, 1-11.
22. Mac Dougall C, Guglielmo BJ. Pharmacokinetics of valacyclovir. J Antimicrob Chemother, 2004; 53: 899-901.
23. Raschilas F, Wolff M, Delatour F. Outcome of and prognostic factors for herpes simplex virus encephalitis in adults: results of a multicenter study. Clin Infect Dis 2002; 35: 254-260.
24. Martinez-Torres F, Menon S, Pritsch M, Victor N, Jenetzky E, Jensen K, Schielke E, Schmutzhard E, de Gans J, Chung Ch-H, Luntz S, Hacke W, Meyding-Lamade U, for the GACHE Investigators. Protocol for German trial of Acyclovir and corticosteroids in Herpes-Simplex-virus-encephalitis (GACHE): a multicenter, multinational, randomized, double-blind, placebo-controlled German, Austrian and Dutch trial (ISRCTN45122933), BMC Neurology 2008;8-40.
25. Gilden D. Varicella Zoster Virus and Central Nervous System Syndromes. Herpes2004; 11(Suppl 2): 89A-94A.
26. Nagel MA, Cohrs RJ, Mahalingam R, Wellish MC, Forghani B, Schiller A, et al. The varicella zoster virus vasculopathies. Clinical, CSF, imaging and virologic features. Neurology 2008;70: 853-860.
27. Griffiths P. Cytomegalovirus Infection of the Central Nervous System. Herpes 2004;11(Suppl 2):95A- 104A.
28. Salamano R, Gervaz E, Mañana G, Peña S, Panuncio A, Puppo C, Mesa P, Legnani C, Sabaris A, Azambuja C. Encefalitis a citomegalovirus en un paciente inmunocompetente. Análisis clínico, neuropatológico y ultraestructural. Arq Neuropsiquiatr 2001; 59(4): 954-958.
29. Dewhurst S. Human Herpesvirus Type 6 and Human Herpesvirus Type 7 Infections of the Central Nervous System. Herpes 2004; 11(Suppl 2): 105 A-111 A.
30. Caserta MT. Human Herpesvirus-6, in Infections of the Central Nervous System. 3th. Edition. Scheld WM, Whitley RJ, Marra Ch M.Baltimore: Lippincott Williams & Wilkins;2004.p.185-196.
31. Hoover SE, Ross JP, Cohen JI. Epstein-Barr Virus, in Infections of the Central Nervous System. 3th. Edition. Scheld WM, Whitley RJ, Marra Ch M. Baltimore: Lippincott Williams & Wilkins; p. 175-184.
32. R, Scavone C, Baz M, Rey A, Gonzalez G, Perna A, Cardinal P,Lewin S, Arbiza J, Ruchanski D. Meningitis y Encefalitis Víricas en Uruguay. Relevamiento mediante técnicas de Reacción en cadena de Polimerasa aplicadas al LCR de los grupos herpes, enterovirus y arbovirus como principales agentes etiológicos. A propósito de 59 casos. Salamano Rev Med Urug 2009; 25: 212-218.
33. Protocolo de Vigilancia de Meningoencefalitis Virales. Ministerio de Salud Pública División de Epidemiología - Departamento de Vigilancia en Salud,Universidad de la República, Centro Hospitalario Pereira Rossell.Uruguay - Agosto 2010. Obtenido en www.msp.gub.uy/andocasociado.aspx?4499,19605.