Services on Demand
Journal
Article
Related links
Share
Archivos de Medicina Interna
Print version ISSN 0250-3816On-line version ISSN 1688-423X
Arch. Med Int vol.33 no.2 Montevideo 2011
Casuística de interés
Malformaciones arteriovenosas pulmonares
Aproximación a una patología poco frecuente a partir de tres casos clínicos
Pulmonary arteriovenous malformations
An approach to a rare condition based on three clinical cases
Dr. Juan Pablo Salisbury
Asistente de la Cátedra de Neumología. Instituto del Tórax. Facultad de Medicina. UdelaR. Montevideo.
Dr. Luis M. Piñeyro
Profesor Director de la Cátedra de Neumología e Instituto del Tórax. Facultad de Medicina. UdelaR. Montevideo.
Recibido: 15/07/11 – Aceptado: 08/08/11
Correspondencia: Juan Pablo Salisbury. Francisco Araucho 1166 apto 5, Montevideo, Uruguay. E-mail: jpsalis@hotmail.com
Resumen:
Resumen: Las malformaciones arteriovenosas pulmonares (MAVP), son verdaderas fístulas vasculares de alto flujo y baja presión carentes de filtro capilar pulmonar. Consisten en la unión de una arteria a una vena mediante un saco aneurismático. Se trata de una patología muy poco frecuente y con una alta asociación con la enfermedad telangiectasica hereditaria. A continuación se realiza un análisis de tres casos con diferentes formas clínicas de presentación. Se destaca la gran importancia de la angio tomografía como método de diagnóstico así como la alta eficacia de la arteriografía con embolizacion para su resolución.
Palabras clave: Síndrome Rendu-Osler-Weber. Telangiectasia hemorrágica hereditaria. Malformaciones arteriovenosas pulmonares, Circulación Pulmonar.
Summary:
Pulmonary arteriovenous malformations (PAVM) are true high-flow and low pressure vascular fistulas lacking a capillar filter. This PAVM consist of an artery joining to a vein by an aneurysm sac. This is a rare condition with a high association with the hereditary telangiectasia disease. The following is an analysis of three cases with different clinical presentations highlighting the importance of the angio CT as a diagnostic test, as well as the high efficacy of arteriography with embolization as a treatment.
Keywords: Rendu-Osler-Weber Syndrome. Inherited Hemorrhagic Telangiectasia. Pulmonary arteriovenous malformations, Pulmonary circulation.
INTRODUCCIÓN
Las malformaciones arteriovenosas pulmonares (MAVP), son verdaderas fístulas vasculares de alto flujo y baja presión, carentes de filtro capilar pulmonar. Consisten en la unión de una arteria a una vena mediante un saco aneurismático(1). Existen dos formas de clasificar a las MAVP. De acuerdo a su etiología en congénitas o adquiridas. Siendo la enfermedad de Rendú-Osler-Weber (ROW), también denominada enfermedad telangiectásica hereditaria (THH) la responsable de entre 80 y 90% de los casos de MAVP congénitas(2). La segunda clasificación, a su vez la más utilizada en la práctica clínica, es la clasificación morfológica. Ésta las divide en simples o complejas, en base al número de vasos nutricios o venas de drenaje. Entre 80 y 90% de los casos se trata de MAVP simples por presentar una única arteria y una única vena de drenaje(3). Las MAVP complejas son aquellas que presentan 2 o más vasos aferentes, o venas de drenaje, presentes en el 10 a 20% restante(3). Aproximadamente 60% de las MAVP son asintomáticas(1-4). Los síntomas principales son la disnea de esfuerzo provocada por la hipoxemia resultante del shunt intra pulmonar, la embolia paradojal fundamentalmente a nivel encefálico responsable de accidentes cerebro vasculares, accidente isquémico transitorio (AIT), migraña y los abscesos cerebrales debidos a bacteriemias favorecidas por la ausencia del filtro capilar pulmonar. Excepcionalmente se pueden romper provocando hemoptisis o hemotórax(3).
El diagnóstico de MAVP requiere de un alto nivel de sospecha debido a su baja incidencia y a sus diferentes formas clínicas de presentación. Se recomienda su búsqueda en todo paciente con diagnóstico de ROW o en aquellos pacientes que presenten evidencia de insuficiencia respiratoria producida por shunt intra pulmonar, absceso o embolia paradojal de etiología no aclarada. Existen diferentes métodos para arribar al diagnóstico. Desde técnicas imagenológicas simples, como la radiografía de tórax (RxTx), hasta angiotomografía (angioTC) con reconstrucción en 3D y métodos más complejos dirigidos a demostrar el shunt intrapulmonar y las alteraciones del intercambio gaseoso(5,6). El diagnóstico de certeza requiere métodos directos como la arteriografía pulmonar, la cual es el método diagnóstico de excelencia(1,2-5). El ecocardiograma con contraste es un excelente método de evaluación del shunt intrapulmonar, ya que identifica pequeñas fracciones de él en ausencia de síntomas clínicos y de alteraciones del intercambio gaseoso. Este método presenta en centros con experiencia una sensibilidad de 97%, con un valor predictivo negativo de 99%, por lo que se recomienda en el screening de pacientes portadores de THH(4). Existen pocas reseñas bibliográficas del papel de la Resonancia Magnética (RM) en el diagnóstico de las MAVP(7). Esto se debe a que presenta múltiples artefactos técnicos, lo que determina un alto porcentaje de falsos positivos(7). En la actualidad se utiliza la angioRM con mejores resultados y una sensibilidad próxima a 100%. Se requieren trabajos con un mayor número de pacientes para que se pueda contar con dicha técnica en forma rutinaria.
Desde principios de la década pasada el tratamiento endovascular ha ganado aceptación en el manejo de las MAVP por su alta eficacia y mínimas complicaciones. Es así que hoy en día la arteriografía con embolización constituye la técnica “gold standard” para su tratamiento(8). La cirugía está cada vez menos indicada, reservándose en la actualidad para casos individuales de MAVP periféricas, que puedan ser resecadas por videocirugía o en centros donde no se cuenta aún con la posibilidad de realizar arteriografía con embolización(9).El objetivo del presente artículo es exponer tres casos clínicos de pacientes portadores de ROW y MAVP con diferentes formas de presentación, destacar la importancia de la sospecha clínica y definir los métodos diagnósticos y terapéuticos actualmente aceptados.
Caso clínico 1
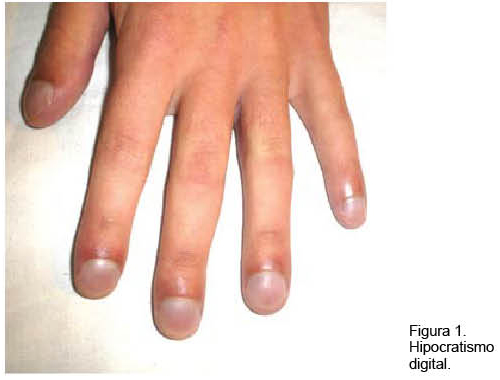
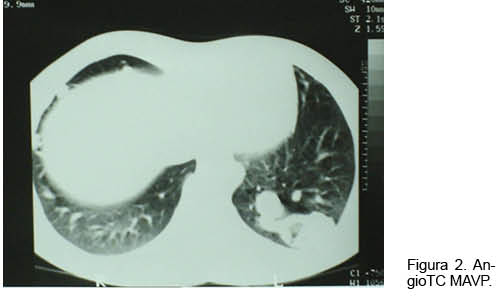
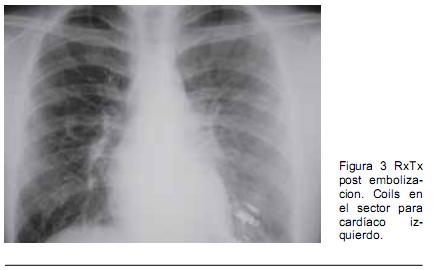
Hombre de 18 años con historia de epistaxis recurrentes y cianosis desde la infancia. Del examen clínico se destacaba: saturación arterial de oxígeno (SaO2) de 80%, mucosas hipercoloreadas e hipocratismo digital (Figura 1). La paraclínica confirmó poliglobulia e insuficiencia respiratoria severa, sin corrección con la administración de oxígeno. La RxTx evidenció una opacidad tenuemente homogénea en la región paracardíaca izquierda. El ecocardiograma descartó alteraciones estructurales. Se realizó angioTC con reconstrucciones 3D (Figura 2), confirmándose dos MAV, una de aspecto nodular, en el lóbulo superior del pulmón derecho, y otra más voluminosa, en la base del pulmón izquierdo (Figura 3). En esta última la arteria que la nutría continuaba la rama lobar inferior izquierda, siendo casi del mismo calibre y drenando en la vena pulmonar inferior. Se observaban múltiples dilataciones vasculares periféricas, bilaterales de aspecto varicoso. Se realizó embolización durante la arteriografía pulmonar con varios “coils” fibrilares de platino. La gasometría de control reportó una presión arterial de oxígeno (PaO2) de 79 mm Hg y una SaO2 de 96%.
Caso clínico 2
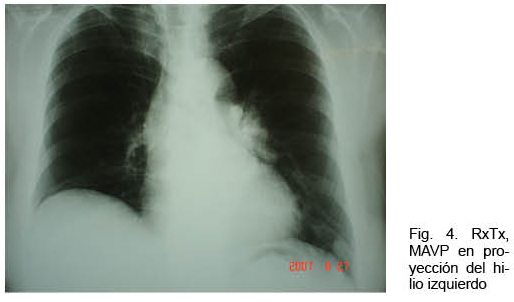
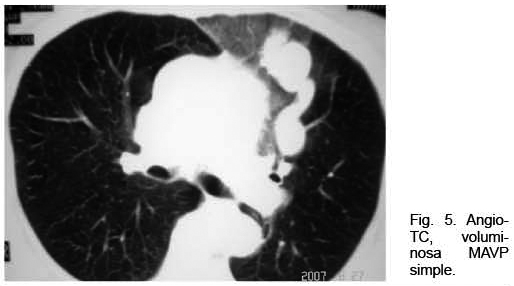
Mujer de 73 años con antecedentes familiares de ROW. Antecedentes personales de AIT un año antes. Ingresó por hemoptisis. Del examen físico se destacaba la presencia de múltiples telangiectasias en piel y mucosas; no presentaba cianosis. La gasometría arterial mostraba una hipoxemia severa. La RxTx mostró una opacidad homogénea polilobulada de 4 centímetros de diámetro mayor, de proyección hiliar izquierda, topografiada a nivel de la língula (Figura 4). Se complementó la valoración con angioTC que confirmó la presencia de múltiples malformaciones arteriovenosas izquierdas pequeñas, junto con una predominante de aproximadamente 5 cm de diámetro de aspecto varicoso, a nivel de língula, con evidencia de sangrado a dicho nivel (Figura 5). Se realizó arteriografía con embolización con “coils” de MAVP predominante con buena evolución.
Caso clínico 3
Mujer de 53 años con antecedentes personales de epistaxis recurrentes. Derivada por el oncólogo por el hallazgo de múltiples nódulos pulmonares a nivel de la RxTx y TC.
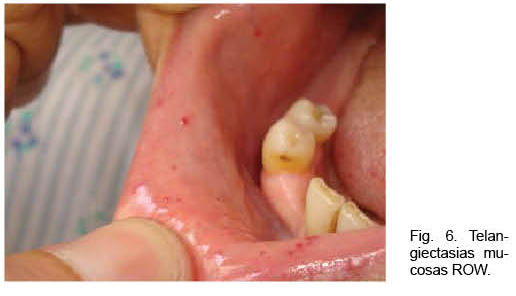
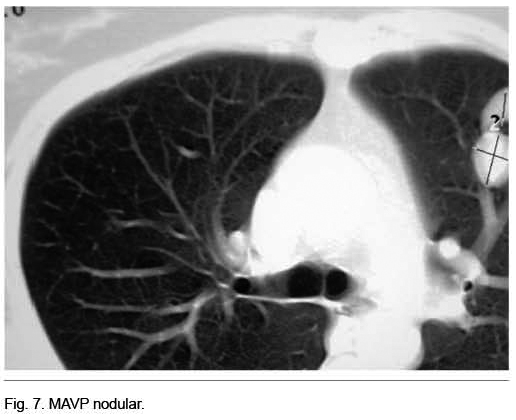
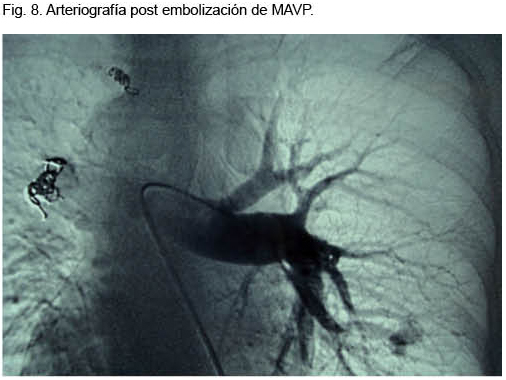
Se destacaba la existencia de múltiples telangiectasias mucocutáneas (Figura 6). Se realizó angioTC que confirmó el diagnóstico de MAVP múltiples (Figura 7); dos a nivel de lóbulo superior izquierdo y otra a nivel de lóbulo inferior derecho. Se realizó arteriografía y, simultáneamente, la embolización de las dos MAVP izquierdas, quedando una malformación a nivel del lóbulo inferior derecho simple de 3 mm (Figura 8).
Discusión y Comentarios
El primer caso se trata de un paciente joven sin antecedentes familiares, pero con antecedentes personales de epistaxis recurrentes, disnea, cianosis e hipocratismo digital de varios años de evolución, motivo por el cual se descartó en varias ocasiones la presencia de cardiopatía congénita, pero sin arribar a un diagnóstico etiológico. Esta tríada denominada clásica integrada por disnea, cianosis e hipocratismo digital sólo se encuentra presente en 30% de los casos de MAVP(1,2). La presentación clínica de las MAVP depende de su número, tamaño y etiología. Lo más frecuente es que sean únicas y asintomáticas, y aparezcan como un hallazgo radiológico. Una MAVP única menor de 2 centímetros de diámetro habitualmente es asintomática, si bien está expuesta a producir complicaciones(2). Asimismo, cuanto mayor sea el número de MAVP, mayor será la sintomatología que presentará dicho paciente. Los síntomas se basan en tres mecanismos fisiopatológicos básicos: shunt intrapulmonar, embolismo paradojal y ruptura de las MAVP. En cuanto a su topografía, predominan en los lóbulos inferiores y en los sectores subpleurales. Las MAVP ubicadas a dicho nivel se asocian característicamente a platipnea y ortodeoxia. Platipnea significa la aparición de disnea al adquirir la posición de pie y se acompaña de caída de la oxemia: ortodeoxia. Al adquirir el paciente la bipedestación, el flujo sanguíneo se redistribuye hacia los lóbulos inferiores aumentando el flujo sanguíneo hacia las MAVP, con el consiguiente aumento del shunt intrapulmonar y caída de la oxemia(6). Afortunadamente el primer caso sólo presentó elementos de shunt intrapulmonar con elementos de hipoxemia crónica, pero sin evidencia de eventos embólicos ni complicaciones infecciosas. En cuanto al diagnóstico de ROW, éste posible por cumplir con dos de los cuatro criterios diagnósticos de Curaçao(3). Éstos son: una historia de epistaxis recurrentes, asociado a MAV viscerales, en este caso pulmonares, en ausencia de antecedentes familiares de la enfermedad, la presencia de telangiectasias mucosas ni cutáneas.
El segundo caso presenta la peculiaridad de contar con el antecedente familiar de ROW, pero en la que nunca se la había detectado ni se habían realizado estudios de screening diagnóstico de malformaciones viscerales. La paciente presentó dos complicaciones mayores: un accidente isquémico transitorio (AIT) y una hemoptisis. Con respecto a la hemoptisis que presentó, debe pensarse que fue secundaria a la ruptura de telangiectasias a nivel del árbol bronquial, ya que fue moderada y no se comprobaron elementos de ruptura de ninguna de la MAVP, lo cual, de ocurrir, se asocia a una alta mortalidad. Se realizó tratamiento en base a arteriografía con embolización de urgencia con resultado favorable. En la enfermedad de ROW la herencia no se encuentra ligada al sexo y es de carácter autosómica dominante, por lo que cada descendiente de una persona afectada tiene 50% de posibilidades de padecer la enfermedad(3). Es por eso que se recomienda en todos los familiares de primer grado la realización de un screening de la enfermedad y de la presencia de malformaciones viscerales(3).
El tercer caso se trata de una paciente de 53 años con antecedentes de epistaxis recurrentes, anemia ferropénica, en estudio de etiología no aclarada y múltiples telangiectasias mucocutáneas. Fue derivada por el oncólogo por presentar nódulos pulmonares bilaterales, catalogados de probable secundarismo pulmonar sin diagnóstico anátomopatológico. En esta paciente la sospecha diagnóstica inicial fue de ROW asociado a MAVP. Los estudios de imágenes fueron fundamentales para poder arribar al diagnóstico correcto.
En cuanto a los métodos de diagnóstico utilizados en los tres casos, debemos de jerarquizar que la RxTx fue patológica en todos; ésta es anormal en el 98% de los casos(2). La gasometría arterial ventilando espontáneamente al aire confirmó la presencia de insuficiencia respiratoria crónica tipo I en los tres casos, y sin corrección luego de la administración de oxígeno por 30 minutos, permitiendo afirmar el mecanismo de shunt. En el caso número 1 también se destacaba clínicamente la presencia de platipnea y ortodeoxia. La angio TC fue el método de diagnóstico en los tres casos, con un excelente rendimiento. Se trata de una técnica sensible, de bajo costo, que permite establecer el diagnóstico de MAVP. Permite la valoración del tamaño, topografía y angioarquitectura, así como el seguimiento de la lesión luego de realizado tratamiento(5). En los tres casos la confirmación diagnóstica fue mediante la angioTC, permitiendo realizar la arteriografía sólo con una finalidad terapéutica. Los tres pacientes fueron sometidos a embolización con coils fibrilares de platino, con excelente evolución clínica. Su objetivo es la oclusión de la arteria aferente (única o múltiple) con el fin de excluir la comunicación arteriovenosa patológica, preservando el máximo posible de parénquima funcionante. Las indicaciones de tratamiento se fundamentan en la elevada morbimortalidad histórica de estos pacientes. Fundamentalmente debido a complicaciones neurológicas, las cuales se observan hasta en 30% de los pacientes no tratados. A esto debemos sumarle las importantes secuelas neurológicas, muchas de ellas invalidantes, a las cuales quedan expuestos. A su vez, los mismos autores reportaron un riesgo de padecer un “stroke” de 1,5% por año si la MAVP presenta una arteria aferente con un diámetro igual o mayor de 3 mm(2-9). Los materiales más utilizados en la actualidad para la embolización son los coils(1-8) y los tapones vasculares(10,11). Los coils son espirales metálicas, expansibles, de diferentes diámetros y longitudes, según el vaso o estructura a tratar y que, por lo general, se encuentran recubiertos de fibras artificiales que aumentan su potencial trombogénico(12).
El tapón vascular de Amplazer es un dispositivo cilíndrico, autoexpansible, confeccionado con una malla metálica de alambre(10,11). Éste permite una oclusión más precisa y su posición puede verificarse antes de ser liberado; si ésta no es satisfactoria, se puede recolocar o retirar. Asimismo puede ser utilizado tanto en embolizaciones arteriales como venosas, presenta un menor riesgo de migración, se libera fácilmente y permite producir una oclusión completa con un solo dispositivo. De esta manera se disminuye el tiempo de embolización así como su costo en fístulas grandes(10,11). Los tres pacientes fueron sometidos a embolizacion con coils fibrilares de platino con excelente evolución clínica. Los casos 1 y 3 requirieron un segundo procedimiento en la evolución por haber alcanzado el tiempo máximo de contraste y presentar múltiples MAVP. Los efectos adversos presentados fueron menores, e incluyeron dolor torácico, tipo puntada de lado, las primeras 24 hs, de fácil control con antiinflamatorios no esteroideos. La mejoría sintomática y fisiopatológica de la insuficiencia respiratoria fue inmediata en todos los casos, objetivada mediante gasometría arterial.
CONCLUSIONES
La sospecha clínica es capital para poder arribar al diagnóstico de esta infrecuente enfermedad. Ante su sospecha se recomienda realizar una angioTC, de ser posible, con reconstrucción en 3 dimensiones. Ante la persistencia de la sospecha diagnóstica o no contar con angioTC se debe continuar la evaluación mediante una arteriografía pulmonar. Se recomienda en la actualidad realizar tratamiento a todas las MAVP con una arteria aferente mayor o igual de 3 milímetros de diámetro, independientemente de su sintomatología(2,9). Algunos autores extienden esta indicación a todas las MAVP que presenten prueba con ecocardiografía contrastada con burbujas positiva(8).
BIBLIOGRAFÍA
1. Gossage JR, Kanj G. Pulmonary arteriovenous malformations: a state of the art review. Am J Respir Crit Care Med 1998; 158:643–661
2. White RI Jr, Pollak JS, Wirth JA: Pulmonary arteriovenous malformations: diagnosis and transcatheter embolotherapy. JVIR 1996; 7:787-804
3. Shovlin CL, Guttmacher AE, Buscarini E et al. Diagnostic criteria for hereditary hemorrhagic telangiectasia (Rendu-Osler-Weber syndrome). Am J Med Genet 2000; 91:66–67.
4. M.W.F. van Gent, M.C. Post, J.G.L.M. Luermans, R.J. Snijder, et al. Screening for pulmonary arteriovenous malformations using transthoracic contrast echocardiography: a prospective study. Eur Resp J 2009; 33: 85–91
5. Remy, J., M. Remy-Jardin, F. Giraud, and L. Wattinne.. Angioarchitecture of pulmonary arteriovenous malformations: clinical utility of three-dimensional helical CT. Radiology 1994; 191:657–664.
6. Terry, P. B., R. I. White, K. H. Barth, S. L. Kaufman, et al . Pulmonary arteriovenous malformations: physiologic observations and results of therapeutic balloon embolization. NEJM1983; 308:1197–1200
7. Maki DD, Siegelman ES, Roberts DA et al Pulmonary arteriovenous malformations: three dimensional gadolinium-enhanced MR angiography-initial experience. Radiology 2001; 2 19(1):243-24
8. M. Grosso F. Groppo Marchisi F. Testa G. et al Pulmonary arteriovenous malformations: percutaneous treatment preserving parenchyma in high-flow fistulae. Radiol Med 2008; 113:395–413
9. Hsu Charlie TC, Kwan Gigi, Shane Thompson A, et al. Terapia de embolización de las malformaciones arteriovenosas pulmonares. Base de Datos Cochrane de Revisiones Sistemáticas. Disponible en: http// www.labibliotecacochrane.com/ número 04, art. N º CD008017. DOI: 10.1002/14651858.CD008017
10. White RI Jr: Re: Bilateral multiple pulmonary arteriovenous malformations: endovascular tratment with the Amplatzer vascular plug. J Vasc Interv Radiol 2006;17(1):141-145
11. Ferro C, Rossi UG, Bovio G, et al: Percutaneous transcatheter embolization of a large pulmonary arteriovenous fistula with an Amplatzer vascular plug. Cardiov Interv Radiol 2007;30(2):328-331
12. Adrian Pick, M.B., B.S., Claude Deschamps, M.D. Anthony W. Stanson, M.D.Pulmonary Arteriovenous Fistula: Presentation, Diagnosis, and Treatment .W J Surg 1999; 23(11).