Introducción
La anestesia espinal se comenzó a utilizar a principios del siglo XIX, para bloquear los movimientos y el dolor de los pacientes durante diferentes procedimientos quirúrgicos.
Hoy en día la anestesia espinal, es parte del quehacer habitual del anestesiólogo, debido a su alto grado de eficacia y seguridad.
Su objetivo es depositar anestésicos locales y/o coadyuvantes en el espacio subaracnoideo, bloqueando la transmisión de impulsos nerviosos hacia el nivel cefálico, donde éstos son procesados e integrados para generar una respuesta de bloqueo tanto sensitivo como motor. Podemos emplear múltiples coadyuvantes para potenciar este efecto, siendo los principales hoy en día los opioides y la epinefrina, que actúan en receptores específicos a nivel del asta posterior medular.
Es bien conocido que la anestesia espinal genera cambios hemodinámicos ampliamente descritos en la literatura, caracterizados principalmente por hipotensión y bradicardia 1).
Fisiología del bloqueo
Estudios realizados hace ya más de 50 años, tanto en animales como humanos indican que una reducción tanto en la resistencia vascular periférica como esplácnica contribuyen de manera importante a la hipotensión secundaria a la anestesia espinal 2)(3).
El bloqueo neuroaxial impide la conducción de impulsos desde la periferia hacia el nivel central. El anestésico local depositado va a bloquear canales de sodio, así como hiperpolarizar neuronas, principalmente actuando sobre canales de calcio inhibiendo la liberación de sustancia P y diferentes neurotransmisores en las neuronas del asta posterior.
La anestesia neuroaxial también va a provocar una simpatectomía variable según la masa de drogas y coadyuvantes 4).
De acuerdo al grosor de las fibras nerviosas, el bloqueo es secuencial, siendo mas rápido y requiriendo una menor concentración de anestésico local en las fibras más delgadas, como las correspondientes al sistema simpático y las que transmiten dolor y temperatura. Las fibras más gruesas que transmiten impulsos motores y del tacto van a requerir más tiempo o mayores concentraciones de anestésicos.
Se ha planteado que la magnitud de los efectos hemodinámicos va a tener una directa relación con la altura del bloqueo. Bloqueos iguales o inferiores a un nivel T10 tienen mínimos efectos cardiovasculares. Las fibras cardioaceleradoras (simpáticas) del corazón tiene origen entre T1 a T4. Así si el bloqueo alcanza alturas superiores se puede agravar la hipotensión secundaria a éste al imposibilitar un aumento de frecuencia cardíaca compensadora del fenómeno vasodilatador.
Hipotensión
El 60-70% del volumen sanguíneo se encuentra almacenado en los vasos venosos. Frente a la pérdida del tono vasomotor secundaria a la denervación simpática propia del empleo de anestésicos locales en la anestesia espinal, se produce una redistribución del flujo sanguíneo central, principalmente a la circulación esplácnica, y en menor medida, a las extremidades inferiores. El tono arteriolar se ve afectado en menor medida. Este fenómeno incidiría directamente en disminuir el retorno venoso y en la precarga, generando hipotensión.
Bradicardia
La frecuencia cardíaca es coordinada a nivel del tronco cerebral, en el centro vasomotor, en la médula oblonga. Los centros cardioacelerador y cardioinhibidor, tienen vías de acción distintas; el primero principalmente a través de fibras simpáticas originadas desde los ganglios simpáticos torácicos, y el segundo por medio de vías originadas en el núcleo dorsal del vago. El bloqueo simpático asociado a niveles anestésicos superiores a la quinta vértebra torácica, bloquea las fibras cardioaceleradoras, limitando el efecto antagonista de estas frente a los estímulos cardioinhibitorios, gatillando una bradicardia leve a moderada.
Un efecto bradicardizante más intenso se puede explicar por el efecto de 3 reflejos, los cuales pueden llegar a producir una asistolía:
El estiramiento de las células marcapaso en el nodo sinoauricular gatilla una mayor frecuencia de depolarización, con el aumento de frecuencia cardiaca. Una disminución en la precarga genera el efecto contrario.
El segundo reflejo se gatilla al estirar baroreceptores ubicados a nivel auricular y de la unión cava-auricular. Al distenderse, generan estímulos aferentes al centro vasomotor, el que estimula fibras cardioaceleradoras. No existe una vía eferente vagal para este reflejo, por lo que una disminución en el retorno venoso va a resultar en una disminución en la estimulación final de las fibras cardioaceleradoras, induciendo una disminución en la frecuencia cardiaca.
El tercer reflejo es el de Bezold -Jarish. Éste está mediado por receptores ubicados en la pared inferoposterior del ventrículo izquierdo. Se puede interpretar como una alteración de la respuesta fisiológica a la disminución del retorno venoso. Al disminuir la precarga del ventrículo izquierdo, baja su volumen, pero simultáneamente aumenta su contractilidad, que es interpretada por los baroreceptores como un aumento de tensión transmural secundaria a distensión ventricular. Esta distensión genera aferencias vagales, las cuales van a generar una mayor respuesta del centro vasomotor, produciendo bradicardia, así como una disminución del estímulo simpático, principalmente a nivel torácico que genera vasodilatación.
La suma de estos factores, determina que la hipotensión y la bradicardia sean efectos esperables y comunes en mayor o menor medida, dependiendo de los valores definidos para diagnosticarla. Se ha definido en la literatura una baja en la presión en un 30%, o bien una presión sistólica bajo 85-90 mmHg ; así como una frecuencia cardíaca menor a 50 latidos por minuto 5,6).
En diferentes estudios realizados de manera invasiva y hace bastantes años, como ya se mencionó, se ha podido establecer que a pesar de esta disminución en el retorno venoso y en la resistencia vascular periférica, el gasto cardíaco tendería a mantenerse constante, conservándose la entrega de oxígeno a los tejidos.
Hoy en día contamos con una herramienta nueva para monitorización hemodinámica no invasiva, la ecocardiografía transtorácica, que permitiría volver a estudiar, evaluar y medir los cambios que se producen en la fisiología cardíaca luego de una anestesia espinal.
La ecocardiografía:
La ecografía (del griego «ἠχώ» ēkhō="eco", y «γραφία» grafía= "escribir"), o ultrasonografía, es una técnica imagenológica que se basa en la emisión de ultrasonidos, es decir sonidos cuya frecuencia se encuentra muy por sobre la capacidad auditiva humana, y la reflexión diferencial que éstos tienen en los distintos tejidos y estructuras. Al analizar estos ecos podemos representar las estructuras reflejadas con diferentes tonalidades de grises.
Necesitamos un emisor/receptor de estas ondas; el transductor, que apoyamos en la superficie y lo direccionamos de acuerdo al tejido que buscamos ver.
El ultrasonido se caracteriza por que puede ser dirigido como un haz, y este haz puede ser reflejado o transmitido según la densidad de los tejidos que atraviesan. En el transductor se encuentra un receptor para estos reflejos, por lo que computacionalmente podemos agrupar y construir imágenes.
La incorporación de la ecocardiografía transtorácica para monitorización hemodinámica perioperatoria es relativamente reciente. Se ha demostrado su utilidad para el manejo de pacientes con compromiso severo de su estado hemodinámico en su postoperatorio 7). También se ha utilizado en el preoperatorio con éxito 8. Pero es durante el intraoperatorio donde puede prestar una gran utilidad, pues permitirá observar de manera directa, no invasiva y focalizada lo que ocurre con el corazón y sus grandes vasos frente a distintos tipos de anestesia y frente a cambios en el estado hemodinámico.
Conociendo así la factibilidad de realizar evaluación hemodinámica con ecocardiografía transtorácica, se plantea reactualizar y volver a estudiar en modelos humanos los efectos a nivel cardiovascular de una anestesia espinal. Así, teniendo presente que el gasto cardíaco (GC) es uno de los parámetros fundamentales de la hemodinamia se decide estudiar los efectos de la anestesia espinal sobre él.
Objetivo primario: Medir con ecocardiografía transtorácica el gasto cardíaco basal y luego de una anestesia espinal en pacientes con corazón sin patología cardiovascular previa, y así evaluar el comportamiento del GC luego de la instalación de una anestesia espinal.
Objetivo secundario: Evaluar la factibilidad de contar con las ventanas ecocardiográficas adecuadas que permitieran realizar las mediciones de GC en pacientes sometidos a cirugía.
Material y Método
De manera prospectiva se estudiaron pacientes ASA I propuestos para cirugía bajo anestesia espinal. Se seleccionó este grupo de pacientes para poder descartar patologías cardiovasculares que pudieran dificultar o agravar tanto la evaluación ecocardiográfica como la respuesta frente a la anestesia espinal.
Todos los pacientes contaban con consentimiento informado escrito. El estudio fue aprobado por la comisión de ética de nuestro hospital.
Se excluyeron aquellos los casos en que durante el examen ecocardiográfico basal se detectó patología cardiovascular previamente no descrita.
Se empleó el ecógrafo SonositeMicromaxx y Sonosite Turbo con un transductor cardiológico P17 y P21 de 5 Mhz phasedarray. Para realizar este trabajo se utilizó un protocolo focalizado de ecocardiografía que se ha descrito en la literatura. Se trata de un examen que corresponde a una evaluación dirigida tendiente a contestar preguntas concretas sobre eventuales causales de compromiso de la función cardíaca perioperatoria 9). Para realizar esta ecocardiografía transtorácica focalizada se utilizan 3 ventanas en que se coloca el transductor, pudiendo obtenerse visiones en eje corto, es decir paralelas al eje más corto del corazón, o bien en eje largo, que correspondieron al eje más largo del corazón (Figura 1).
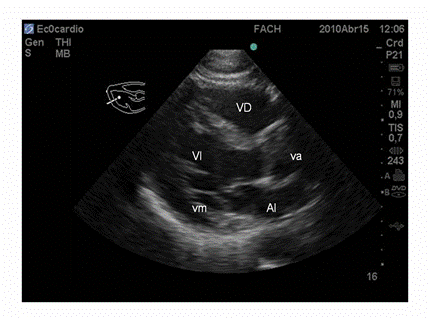
Figura 1: Eje largo del ventrículo izquierdo (VI). VD = ventrículo derecho, va = válvula aórtica, vm = válvula mitral, AI = aurícula izquierda
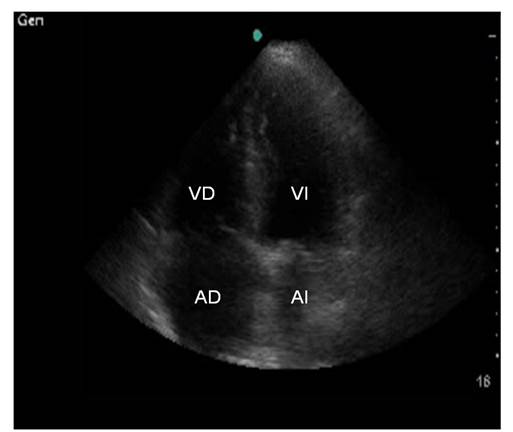
También se utilizaron visiones del eje apical en que se obtienen imágenes en 4 cámaras (ambas aurículas y ventrículos) y de 5 cámaras (ambas aurículas, ambos ventrículos y tracto de salida del ventrículo izquierdo) (Figura 2).
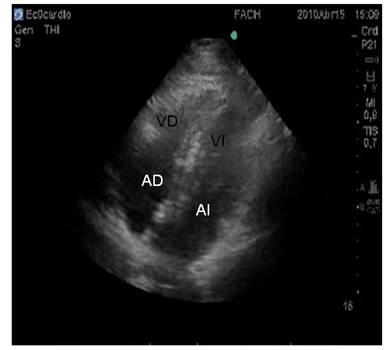
En nuestro estudio empleamos principalmente la ventana paraesternal izquierda y apical en 5 cámaras. (Figura 3)
Ventana paraesternal izquierda
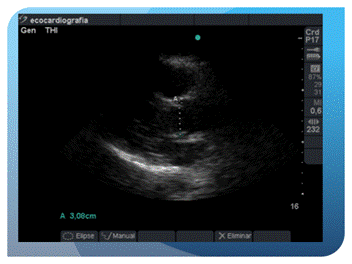
Se colocó el transductor en la región paraesternal izquierda, entre la 3º y la 4º costilla. En este eje largo evaluamos el ventrículo izquierdo (VI), ventrículo derecho, aurícula izquierda y las válvulas mitral y aórtica. La medición fundamental que se realizó a este nivel fue el tracto de salida del VI, justo por debajo de la válvula aórtica Utilizando la ventana paraesternal izquierda se midió el diámetro del tracto de salida (la mitad del diámetro corresponde al radio = r) del ventrículo izquierdo y se le calculó su área.(Figura 4).
Ventana apical
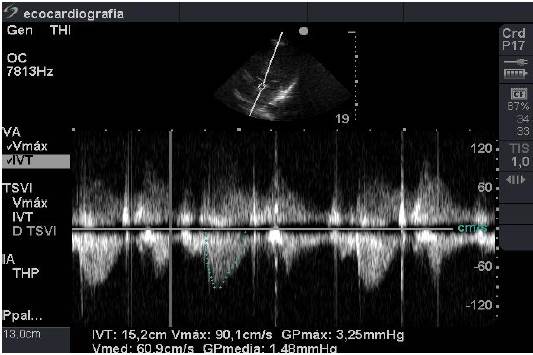
Se ubicó el transductor a nivel del ápex cardiaco, en la parrilla costal izquierda, bajo la mamila del mismo lado. Al orientar el transductor obtuvimos una imagen en 4 y 5 cámaras. En esta visión se realizaron las mediciones de la velocidad del tracto de salida con Doppler continuo, ya que en este lugar se logró una alineación paralela entre el flujo sanguíneo y el transductor, minimizándose la probabilidad de errores en la medición (Figura 5).
Empleando estas ventanas, obtuvimos la información suficiente para calcular el gasto cardiaco.
Cálculo de Gasto cardíaco
El gasto cardiaco se obtuvo midiendo flujo a través de esta área conocida.
Para obtener el flujo deberíamos poder medir todas las partículas que conforman la sangre, lo que es imposible. Para resolver este problema se midió con Doppler continuo la integral de la velocidad máxima del tracto de salida (IVT), en una ventana apical en cinco cámaras. Al multiplicar IVT por su área se obtuvo el volumen de eyección (VE) que se multiplicó por la frecuencia cardíaca (FC), obteniéndose el GC.
Todas estas mediciones se realizaron con el paciente monitorizado, sin sedación y en decúbito dorsal.
Luego se instaló la anestesia espinal utilizando una mezcla estandarizada con chirocaína al 0,5% (7.5-10mg) y fentanyl 20 microgramos en un volumen entre 2,5 y 3 ml., dependiendo de la altura del paciente.
El mismo examen ecocardiográfico para medir GC se realizó una vez comprobada la instalación del bloqueo espinal, al momento de iniciarse la cirugía.
Se restringió el aporte de volumen entre ambas mediciones a 5-7 ml/ kg de solución ringer lactato, y no fue necesario empelar drogas vasoactivas durante este período.
Análisis estadístico:
En el análisis estadístico se utilizó software STATA 10.0. Los datos se expresaron como promedios ±desvio estándar (DS). Para el cálculo del tamaño muestral se estimó que una diferencia de un 20% entre las mediciones basales y las realizadas después de instalada la anestesia espinal como significativas, con un poder de 80%. Para esto el tamaño muestral resultó en 28 pacientes. Se utilizó una prueba para docimar las diferencias entre muestras pareadas, en el análisis de los datos ecocardiográficos antes y después de la anestesia espinal. Se definió Ho estableciendo inexistencia de diferencias entre los valores hemodinámicos y ecocardiográficos antes y después de la anestesia espinal. Para comprobar diferencias entre grupos se utilizó análisis de varianza (ANOVA) clásico o paramétrico para los datos con distribución normal y la prueba de Kruskal - Wallis para las distribuciones no paramétricas. Se consideró un p < 0,05 como estadísticamente significativo.
Resultados
Se estudió un total de 52 pacientes (Tabla 1), en sólo 2 no hubo ventanas ecocardiográficas satisfactorias para poder ser incluidos en el estudio. La edad promedio fue de 44,8 ± 11 años.
Tabla 1: Características de la población
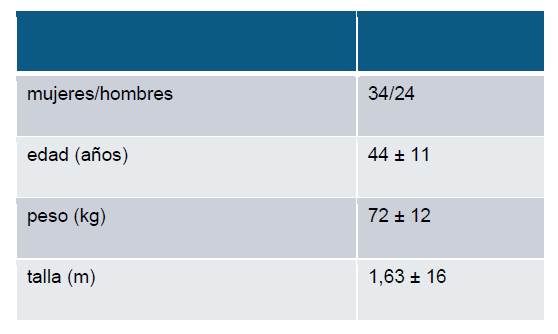
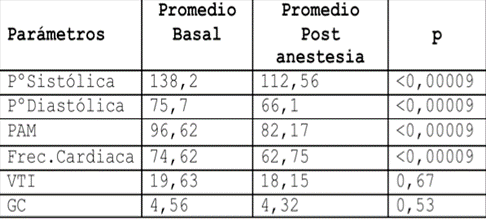
En todos los casos se realizó la cirugía con el bloqueo espinal. El nivel de bloqueo alcanzado fue T6 en un 36,36% de los casos y T4 en un 32,73%. Las variaciones de la presión arterial sistólica, diastólica y frecuencia cardíaca tuvieron una disminución estadísticamente significativa (Tabla 2).
No se observó una diferencia significativa en el GC previo y posterior a la anestesia espinal. La altura sensitiva máxima del bloqueo subaracnoideo tampoco se correlacionó con la disminución de la PAM ni con los parámetros ecocardiograficos.
Discusión
En este estudio realizado con ecocardiografía transtorácica a pacientes sanos sometidos a anestesia espinal, no se demostró una variación significativa del gasto cardíaco después de la instalación de ésta.
Eso sí, la anestesia espinal produjo una categórica disminución en la presión arterial y en la frecuencia cardíaca, lo que es concordante por las descripciones existentes en la literatura, parámetros obtenidos de manera invasiva. Esta concordancia valida la ecografía transtorácica como una manera fiel de medir variables hemodinámicas en cada momento y así el uso de la ecocardiografía transtorácica intraoperatoria permitió el estudio directo y real de la fisiología cardiovascular.
La mantención del gasto cardíaco se puede deber principalmente a un efecto beneficioso en la contractilidad del miocardio, optimizando eventualmente la diástole y la funcionalidad miocárdica.
En anestesiología es fundamental la monitorización hemodinámica en el perioperatorio. La ecografía transtorácica permite evaluar en tiempo real la función cardíaca de los pacientes, en el preoperatorio, en el intraoperatorio o bien en el postoperatorio en todos aquellos pacientes a los que se pueda acceder al tórax.
La ecografía transtorácica presenta algunas ventajas comparativas con la transesofágica, como el hecho de ser más accesible para todos los anestesiólogos, por lo simple en su realización, rápida realización y medición en tiempo real 9). Probablemente la gran ventaja de la ecografía en general, es que permite visualizar de manera directa y en tiempo real el corazón y sus grandes vasos y así permite estimar volúmenes y presiones.
Sloth y sus colaboradores 10 publicaron una serie de 232 pacientes que en su periodo postoperatorio presentaron compromiso hemodinámico severo. Con la utilización de ecocardiografía transtorácica y utilizando un protocolo focalizado fueron capaces de manejar estos casos en más del 40% de ellos de manera exitosa. Por otra parte Cowie 11 evaluó el uso de ecocardiografía transtorácica por un periodo de tres años, recomendando y sustentando su alta utilidad, tanto en el periodo postoperatorio, como durante el intraoperatorio. Nuestro grupo de trabajo también evaluó la factibilidad de realizar ecocardiografía focalizada perioperatoria demostrándose su gran utilidad sobre todo durante el intraoperatorio 12).
Las principales debilidades de este estudio corresponden a que siempre son necesarias imágenes de buena calidad para así poder minimizar los errores al momento de medir. Tampoco fue posible posicionar al paciente en decúbito lateral izquierdo, pero se determinó que a pesar de no poder posicionar al paciente de manera ideal, como se ha descrito, en decúbito lateral izquierdo, ni de tener un acceso óptimo al tórax del paciente (por los campos quirúrgicos), fue posible en casi todos ellos (98%) obtener dos ventanas, las cuales permitieron realizar la medición del gasto cardíaco.
Conclusión:
La ecocardiografía transtorácica (ETT) es una herramienta útil, que permite el estudio de variables hemodinámicas como el gasto cardíaco. En el futuro la ETT puede ser una herramienta de estudio para evaluar qué ocurre con diferentes fármacos anestésicos y diferentes tipos de pacientes (obstétricas, cardióptas) de manera no invasiva y en tiempo real13)(14