Services on Demand
Journal
Article
Related links
Share
Anestesia Analgesia Reanimación
On-line version ISSN 1688-1273
Anest Analg Reanim vol.22 no.2 Montevideo Dec. 2009
Rotación a metadona para el dolor por cáncer: estudio prospectivo
Dra. Patricia Papa de la Rosa*
Unidad de Cuidados Paliativos. Médica Uruguaya
Montevideo-Uruguay
Dra. Patricia Papa de la Rosa
Araucana 1379
E-mail: papapatr@adinet.com.uy
* Médica Anestesióloga
Departamento de Anestesiología y Terapia del Dolor
Sanatorio Médica Uruguaya
RESUMEN
El objetivo de este estudio fue evaluar los beneficios de la rotación de morfina a metadona oral en pacientes con poca respuesta analgésica o efectos adversos derivados de la morfina.
Diecisiete pacientes con cáncer avanzado que recibían morfina por dolor no controlado o efectos adversos severos fueron rotados a metadona cada ocho o doce horas, según un esquema de rotación rápida utilizando diferentes dosis ratios. La intensidad del dolor y efectos adversos fueron evaluados diariamente y comparados antes y después del cambio. Se documentó la dosis de morfina prerrotación, la dosis media inicial de metadona, dosis al séptimo día así como la dosis media final.
Antes de la rotación la dosis media equivalente de morfina oral fue 118.71 mg/día, luego de la misma la dosis media inicial de metadona fue de 17.94 mg/día, al séptimo día fue 27.06 mg/día y la dosis media final de metadona fue 34.12 mg/día. Los motivos de la rotación fueron: dolor no controlado, efectos adversos limitantes o la suma de ambos. Se encontraron mejorías significativas en la analgesia (p<0.05) así como alivio sintomático relevante en los efectos adversos. Se registraron efectos colaterales debidos a la utilización de metadona en ocho pacientes que revirtieron con el tratamiento sintomático.
La metadona demostró ser una opción terapéutica válida para el grupo de pacientes estudiados. Se recomienda precaución en la rotación a metadona en pacientes tolerantes a altas dosis de opioides.
palabras clave
Opioides, dosis ratio, rotación de opioides, toxicidad opioide, metadona.
SUMMARY
The aim of this study was to evidence the clinical benefits of switching from morphine to oral methadone in patients who experience poor analgesia or adverse effects from morphine.
Seventeen advanced cancer patients receiving morphine but with uncontrolled pain or severe opioid adverse effects were switched to oral methadone administered every 8 or 12 hours according to a scheme of rapid switching using different dose ratios.
Intensity of pain and adverse effects were assessed daily and compared before and after switching. Pre switching doses of morphine, initial, day 7 and final methadone doses were recorded.
Before the switch, the median equivalent daily dose of morphine was 118.71 mg/day; after the switch the initial dose of methadone (median) was 17.94 mg/day, 27.06 mg/day at day 7 and the final dose of methadone (median) was 34.12 mg/day.
The reasons for switching were: uncontrolled pain, adverse effects or both. Significant improvements in pain (p<0.05) and relevant changes in adverse effects were reported. Methadone - related side effects reported in 8 patients were relieved after treatment.
In patients with cancer pain and/or adverse effects of oral methadone is a valid therapeutic option.
Caution is recommended when switching from any opioid to methadone, in patients who are tolerant to high doses of opioids.
key words
Opioids, dose ratio, opioid rotation, opioid toxicity, uncontrolled pain, methadone.
Resumo
O objetivo deste estudo foi avaliar os benefícios da passagem de morfina a metadona oral em pacientes com pouca resposta analgésica o efeitos adversos derivados da morfina.
Dezessete pacientes com câncer avançado que recebiam morfina por dor não controlada o efeitos adversos severos foram medicados com metadona cada 8 ou 12 horas, adotando um esquema de conversão rápida utilizando diferentes doses-ratios.
A intensidade da dor e efeitos adversos foi avaliada diariamente e comparados antes e depois da troca.
Foi documentado a doses de morfina pré-conversão, a doses media inicial de metadona, a dosagem ao dia 7, como também a doses media final.
Antes da troca a doses media equivalente de morfina oral foi de 118.71 mg/dia, logo após as doses media inicial de metadona foi de 17.94 mg/dia, ao dia 7 foi de 27.06 mg/dia e a doses final de metadona foi 34.12 mg/dia. O motivo da passagem a metadona foi: dor não controlada, efeitos adversos limitantes o a soma deles.
Foram encontradas melhorias significativas na analgesia (p<0.05) alem do alivio relevante dos efeitos adversos. Se registraram efeitos colaterais pela utilização da metadona em 8 pacientes que melhoraram com o tratamento sintomático.
A metadona demonstrou ser uma opção terapêutica valida para o grupo de pacientes estudados. Recomendamos cuidados na passagem a metadona em pacientes tolerantes a altas doses de opioides.
Unitermos: opioides, doses-ratios, troca de opioide, toxicidade opioide, metadona.
INTRODUCCIÓN
De acuerdo a las guías de la Organización Mundial de la Salud (OMS) los opioides, entre los que la morfina es la droga más utilizada, constituyen el pilar del tratamiento para el dolor moderado a severo por cáncer (1).
Un 10% a 30% de los pacientes presentan poca respuesta al tratamiento opioide durante la administración de rutina (2,3). Esto se debe a un fenómeno complejo relacionado a diversos factores como progresión de la enfermedad y desarrollo de tolerancia, tipo y características fisiopatológicas del dolor, acumulación de metabolitos activos, etcétera (4).
En la práctica los pacientes tratados con morfina pueden presentar alguna de las siguientes situaciones clínicas (5): 1- dolor controlado en presencia de efectos adversos intolerables, 2- dolor no controlado con efectos adversos limitantes derivados del incremento de la dosis del opioide, 3- dolor no controlado con el aumento continuo de morfina, pero sin aparición de efectos adversos. Varias estrategias terapéuticas han sido propuestas para el tratamiento de estas situaciones (4):
Ampliación de la ventana terapéutica con un manejo más agresivo de los efectos adversos (por ejemplo: uso de psicoestimulantes en la sedación por opiáceos).
Utilización de drogas adyuvantes o procedimientos invasivos que disminuyan los requerimientos de opioides (catéteres epidurales, bloqueos nerviosos).
Administración de un opioide alternativo para obtener un balance más favorable entre analgesia y toxicidad, ya que los pacientes que tienen pobre respuesta analgésica o tolerabilidad a un opioide frecuentemente toleran adecuadamente otro opiáceo.
La variabilidad en la respuesta analgésica o aparición de efectos adversos a diferentes opioides es un fenómeno común, y probablemente se deba al desarrollo de tolerancia cruzada incompleta entre opiáceos. En algunos pacientes la falta de respuesta a la morfina se debería al desarrollo de tolerancia farmacodinámica al opiáceo, la que se asume como una disminución del efecto analgésico debido a un proceso de adaptación neural.
Sin embargo, el desarrollo de tolerancia para los efectos analgésicos y para los efectos tóxicos se puede ver como eventos disociados en el tiempo durante la administración del opiáceo (4). En algunos pacientes la falta de respuesta analgésica a la morfina puede provenir del desarrollo de tolerancia analgésica, en tanto que no se desarrolla tolerancia a los efectos adversos en la misma magnitud; como consecuencia con el aumento de dosis de morfina se puede llegar a un nivel donde sus efectos colaterales sean intolerables, sin lograrse alivio del dolor.
La metadona es una buena alternativa analgésica en estos casos, ya que se trata de una droga liposoluble, con amplia distribución en los tejidos, lo que mantiene su concentración plasmática durante la administración crónica. Carece de metabolitos activos, siendo su eliminación independiente de la función renal. Presenta buena biodisponibilidad oral y larga vida media, sumadas a actividad antagonista sobre el receptor N-Metil D-Aspartato (NMDA) lo que aumenta su efectividad en los casos de tolerancia opioide. Además comparte actividad delta previniendo potencialmente la recaptación de monoaminas en el sistema nervioso (7).
A pesar de que la rotación a metadona es una práctica cada vez más frecuente en pacientes con poca respuesta analgésica a la morfina no hay una estandarización en cuanto a las modalidades de sustitución ni en la dosis ratio a utilizar (8,9).
El objetivo de este estudio fue evaluar los beneficios clínicos, en términos de mejoría en la respuesta analgésica y tolerabilidad de la rotación de morfina a metadona oral en pacientes tratados con morfina oral, intravenosa o subcutánea con dolor no controlado adecuadamente a pesar del aumento progresivo de dosis y/o efectos adversos intolerables.
PACIENTES Y MÉTODO
Se diseñó un estudio de tipo analítico, prospectivo desde marzo de 2008 a diciembre de 2009, para un grupo de 17 pacientes con cáncer avanzado tratados con morfina para el manejo del dolor por vía oral o subcutánea en quienes no se logró un control adecuado del mismo a pesar del aumento progresivo de la dosis y/o se comprobó aparición de efectos adversos limitantes a su uso sin respuesta al tratamiento sintomático.
El seguimiento promedio que se realizó a los pacientes en estudio fue de 77 ± 20 días con un mínimo de nueve días y un máximo de 365.
Se incluyeron pacientes ambulatorios o internados, mayores de 18 años, tratados con morfina oral, subcutánea o intravenosa para el control del dolor en los cuales el aumento progresivo de dosis no logró analgesia adecuada: Escala Visual Análoga (EVA) > 4 con interferencia en las funciones habituales del paciente y alteración del sueño. Se utilizó la Escala Visual Análoga, con una intensidad del dolor mayor a 4 en una escala numérica de 0 a 10, que es considerada un punto de corte válido para definir una población con dolor moderado a severo (10,11). También se usó en pacientes en quienes el tratamiento analgésico fue limitado por la aparición de efectos adversos severos no controlables con tratamiento sintomático: somnolencia, náuseas y vómitos, confusión, mioclonias, excitación, alucinaciones, delirium y constipación.
Se excluyeron pacientes con enfermedad renal o hepática severa, bajo Performance Status: Eastern Cooperative Oncology Group (ECOG) mayor a 3, deterioro cognitivo clínicamente evaluado y documentado previo al inicio del estudio o alteraciones mayores del medio interno.
Se mantuvieron las drogas adyuvantes consideradas adecuadas que eran administradas junto a la morfina durante el curso del estudio (corticoides, anticonvulsivantes, etcétera) y se agregaron otras drogas en el caso de considerarse apropiado durante el desarrollo del mismo.
De los 17 pacientes estudiados, antes del cambio 13 de ellos recibían morfina oral, tres pacientes morfina por vía subcutánea y uno, morfina intravenosa continua. Por razones comparativas todas las dosis de morfina fueron calculadas a sus dosis equivalentes diarias orales.
modalidad de rotación y dosis ratio utilizada
Se utilizó un esquema de rotación rápida (stop and go approach) (9) suspendiendo completamente la morfina y sustituyéndola por metadona. Se utilizó una dosis ratio de 4:1 (4mg morfina = 1 mg metadona) para aquellos pacientes que recibían una dosis ≤100 mg de morfina diarios (ocho pacientes). El resto fue rotado utilizando una dosis ratio de 8:1 (8 mg morfina = 1 mg metadona) para dosis de 100 mg a 300 mg (ocho pacientes) y 12:1 (12 mg morfina = 1 mg metadona para dosis mayores de 300 mg/día (un paciente). Luego de la dosis inicial la administración progresiva de metadona fue titulada para cada paciente según su respuesta clínica.
La metadona se administró por vía oral cada ocho o 12 horas. La aparición de dolor episódico se manejó con opiáceos de acción corta.
Los pacientes ambulatorios fueron monitorizados por medio de contactos telefónicos diarios y en policlínica, de modo de poder detectar precozmente la aparición de efectos adversos durante el proceso de sustitución.
recolección de datos y análisis estadístico
Se solicitó el consentimiento de la institución para la recolección de datos de los pacientes.
Para cada uno de ellos se documentó el sitio del tumor primario, presencia de metástasis, edad, sexo e intensidad del dolor así como efectos adversos relacionados con la morfina. Se consignó la dosis de morfina previa a la rotación y su ruta de administración, la dosis inicial de metadona, dosis al séptimo día, así como la dosis final que recibía el paciente al finalizar su seguimiento.
La intensidad del dolor fue medida diariamente usando una Escala Visual Análoga de autoevaluación (EVA) en una escala numérica de 0 a 10.
Los síntomas asociados con la terapia opioide (somnolencia, confusión, náuseas y vómitos, excitación, alucinaciones, mioclonias, delirium, constipación) fueron evaluados diariamente utilizando una escala numérica de 0 a 10.
La rotación fue considerada efectiva cuando la EVA para dolor disminuyó a menos de 4 y la intensidad de los efectos adversos se redujo a niveles clínicamente aceptables (10).
Para analizar cambios en variables ordinales se utilizó la prueba de Wilcoxon, para variables nominales el Test de Chi Cuadrado y para la comparación de medias de variables continuas el Test de T para muestras dependientes.
Se tomó como umbral para significación estadística un valor de α = 0.05.
RESULTADOS
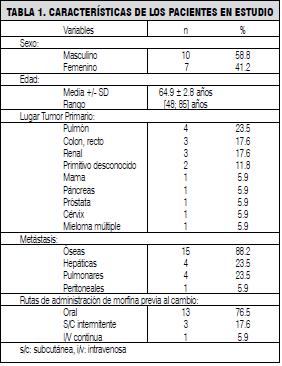
Desde marzo de 2008 a diciembre de 2009 los pacientes que cumplían los criterios de selección del estudio fueron rotados de morfina a metadona. La tabla 1 muestra las características de los pacientes: edad, sexo, lugar del tumor primario, presencia de metástasis y vías de administración de morfina.
En cuanto a los motivos de la rotación a metadona (como se muestra en la tabla 2), tres de los pacientes fueron rotados por dolor no controlado (con una puntuación de 9 y 10 en la EVA). La dosis media de morfina en éstos fue de 173.3 mg/día.
Seis pacientes fueron rotados por efectos adversos severos en presencia de aceptable control del dolor (EVA<4) y los ocho restantes fueron rotados por dolor no controlado asociado a la presencia de efectos adversos.
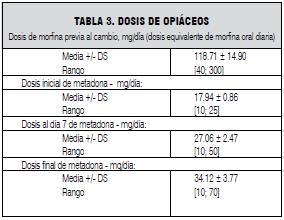
En la tabla 3 se muestra la dosis media de morfina oral (118.71mg/día) previa al cambio, la dosis media de metadona inicial (17.94 mg/día) luego de discontinuar la morfina y se documenta la dosis media de metadona a los siete días de la rotación (27.06 mg/día).
Se destaca que del grupo de 17 pacientes analizados, uno disminuyó un 33% la dosis inicial y dos de ellos mantuvieron estables las dosis de inicio.
La dosis final media de metadona (34.12 mg/día) corresponde al tiempo promedio de seguimiento (77± 20 días) presentando un incremento con respecto a la dosis media inicial de 16.18 mg.
Al fin del seguimiento un paciente mantuvo la disminución de la dosis inicial de un 33% (tiempo total: 30 días) y un paciente mantuvo estable la dosis inicial (tiempo total: 10 días).
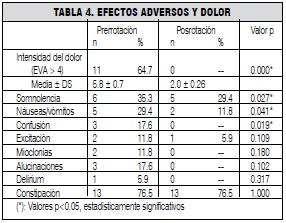
Respecto a la intensidad del dolor se verificó un descenso del valor promedio del EVA de 5.8 ± 0.7 a 2.0 ±0.3 posrotación. (Se detalla en la tabla 4). Tomando 4 como punto de corte para el EVA, en 11 pacientes que presentaban un valor mayor (variando de 5 a 10), se registró un valor menor a 4 luego de la rotación, que resulta estadísticamente significativo (p<0.05).
En este estudio se encontraron mejorías significativas en la analgesia, así como en la mayoría de los efectos adversos (tabla 4). Existió una importante reducción de la intensidad de los síntomas estudiados, específicamente modificaciones importantes en efectos adversos centrales como: somnolencia (p<0.05) y confusión (p<0.05).
En cuanto a los síntomas gastrointestinales mejoraron sustancialmente las náuseas y vómitos (p<0.05) aunque no se encontraron diferencias en cuanto a la constipación.
Se registraron efectos colaterales debidos a la utilización de metadona en ocho pacientes: somnolencia (cinco), confusión (uno), náuseas (uno) y delirium (1).
DISCUSIÓN
En un grupo de pacientes con cáncer avanzado y dolor severo, el tipo de analgésico y la ruta de administración o ambos deben ser cambiados una o más veces de modo que la terapia pueda ser individualizada para mejorar la analgesia, disminuir la toxicidad o ambos.
Es importante señalar que el dolor no controlado a pesar del aumento progresivo de la droga, en ausencia de elementos de toxicidad, es un punto controvertido para definir la rotación, dado que mayores aumentos podrían lograr analgesia adecuada. Sin embargo un aumento rápido del opiáceo fue reconocido como un factor negativo para lograr la respuesta clínica esperada, ya que aumenta las posibilidades de aparición de efectos adversos (5).
En los casos en que estos sean intolerables o se sumen a una falta de respuesta analgésica se recomienda realizar, en primera instancia, tratamiento agresivo de los mismos que permita aumentar la dosis analgésica y, si estas intervenciones fallan, debe considerarse la rotación de opioides.
El amplio espectro de la metadona la coloca como una droga alternativa específica cuando se requiere revertir la tolerancia opioide y suprimir el efecto de sensibilización central, como en los casos de dolor neuropático asociado. Se ha sugerido que el fenómeno de tolerancia cruzada asimétrica entre opioides además de involucrar selectividad diferencial a nivel de receptores opiáceos también podría deberse a las diferentes eficacias agonistas (4).
De acuerdo con esta teoría, a mayor reserva de receptores mayor eficacia intrínseca. La metadona presenta mayor eficacia que la morfina, debido a su mayor reserva de receptores (cantidad de receptores no ocupados por el opiáceo).
Se eligió como forma de rotación la discontinuación de la morfina e inicio inmediato de metadona (stop and go approach), dado que este tipo de sustitución permite una eliminación rápida de los metabolitos de la morfina, que se involucran como responsables de la toxicidad clínica.
Teniendo en cuenta que el tiempo de estabilización de la dosis de metadona (12) –tres días con la misma dosis pautada sin cambios y menos de tres rescates diarios– ha demostrado variabilidad según el motivo del cambio (dolor no controlado, dolor neuropático, neurotoxicidad, etcétera) (5) sumado a que esta droga requiere aproximadamente 48 horas para alcanzar niveles de equilibrio en sangre por su amplio volumen de distribución, se valoró la dosis media al séptimo día, documentándose el cambio en el dolor y efectos adversos en este punto.
Con respecto a las dosis ratio utilizadas para definir la dosis inicial de metadona y dado que esta puede ser hasta 10 veces más potente en pacientes que reciben dosis diarias mayores de 500 mg de morfina que en aquellos que reciben menos de 100 mg diarios (13), utilizamos una dosis ratio de 4:1 para el grupo de pacientes que recibía una dosis de morfina ≤ 100 mg/día, 8:1 para el grupo que recibía de 100 a 300 mg/día y 12:1 para las dosis de morfina > 300 mg/día. En todos los casos nos basamos en la dosis previa de morfina administrada al paciente dado que se comprobó que la proporción de dosis entre morfina y metadona varía claramente con la exposición previa a opioides (14) (15).
En este estudio no se correlacionaron las dosis de metadona con las razones del cambio (dolor no controlado, efectos adversos o ambos) pero, de acuerdo a estudios previos (10,12,), en presencia de dolor no controlado solo o asociado a efectos adversos se requerirían mayores dosis de metadona que las descritas en las tablas equianalgésicas utilizadas para lograr alivio de la sintomatología en menor tiempo. Esta puede ser una de la razones para el incremento del 50% en la dosis al séptimo día dado que el 17.7% (n: 3) de los pacientes estudiados fueron rotados por dolor no controlado y el 47% (n: 8) por la suma de dolor y efectos adversos.
La dosis media final de metadona tuvo un incremento de 16.18 mg con respecto a la inicial. Con el tratamiento prolongado es frecuente verse obligado a disminuir la dosis, en general por presentarse somnolencia excesiva (12). Este fue el efecto adverso más frecuente de la metadona encontrado en este estudio (29.4% de los pacientes) que revirtió con el uso de psicoestimulantes (metilfenidato), lo que probablemente permitió el aumento de la dosis en los casos necesarios.
En la práctica clínica, la indicación más común para la rotación es el desequilibrio entre analgesia y efectos adversos. En nuestro caso, la rotación fue considerada efectiva para disminuir la intensidad del dolor (p<0.05) y la mayoría de los efectos adversos disminuyeron luego de la rotación, siendo esta disminución estadísticamente significativa para náuseas y vómitos, confusión y somnolencia (p<0.05).
En el resto de los casos (mioclonias, delirium, alucinaciones, exitación) el valor p no mostró diferencias significativas, pero se constató una disminución de la puntuación de la escala numérica utilizada (0 a 10) que en todos los casos se expresó como una mejoría clínica del síntoma considerado o bien la desaparición de este luego de la rotación.
Esto puede ser debido al bajo tamaño muestral o a que el cambio consistió en la baja de 1 ó 2 puntos en la escala utilizada, por lo cual no se encuentra estadísticamente significación para el cambio. Es el caso de la excitación (dos pacientes) que disminuyó en un paciente y revirtió completamente en el otro; delirium (un paciente); mioclonias (dos pacientes) y alucinaciones (tres pacientes) que revirtieron totalmente posrotación.
La constipación se mantuvo incambiada; a pesar de que hay reportes que expresan una tendencia a la mejoría de este síntoma al utilizar metadona no lo pudimos comprobar en este estudio.
Respecto a los efectos adversos de la metadona registrados al séptimo día predominó la somnolencia (cinco pacientes) y luego náuseas (uno), confusión (uno) y delirium (uno).
De los cinco pacientes con somnolencia, cuatro de ellos requirieron psicoestimulantes (metilfenidato) para lograr la reversión del síntoma. Las náuseas y la confusión y delirium también respondieron a la medicación sintomática.
El episodio de delirium se registra en un paciente que es ingresado por descompensación de su enfermedad oncológica sumado a claros signos de deshidratación y disionías, instalando en la evolución un episodio severo de delirium que fue tratado con hidratación, corrección del medio interno y neurolépticos, suspendiéndose la metadona. Una vez revertido el cuadro se reinstaló la metadona a una dosis menor con buena tolerancia, siendo dado de alta a domicilio.
Debemos tener en cuenta en la interpretación de los resultados que, en el paciente oncológico con enfermedad avanzada y dolor o efectos adversos surgidos de su tratamiento, nuestro objetivo es lograr la mejor calidad de analgesia en el menor tiempo posible, por lo cual es difícil y/o éticamente imposible realizar estudios randomizados y controlados de acuerdo a las pautas de la medicina basada en la evidencia.
CONCLUSIONES
Para el grupo de pacientes estudiados, que en su mayoría experimentaban mal control del dolor sumado o no a efectos adversos con la administración de morfina, la rotación a metadona demostró ser una opción terapéutica válida que mejoró el nivel de analgesia de los mismos y redujo la incidencia e intensidad de efectos adversos.
El estudio realizado demuestra la efectividad de la rotación, de acuerdo al plan basado en las dosis previas de morfina.
El problema más importante que surge de la literatura acerca del tema continúa siendo la determinación de la dosis ratio equianalgésica en pacientes con poca respuesta a un opioide. De acuerdo con otros autores pensamos que las tablas equianalgésicas deben ser consideradas como guías útiles, pero que no toman en cuenta las amplias variaciones interindividuales ni los efectos adversos. Teniendo en cuenta la larga e impredecible vida media de la metadona (vida media beta de 15 a 60 horas) y su potencial toxicidad retrasada debe procederse con precaución en la rotación en un régimen que permita la observación cercana y eventuales ajustes de dosis individualizados para cada paciente.
AGRADECIMIENTOS
Agradezco a la Br. Anaulina Silveira, docente del Departamento de Métodos Cuantitativos, Facultad de Medicina, Udelar y a la auxiliar de Enfermería Lorena Rozano, de Médica Uruguaya, por su colaboración.
Bibliografía
1- World Health Organization. Cancer pain relief. 2nd ed. Geneva: World Health Organization, 1996
2- Mejía GE, Infante G, Delgado E. Rotación de morfina a metadona en domicilio: Descripción de cuatro casos. Rev Soc Esp Dolor 2007; 14(7): 486-9
3- Quigley C.Cambio de opiáceo para mejorar el alivio del dolor y la tolerancia del fármaco (Revisión Cochrane traducida). In: La Biblioteca Cochrane Plus. 2008; Número 2. Oxford Update Software Ltd
4- Mercadante S. Opioid rotation for cancer pain: rationale and clinical aspects. Cancer 1999;86(9):1856-66
5- Mercadante S, Bruera E. Opioid switching: a systematic and critical review. Cancer Treat Rev 2006; 32 (4): 304-15
6- Mammana G, Bertolino M. Rotación o sustitución. In: Leone F. Guía para la utilización de analgésicos opioides. Buenos Aires, La Letra. 2004; p. 119-68
7- Ripamonti C, Bianchi M. The use of methadone for cancer pain. Hematol Oncol Clin North Am 2002;16(3): 543-55
8- Papa MP. Modalidades de rotación morfina a metadona en pacientes con dolor oncológico. Rev Med Urug 2009; 25:124-30
9- Mercadante S, Casuccio A, Calderone L. Rapid switching from morphine to methadone in cancer patients with poor response to morphine. J Clin Oncol 1999: 17(10): 3307-12
10- Mercadante S, Casuccio A, Fulfaro F, Groff L, Boffi R, Villari P, et al. Switching from morphine to methadone to improve analgesia and tolerability in cancer patients: a prospective study. J Clin Oncol 2001; 19(11): 2898-904
11- Serlin RC, Mendoza TR, Nakamura Y, Edwuards KR, Cleeland CS. When is cancer pain mild, moderate or severe? Grading pain severity by its interference with function. Pain 1995;61(2):277-84
12- Centeno C, Sánchez R, Vara F. Metadona en el tratamiento del dolor por cáncer: experiencia del Hospital Los Montalvos, Salamanca. Med Pal 2004;11(2): 157-63
13- Bruera E, Sweeney C. Methadone use in cancer pain: a review. J Palliat Med 2002; 5(1): 127-38
14- Ripamonti C, Groff L, Brunelli C, Polastri D, Stavrakis A, De Conno F. Switching from morphine to oral methadone in treating cancer pain: what is the equianalgesic dose ratio? J Clin Oncol 1998; 16(10): 3216-21
15- Pereira J, Lawlor P, Vigano A, Dorgan M, Bruera E. Equianalgesic dose ratios for opioids: a critical review and proposals for long term dosing. J Pain Symptom Manage 2001; 22 (2): 672-87