Serviços Personalizados
Journal
Artigo
Links relacionados
Compartilhar
Anestesia Analgesia Reanimación
versão On-line ISSN 1688-1273
Anest Analg Reanim vol.20 no.1 Montevideo ago. 2005
Analgesia intratecal con morfina-fentanil en cirugía cardíaca
Dra. Anabella Samaniego1, Dr. Pablo Mourelle1,
Dr. Juan Riva2, Dr. Hugo Piñeyro3
1 Asistente Departamento y Cátedra de Anestesiología.
2 Prof. Adjunto Departamento y Cátedra de Anestesiología.
3 Asistente Departamento y Cátedra de Cirugía Cardíaca.
Trabajo realizado en: Departamento y Cátedra de Anestesiología y Departamento y Cátedra de Cirugía Cardíaca. Hospital de Clínicas "Dr. Manuel Quintela". Facultad de Medicina. Universidad de la República.
Correspondencia: Dra. Anabella Samaniego
E-mail: anizzettee@hotmail.com
resumen
objetivo
Evaluar los efectos analgésicos intra y posoperatorios de la administración intratecal de morfina y fentanil, en cirugía cardíaca.
material y métodos
Estudio prospectivo, randomizado, controlado, simple ciego. Se analizaron 21 pacientes coordinados para cirugía cardíaca. Diez pacientes (grupo intratecal: IT) recibieron 1mcg/kg de fentanil más 500 mcg de morfina intratecales, previo a la inducción anestésica. Once pacientes (grupo control: C) no recibieron opiáceos intratecales.
resultados
No hubo diferencias estadísticamente significativas en: características demográficas y quirúrgicas, consumo de fármacos intraoperatorios ni en las variables hemodinámicas intraoperatorias. Se observó una menor intensidad de dolor, significativamente diferente para las 24 horas y menor consumo de analgésicos posoperatorios en el grupo IT.
Los tiempos de extubación fueron más prolongados y la PaCO2 posoperatoria fue más elevada, pero en forma no significativa en el grupo IT. Un paciente requirió apoyo ventilatorio no invasivo por 12 horas.
conclusiones
La combinación de 1mcg/kg de fentanil más 500 mcg de morfina intratecales determinó analgesia posoperatoria.
palabras claves
Opiáceos intratecales.
Morfina.
Fentanil.
Cirugía cardíaca.
Analgesia posoperatoria.
summary
purpose
To evaluate the intra and postoperative effect of an intrathecal combination of morphine and fentanil during cardiac surgery.
methods
A prospective, randomized, single-blind and controlled study was carried out. 21 patients undergoing cardiac surgery were analyzed: 10 patients (Intrathecal group: I T) received a spinal injection of 500 mcg of morphine plus fentanil 1mcg/kg before anesthetic induction. 11 patients (control group:C) did not receive intrathecal opioids.
results
Patient and surgery characteristics, operative drugs consumption and hemodynamic variables were similar in both groups.
Pain intensity and analgesics consumption were significantly lower in the IT group within the first 24 hours in the post-operative period. Even though higher paCO2 values and extubation time were observed in the IT group they were not significant.. One patient required 12 hours of non-invasive respiratory support.
conclusions
Morphine (500 mcg) combined with fentanil (1mcg/kg) provided post-operative analgesia.
key words
Intrathecals opiods.
Morphine.
Fentanil.
Cardiac surgery.
Postoperative analgesia.
resumo
objetivo
Avaliar os efeitos analgèsicos intra e pós-operatórios da administração
Intratecal de morfina e fentanil, em cirurgia cardíaca.
material e método
Estudo prospectivo, randomizado, controlado, simples cego.
Foram analisados 21 pacientes eletivos para cirurgia cardíaca.
10 pacientes (grupo intratecal: IT) receberam 1mcg/Kg de fentanil mais 500 mcg de morfina intratecais, previamente a indução anestésica.
11 pacientes (grupo controle: C) não receberam opioides intratecais.
resultados
Não houve diferença estatisticamente significativa em: características demográficas e cirúrgicas, consumo de fármacos intraoperatórios, tão pouco nas variáveis hemodinâmicas intraoperatórias. Se observou uma menor intencidade de dor, significativamente diferente nas primeiras 24 hs e menor consumo de analgésicos postoperatórios no grupo IT. Os tempos de extubação foram mais prolongados e a PaCO2 pós-operatória foi mais elevada, mas de forma não significativa, no grupo IT. Um paciente necessitou apoio ventilatório não invasivo por 12 hs.
conclusões
A combinação de 1mcg/Kg de fentanil mais 500 mcg de morfina intratecais determinou analgesia pósoperatória.
unitermos
Opioides intratecales.
Morfina.
Fentanil.
Cirurgia cardíaca.
Analgesia pósoperatoria.
introducción
Existe un marcado incremento del uso de anestesia y/o analgesia regional en cirugía cardíaca (CC). Las técnicas peridurales han mostrado como ventaja una intensa analgesia intra y posoperatoria, atenuación de la respuesta al estrés y reducción de isquemia miocárdica perioperatoria por su efecto simpaticolítico(1-3).
Sin embargo presentan el riesgo potencial de hematoma peridural secundario a la heparinización total. Esto ha llevado a utilizar técnicas raquídeas con morfina, que permiten reducir significativamente el tamaño de las agujas y por tanto del traumatismo(4).
Si bien los resultados son prometedores con respecto a la analgesia posoperatoria(5-7) y parciales en la atenuación al estrés(8), presenta la limitación de que el pico máximo de inicio de acción de la morfina intratecal puede demorar hasta seis horas. Por tanto los máximos estímulos (intubación orotraqueal, incisión de piel, esternotomía y pericardiotomía) ocurren antes de que se alcance esa concentración. Algunos autores ven el agregado de opiáceos más liposolubles, con un inicio de acción más rápido, lo que permitiría corregir esta limitación(8-10)..
El objetivo del presente estudio prospectivo fue evaluar los efectos de la administración intratecal única de morfina y fentanil sobre el dolor intra y posoperatorio en CC.
pacientes y métodos
Se realizó un estudio prospectivo, controlado, al azar y simple ciego.
El proyecto fue aprobado por el Comité de Ética del Hospital de Clínicas. Previa solicitud de consentimiento informado a los pacientes, se seleccionaron de acuerdo a los siguientes criterios:
1) Criterios de inclusión: pacientes coordinados para cirugía de revascularización coronaria con o sin circulación extracorpórea o cambio valvular de elección.
2) Criterios de exclusión: pacientes que no cumplan con los criterios anteriores, coordinados para cirugía de aorta torácica, combinados, reintervenciones, que presenten contraindicaciones para las técnicas regionales, Fracción de Eyección (FE) menor a un 40%, apoyo de balón intraórtico, necesidad de ventilación mecánica durante el preoperatorio o patología médica asociada que condicionen ventilación mecánica posoperatoria.
Si el paciente recibía medicación anticoagulante se procedió de acuerdo al siguiente esquema, con:
- Warfarina: se suspendió siete a 10 días antes de la cirugía, sustituyéndose por heparina según protocolo del servicio de cirugía cardíaca.
- Aspirina o clopidogrel: se suspendió siete a 10 días antes de la cirugía.
- Heparinas de bajo peso molecular: se suspendieron 24 horas antes.
- Heparinas estándar: se suspendieron ocho horas antes.
En todos los casos se exigió estudio de la crasis sanguínea y recuento plaquetario normal el día de la cirugía.
Cumplidos estos criterios los pacientes fueron asignados al azar en dos grupos: Grupo Control (C) a los que se les realizó anestesia intravenosa total, de acuerdo a las pautas del Servicio.
Grupo Intratecal (IT), al cual previo a la inducción anestésica se le administró 1 microgramo/kg de fentanil y 500 microgramos de morfina libre de conservantes por vía intratecal en jeringas diferentes.
procedimiento
A la llegada de los pacientes a sala de operaciones se les colocó una vía venosa periférica y monitorización básica no invasiva (presión arterial no invasiva, electrocardiografía de cinco derivaciones con analizador del segmento ST y pulsioximetría).
Se colocó al paciente en posición sentado y en estrictas condiciones de asepsia se realizó infiltración de la piel, a nivel lumbar, con 3 cc de lidocaína al 1%. Para el grupo C se cubrió la zona con un apósito estéril.
Para el grupo IT se continuó con la punción lumbar con una aguja número 27 punta de lápiz, a través de un introductor, a nivel L1-L2 o L2-L3, por donde se administraron los opiáceos.
Si al tercer intento no fue posible verificar el flujo de líquido cefalorraquídeo por la aguja se suspendió el procedimiento. En caso de verificarse la presencia de sangre a través de la aguja de punción lumbar se pospuso la cirugía por 24 horas.
El resto de la monitorización invasiva (presión arterial invasiva y presión venosa central y sonda vesical) se completó luego de la inducción anestésica.
protocolo anestésico
Para la inducción anestésica se administró en bolo, lento, 5 mcg/k de fentanil. Para lograr la hipnosis, bolos de 50 mg de propofol, administrados lentamente y 0,5 mg/kg de atracurio para facilitar la intubación.
El mantenimiento fue con fentanil en perfusión de 5 mcg/kg/h y propofol 5 mg/kg/h. Frente a un plano anestésico insuficiente se administraron bolos de fentanil de 200 mcg; de persistir el mismo se ajustó el ritmo de infusión.
La respuesta al dolor y el ajuste de las drogas se valoró por la clínica y las modificaciones hemodinámicas (presión arterial media y frecuencia cardíaca), manteniendo éstas en un 20% de los valores basales.
Al comienzo del cierre de la piel se suspendieron las infusiones.
Finalizada la cirugía se evaluó la posibilidad de extubar al paciente en sala de operaciones (SO), de acuerdo a los siguientes requisitos:
a) Estar despierto y responder órdenes.
b) Saturación de oxígeno de 95% o más con FiO2 de 1 y PEtCO2 menor de 45 mmHg con ventilación espontánea.
c) Frecuencia respiratoria entre 10 y 30 rpm, volumen corriente mayor a 5 ml/kg y movimientos torácicos regulares valorados por impedancia.
d) Temperatura central mayor de 36 grados.
e) Hemodinamia estable, con o sin drogas.
f) Cirugía sin incidentes mayores.
El paciente fue trasladado a la Unidad de Cuidados Intensivos (UCI) donde se continuó con las pautas de ese Servicio respecto a la analgesia posoperatoria y la extubación.
variables a estudiar
Durante el intraoperatorio un investigador independiente, que desconocía el grupo al que pertenecía el paciente, recogió los datos de la memoria digital del monitor de anestesia (Datex-Ohmeda Cardiocap/5.) y de la ficha de anestesia.
La analgesia intraoperatoria se valoró a través de las siguientes variables:
a- Respuesta hemodinámica a la intubación orotraqueal, incisión de piel, pericardiotomía y a la esternotomía a través de la variación de la presión arterial media invasiva y de la frecuencia cardíaca, inmediatamente antes y durante los siguientes 10 minutos al estímulo.
b- Dosis total de fentanil y propofol utilizados durante la cirugía.
Durante el posoperatorio un investigador independiente y sin interferir con las pautas de la UCI evaluó:
- Analgesia posoperatoria a través de:
a) Escala Visual Análoga (EVA) consultando por el máximo dolor en las primeras seis horas y a las 24 horas. En el preoperatorio se instruyó a cada paciente el método de evaluación del dolor de la EVA. Esta tiene un rango de 0 a 10, en donde 10 se atribuye al dolor más intenso que haya sentido alguna vez en su vida, y 0 cuando no siente dolor.
b) Tipo y dosis de analgésicos utilizados en ese período.
- Medida de la PaCO2 luego de la extubación.
Se consignó además tiempo de extubación orotraqueal, cuando ésta no fue posible en SO.
Un investigador independiente evaluó de la presencia de efectos colaterales: depresión respiratoria que requiriera reintubación y/o apoyo ventilatorio, náuseas, vómitos, prurito y cefaleas, así como la necesidad y tipo de tratamiento. En todos los casos se realizó un seguimiento de la motilidad y sensibilidad de miembros inferiores así como de la presencia de dolor de espalda.
El análisis estadístico se realizó con el test de Student para muestras no pareadas cuando se comparó características de la población, de la cirugía (tiempos quirúrgicos, de CEC y de clampeo aórtico), consumo de fentanil, propofol y analgésicos posoperatorio, tiempo de extubación y PaCo2 posoperatoria. Para el estudio de las variables hemodinámicas durante el intraoperatorio se usó el análisis de varianza múltiple. Para el análisis de las escalas de dolor posoperatorio se utilizó el test de Mac-Withney. Se consideró significativo una p<0.05.
resultados
Diez pacientes fueron evaluados en el grupo IT y 11 en el grupo C.
No hubo diferencias significativas en cuanto a sus características demográficas y clínicas, como se detalla en la Tabla 1, ni quirúrgicas como se muestra en la Tabla 2.
La dosis de fentanil intratecal fue de 73 ± 14 mcg y el tiempo entre la punción y la administración de heparina de 107± 13 minutos.
Respecto al intraoperatorio no se presentaron diferencias significativas en el consumo de fentanil intraoperatorio (2379±339 mcg para el grupo C y 2119±634 para el grupo IT), ni de propofol (994±497 mg para el grupo C y 1151± 611 para el IT).
Tampoco hubo diferencias entre los grupos cuando se analizó la variación de la presión arterial media (PAM) y de la frecuencia cardíaca (FC), frente a los diferentes estímulos. Encontramos una tendencia a una mayor variación en la PAM durante la incisión de piel en el grupo C, ya que fue el único momento en que se mantuvo con un cambio de más de un 20% del valor basal.
Nueve de 10 pacientes no tuvieron dolor (EVA=0) en reposo durante las primeras seis horas en el grupo IT, mientras que seis de 11 tampoco lo tuvieron en el grupo C. En las 24 horas esto fue de 7/10 y 3 /11 respectivamente.
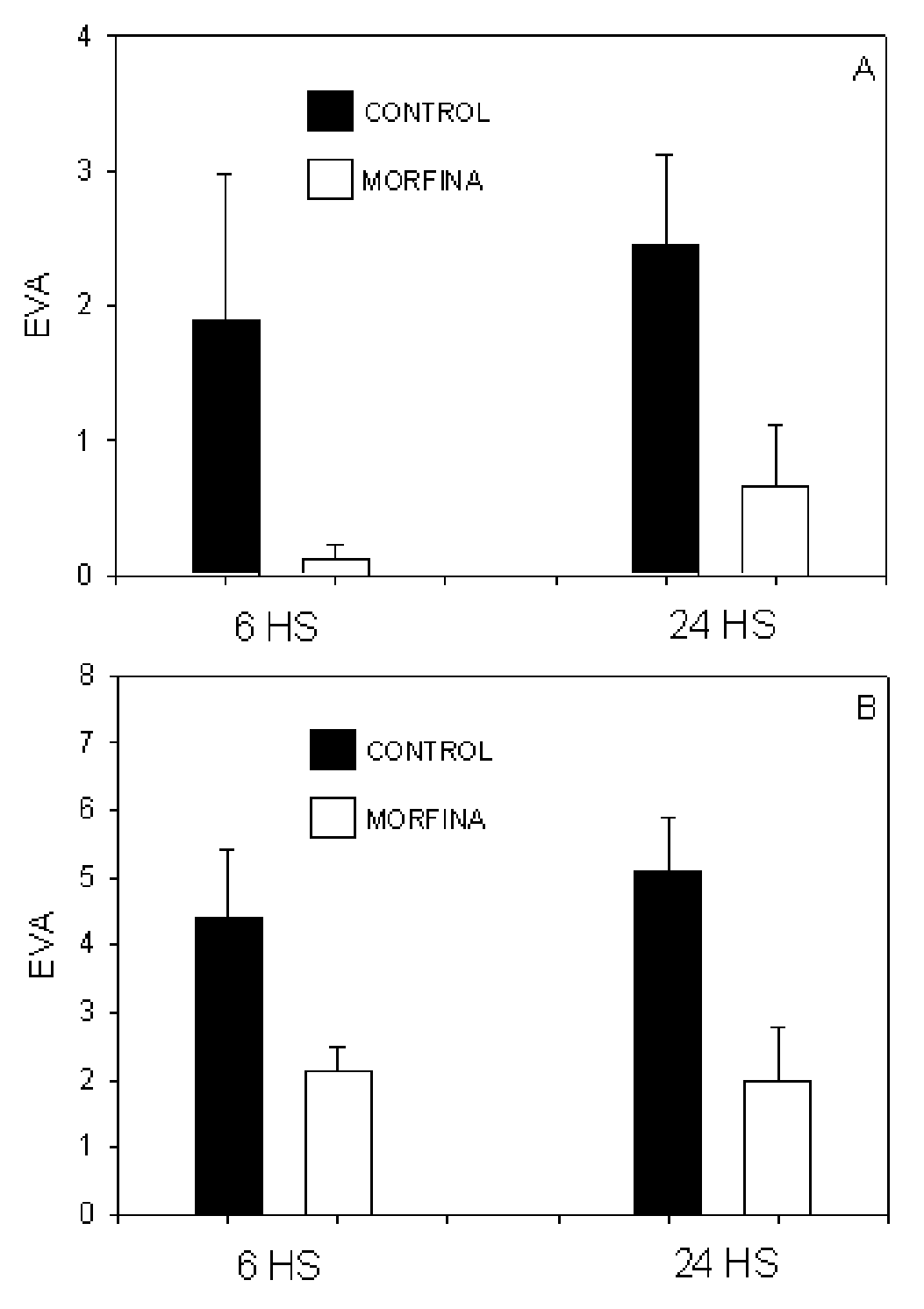
Observamos menor intensidad del dolor en el reposo y en el esfuerzo, como se muestra en la Figura 1, tanto a las seis como a las 24 horas para el grupo IT, siendo esta diferencia estadísticamente significativa, a las 24 horas (p= 0.04 y p= 0.01 respectivamente). Se observó, además, un menor consumo de analgésicos durante el posoperatorio para el grupo morfina IT, como se muestra en la Tabla 3, con menor número de pacientes que requirió analgésicos y menor dosis cuando fue necesario administrarlos.
Un paciente del grupo morfina IT se extubó en sala de operaciones. En las horas siguientes en la UCI presentó una hipercapnia mantenida ( paCO2 de 58 mmHg) que obligó a ventilación no invasiva durante 12 horas, con una evolución posterior favorable.
Los tiempos de extubación de los restantes pacientes fueron de 252±59 min para el grupo C y 363±121 para el grupo IT, diferencia que no fue significativa.
Las gasometrías de control posextubación no mostraron diferencias estadísticamente significativas, con una PaCO2 de 40.2±5 para el grupo C y de 47.6±6 para el grupo IT.
discusión
Focalizamos este estudio en dos aspectos que deben ser diferenciados, uno es la analgesia intraoperatoria y el otro la analgesia posoperatoria y sus complicaciones.
Analgesia intraoperatoria.
De acuerdo a nuestros resultados, la utilización de 1 mcg/kg de fentanil intratecal no permitió reducir el consumo de opiáceos intravenosos, ni atenuar los cambios hemodinámicos durante la cirugía. Estos hallazgos son diferentes a los encontrados por otros autores utilizando fentanil(11) o sufentanil(9) intratecal en cirugía cardíaca. Esta discrepancia puede ser explicada por diferentes causas. En primer lugar la dosis utilizada. Nader y cols.(11) demostraron un menor consumo de opiáceos intraoperatorios, pero con una dosis de fentanil intratecal de 1.5 mcg/kg.
La mayoría de los autores que realizaron estudios al respecto utilizan sufentanil (9,10) de disponibilidad limitada en nuestro medio. Las dosis utilizadas por ellos oscilaron entre 20 y 50 mcg. Las dosis equipotentes de fentanil y sufentanil administrados por vía IT para los valores de ED50 son 5:1 (f:s).(12) . Es decir que las dosis necesarias de fentanil IT para lograr una adecuada analgesia oscilarían entre 100 a 250 mcg, similares a las utilizadas por Nader(11) y superiores a las utilizadas en nuestro estudio.
En segundo lugar el tipo de opiáceo: siendo el sufentanil el fármaco más utilizado, estudios de su farmacocinética muestran un cleareance más rápido desde el líquido cefalorraquídeo(LCR) y una absorción rápida hacia el plasma, lo que explica el rápido comienzo de acción y la corta duración cuando se lo compara con el fentanil. Las diferencias farmacocinéticas de los distintos opiáceos en el LCR podrían explicar las diferencias fármaco-dinámicas.(13). El sufentanil es dos veces más liposoluble que el fentanil, por lo que se tiene un inicio de acción más rápido, salvo que se utilicen dosis equipotentes como lo muestra Fournier(12) en pacientes bajo cirugía de reemplazo total de cadera.
En tercer lugar el volumen total de la mezcla de opiáceos a usar: es bien conocido que al aumentar el volumen inyectado, incluso sin modificar la dosis, es posible aumentar la extensión del bloqueo. Volúmenes pequeños de hasta 4cc tienen escaso efecto sobre la extensión, en tanto que volúmenes de 5 a 10 ml lo modifican significativamente (14). Nosotros usamos un volumen total de hasta 2 ml cuando el utilizado por quienes tuvieron una significativa analgesia intraoperatoria fue de hasta 6 ml.
No consideramos a la morfina IT para analgesia durante el intraoperatorio. Debido a su farmacocinética, el pico de acción se ve retardado hasta aproximadamente seis horas luego de su inyección, por lo que ésta no ofrece una adecuada analgesia para este periodo. Esto fue demostrado por Nordberg en un estudio sobre farmacocinética de morfina intratecal donde observa que el comienzo de la analgesia torácica es retardada con la inyección lumbar (15).
Este es el motivo por el cual diferentes autores estudiaron el uso concomitante de morfina con un opiáceo de comienzo de acción rápido como sufentanil (9,10) con el fin de obtener analgesia intraoperatoria y disminuir efectos adversos debido a sus diferentes picos de actividad (16). Para lograr analgesia intraoperatoria solamente con morfina sería necesario aumentar la dosis de tal forma que aumentarían sus efectos colaterales. Si bien existe un estudio (17) no controlado, que muestra que 1 mg de morfina administrada intratecalmente provee adecuada analgesia intra y posoperatoria, permitiendo una extubación temprana, la mayoría de los autores opinan lo contrario, como veremos más adelante.
Analgesia posoperatoria.
Al igual que otros autores (5,7,9,11) encontramos que el grupo que recibió morfina IT presentó una mejor analgesia posoperatoria, evidenciada por menores valores de EVA, mayor porcentaje de pacientes que no requirieron analgésicos durante el posoperatorio y un menor consumo de ellos cuando los necesitaron. La dosis óptima de morfina IT ha sido motivo de controversia, buscando aquella que provee adecuada analgesia con mínima depresión respiratoria. La incidencia de esta está en relación con la dosis usada, como lo demuestran diferentes estudios. Vincenty (18) usando 10 mg encuentra adecuada analgesia posoperatoria pero con depresión respiratoria 24 horas luego de la inyección. Chaneys11 (19) utilizó 4 mg, dosis que mostró un excelente control del dolor posoperatorio, pero asociado con sedación, retardo del despertar y en la extubación.
Fitzpatrick (20) demuestra adecuada analgesia con dosis de 1 y 2 mg, aunque con las más altas se vieron valores mayores de PaCO2, sin mejorar significativamente la analgesia. Bettex (9) y Vanstrum (5) utilizaron 500 mcg de morfina IT logrando analgesia e incluso mejorando la función respiratoria posoperatoria. Alhashemi(6) comparó dos dosis de 250 mcg y 500 mcg contra placebo, establece como óptima la dosis de 250 mcg para lograr analgesia posoperatoria sin retardar la extubación. Sin embargo dosis bajas de 250 mcg son consideradas por otros como insuficientes para proveer analgesia adecuada en el posoperatorio, agregando el riesgo potencial de complicaciones derivadas de la punción espinal (21).
De acuerdo a estos resultados se seleccionó la dosis de 500 mcg para este estudio. De esta forma obtuvimos una adecuada analgesia posoperatoria, y un solo paciente requirió apoyo ventilatorio no invasivo por 12 horas por presentar cifras elevadas de PaCO2 en el posoperatorio. Una posible explicación es que se mantuvo la infusión de fentanil i/v continuo durante la cirugía en ambos grupos, provocando una sobredosificación en el grupo IT. Además de la dosis, el uso concomitante de analgésicos y sedantes son identificados como predisponentes para la depresión respiratoria (22).. La administración de opiáceos por esta vía produce una ocupación de receptores espinales (kappa) 20 y supraespinales (mu) vinculados a depresión respiratoria, diferente de lo que ocurre con la administración de opiáceos por vía IT, con una predominante ocupación de receptores kappa. En el mismo sentido un estudio prospectivo, randomizado y controlado (23), con una dosis de morfina intratecal de 10 mcg/kg, evidenció una intensa y prolongada analgesia posoperatoria con prolongación del tiempo de extubación. En este, se realizó la misma dosis de opiáceos i/v en los dos grupos, lo que puede haber contribuido a estos resultados. Esto fue confirmado por el mismo autor en un estudio posterior (24).
Por el contrario, Nader y cols.(11) utilizando morfina a 7 mcg/kg (0.49 mg), similar a la usada por nuestro grupo, combinada con 1.5 mcg/kg de fentanil y sin perfusión continua de opiáceos, observaron analgesia posoperatoria con preservación de la función respiratoria.
No se presentaron complicaciones neurológicas, pero dado el número pequeño de pacientes no podemos ser concluyentes al respecto.
La incidencia de hematoma espinal pospunción raquídea es baja en la población general (25) y no está descrita para pacientes sometidos a cirugía cardíaca (3-5,7,20). Fitzpatrick y Moriarty (20) en una serie de 3.400 pacientes y Vanstrum (5) en 1.000 pacientes, ambas poblaciones sometidas a cirugía cardíaca con heparinización total, han informado el uso de analgesia por vía intratecal sin evidencias de hematoma espinal.
Usando un modelo matemático, el riesgo potencial de daño espinal a partir de un hematoma en cirugía cardíaca convencional se estimó en 1:220000 a 1:3600, con un intervalo de confianza de 95% y de 1:2400 para un intervalo de confianza de 99% (7,24).
Dado este riesgo potencial se han establecido una serie de precauciones basadas en el uso combinado de una técnica cuidadosa (26) y una monitorización neurológica estricta en el posoperatorio. Se recomienda que la técnica no sea realizada en pacientes con coagulopatías preoperatorias conocidas, que la cirugía sea diferida por 24 horas si ocurre sangrado por la aguja y que el tiempo entre la punción y la anticoagulación con heparina sea mayor de 60 minutos (5,26). Aunque existen estudios realizados con aguja Nº 25 (9) y 22 (23) es bien conocido que a menor tamaño menor el riesgo de hematoma.
En este estudio fuimos estrictos en el cumplimiento de estas recomendaciones: se utilizaron agujas punta de lápiz Nº 27, no hubo punciones traumáticas, en ningún caso se registró sangrado a través de la aguja ni se realizaron más de dos intentos de punción, y el tiempo entre la punción raquídea y la heparinización fue mayor de 60 minutos. En todos los casos se respetaron las recomendaciones realizadas por la Sociedad Americana de Anestesia Regional (27) en cuanto al manejo de la anticoagulación. A todos los pacientes se les realizó la reversión con protamina al final de la cirugía. Por último se realizó un seguimiento neurológico clínico durante las primeras 24 horas del posoperatorio.
Respecto a náuseas, vómitos y prurito, su incidencia fue baja en nuestra población y no hubo diferencias significativas entre los dos grupos.
conclusiones
La combinación de 0,5 mg de morfina más 1 mcg/kg de fentanil intratecal determinó analgesia posoperatoria, con 90% de los pacientes del grupo morfina IT con EVA= 0 a las seis horas, con valores de EVA significativamente menores con respecto al grupo control, a las 24 horas, tanto en reposo como en esfuerzo.
Con respecto a la analgesia intraoperatoria, esta no fue efectiva.
Las limitaciones de este estudio fueron la elección de una dosis insuficiente de fentanil y el diseño del mismo, lo que determinó la administración de dosis altas de opiáceos i/v en ambos grupos. Esto podría llevar a que se ocultaran las diferencias en la analgesia dado que por si sola esta dosis puede producir analgesia y combinado con la morfina intratecal aumentar los efectos adversos posoperatorios.
Sería adecuado un diseño de estudio donde se comparen dos técnicas diferentes, una con opiáceos IT y la otra solamente i/v.
Características demográficasy clínicas de la población
Grupo C (n=11) Grupo IT (n=10) p
Edad (años) 59.9±12 (39-73) 63.4±5.7 (57-73) Ns***
Sexo (F/M)* 6/5 3/7 Ns
Peso (kg) 73±15 (50-95) 71±13 (50-94) Ns
Talla (cm) 162±9 169±6 Ns
Medicación preoperatoria
Betabloqueantes 5 5 Ns
Calcio antagonistas 2 3 Ns
Nitritos 2 2 Ns
IECA** 5 4 Ns
Diuréticos 2 2 Ns
Los valores se expresan como número de pacientes o media ± desvío
estándar y rango ( ).
*F/M : femenino/ masculino
**IECA : Inhibidores de la Enzima de Conversión de Angiotensina
***Ns: no significativo
Tabla 2 - Características de la cirugía
Grupo C Grupo IT p
Tipo de cirugía Ns****
RVM con CEC* 6 6 Ns
RVM sin CEC - 1 Ns
RA** 2 - Ns
RM*** 3 3 Ns
Tiempo quirúrgico (min) 233±35 268±12 Ns
Tiempo de CEC (min) 96±17 100±23 Ns
Tiempo de clampeo (min) 63±9 65±13 Ns
Valores expresados como número de pacientes o media ± desvío estándar
*RVM Revascularización Miocárdica, CEC Circulación Extracorpórea.
* *RA :Reemplazo Aórtico. ***RM: Reemplazo Mitral. ****Ns : no significativo
Tabla 3 - Consumo de analgésicos
en el posoperatorio
N° paciente Morfina IT Control
1 no 100 mcg de fentanil
2 no 300 mg de ketoprofeno
3 1 mg de morfina 4 mg de morfina
4 no 300 mg de ketoprofeno
5 no ———
6 no 100 mg de ketoprofeno +
50 mcg de fentanil
7 no 6 mg de morfina +
200 mg de ketoprofeno
8 no 100 mg de ketoprofeno
9 1.5 mg de morfina 3 mg de morfina
10 2 mg de morfina 2 g de dipirona
11 2 g de dipirona +
200 mg de ketoprofeno
Bibliografía
1- Goldstein S, Dean D, Kim SJ, Cocozello K, Grofsik J, Silver P, et al. A survey of spinal and epidural techniques in adult cardiac surgery. J Cardiothorac Vasc Anesth 2001; 15(2): 158-68.2- Salvi L, Sisillo E, Brambillasca C, Juliano G. High Thoracic Epidural Anestesia for off-pump Coronary Artery Bypass Surgery. J Cardiothorac Vascular Anesth 2004; 18(3): 256-62.
3- Chaney M. Intrathecal and epidural anesthesia and analgesia for cardiac surgery. Anesth Analg 1997; 84(6): 1211–21.
4- Ho AM, Chung DC, Joynt GM. Neuraxial blockade and hematoma in cardiac surgery: estimating the risk of a rare adverse event that has not (yet) occurred. Chest 2000; 117(2): 551-5.
5- Vanstrum GS, Bjornson KM, Ilko R. Postoperative effects of intrathecal morphine in coronary artery bypass surgery. Anesth Analg 1988; 67(3): 261-7.
6- Alhashemi JA, Sharpe MD, Harris CL, Sherman V, Boyd D. Effect of subarachnoid morphine administration on extubation time after coronary artery bypass graft surgery. J Cardiothorac Vasc Anesth 2000; 14: 639-44.
7- Liu S, Carpenter RL, Neal JM. Epidural anesthesia and analgesia. Their role in postoperative outcome. Anesthesiology 1995; 82(6): 1474-506.
8- Hall R, Adderley N, MacLaren C, McIntyre A, Barrer R, Imrie D, et al. Does intrathecal morphine alter the stress response following coronary artery bypass grafting surgery?. Can J Anaesth 2000; 47(5): 463-6.
9- Bettex DA, Schnidlin D, Chassot PG, Schmid ER. Intrathecal sufentanil-morphine shortens the duration of intubation and improves analgesia in fast-track cardiac surgery. Can J Anesth 2002; 49(7): 711-7.
10- Mason N, Gondret R, Junca A, Bonnet F. Intrathecal sufenanil and morphine for post-thoracotomy pain relief. Br J Anaesth 2001; 86 (2): 236-40.
11- Nader ND, Peppriell JE, Panos AL, Bacon DR. Potencial Beneficial Effects of Intrathecal Opioid in Cardiac Surgical Patients. The Internet Journal Anesthesiology 2000 vol 4 nº 2.
12- Fournier R, Van Gessel E, Weber A, Gamulin Z. A Comparison of Intrathecal Analgesia with Fentanyl or Sufentanil After Total Hip Replacement. Anesth Analg 2000; 90(4): 918-22.
13- Ummenhofer WC, Arends RH, Shen DD, Bernards CM. Comparative spinal distribution and clearance kinetics of intrathecally administered morphine, fentanyl, alfentanil and sufentanil. Anesthesiology 2000 Mar; 92(3): 739-53.
14- Collins VJ. Principios de Anestesia Raquídea. In Collins VJ. Anestesiología general y regional. 3ª ed., México, Mac Graw-Hill, 1996. p.1465-1519.
15- Nordberg G, Hedner T, Mellstrand T, Dahlstrom B. Pharmacokinetic aspects of intrathecal morphine analgesia. Anesthesiology 1984; 60(5): 448-54.
16- Swenson JD, Hullander RM, Wingler K, Leivers D. Early extubation after cardiac surgery using combined intrathecal morphine. J Cardiothorac Vasc Anesth 1994; 8(5): 509-14.
17- Diurno F, Imperatore F, Davies I. Morphine analgesia by intrathecal route in cardiopulmonary bypass surgery patiens. Anesth Analg 1999; 88: SCA 119.
18- Vincenty C, Malone B, Mathru M, Venus B. Comparison of intrathecal and intavenous morphine in post coronary bypass surgery. Crit Care Med 1985: 308.
19- Chaney MA, Smith KR, Barclay JC, Slogoff S. Large –dose intrathecal morphine for coronary artery bypass grafting. Anesth Analg 1996; 83 (2): 215-22.
20- Fitzpatrick GJ, Moriarty DC. Intrathecal morphine in the management of pain following cardiac surgery. Br J Anesth 1988; 60(6): 639-44.
21- Tamayo E, Álvarez J, De Temiño R, Martínez A, Florez S. What is the optimal morphine dose to be administered intrathecally in postoperative analgesia of cardiac surgery?. J Cardiothorac Vasc Anesth 2002; 16(11): 132-4.
22- Chaney MA. Side effects of intrathecal and epidural opiods. Can J Anesth 1995; 42(10): 891-903.
23- Chaney MA, Slogoff S. Intrathecal morphine for cardiac surgery and early extubation. Anesth Analg 1996; 82. SCA1-SCA130.
24- Chaney MA, Nikolov MP, Blakeman BP, Bakhos M. Intrathecal morphine for coronary artery bypass graft procedure and early extubation revisited. J Cardiothorac Vasc Anesth 1999; 13(5): 574-78.
25- Vandermeulen E, Van Aken H, Vermylen J. Anticoagulants and spinal-epidural anesthesia. Anesth Analg 1994; 79(6): 1165–77.
26- Rao TL, El-Etr AA. Anticoagulation following placement of epidural and subarachnoid catheters: and evaluation of neurologic sequelae. Anesthesiology 1981: 55(6): 618-20.
27- Anestesia neuroaxial y anticoagulación. Conferencia de opinión Chicago, Ilinois. Regional Anesthesia and Pain Medicine 1998; 23: 6 Suppl 2.














