Introducción
El déficit de hierro es la causa más común de anemia debido a carencia nutricional. Su máxima prevalencia ocurre en niños pequeños, adolescentes de sexo femenino y mujeres embarazadas1-3.
Muchos factores predisponen a la anemia por deficiencia de hierro, incluida la privación nutricional, la malabsorción intestinal y pérdidas de sangre. Durante los primeros dos años de vida existe un riesgo elevado de ferropenia, debido fundamentalmente a las limitadas fuentes dietéticas de hierro y a las necesidades incrementadas por el crecimiento1-3.
El tratamiento de la anemia por deficiencia de hierro consiste en mejorar la nutrición, seleccionando alimentos ricos en hierro biodisponible junto con la administración de hierro por vía oral, intramuscular o intravenosa4-8. En pediatría, se prefiere el uso de hierro oral, dado que es conveniente, económico y eficaz cuando la absorción intestinal no está comprometida. Uno de sus principales inconvenientes es la falta de adherencia al tratamiento, ya sea por intolerancia o incumplimiento4-8.
En casos bien establecidos debe recurrirse al tratamiento con hierro intravenoso. Actualmente se lo considera un método seguro y efectivo para tratar la deficiencia de hierro en niños que no pueden recibir o no responden adecuadamente al tratamiento con este fármaco por vía oral5-11.
El objetivo de esta comunicación es describir el abordaje diagnóstico y terapéutico de un niño en edad preescolar portador de anemia ferropénica severa secundaria a mala adherencia al tratamiento con hierro oral en el que se utilizó hierro intravenoso.
Caso clínico
Veintiún meses, sexo masculino, raza blanca, procedente de zona urbana de Montevideo. Sin antecedentes perinatales patológicos ni familiares a destacar. Medio socioeconómico y cultural deficitario. Buen crecimiento y desarrollo. Inmunizaciones vigentes.
Alimentado con pecho directo exclusivo hasta los 3 meses. Inicia alimentación complementaria a los 6 meses, actualmente consume leche de vaca entera, dos litros al día, dieta pobre en carne y en alimentos ricos en hierro biodisponible. Profilaxis con hierro oral de cumplimiento irregular, refieren intolerancia digestiva y olvidos en la administración por parte de los cuidadores.
Portador de anemia ferropénica, diagnosticada a los 14 meses, requirió hospitalización y transfusión de sangre desplasmatizada por cifras de severidad (hemoglobina 5 g/dl) y por presentarse con repercusión hemodinámica (taquicardia y soplo). Al alta se indicó tratamiento con hierro oral, presentando falta de adherencia y cumplimiento.
Consulta por rinorrea serosa, tos catarral y fiebre de 24 horas de evolución, acompañada de decaimiento marcado, apatía y anorexia.
Examen físico actual. Constantes vitales: FC 104 lpm, FR 46 rpm, TAX 36,5 °C, saturación de oxígeno 97% ventilando espontáneamente al aire. Intensa palidez cutáneo mucosa. Panículo adiposo hipoturgente en abdomen y muslos, masas musculares conservadas. Punta cardíaca normoposicionada. Ritmo regular, sin soplos. Extremidades cálidas, pulsos periféricos presentes, tiempo de recoloración menor a dos segundos. Tiraje subcostal, subcrepitantes y sibilancias espiratorias bilaterales. No adenopatías, ni visceromegalias. Resto del examen físico normal.
Los planteos clínicos iniciales fueron: infección respiratoria aguda baja con insuficiencia respiratoria, anemia y desnutrición aguda. Conducta: oxigenoterapia por cánula nasal de bajo flujo a 1 L/min, broncodilatadores inhalados, se solicitan estudios de laboratorio e ingreso a sala de cuidados moderados.
Estudios complementarios de laboratorio evidencian hemograma: hemoglobina (Hb) 5,7 g/dL, Hct 23%, volumen corpuscular medio (VCM) 52 fL, hemoglobina corpuscular media (HCM) 12,9 pg, ancho de distribucción eritrocitaria (ADE) 24,7%, reticulocitosis 1%. Lámina periférica: hipocromía, microcitosis, anisocitosis, poiquilocitosis. Serie blanca y plaquetaria normal. Estudio del metabolismo del hierro: sideremia 11 ug/dL, transferrina 256 unidades, índice de saturación de transferrina 3%, ferritina 5 ng/ml. Se confirma la presencia de anemia severa microcítica hipocrómica arregenerativa con ADE elevado de etiología carencial, ferropénica. Radiografía de tórax anteroposterior: índice cardiopericárdico normal, no imágenes patológicas a nivel del parénquima pulmonar.
Si bien el paciente presentaba factores de riesgo para ferropenia, dada la severidad de la anemia y la recaída, se solicitaron estudios para pesquisar otras etiologías. Anticuerpos para enfermedad celíaca (negativos), dosificación de IgA (normal), virus de la inmunodeficiencia humana (VIH) no reactivo, funcional y enzimograma hepático normal.
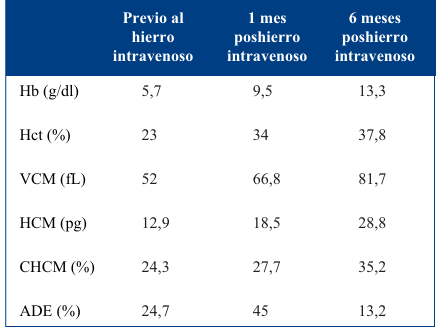
Se realizó interconsulta con médico hemoterapeuta, y, en conjunto, se indicó hierro sacarato parenteral con el objetivo de alcanzar una cifra de Hb inicial de al menos 9 g/dL. Se calculó el déficit de hierro según fórmula de Ganzoni (300 mg de hierro elemental). Se administraron 50 mg/día de hierro elemental diluidos en 100 ml de suero fisiológico (4 mg/kg/día), requiriendo en total seis días de tratamiento intravenoso. Se realizó la primera dosis de prueba, monitorizando la respuesta, mediante infusión intravenosa lenta de 25 mg en 30 minutos. Los días posteriores se administraron 50 mg en 30 minutos. No se detectaron reacciones adversas. Buena evolución. Previo al alta, se realizaron recomendaciones nutricionales y se indicó tratamiento con hierro oral polimaltosado una semana posterior a la última dosis de hierro intravenoso. En la (Tabla 1) se evidencia la evolución de los índices hematimétricos.
Discusión
En este caso se identificaron múltiples factores de riesgo para padecer anemia ferropénica. La duración de la lactancia materna fue escasa y precoz la introducción de leche de vaca. El niño recibía escasos alimentos ricos en hierro biodisponible y alto consumo lácteo. Este último factor es reconocido por inhibir la absorción de hierro y producir microsangrados intestinales con las consiguientes pérdidas digestivas2-5.
Además, se trataba de una familia que manifestaba dificultades en el cumplimiento de la profilaxis con hierro oral. Estas dificultades en la adherencia pueden deberse a su palatabilidad, efectos adversos gastrointestinales como náuseas, vómitos, dolor abdominal, diarrea, estreñimiento o a olvidos por parte de los cuidadores8,9,12-19. Este último punto resulta importante en el abordaje etiológico inicial, ya que ante el antecedente de anemia ferropénica es crucial identificar si el paciente no responde al hierro administrado por vía oral o simplemente no lo recibe.
Frente a un niño pequeño que se presenta con anemia severa de perfil ferropénico, suele ser necesario descartar diagnósticos etiológicos diferenciales, con otras entidades que cursan con anemia microcítica hipocrómica, como las talasemias y la anemia de las enfermedades crónicas. En este contexto se pesquisó la posibilidad de enfermedad celíaca o la infección por VIH que fueron descartadas, alejando la posibilidad de una talasemia el perfil hematimétrico de microcitosis elevada acompañada de un ancho elevado de distribución eritrocitaria.
El tratamiento de la anemia ferropénica tiene por objetivo reponer las reservas corporales de hierro, además de identificar y tratar la causa de la deficiencia, que en ocasiones puede ser una enfermedad grave subyacente. En cualquier circunstancia será necesario evaluar el estado del hierro en el paciente antes y durante el tratamiento2,4,7,20.
El tratamiento con transfusión con sangre desplasmatizada está indicado en situaciones específicas, en pacientes con anemia severa y disfunción cardíaca, insuficiencia respiratoria o infección concomitante2,4,7,20. En este caso, dado el antecedente de anemia ferropénica severa, con mala respuesta al tratamiento con hierro oral por dificultades en el cumplimiento y el haber requerido transfusión de sangre desplasmatizada justifica la indicación de hierro parenteral.
El hierro intravenoso es utilizado en pacientes con anemia ferropénica resistente al tratamiento y en aquellos casos en que los depósitos deben ser aumentados rápidamente, previo a procedimientos quirúrgicos. Otros motivos de indicación son la anemia ferropénica en niños con insuficiencia renal crónica, intolerancia demostrada al hierro oral, patología digestiva que inhiba la absorción o contraindique la vía oral y antecedentes de anemia severa que requirieron transfusión. La indicación de hierro intravenoso debe realizarse en conjunto con el médico hemoterapeuta6,8-10,12-14,18,19.
Existen diferentes formulaciones de hierro parenteral. La utilizada en este caso fue el hierro sacarato (Venofer®). Es una formulación segura y bien tolerada, su desventaja radica en que requiere ser administrada en múltiples dosis para no superar los 200 mg/día, o 5 mg/kg/día. La media de días de tratamiento con hierro sacarato dependerá del déficit de hierro calculado en relación con la dosis máxima diaria permitida. Existen otras formulaciones de uso menos frecuente en pediatría, como el hierro dextrano de bajo peso molecular, que presenta reacciones alérgicas y adversas frecuentemente, y el hierro carboximaltosa de uso con restricciones y limitaciones en pediatría, ambos permiten corregir el déficit total de hierro en una sola infusión6,9,13,14,20-24. En Uruguay están disponibles únicamente el hierro sacarato y el carboximaltosa25.
Previo a la prescripción del hierro intravenoso se deberá calcular el déficit de hierro, la dosis total a administrar, el ritmo de infusión y el número de días que requerirá de tratamiento. Para el cálculo del déficit de hierro se usan diferentes fórmulas. En este caso se utilizó la fórmula de Ganzoni: déficit de hierro (mg) = (peso (kg) x (Hb deseada (g/dL) - Hb actual (g/dL)) x 2,4 + depósito de hierro (mg). Para niños de hasta 35 kg, el cálculo del depósito de hierro se realiza a razón de 15 mg/kg de peso. Por encima de 35 kg, el depósito de hierro se considera 500 mg. La Hb deseada dependerá de la edad del paciente, según los valores de la Organización Mundial de la Salud. En este caso sería de 12,5 g/dl. El ritmo de infusión debe ser lento, es decir, se recomienda diluir una ampolla de Venofer® en 100 ml de suero salino fisiológico y pasarlo en al menos 30 minutos, controlando frecuencia cardíaca, presión arterial y temperatura. La dosis no deberá exceder los 5 mg/kg/día6,7.
Previo a iniciar el tratamiento, se recomienda realizar una dosis de prueba. La administración de la primera dosis se sugiere realizarla en el ámbito hospitalario, las dosis siguientes pueden administrarse en hospital de día o policlínica de referencia6. En este caso la administración se realizó en sala de cuidados moderados, sin incidentes.
Los efectos adversos son similares entre los diferentes preparados de hierro intravenoso, predominando el dolor en el sitio de inyección, linfadenitis regional e hipotensión arterial. Estos efectos adversos están vinculados a la velocidad de infusión. Se ha descrito también cefalea, malestar general, urticaria, fiebre, mialgias, artralgias, siendo en su gran mayoría leves. Las reacciones anafilácticas son raras a las dosis recomendadas6,8,13,14,20-24,26. En esta oportunidad no se registraron efectos adversos.
Las pautas de control y seguimiento de niños con anemia ferropénica son similares independientemente de la vía de administración del hierro. A la semana de iniciado el tratamiento, suele objetivarse mejoría clínica.
Se sugieren controles clínicos seriados y con hemograma al mes de culminado el tratamiento con hierro intravenoso. Se retomará el tratamiento con hierro oral luego de cinco a siete días de culminada la terapia intravenosa6,8,10-14,18,27,28.
En los pacientes con anemia severa los controles paraclínicos se solicitarán en forma individualizada según la evolución clínica7.
Parece necesario fortalecer en todos los controles pediátricos la importancia de prevenir la anemia ferropénica, en todas las etapas de la vida, reconociendo la presencia de factores de riesgo prenatales, peri y posnatales2-5,7,11. En este niño debe asegurarse un seguimiento clínico adecuado, haciendo hincapié en la prevención secundaria de esta enfermedad para evitar recaídas o detectarlas oportunamente.
Conclusiones
La mala adherencia al tratamiento por presencia de efectos adversos o incumplimiento son frecuentes y constituyen una de las principales indicaciones del hierro intravenoso, como ocurrió en este caso. El paciente presentó buena respuesta, con mejoría clínica y paraclínica que mantuvo en el período de seguimiento. La evidencia disponible presenta al hierro intravenoso como una herramienta eficaz y segura con indicaciones bien establecidas. Es importante insistir en el control pediátrico en la prevención primaria y secundaria.