Introducción
La tos es un motivo de consulta frecuente en pediatría. Predomina en la edad preescolar y constituye entre el 5%-10% de las consultas en niños de 6 a 12 años1,2.
Es un signo inespecífico que está presente en diferentes patologías pediátricas. Cuando se prolonga y se reitera en el correr del tiempo puede tener un impacto negativo en el sueño, la actividad diaria y la calidad de vida del niño y de sus padres, lo que les genera preocupación y motiva la consulta médica1,2.
La principal función del síntoma es proteger el organismo de agentes patológicos externos1,3. La fisiopatología de la tos está vinculada a la presencia de un arco reflejo complejo mediado por el nervio vago. Los receptores de la tos están localizados a lo largo de las vías respiratorias, desde la laringe hasta los bronquios segmentarios; y se estimulan por irritación química, estimulación táctil o fuerzas mecánicas1-5.
Desde el punto de vista práctico, puede clasificarse según tipo y tiempo de duración del síntoma.
En cuanto al tipo, la tos puede ser productiva o no productiva. La tos productiva es aquella que moviliza secreciones y en las infecciones respiratorias agudas permite mantener un adecuado clearence de las mismas. No es recomendable su supresión, ya que forma parte de una barrera defensiva del sistema inmunológico y respiratorio5. La tos no productiva, también llamada irritativa o seca, no cumple el propósito fisiológico antes referido y muchas veces constituye un síntoma molesto que puede inducir vómitos, dificultad en la alimentación o el sueño e influir en la calidad de vida de los niños. Es en este contexto donde muchas veces los pediatras consideramos el uso de un agente antitusivo5,6.
En cuanto al tiempo de duración, la tos puede clasificarse como aguda, subaguda o crónica. El American College of Chest Physicians define como tos aguda a aquella cuya duración es menor de tres semanas; subaguda a la que se prolonga más de tres semanas y crónica a la de más de cuatro semanas3-7.
Los antitusígenos y expectorantes son fármacos muy solicitados por los padres. Muchos de estos medicamentos son de venta libre desde larga data con dosis extrapoladas de adultos y ocupan los primeros lugares en cuanto a consumo en atención primaria y en ventas en el mundo1,2,8,9.
El objetivo de esta revisión es evaluar la eficacia y seguridad del uso de antitusígenos sintéticos en el tratamiento de las infecciones respiratorias en niños y adolescentes.
Tratamiento antitusivo
La tos aguda con frecuencia se produce en el contexto de infecciones respiratorias agudas. En general es un síntoma autolimitado y no se recomienda el uso de antitusígenos1,6.
El tratamiento de la tos crónica debe realizarse tras una exhaustiva investigación etiológica, con el objetivo de eliminar el agente causal4,6,10.
El tratamiento inespecífico o sintomático está dirigido al alivio del síntoma, independientemente de la enfermedad de base y del mecanismo fisiopatogénico implicado1.
El tratamiento se define como específico cuando está dirigido a la causa o mecanismo fisiopatológico posiblemente implicado4.
Tratamientos específicos
Los tratamientos específicos empiezan con la educación a padres y niños sobre los motivos frecuentes de la tos; se recordará a la familia la importancia de evitar el humo del tabaco y otros irritantes ambientales6,7.
Antihistamínicos
La eficacia en el tratamiento de la tos aguda o crónica es incierta. En una revisión Cochrane realizada con esta búsqueda no se encontró una mejoría sintomática respecto a placebo por lo que no pueden recomendarse como terapia empírica para niños11.
Beta 2 agonistas y corticoides
Según dos revisiones (Cochrane y guías de práctica clínica), no existe mejoría sintomática significativa respecto a placebo con el uso de beta 2 agonistas o corticoides en el tratamiento de la tos aguda o crónica de niños no asmáticos. Por este motivo no están indicados a menos que exista evidencia clínica que sugiera asma4,12,13.
Las guías americanas de tos crónica sugieren realizar una prueba terapéutica con corticoides inhalados durante dos semanas cuando se sospeche diagnóstico de asma y si no hay mejoría en ese lapso interrumpir el tratamiento y revalorar la posibilidad de otras etiologías específicas4,5.
Antibióticos
No se recomienda el uso de antibióticos de forma sistemática.
Frente a tos crónica (más de cuatro semanas) y productiva, en ausencia de otros diagnósticos específicos, algunos autores consideran que 40% de los casos puede tratarse de una bronquitis bacteriana persistente (BBP)2,4,5,14-16.
En este caso, según una revisión Cochrane y varias guías de práctica clínica, se sugiere el uso de antibióticos en un pulso prolongado de dos a seis semanas dirigidos a los siguientes gérmenes: Streptococopneumoniae, Haemophilus influenza, Moraxela catarrhalis4-6.
Amoxicilina-clavulánico es el antibiótico más frecuentemente utilizado por su cobertura contra los patógenos comunes identificados. Pueden utilizarse también cefalosporinas, trimetoprim-sulfametoxazol o macrólidos10,14,15.En el caso de un diagnóstico de tos convulsa o infección por Mycoplasma pneumoniae debe realizarse tratamiento con macrólidos, como azitromicina o claritromicina6,10.
Antiácidos y reguladores de la motilidad digestiva
Las pruebas de que la enfermedad por reflujo gastroesofágico sea causa de tos crónica en los niños son escasas y su asociación es probablemente más compleja, por lo que no se sugiere la prescripción rutinaria de antiácidos o reguladores de la motilidad digestiva en niños a no ser que exista una confirmación etiológica de la enfermedad4,5,10,16.
Tratamiento inespecífico
Está dirigido a la mejoría sintomática de la tos cuando esta se transforma en un síntoma molesto que altera la calidad de vida de los niños y sus familias.
Las recomendaciones de las agencias europea y estadounidense indican no administrar jarabes para la tos en menores de 2 años y la agencia canadiense en menores de 6 años8.
Una revisión de Cochrane de uso de antitusígenos para la tos aguda en niños y adultos en escenarios comunitarios que incluyó más de 1000 niños no encontró que el uso de antitusivos, antihistamínicos, descongestivos o sus combinaciones fueran más eficaces que placebo17.
Sin embargo, es importante destacar el efecto placebo de los antitusígenos, el cual está ampliamente demostrado en la literatura y en ensayos clínicos8.
Se han informado efectos adversos con la administración de antitusígenos, sobre todo en las preparaciones combinadas que contenían antihistamínicos y dextrometorfano8.
Clasificación de los antitusígenos
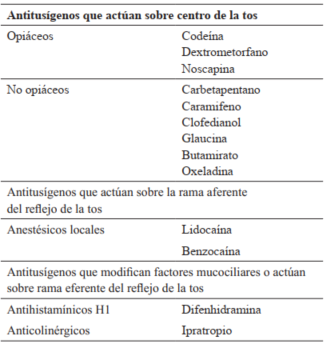
Los antitusígenos se clasifican desde el punto de vista fisiopatológico según su sitio de acción: el centro de la tos, rama aferente del reflejo de tos o rama eferente1,8,18.
En la (Tabla 1) se muestran los antitusígenos según sitio de acción.
Antitusivos opioides
Nos referiremos a las características de la codeína y el dextrometorfano, ya que son los dos opioides más utilizados para el tratamiento sintomático de la tos.
Codeína
Es un opioide con efectos analgésicos y antitusivos. El efecto antitusivo se evidencia en dosis inferiores a las analgésicas. En el 10% la codeína sufre desmetilación a morfina, que es la responsable de su efecto analgésico y sus efectos adversos. Presenta metabolismo hepático y su excreción es urinaria1,8,19.
Dosis recomendada en mayores de 18 años: 1 mg/ kg/día c/6 horas (dosis máxima 60 mg)1,19.
En cuanto a la seguridad, el efecto adverso más importante es la depresión respiratoria. Comparte el resto de los efectos adversos con otros opioides, como los digestivos (náuseas, vómitos, estreñimiento), miosis, retención urinaria. Debido a la liberación de histamina puede aparecer hipotensión o prurito19.
La codeína está contraindicada en menores de 18 años para el tratamiento sintomático de la tos8,20.
La hidrocodona (dihidrocodeinona) no ha demostrado ventajas comparada con la codeína y presenta similares efectos adversos8,20.
La FDA emitió́ dos alertas respecto a los medicamentos para la tos que contienen codeína o hidrocodona, con el fin de limitar su uso a jóvenes y adultos mayores de 18 años, porque los riesgos de estos medicamentos superan sus beneficios en este grupo etario21,22.
Dextrometorfano
Es el d-isómero del análogo de la codeína levorfanol. Presenta un efecto antitusivo similar al de la codeína, pero carece de propiedades analgésicas y no actúa en receptores opioides1,8,23,24.
Desde el punto de vista del mecanismo de acción, eleva el umbral de la tos.
El dextrometorfano se metaboliza por el citocromo hepático P450 y posee excreción urinaria. Está contraindicado en menores de 12 años, pacientes con hipersensibilidad al dextrometorfano o sus excipientes, tos asmática, tos productiva e insuficiencia respiratoria. Además, contiene etanol en su formulación24.
En Uruguay se lo puede encontrar en formulación de jarabe (Dextro toss) o como parte de formulaciones combinadas (Benadrex).
Dosis recomendada en mayores de 12 años: 5 a 10 mg cada 4 horas o 15 mg cada 6 a 8 horas24.
En cuanto a su perfil de seguridad, se han comunicado efectos serotoninérgicos, incluida la aparición de síndrome serotoninérgico, potencialmente mortal con la administración concomitante de agentes serotoninérgicos24.
Su sobredosis puede estar asociada con náuseas, vómitos, distonía, agitación, confusión, somnolencia, estupor, nistagmo, cardiotoxicidad (taquicardia, prolongación de QTc), ataxia, psicosis tóxica con alucinaciones visuales, hiperexcitabilidad. Su uso prolongado puede provocar tolerancia y dependencia mental y física23,24.
Antitusivos no opioides de acción central
Estos compuestos pertenecen a un grupo farmacológico diferente, no relacionado con los opioides, e incluyen: carbetapentano, caramifeno, clofedianol, glaucina, butamirato, oxeladina1,8.
No se ha encontrado mejoría significativa en pediatría con su uso respecto al placebo y sí se han reportado reacciones adversas, por lo que no está recomendado su uso en esta población8.
Medicamentos protrusivos
Son modificadores de las características de la secreción bronquial cuyo objetivo es facilitar su expulsión. No están recomendados en pediatría para el tratamiento de la tos1.
Agentes mucolíticos
Modifican las propiedades físico-químicas de la secreción traqueobronquial con el objetivo de que la expectoración sea más eficaz y cómoda.
Se clasifican en:
N Acetil L Cisteína
No está recomendado en el uso de la tos aguda o crónica como medicamento inespecífico sintomático1.
Puede utilizarse como tratamiento coadyuvante en los procesos respiratorios que cursan con hipersecreción mucosa excesiva o espesa, tales como bronquitis crónica de pacientes con enfermedad pulmonar obstructiva crónica, enfisema, atelectasia debida a obstrucción mucosa, complicaciones pulmonares de la fibrosis quística y otras patologías relacionadas25.
En cuanto a su mecanismo de acción, rompe puentes disulfuros de cistina en mucoproteínas, reduciendo la viscosidad del moco. También se le ha atribuido por su carácter reductor propiedades antioxidantes que ejercen una acción antiinflamatoria en el aparato respiratorio25.
Tiene una rápida absorción, circula unida a proteínas plasmáticas. Su eliminación es renal25.
Dosis recomendada vía oral:
- niños de 2-7 años: 100 mg cada 8 horas o 300 mg/día.
- mayores de 7 años y adultos: 200 mg cada 8 horas o 600 mg/día.
Puede usarse también en nebulización y vía instilación traqueal en solución al 10-20 %.
Los efectos adversos incluyen digestivos (náuseas, vómitos), cefaleas, rinorrea, hipersensibilidad a la droga, broncoespasmo y olor sulfúreo25.
Bromhexina y ambroxol
Actúan in vitro por despolimerización de sialomucinas, con reducción de la viscosidad, pero sus efectos in vivo no son constantes.
El ambroxol es el metabolito de bromhexina.
Tienen absorción oral e inhalatoria y se difunden a los tejidos, incluido el epitelio bronquial18.
Dosis recomendada oral ambroxol:
- 2 a 5 años: 7,5 mg 3 veces /día.
- mayores de 5 años: 15 mg 3 veces /día.
Bromhexina:
- niños de 2 a 6 años: 2 mg 3 veces/día.
- niños de 6 a 12 años: 4 mg 3 veces/día.
- adultos y niños mayores de 12 años: 8 mg 3 veces/día.
En cuanto a su perfil de seguridad se han notificado mareos, cefaleas, crisis broncobstructivas (poco frecuente), síntomas gastrointestinales (vómitos, náuseas, diarrea, pirosis)26.
La agencia de medicamentos belga (AFMPS) en el año 2015 recibió notificaciones espontáneas de reacciones adversas graves en la esfera dermatológica con el uso de bromhexina y ambroxol, como eritema multiforme, el síndrome de Stevens-Johnson y el exantema pustuloso25,26.
Agentes expectorantes
Estimulan mecanismos de expulsión del moco al aumentar el movimiento ciliar, el reflejo tusígeno o el volumen hídrico. Su principal función es la fluidificación del moco.
Ninguno está aprobado por la FDA y no se recomiendan en pediatría1.
Formulaciones combinadas a dosis fijas
En el mercado farmacéutico se comercializan diversos preparados conocidos vulgarmente como jarabes para la tos, que incluyen combinaciones a dosis fijas de diferentes grupos farmacológicos, como dextrometorfano o codeína con antihistamínicos, agentes mucolíticos, descongestivos (catecolaminas) y antipiréticos. Se debe estar atentos a estas formulaciones que pueden determinar interacciones farmacológicas o un perfil de seguridad peligroso en pediatría18.
En ningún caso se ha encontrado evidencia significativa de estas formulaciones respecto al placebo18.
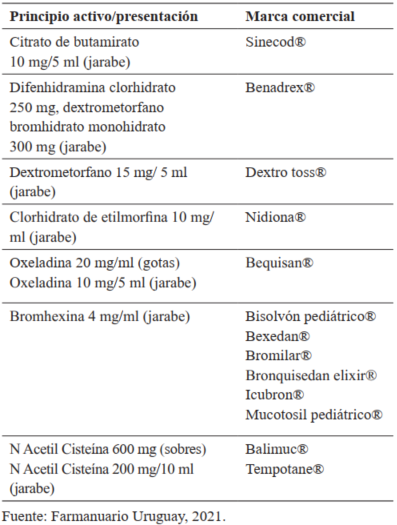
En la (Tabla 2) se presentan formulaciones de antitusígenos o protusivos sintéticos disponibles en Uruguay.