Introducción
Los antihistamínicos son uno de los grupos farmacológicos más utilizados mundialmente, al ser además de muy fácil acceso. Estos fármacos están constituidos por grupos moleculares estructuralmente similares a la histamina; este concepto es clave para su interpretación y aplicación clínica en relación con los efectos deseados y adversos.
Si bien son prescritos en el tratamiento de la rinitis alérgica, urticaria e incluso en el asma, su seguridad y eficacia no se ha comprobado en niños pequeños. En otros casos, según el fármaco, la forma de presentación, el motivo de su indicación o la duración del tratamiento, su uso puede no estar recomendado en niños menores de 6 años.
Actividad fisiológica de la histamina
La histamina (aminoetilimidazol ß) es una amina biógena con propiedades pleiotrópica que determina un espectro de efectos en el sistema nervioso central (SNC), se comporta como neurotransmisor, también interviene en la modulación endocrina mediando la secreción ácida gástrica1-3.
El principal sitio de síntesis y almacenamiento de histamina ocurre a nivel de las células cebadas, y su precursor es la histidina. Esta es metabolizada por la enzima L-histidina descarboxilasa e hidrolizada por la N-metiltransferasa y diaminooxidasa para ser posteriormente almacenada en gránulos, de los cuáles es liberada mediante diferentes procesos de transporte celulares. A nivel de SNC, mucosa gástrica y epidermis se puede observar secreción continua sin almacenamiento previo1-3.
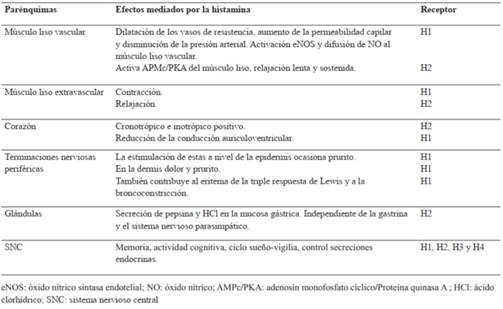
La histamina liberada interactúa con las estructuras receptoriales en unidades efectoras. Actualmente se conocen cuatro receptores para histamina: H1, H2, H3 y H4, estos son de tipo metabotrópico y por ello asociada a proteínas G, responsables de los diferentes perfiles de efectos en las estructuras efectoras. El receptor H1 media la contracción del músculo liso, el aumento de la permeabilidad vascular y vasodilatación y el receptor H2 media la estimulación gástrica y cardíaca1-4) (Tabla 1).
Los antihistamínicos antiH1 farmacodinámicamente se comportan como agonistas inversos, por lo que disminuyen la actividad constitutiva receptorial y compiten con la histamina al favorecer la expresión del receptor en estado inactivo. En tanto que la interacción de histamina con el receptor induce una conformación totalmente activa, la interacción con antihistamínicos genera una conformación inactiva1-3.
En términos generales, los antihistamínicos antiH1 poseen un perfil farmacológico y aplicaciones terapéuticas similares, de modo que sus efectos son predecibles a partir del conocimiento de la acción de la histamina1-3.
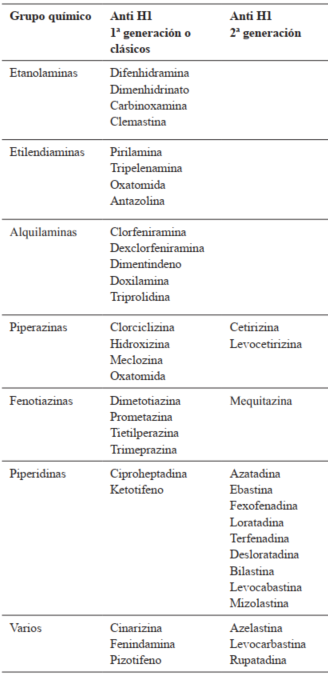
Desde el punto de vista molecular, los antihistamínicos se clasifican según su estructura química en los siguientes grupos: etanolaminas, etilendiaminas, alquilaminas, piperazinas, fenotiazinas y piperidinas. Esta clasificación carece de aplicabilidad en la práctica clínica, por lo que resulta más práctico clasificarlos en generaciones: primera generación o clásicos y segunda generación1-3 (Tabla 2). La disponibilidad de los antihistamínicos en Uruguay se muestra en la (Tabla 3).
Antihistamínicos de primera generación o clásicos
La mayoría de los antihistamínicos de primera generación derivan de una molécula madre similar en estructura a la de los antagonistas muscarínicos, antipsicóticos o antihipertensivos (antagonistas alfa 1). Por esta razón suelen presentar interacciones con las estructuras receptoriales antes mencionadas y se observan efectos antimuscarínicos, antidopaminérgicos, antiserotoninérgicos e incluso hipotensión por antagonismo alfa. Básicamente este grupo se caracteriza por presentar baja selectividad por los receptores H1.
Su principal inconveniente reside en la capacidad de atravesar la barrera hematoencefálica (BHE) e interferir en diferentes tipos de neurotransmisores, originando su característico efecto sedante.
La baja selectividad por H1, además de vincularse con el potencial perfil de efectos adversos, ha provisto a los antihistamínicos de primera generación de otros nichos terapéuticos: cinetósis, antiemético y síndrome serotoninérgico leve a moderado1-5.
Antihistamínicos de segunda generación
Este grupo se caracteriza por presentar gran selectividad por los receptores H1 y poca capacidad de modulación sobre otros receptores. Estas propiedades en adición a la menor capacidad para atravesar la BHE les brinda un menor perfil sedativo. Este grupo de antihistamínicos se introdujo en la década de 1980 con terfenadina, la cual se ha discontinuado dada la presentación de efectos adversos cardiovasculares (prolongación del intervalo QT). Posteriormente se incorporaron loratadina, ebastina, bilastina, etc., que se caracterizan por presentan perfiles farmacológicos similares. De forma concomitante y con la finalidad de mitigar los efectos adversos de los primeros fármacos de este grupo comenzaron a comercializarse sus metabolitos activos, como fexofenadina (terfenadina) y desloratadina (loratadina), estrategia que no garantiza disminuir los potenciales eventos adversos mencionados1-5.
Farmacocinética
Todos los antihistamínicos presentan adecuada absorción oral, pero con biodisponibilidad inferior al 50%, dado su importante efecto de primer paso hepático. La mayoría son metabolizados por CYP3A4, hecho a considerar principalmente con los antihistamínicos de segunda generación que pueden ocasionar trastornos del ritmo cardiaco (terfenadina, no así su metabolito activo fexofenadina, y astemizol ya retirados del mercado). También se comportan como inductores de los CYP450 lo que facilita su propio metabolismo.
En general alcanzan la Cmáx a las 2-3 horas y su efecto se mantiene aproximadamente por 4-6 horas, distribuyéndose ampliamente por el organismo hasta el SNC. Los antihistamínicos de segunda generación se caracterizan por no atravesar la BHE y presentan una duración de acción de 12-24 horas, lo que permite que se administre una vez al día. Las concentraciones máximas de estos en la piel persisten incluso después del descenso plasmático. Tienden a ser eliminados más rápidamente por niños que en adultos con hepatopatía grave. La gran mayoría de los antihistamínicos presenta eliminación renal.
Tienen la capacidad de atravesar la placenta, por lo que deben usarse con precaución en el embarazo1-3.
Eventos adversos de los antagonistas H1
- Sistema nervioso central: sedación, mareos, tinnitus, incoordinación, fatiga, visión borrosa, diplopía, euforia, nerviosismo, insomnio, temblores.
- Digestivo: anorexia, náuseas, vómitos, estreñimiento, diarrea, epigastralgia.
- Piel: dermatitis alérgica fiebre medicamentosa, fotosensibilización.
- Hematológicos (raros): leucopenia, anemia hemolítica, agranulocitosis.
- Anticolinérgicos (primera generación): pueden producir xerostomía, sequedad de las vías respiratorias, retención de orina.
- Cardiovasculares: taquicardia, hipertensión o hipotensión (sobre todo las fenotiazinas que producen antagonismo alfa adrenérgico). Dentro de los eventos graves existen reportes de torsade des pointes, en principio con astemizol y terfenadina. Los casos que incluyen este último también asociaban macrólidos. No se puede descartar que dicho fenómeno constituya un efecto de grupo1-3.
Evidencia científica en relación con el uso de antihistamínicos en las infecciones respiratorias
Las infecciones respiratorias son enfermedades pediátricas extremadamente comunes, y los antihistamínicos, al ser de venta libre, están disponibles para su uso de forma indiscriminada.
La literatura reporta que algunos virus respiratorios podrían inhibir la actividad de la enzima N-metiltransferasa, la cual participa en la hidrólisis de la histamina. Por lo tanto, en el contexto de las infecciones virales habría una mayor expresión de la histamina, lo que podría tener más estímulo sobre los receptores H1. En algunos casos de infecciones bacterianas, el metabolismo propio bacteriano estimularía la síntesis de histamina, produciendo mayor estímulo sobre los receptores histamínicos6,7.
Resfrío común
El tratamiento fundamental para este tipo infección respiratoria son las medidas de soporte, posicionamiento y desobstrucción nasal, si lo requiere el niño. Sin embargo, para el tratamiento sintomático en algunos casos se prescriben analgésico, descongestivo nasal, antihistamínico o antitusígeno. Los datos sobre eficacia y seguridad de dichos fármacos son limitados y de muy baja calidad. La Food and Drug Administration (FDA) no recomienda su uso en menores de 2 años y la Academia Americana de Pediatría (AAP) en niños menores de 4 a 6 años.
Los antihistamínicos de primera generación podrían reducir el síntoma rinorrea en 25-30%, debido a su acción anticolinérgica. Una revisión Cochrane concluye que no hay evidencia para recomendar el uso de estos grupos terapéuticos en las infecciones respiratorias, ya que la histamina no tiene un papel significativo en los síntomas del resfrío común en pacientes no atópicos. A la vez faltan ensayos clínicos controlados para niños que incluyan a menores de 12 años8-12.
Sinusitis bacteriana
Los datos actuales son insuficientes para recomendar el uso de descongestivos nasales orales y tópicos, mucolíticos o antihistamínicos como terapia coadyuvante. Están desaconsejados, ya que su efecto anticolinérgico hace que las secreciones sean más espesas. Podrían ser útiles en reducir los síntomas alérgicos en pacientes con atopia13,14.
Otitis media aguda
En la otitis media aguda el tratamiento con combinaciones de antihistamínicos-descongestivos, antihistamínicos o descongestivos solos o antitusígenos no son eficaces15.
Recomendaciones finales
La racionalidad de la prescripción farmacológica exige al clínico la selección de uno o varios medicamentos que mejor se ajuste a las necesidades clínicas del paciente.
Para esto debe tenerse en cuenta, entre otras cosas, la eficacia y seguridad de los fármacos. Basados en la evidencia científica disponible actualmente, no se recomienda el uso en forma sistemática de antihistamínicos de primera ni de segunda generación en las infecciones respiratorias en la edad pediátrica16.