Introducción
El paludismo es un problema de salud pública a nivel mundial, siendo causa importante de morbimortalidad en países donde es endémico. La enfermedad es causada por protozoos del género Plasmodium que se transmiten por mosquitos hembra del género Anopheles. Existen cinco especies de Plasmodium capaces de causar enfermedad al ser humano: P. falciparum, P. vivax, P. ovale, P. malariae y P. knowlesi1. P. vivax predomina en el continente americano, representando 75% de los casos de malaria en la región; P. falciparum es más frecuente en África, Asia sudoriental, Mediterráneo oriental y Pacífico occidental1-3.
La mayoría de los casos de malaria se producen en África, principalmente en la región subsahariana, Asia sudoriental, el Mediterráneo oriental, América Central y del Sur. Según el último informe de la Organización Mundial de la Salud (OMS), en 2018 se registraron 228 millones de casos en todo el mundo, observándose un descenso en el número de casos globales. Fallecieron 405.000 personas, 67% eran menores de 5 años, grupo de mayor vulnerabilidad. En las Américas, la incidencia ha aumentado debido al incremento de la transmisión de la enfermedad en Venezuela y los cambios migratorios en los últimos años3.
La migración es un problema creciente a nivel mundial, principalmente desde áreas endémicas a no endémicas, produciéndose casos de malaria importada en el nuevo lugar de residencia, de los cuales aproximadamente 15%-20% corresponden a pacientes en edad pediátrica4).
Se han estudiado los determinantes sociales asociados a la malaria, estableciendo la influencia del medio socioeconómico deficitario, por relacionarse con dificultad en el acceso a la atención en salud, condiciones de higiene deficientes y viviendas precarias que ofrecen escasa protección frente al vector. También se consideran población de riesgo las personas de alto nivel socioeconómico que residen en áreas no endémicas y viajan a áreas endémicas4,5.
Uruguay es considerado un país no endémico, sin transmisión activa de la enfermedad6.
En nuestro territorio las especies de Anopheles predominantes y de amplia distribucción, sobre todo Anopheles albopictus, no son capaces de transmitir los agentes de malaria. Entre los años 1985-1987 data la última identificación de un número reducido de ejemplares de Anopheles albitaris var domesticus, única especie en el país con capacidad de transmitir malaria. Esta identificación se realizó en zonas de montes próximos al río Uruguay, en el departamento de Artigas2-7.
Se han registrado casos importados en adultos, sin existir hasta el momento reporte de casos en niños8.
Se comunica el primer caso de un niño con malaria no complicada por Plasmodium falciparum en Uruguay.
El objetivo es sensibilizar a la comunidad médica sobre una enfermedad infrecuente reemergente en nuestro medio a partir de los movimientos migratorios, y analizar su abordaje diagnóstico y terapéutico.
Caso clínico
Ocho años, sexo femenino, procedente de Bolívar, Venezuela (área endémica de malaria y dengue). Reside en Uruguay desde 15 días previos a la consulta. Sin antecedentes patológicos, buen crecimiento y desarrollo. Inmunizaciones vigentes según esquema venezolano (1 dosis de vacuna antituberculosa; 5 dosis antidifteria, pertussis y tétanos; 4 dosis anti-H. influenzae tipo b; 3 dosis antineumocócica 13 valente; 2 dosis antimeningocócica serotipos A, C, W, Y; 4 dosis antihepatitis B; 2 dosis antihepatitis A; 4 dosis antipoliomielítica; 2 dosis antisarampión, rubéola y paperas; 2 dosis antivaricela; 1 dosis antifiebre amarilla y 3 dosis antirrotavirus). Sin antecedentes familiares a destacar.
Comienza cinco días previos al ingreso con fiebre de hasta 41 °C, acompañada de escasa rinorrea y tos seca. Dos vómitos en las últimas 24 horas, sin dolor abdominal, tránsito digestivo bajo y urinario sin alteraciones. Anorexia y marcado decaimiento, sin adelgazamiento. No lesiones de piel, no cefalea ni artromialgias.
Examen físico: decaída, FR 16 rpm, FC 104 cpm, temperatura axilar 38,2 °C, chucho febril durante el examen. Bien hidratada y perfundida, normocoloreada, sin lesiones en piel. Se constata dolor abdominal difuso; borde inferior hepático a 4 cm del reborde costal, regular, indoloro, y esplenomegalia grado dos. Resto del examen normal.
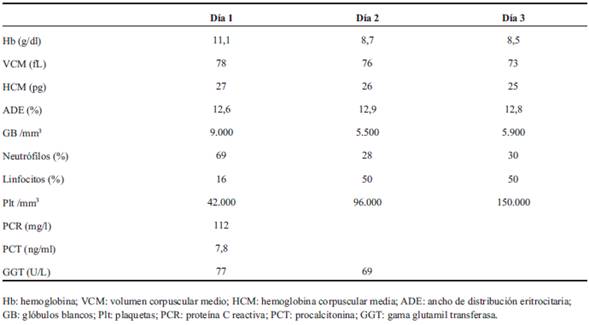
Dados los hallazgos clínicos y antecedentes epidemiológicos se plantea una enfermedad infecciosa importada como malaria o dengue, o una infección viral inespecífica. Se solicitan estudios complementarios de valoración general (Tabla 1) en los que se destaca anemia, plaquetopenia, elevación de reactantes de fase aguda y de gamma glutamil transferasa. Glicemia, función renal, gasometría venosa, crasis sanguínea, examen de orina y radiografía de tórax normales. Ecografía abdominal confirmó hepatoesplenomegalia moderada.
Se solicitaron exámenes de valoración etiológica: estudio parasitológico de sangre periférica para búsqueda de Plasmodium, serologías para citomegalovirus (CMV), virus de Epstein-Barr (VEB), virus de la inmunodeficiencia humana (VIH), reacción en cadena de la polimerasa (PCR) para dengue, zika, chikungunya y cultivos bacterianos de sangre y orina.
En el estudio parasitológico de sangre se observó trofozoitos de Plasmodium falciparum confirmando el diagnóstico de paludismo, con una parasitemia menor a 10% (Figura 1) y (Figura 2).
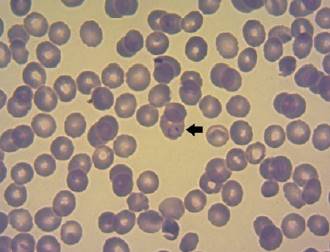
Figura 1: Frotis de sangre-tinción de May-Grünwald Giemsa. Trofozoito de Plasmodium falciparum (forma de anillo). MO x 1000.
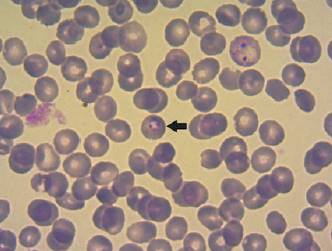
Figura 2: Frotis de sangre-tinción de May-Grünwald Giemsa. Trofozoito de Plasmodium falciparum (con doble cromatina). MO x 1000.
La serología para CMV, VEB y VIH fue negativa, así como la PCR para dengue, zika y chikungunya. Hemocultivo y urocultivo sin desarrollo bacteriano.
Se administra artemeter-lumefantrina durante tres días, seguido de primaquina que recibe por 14 días, con buena tolerancia, sin efectos adversos.
Se mantuvieron controles clínicos y paraclínicos diarios, no se registraron criterios de malaria grave durante la evolución, manteniendo la apirexia luego del primer día de tratamiento. Se realizó control diario de parasitemia por frotis sanguíneo, con descenso progresivo y negativización al séptimo día, por lo que se otorga el alta a domicilio.
Al cuarto día del alta se constató la normalización de la anemia y plaquetopenia, al décimo día el de los valores de gamma glutamil transferasa.
Discusión
La malaria en pediatría presenta algunas particularidades que es necesario conocer. Los hallazgos clínicos en oportunidades son inespecíficos y comunes a muchas enfermedades, por lo que los antecedentes epidemiológicos adquieren valor para orientar el diagnóstico. Teniendo en cuenta esta premisa, la literatura recomienda sospechar malaria en todo niño febril proveniente de un país endémico, independientemente de la edad y sintomatología acompañante, incluso si la llegada del país de origen ocurrió hasta un año atrás9-12. En el caso que se presenta la niña provenía del estado de Bolívar, Venezuela, siendo esta una de las zonas más afectadas13.
Clínicamente se presenta con síntomas inespecíficos, siendo la fiebre el más frecuente en niños. La duración de este síntoma puede ser variable y generalmente no se evidencian los paroxismos clásicos que se observan en adultos, relacionados con el ciclo vital del parásito. Le siguen en frecuencia: cefalea, sudoración, artromialgias, vómitos, diarrea y menos frecuentemente síntomas respiratorios, como tos. Al examen físico es casi constante la afectación del estado general, asociado en ocasiones a hepato-esplenomegalia y en menor medida a anemia clínica y signos de deshidratación. Varios de los elementos descritos se manifestaron en la paciente, incluso un episodio de chucho febril en el momento de realizarse el examen clínico inicial9,10,14-17.
La búsqueda etiológica de una enfermedad infecciosa febril en extranjeros debe orientarse según la presentación clínica y la epidemiología del país de donde proviene. En este caso se solicitaron estudios para malaria, dengue, zika y chikungunya, así como también se valoraron otras causas comunes de síndrome febril agudo en niños9,18.
El diagnóstico se realizó a través de una muestra de sangre venosa periférica obtenida mediante punción digital. Se confeccionaron varios extendidos sanguíneos (frotis) que se tiñeron con May-Grünwald Giemsa, siendo esta la técnica de elección para la confirmación del diagnóstico etiológico. Esta técnica permite diagnosticar la especie, estimar la parasitemia y controlar la respuesta al tratamiento. Puede también tomarse la muestra de gota gruesa, que tiene mayor sensibilidad (20 a 30 veces), al valorar mayor volumen de sangre, pero no permite identificar la especie. Un estudio del frotis normal no descarta el diagnóstico. En caso de alta sospecha clínica de malaria, se solicitará la toma de muestra de gota gruesa cada 12 horas o luego del siguiente registro febril, para aumentar la sensibilidad de la técnica. Esta enfermedad constituye una urgencia parasitológica9-11,19-21).
Existen también test rápidos que detectan antígenos en sangre, con buena sensibilidad y especificidad si la parasitemia es alta, de lo contrario pueden dar falsos negativos. Su beneficio radica en la rapidez para obtener el resultado, siendo también útil si no se cuenta con un parasitólogo entrenado para el diagnóstico. Estos tienen menor sensibilidad que la microscopía, no permiten calcular la parasitemia y no sirven para el seguimiento9,10,20-24. Por último, la reacción en cadena de la polimerasa (PCR) es otra opción diagnóstica con alta sensibilidad y especificidad, pero de difícil acceso, solo se utiliza cuando es difícil identificar la especie, principalmente en infecciones mixtas10-25.
En la analítica sanguínea de valoración general el hallazgo más frecuente es la anemia, la elevación de los reactantes de fase aguda y menos frecuentemente un leve aumento de las enzimas hepáticas14,15. La plaquetopenia puede observarse en casos de infección por P. falciparum, pero es más orientador de infección por P. vivax. Los hallazgos analíticos orientadores en este caso estuvieron presentes16,17.
Un punto relevante en la evaluación inicial y abordaje terapéutico de un niño con malaria es definir si presenta criterios clínicos o paraclínicos de malaria grave1,11,12,16,22).
Las manifestaciones clínicas de malaria grave son pleomórficas, difieren según edad de presentación, especie involucrada y zona de donde proviene16,22. Puede presentarse con depresión de conciencia, anemia severa, acidosis metabólica, hipoglicemia, falla renal o edema pulmonar, siendo la anemia la complicación más frecuente. Otro criterio de gravedad lo constituye la parasitemia mayor a 10%. En el presente caso no se observaron criterios clínicos ni paraclínicos de malaria grave, se trató de un caso de malaria no complicada de diagnóstico precoz9,11,26.
Otro criterio que permite guiar el abordaje terapéutico consiste en la identificación de la especie de Plasmodium implicada y la zona geográfica de la que proviene el niño, evaluando la posibilidad de resistencia a cloroquina1,2,9,27. La rapidez con que el parásito se adapta y adquiere resistencia a los antimaláricos constituye un problema mundial28. En este caso, la niña era procedente de un área con resistencia conocida a cloroquina, en la cual se identificó P. falciparum como el agente causal. Por lo antes mencionado, el tratamiento indicado de primera línea se basó en terapias combinadas con artemisina (artemeter-lumefantrina) con buena respuesta1,2,9-11. Algunos autores sugieren que en áreas con presencia de P. falciparum y P. vivax, o ante coinfecciones, es necesario prescribir primaquina por 14 días, con el objetivo de evitar la reactivación de formas intrahepatocíticas de P. vivax1,9,11,29. Dado que P. vivax tiene más incidencia en la región de donde provenía la niña y es la especie más involucrada en casos pediátricos de malaria, se optó por un abordaje terapéutico que incluyera los dos agentes2,12,30.
La estrategia mundial para el control del paludismo pone su foco en el control del vector y el acceso a tratamiento antimalárico efectivo. Como medidas para control del vector se proponen dos estrategias poblacionales básicas y complementarias: el uso de mosquiteros tratados con insecticida y el rociado intradomiciliario con insecticidas de acción residual. Para la protección personal se recomienda el uso de repelentes con N,N-Dietil-meta-toluamida (DEET) y utilizar ropa tratada con insecticida9,13,31. Además, existen varias recomendaciones de quimioprofilaxis que incluye a los viajeros que concurrirán a áreas endémicas, embarazadas residentes en zonas de transmisión moderada o alta y menores de 5 años en ciertas regiones de África, en forma intermitente junto con las vacunaciones sistemáticas1,9,18. La vacuna RTS, S es la primera contra la malaria que completó la fase 3 de desarrollo y está siendo administrada desde 2019 en niños de Ghana, Kenya y Malawi como plan piloto. Tiene como diana los esporozoitos de P. falciparum, principal agente etiológico de malaria grave y el de mayor incidencia en África32-34.
Se estima que para lograr el control del paludismo es necesario implementar intervenciones masivas combinadas, actuando en forma sinérgica para disminuir la transmisión de la enfermedad, incluyendo el control del vector, la indicación de quimioprofilaxis y la vacunación32,35.
Conclusiones
La migración y la globalización nos exponen a la presentación de enfermedades importadas, poco conocidas en nuestro país. La malaria debe ser considerada en un niño que proviene de zonas endémicas y se presenta con una enfermedad febril aguda, acompañada de chuchos, decaimiento y hepatoesplenomegalia. El estudio del frotis sanguíneo y gota gruesa realizado por el parasitólogo permitirá confirmar el diagnóstico y definir el abordaje terapéutico. Para disminuir la mortalidad es importante el diagnóstico oportuno y la identificación precoz de signos de malaria grave. El tratamiento será dirigido según la especie involucrada y el riesgo de resistencia a los antimaláricos.