Introducción
La hemofilia A (HA, MIM # 306700) es la coagulopatía ligada al cromosoma X más frecuente, afectando a 1-2 en 10.000 varones en todas las poblaciones humanas1. Muestra grados variables de severidad clínica-bioquímica y se puede clasificar como HA severa cuando la actividad del factor VIII de la coagulación es menor a 1% (FVIII: C<1 IU/dL), HA moderada cuando los valores son de 2% a 5% (FVIII: C: 2 - 5 IU/dL) y HA leve con valores de 6% a 30% (FVIII: C: 6 - 30 IU/dL)2). En proporción, cerca del 50 % de los casos de HA son severos, 10% moderados y aproximadamente un 40% son leves. Se ha observado que las articulaciones son las regiones del cuerpo afectadas más comúnmente, produciéndose inflamación, dolor, disminución de la función y artritis degenerativa1.
Las articulaciones afectadas con mayor frecuencia son las rodillas, los codos, los tobillos, los hombros y las caderas. La artropatía hemofílica puede producir una afección inflamatoria progresiva que genere limitación del movimiento y discapacidad permanente; las hemorragias musculares pueden causar necrosis y neuropatía; por otra parte, la hemorragia intracraneal muestra ser poco común, pero puede ocurrir luego de algún trauma leve en la cabeza y conlleva severas complicaciones. La hematuria suele ser ocasional y generalmente es indolora, el sangrado de la lengua o laceraciones de los labios es a menudo persistente1,2. Los pacientes con HA severa experimentan sus primeros sangrados articulares, en promedio, entre los 13,8 - 16,1 meses de vida y san grados generales entre los 9,7 - 10,9 meses3.
Debido a su patrón de herencia ligado al sexo (cromosoma X), la HA afecta casi exclusivamente a los varones; sin embargo, algunas mujeres portadoras pueden tener valores de 50% de la actividad del FVIII y mostrar coagulabilidad disminuida sin signos clínicos4. Por otra parte, se ha encontrado que las mujeres portadoras de hemofilia A y B sangran con más frecuencia que las mujeres no portadoras, especialmente después de procedimientos médicos, como extracción de dientes o amigdalectomía. Los niveles reducidos del FVIII se han correlacionado con un fenotipo de hemofilia leve5.
La HA es causada por mutaciones deletéreas en el gen del factor VIII (FVIII) de coagulación (F8). Casi la mitad de las HA severas están asociadas a inversiones del F8, la inversión del intrón 22 (Inv22)6,7 y del intrón 1 (Inv1)8. En el intrón 22 del F8 se extiende una secuencia de 9,5 kb (int22h-1) que posee dos copias extragénicas (int22h-2 y -3) a una distancia de alrededor de 500 kb a 600 kb del F8. Estas copias promueven la recombinación intracromosómica principalmente durante la gametogénesis masculina9. La Inv22 puede ser de tipo 1, cuando recombina la copia int22h-1 y la int22h-3, o tipo 2, cuando la recombinación ocurre entre las copias int22h-1, y int22h-210-11. Por su parte, el intrón 1 posee un segmento de 1041 pb (int1h-1) con una copia extragénica (int1h-2) a unas 140 kb hacia el telómero Xq, cuya recombinación puede generar la Inv18.
Según datos de la Federación Mundial de Hemofilia (WFH), para el 2018, se estimó que existían en Latinoamérica más de 32.400 personas que vivían con algún tipo de hemofilia12. En Uruguay, en el año 2013, se reportaron 236 personas con hemofilia13, y para 2018, según el último reporte de la WFH, existían 278 casos12, evidenciando un incremento de 17,8%. Por otra parte, con respecto a la causa genética de la HA severa en países de la región, como Argentina, Brasil y México, se ha estimado que la Inv22 es la causa de 45%-46% de los pacientes con HA severa y la Inv1 de 0,5-1,5%14-20.
La caracterización de la etiología genética de la hemofilia permite una correlación precisa del fenotipo y su severidad, lo cual resulta útil para un seguimiento adecuado del paciente, facilita el diagnóstico de portadoras y permite conocer la distribución de estas mutaciones causales de HA en la población. Este trabajo fue realizado con el objetivo de investigar la presencia de Inv1 e Inv22 del F8 en pacientes con HA severa del noreste de Uruguay, detectar portadoras y comparar la frecuencia (preliminar) estimada de las inversiones con datos de países de la región.
Pacientes y método
Pacientes
Se estudiaron un total de 14 individuos (ocho pacientes con HA severa, cuatro madres y dos hermanas) pertenecientes a cinco familias no relacionadas del noreste de Uruguay, de las ciudades de Tacuarembó, Rivera y Melo. Todos los individuos autorizaron su participación en el estudio por medio del consentimiento informado previamente aprobado por el Comité de Ética de la Facultad de Humanidades y Ciencias de la Educación, Universidad de la República (Exp. 121900- 000602-19). Los pacientes con HA severa fueron diagnosticados previamente, con base en su clínica y por tener disminuida la actividad del FVIII en menos de 1%.
Extracción de ADN
Se realizó la extracción del ADN genómico a partir de leucocitos de sangre periférica congelada por el método de salting-out y precipitación alcohólica21.
Detección de las inversiones
La investigación de la Inv1 e Inv22 se realizó aplicando las pruebas de inverse shifting-PCR (IS-PCR)22. En resumen, este protocolo consta de los siguientes pasos:
La ausencia de Inv22 se observa por la presencia de los fragmentos de 487 pares de bases (pb) (prueba diagnóstica) y de 405/457 pb (prueba complementaria). La inversión 22 tipo 1 se observa al encontrar el fragmento de 333 pb para la prueba diagnóstica y los fragmentos de 457/559 pb en la prueba complementaria. La Inv22 tipo 2 se observa al encontrar el fragmento de amplificación de 385 pb en la prueba diagnóstica y los fragmentos de 405/559 pb. La ausencia de Inv1se observa con el fragmento de 304 pb, mientras que su presencia se observa al encontrar el fragmento de 224 pb.
Los fragmentos de las amplificaciones obtenidas en la IS-PCR fueron observados y analizados por electroforesis en gel de poliacrilamida al 8% y se emplearon controles positivos para Inv1 e Inv22, cedidos por el equipo de genética de la hemofilia de la Academia Nacional de Medicina de Buenos Aires.
Resultados y discusión
En ocho individuos estudiados (cinco pacientes, dos madres y una hermana), pertenecientes a tres familias no relacionadas, se observó la ausencia de Inv22 e Inv1, encontrándose las señales de amplificación de los fragmentos de 487 pares de bases (pb) en la prueba diagnóstica de Inv22, las señales de 405/457 pb en la prueba complementaria de Inv22 y la señal de 304 pb de Inv1.
Por otra parte, en una familia proveniente de Rivera (Figura 1A), se encontró que un paciente resultó positivo para Inv22 tipo 1 (Figura 1A. H1) al mostrar el fragmento de 333 pb para la prueba diagnóstica de Inv22 y los fragmentos de 457/559 pb en la prueba complementaria de Inv22, su madre (Figura 1A. II-4) mostró los fragmentos de 333/487 pb y de 405/459/559 pb en la prueba diagnóstica y complementaria para Inv22, respectivamente (Figura 1B), confirmando su estado de portadora.
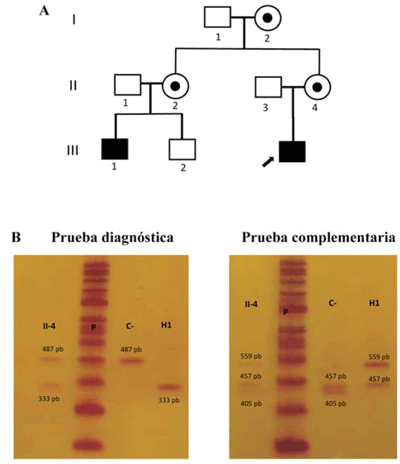
Figura 1: Familia con inversión del intrón 22. El panel A muestra la genealogía de la familia con un caso índice positivo para Inv22 (señalado con la flecha) y su madre (portadora); el paciente III-1 y su madre (II-2) no fueron estudiados. El panel B muestra los resultados de la IS-PCR observada en geles de poliacrilamida. Se muestra que el caso índice (H1) tiene en la prueba diagnóstica el fragmento de 333 pb y en la prueba complementaria los fragmentos de 457 pb y 559 pb, lo que confirma la presencia de Inv22 tipo 1. Su progenitora (II-4) muestra los fragmentos de 333 pb y 487 pb en la prueba diagnóstica y de 405 pb, 457 pb y 559 pb en la prueba complementaria, demostrando su estado de portadora de Inv22 tipo 1. La banda C- representa un control negativo para Inv22. P representa el patrón de peso molecular.
En una familia de Tacuarembó (Figura 2A) se encontró que dos pacientes (hermanos) resultaron ser positivos para Inv1 (fragmento de 224 pb); su hermana y madre mostraron los fragmentos de 224/324 pb, representativo del estado de portadoras de Inv1 (Figura 2B).
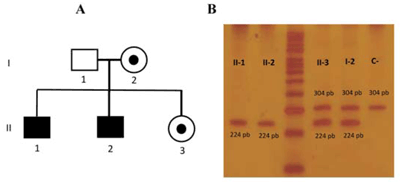
Figura 2: Familia con la inversión del intrón 1. El panel A muestra la genealogía de la familia con dos pacientes positivos para la Inv1 (II-1 y II-2) y a la madre (I-2) y hermana (II-3) como portadoras. El panel B muestra los resultados de las IS-PCR observadas en geles de poliacrilamida, se muestra que los pacientes (II-1 y II-2) tienen el fragmento de 224 pb, confirmando la presencia de la Inv1. La progenitora (I-2) y su hija (II-3) muestran los fragmentos de 224 pb y 304 pb, demostrando su estado de portadoras de la Inv1. La banda C- representa el control negativo para Inv1. P representa el patrón de peso molecular.
La estimación de la frecuencia de las inversiones en los pacientes del noreste de Uruguay muestra que preliminarmente el 40% de las familias con HA severa poseen Inv22 o Inv1 (2/5), mientras que por tipos de inversiones, Inv22 es la causa en el 20% (1/5) de las familias estudiadas y la Inv1 es la causa del restante 20% (1/5).
Estos resultados pueden considerarse como preliminares, representan un primer reporte de ocho pacientes pertenecientes a cinco familias con HA severa. Teniendo en cuenta la baja densidad de la población en esta región, que representa un poco más del 8% del total de los habitantes del país (3.440.157), en un área que comprende el 22% del territorio (38.456 km2)23, el número de individuos estudiados en la región noreste de Uruguay es pequeño en comparación con series similares de países de la región, como Argentina y Brasil. Por tal motivo no resultan extrapolables; sin embargo, es interesante observar que un estudio realizado en Argentina en 80 familias con HA severa, se muestra una frecuencia de 46% para Inv22 e Inv1 en conjunto17-19. En Brasil, en tres estudios realizados que incluyeron a 189 familias, se observó una frecuencia en promedio igual a la de Argentina (46%)15-16,20, lo cual dista en 6% de esta primera aproximación obtenida en el noreste de Uruguay.
Por otra parte, si se clasifica por tipos de inversión, este reporte preliminar muestra que en la región noreste de Uruguay, Inv22 es la causa de la HA severa en el 20% de las familias estudiadas y la Inv1 del restante 20% (si se analiza por pacientes, la frecuencia de Inv22 es aun menor, siendo de 12,5%, y la Inv1 es considerablemente mayor al ser de 25%). En un reporte de 2.093 pacientes con HA severa, estudiados por investigadores de 14 países, se estimó en 42% la frecuencia de Inv2211, y en otra estimación que incluye datos de 3.871 pacientes de 13 países de Europa, Oceanía y Latinoamérica (Argentina, Brasil y México), la frecuencia de Inv22 va de 40% a 49%20. Con respecto a Inv1, las frecuencias varían de 0 a 5% en parte de los países mencionados anteriormente, y en Argentina y Brasil la frecuencia es de 1%15-20. En el noreste de Uruguay se observa un valor preliminar de 20%.
Un dato importante se encontró al estudiar a la hermana de los pacientes con Inv1 (Figura 2A y B), cuya actividad del FVIII fue de 97%. Teniendo en cuenta que la mayoría de las portadoras tienen disminuida la actividad del FVIII en un 50%24, se sospechaba la ausencia de Inv1; sin embargo, el estudio molecular permitió determinar su estado de portadora al encontrar las señales de 204/324 pb en la IS-PCR (Figura 2. II-3). La investigación y caracterización de las portadoras es una parte importante en el manejo de la hemofilia que posibilita el adecuado asesoramiento genético de las familias.
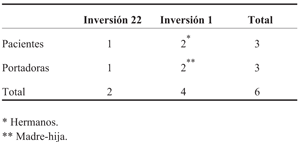
El estudio de la inversión del Inv1 y del Inv22 resulta crucial en la determinación de la etiología genética de los pacientes con HA, considerando que entre 40% y 50% de los pacientes con HA severa tienen dichos rearreglos en F89-11, así como para la detección de portadoras. Estos resultados representan el primer estudio realizado en Uruguay para determinar la presencia de Inv1 e Inv22 en pacientes con HA severa de la región noreste, así como la presencia de portadoras en las familias informativas (Tabla 1). Dada su aplicabilidad y por ser un estudio adecuado y costo-efectivo para la caracterización de las mutaciones causales de HA severa, consideramos valioso y pertinente que se estudie el total de los pacientes de Uruguay.












 Curriculum ScienTI
Curriculum ScienTI