Introducción
Las infecciones intrahospitalarias (IIH) constituyen una complicación frecuente de los cuidados sanitarios en las unidades de cuidados intensivos, aumentando la morbimortalidad1. La neumonía asociada a la ventilación mecánica (NAVM) es la segunda en frecuencia luego de la bacteriemia asociada a catéteres centrales2-4. A su vez, es la IIH con mayor mortalidad2. En adultos se ha establecido que afecta a 20%-25% de los pacientes en asistencia ventilatoria mecánica (AVM)1. En la edad pediátrica la incidencia es variable, estimándose que afecta a 8%-9% de los pacientes ventilados, siendo más frecuente en menores de 12 meses3,5-8.
El National Nosocomial Infection Surveillance (NNIS) estableció, en 1999, una incidencia de 6 casos/1.000 días de AVM en unidades de cuidados intensivos pediátricos (UCIP). En los años sucesivos la incidencia disminuyó y en el año 2013 fue de 0,7 casos/1.000 días de AVM3,8,9.
La NAVM es una neumonía infecciosa que se desarrolla en un paciente asistido con VM. La etiología depende del momento de aparición y se clasifica en precoz o tardía antes o después de 96 horas de AVM10. En la precoz, los gérmenes involucrados suelen ser patógenos comunitarios: Streptoccocus pneumoniae, Haemophilus influenzae y Moraxella catarralis. Las tardías son causadas por gérmenes nosocomiales: Pseudomonas aureginosa, Enterobacter cloacae, Klebsiella pneu moniae, Staphylococcus aureus)4,10. Las NAVM polimicrobianas también son frecuentes de observar1,2,9.
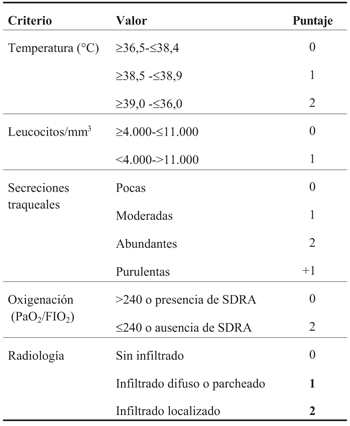
El diagnóstico debe ser precoz para mejorar el pronóstico. La precisión en el diagnóstico permite disminuir el uso excesivo de antibióticos (ATB). No existe un gold standard para el mismo y se realiza a partir de criterios clínicos, radiológicos y microbiológicos. Los criterios del Center for Diseases Control (CDC) son los más utilizados. Pugin y colaboradores desarrollaron el Clinical Pulmonary Infection Score (CPIS) (Tabla 1). Un puntaje > de 6 en CIPS predice la presencia de NAVM, con una sensibilidad de 70% y especificidad variable de 42%-85%11-14. El uso de criterios microbiológicos debe realizarse asociado con la sospecha clínica y radiológica. En pediatría no se dispone de estudios que establezcan la estrategia más apropiada para la toma de muestras microbiológicas. Las técnicas no invasivas se recomiendan por su mayor facilidad operativa, menor costo y disponibilidad continua1,2. Se han observado resultados similares cuando se utilizan técnicas tanto invasivas como no invasivas13.
En nuestro medio no se disponen de datos que analicen el impacto de la NAVM en UCIP, desconociéndose la incidencia de ésta.
Objetivo. El siguiente estudio se realizó con el objetivo principal de determinar la incidencia de NAVM con los criterios del CDC en la Unidad de Cuidados Intensivos de Niños (UCIN) del Centro Hospitalario Pereira Rossell (CHPR) durante el año 2015.
Material y método
Se realizó un estudio descriptivo y prospectivo entre el 1 de enero y el 31 de diciembre del año 2015 en UCIN del CHPR. Se incluyeron todos los pacientes hospitalizados en UCIN que requirieron AVM por más de 24 horas. Se registraron datos patronímicos, duración de estadía en UCIN y días de AVM, dato necesario para posteriormente calcular la incidencia de NAVM. La fuente de recolección de datos fueron las historias clínicas.
En aquellos pacientes en que se sospechó la presencia de NAVM por parte del equipo tratante, se les aplicó los criterios del CDC y el score CPIS por parte de los autores. Se consideró NAVM cuando se cumplieron los criterios del CDC. Se compararon cuántos casos en los que se sospechó la presencia de NAVM por parte del equipo tratante posteriormente cumplieron con los criterios del CDC.
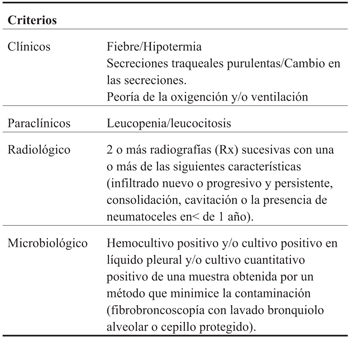
Los criterios del CDC de Estados Unidos se basan en aspectos clínicos, paraclínicos, radiológicos y microbiológicos10,11 (Tabla 2). De la interacción de estos criterios se definen tres tipos de neumonías nosocomiales: PNEU1, definida clínicamente y que requiere la presencia de criterio radiológico, deterioro en el intercambio de gases y tres o más de los siguientes: inestabilidad de la temperatura, leucopenia: (<4.000 leucocitos/mm3) o hiperleucocitosis (>15.000 leucocitos/mm3), secreciones purulentas, cambio de las características o aumento de las secreciones respiratorias o aumento en la necesidad de aspiraciones. PNEU tipo 2 es la definida clínica y microbiológicamente y requiere la presencia de criterio radiológico, al menos uno de los siguientes: fiebre o hipotermia, leucopenia (<4.000 leucocitos/mm3) o leucocitosis (>12.000 leucocitos/mm3) y uno de los siguientes: expectoración purulenta nueva, aumento o cambio en las características de las secreciones o mayor requerimiento de las aspiraciones, asociado a la presencia de hemocultivo positivo y/o cultivo positivo del líquido pleural y/o cultivo cuantitativo positivo obtenido por fibrobroncoscopía o cepillo protegido. PNEU tipo 3 es la que se produce en el paciente inmunodeprimido10.
En UCIN para el diagnóstico microbiológico se utilizan técnicas cualitativas, ya que son las utilizadas por el laboratorio de Microbiología del CHPR. Se consideró contaminado el cultivo de secreciones traqueales cuando desarrolló flora polimicrobiana o germen productor de NAVM pero sin síntomas compatibles.
La tasa de NAVM se expresó como la densidad de incidencia de NAVM (número de pacientes con NAVM/días de AVM) por 1.000. La incidencia se comparó con los últimos datos publicados por la NNIS de 2013 (último año disponible) para unidades de cuidados intensivos pediátricas médico-quirúrgicas.
Resultados
En el año 2015 el total de egresos de UCIN fue de 758 niños. De ellos, 147 cumplieron con los criterios de inclusión, 100 varones y 47 niñas. La mayoría fue menor de 1 año (n = 80). El total de días de AVM fue de 686. La mediana de la duración de la AVM fue de 5 días (rango 2-21 días).
En 15 de los 147, se sospechó la presencia de NAVM por parte del equipo tratante. En estos, la duración promedio de AVM fue de 12 días. Al momento de la sospecha de NAVM se obtuvo muestra de cultivos y dosificación de reactantes de fase aguda en los quince casos. A estos 15 niños se aplicaron los criterios del CDC y el CPIS por parte de los autores.
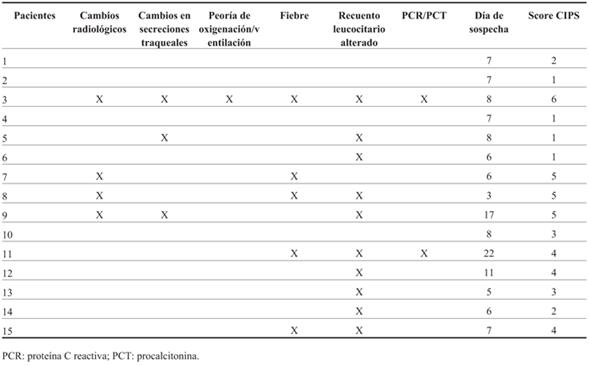
De los 15 pacientes en quienes se sospechó, un caso cumplió con los criterios del CDC para PNEU 1 (definida de forma clínica). En la (Tabla 2) se muestran los resultados de los 15 niños incluidos. En los 14 pacientes restantes que no cumplieron los criterios del CDC, cuatro presentaron el criterio radiológico; diez aumento del recuento leucocitario; cinco desarrollaron fiebre; dos, cambios de las secreciones traqueales. Ninguno requirió aumento de los parámetros ventilatorios. El paciente en que se diagnosticó PNEU 1 presentó aumento del recuento leucocitario, fiebre, secreciones traqueales purulentas, nuevos infiltrados radiológicos, así como aumento de los parámetros de ventilación y oxigenación. En el score de CPIS obtuvo un puntaje mayor a 6 (Tabla 3). En los 14 casos restantes el valor del CPIS fue menor de 6. En 13/15 se cambió el tratamiento antibiótico en forma empírica por una terapia combinada y de amplio espectro. En 8/13, la combinación antibiótica seleccio nada fue la asociación de vancomicina con meropenem. No se realizó decalaje de antibióticos en ningún caso una vez que se descartó la NAVM.
La presencia de un caso de NAVM en 686 días de AVM determina una incidencia de 1,45 casos/1.000 días de AVM en el año 2015. Los gérmenes aislados en cultivo de secreciones fueron Enterobacter cloacae sensible a piperacilina tazobactam, amicacina, gentamicina, ceftazidime, cefotaxime, ciprofloxacina y trimeptroprim sulfametoxazol y Acinetobacter baumannii complex, sensible a ampicilina sulbactam, piperacilina tazobac tam, ceftazidime, gentamicina y ciprofloxacina.
Discusión
Este es el primer estudio que aborda la incidencia de la NAVM en la UCIP de referencia nacional. En UCIN, durante el año 2015, la incidencia fue de 1,45 casos por 1.000 días de AVM. En nuestro medio no se dispone de estudios previos sobre NAVM en UCIP para poder comparar nuestros resultados. Los datos locales son provenientes de UCI de adultos, presentando una incidencia de NAVM de 9,6/1.000 días en el año 2013). Asimismo, se dispone de datos provenientes de recién nacidos, en especial pretérmino, considerados como Nursery de alto riesgo. En el año 2010 se informó la incidencia de NAVM, que fue de 4,78/1.000 días de AVM12. Por lo tanto, este estudio aporta los primeros datos nacionales sobre el tema.
En el año 2013 el NNIS reportó el percentil 50 de incidencia de NAVM en 0,7 casos/1.000 días de AVM para unidades de cuidados intensivos pediátricos médico-quirúrgicas10. En este reporte se establece el percentil 90 en 1,3 casos/1.000 días de AVM. Al comparar nuestros resultados con los datos del NNIS, la misma se ubicó por encima del percentil 90. En este reporte se establece que el 70% de las NAVM son de tipo PNEU 110. Si bien al comparar la incidencia hallada con el reporte del NNIS, ésta fue elevada, cabe destacar que pueden existir diferencias asistenciales que influyan sobre la incidencia. No se dispone de un sistema similar al NNIS para nuestra región, lo que haría la comparación más fidedigna.
A nivel regional, en la Unidad de Cuidados Intensivos Pediátricos del Hospital Italiano de la Ciudad de Buenos Aires, en el año 2010, la incidencia de NAVM fue de 6,3 casos/1.000 días de AVM. Luego de la aplicación de un paquete de cuatro medidas de prevención (cabeza a 30°, higiene bucal, suspensión diaria de la sedación y mantener limpio y seco el circuito del ventilador), la incidencia disminuyó a 2,38 casos/1.000 días de AVM16. En otras publicaciones se ha reportado una incidencia variable, entre 0,6-2,3/1.000 días de AVM, según el tipo de UCIP 1,2,14-20.
La media de la duración de la AVM de la población estudiada fue de 4,85 días. En los 15 niños con sospecha el promedio fue de 12 días. Esto concuerda con todas las comunicaciones sobre NAVM, en las que se resalta la duración de la AVM como el principal factor de riesgo para su desarrollo1-5,11. En el caso con PNEU1 duró 30 días.
Con respecto a la dificultad del diagnóstico, el uso de criterios en la definición de NAVM está limitado por dos factores. Por un lado, el amplio rango de diagnósticos diferenciales que pueden imitar la NAVM y que la mayoría de los criterios son clínicos y subjetivos. La mayor efectividad de los criterios propuestos por el CDC se obtuvo cuando se combinaron todos los criterios: los radiográficos y clínicos, teniendo una sensibilidad de 69% y una especificidad de 75%15. Dentro de los resultados obtenidos, se destaca que en los 15 casos en que se sospechó NAVM se confirmó en uno. Una de las posibles explicaciones para esto es que exista escasa adherencia a los criterios propuestos por el CDC. A su vez, al comparar los resultados de los criterios del CDC con el score de CPIS, se observó un comportamiento similar. El único caso con un score CIPS mayor de 6 fue el paciente con PNEU1, según los criterios del CDC. En los pacientes en que se sospechó NAVM y no cumplieron con los criterios del CDC, el score de CPIS siempre fue menor de 6. De estos resultados surge la necesidad de adherirse a los criterios diagnósticos sugeridos. Es probable que esto permita evitar el sobrediagnóstico de NAVM y racionalizar el uso de ATB de amplio espectro para aquellas situaciones en la que es elevada la probabilidad de presencia de NAVM.
Uno de los hallazgos del estudio fue que en los 15 casos de sospecha de NAVM se realizó rotación de ATB. Esta es una conducta acorde al planteo clínico, debido a que el retraso en el inicio del tratamiento antibiótico es un factor de riesgo de mala evolución1,2. Posteriormente se cumplió tratamiento completo de NAVM en todos los casos, a pesar de no cumplir con los criterios del CDC. Este último dato puede reflejar uno de los problemas frecuentes relacionados al uso de ATB en las UCIP, que es la resistencia a la suspensión o descalar el tratamiento antibiótico.
En nuestra experiencia la mayoría de las muestras fueron tomadas por aspiración de las secreciones traqueales. El aislamiento del patógeno es fundamental en cualquier enfermedad infecciosa para guiar el tratamiento según el antibiograma. Esto puede ser difícil en pacientes que cursan NAVM, ya que habitualmente desde el inicio de la AVM se encuentran bajo tratamiento antibiótico21-24. Los criterios del CDC exigen para catalogar la NAVM como PNEU2 (con confirmación bacteriológica) que la toma de muestra para cultivo sea realizada a través de fibrobroncoscopía . Sin embargo, se ha demostrado que las técnicas no invasivas (como el aspirado traqueal) tienen una especificidad comparable a las técnicas invasivas, con mayor facilidad para la toma de la muestra, menos costo y menores efectos adver sos1,2,15.
Para lograr disminuir la incidencia de NAVM es necesario el trabajo en conjunto entre los equipos médicos y de enfermería. Los mejores resultados se han logrado a través de la implementación de los paquetes de medidas dentro de las que se destacan: posición de la cama a 30º, higiene bucal con clorhexidina, mantener limpio y seco el circuito del ventilador y la suspensión de la sedación de forma diaria15).
Conclusiones
La incidencia de NAVM fue elevada en comparación con el reporte de NNIS 2013, pero baja al compararla con los datos regionales disponibles.
Se observó escasa adherencia a los criterios propuestos por el CDC para el diagnóstico de NAVM. Una mayor adherencia permitiría disminuir el número de casos en los que se sospecha y no se logra confirmar el diagnóstico. A su vez, esta mayor adherencia permitirá racionalizar el uso de ATB, logrando indicarlos cuando se cumplan los criterios diagnósticos.