Introducción
La entrada de las vacunas conjugadas neumocóccicas (VCN) en el calendario vacunal de Uruguay (7 valente en 2008 y 13 valente en 2010) determinó cambios en la epidemiología de las infecciones por Streptococcus pneumoniae, con reducción de la mortalidad y la morbilidad en niños menores de 5 años de edad. La especie Streptococcus pneumoniae agrupa más de 90 serotipos capsulares, con polisacáridos inmunológicamente distintos, pero un número relativamente reducido causa infecciones invasoras1. Las VCN son efectivas para prevenir infecciones severas causadas por los serotipos que integran sus fórmulas y además limitan la colonización por esos serotipos y en consecuencia reducen su transmisión y diseminación en la comunidad2.
La nasofaringe del ser humano es el reservorio de S. pneumoniae. Sus diferentes serotipos son integrantes habituales de la flora de ese sector, que es colonizado en porcentajes variables en diferentes etapas de la vida. Generalmente la portación es asintomática, pero algunos serotipos pueden causar infecciones invasoras3. Otros agentes cohabitan la nasofaringe en un equilibrio en el que influyen factores geográficos, climáticos, socio- culturales y patogénicos4-6. Este reservorio nasofaríngeo es fuente de diseminación de diferentes serotipos en la comunidad, proceso que es favorecido por las secreciones de las infecciones respiratorias agudas7. Virus y bacterias, que coexisten en la nasofaringe, se potencian mutuamente. La adherencia de los neumococos a la mucosa respiratoria es incrementada por las neuraminidasas virales, en tanto que las enzimas bacterianas clivan las hemaglutininas virales aumentando la replicación de algunos virus8-11.
Publicaciones internacionales sobre portación nasofaríngea, pre y posempleo de las vacunas conjugadas, proporcionan información sobre la circulación de los serotipos incluidos en las VCN y la potencial aparición de otros serotipos en reemplazo de los controlados por la vacunación12,13. En Uruguay, no se dispone de datos recientes de portación nasofaríngea en niños, ni antes de la introducción de la VCN 7-valente (serotipos: 4, 6B, 9V, 14, 18C, 19F y 23F) en el año 2008, ni luego de la incorporación, en el 2010, de la VCN 13-valente (con serotipos adicionales: 1, 3, 5, 6A, 7F y 19A). La vigilancia de los neumococos que colonizan la nasofaringe de niños permite reconocer cambios en la frecuencia de serotipos, la persistencia de algunos o la sustitución por otros, así como medir el impacto de las VCN14.
El objetivo de este trabajo es caracterizar la colonización nasofaríngea de niños menores de 2 años y describir los serotipos de S. pneumoniae identificados antes y después de la introducción de las vacunas conjugadas antineumocóccicas en el certificado esquema de vacunación (CEV) de Uruguay, en tres momentos epidemiológicos diferentes, y en los departamentos de Montevideo y Paysandú.
Método
Se llevó a cabo un estudio observacional, descriptivo, retrospectivo. Se consideraron tres períodos de tiempo en que se incluyeron los casos de neumococos obtenidos de aspirados/hisopados nasofaríngeos o de hisopados faríngeos mayoritariamente de niños desde recién nacidos a 2 años de edad en 2002-2003 (antes de la introducción de las VCN) y en 2014-2015 en centros de Paysandú, y mayoritariamente en 2012-2013 en Montevideo (ambos períodos posteriores a la introducción de VCN). Se seleccionó una muestra de conveniencia. La fuente de datos fueron los registros de laboratorio y las historias clínicas. Se consideraron variables epidemiológicas, clínicas y microbiológicas.
En el análisis microbiológico, dado que no se disponía en todos los casos de información precisa sobre la técnica empleada para la recolección, se consideró esta variable como “muestra”. En dos de los estudios (estudio I: años 2002/03 y estudio III: años 2014/15) la recolección de muestras se realizó en servicios pediátricos públicos de la capital del departamento de Paysandú. Para la recolección de las muestras se contó con la cooperación voluntaria de médicos y personal de salud. En las policlínicas no se registró el motivo de consulta, ni antecedentes de vacunaciones, pero consta que los niños hospitalizados cursaban infecciones respiratorias agudas.
El estudio II (años 2012/2013) se efectuó en población ambulatoria asistida en la policlínica Materno-Infantil de VIH del Centro Hospitalario Pereira Rossell (CHPR) de Montevideo. Las muestras correspondieron a hijos de madres infectadas con VIH/SIDA, que concurrían a la policlínica para su seguimiento serológico, imprescindible para confirmar o descartar la transmisión vertical de la infección. En este estudio se recabó la información en un formulario con datos filiatorios y antecedentes de cada niño. La recolección de muestras y los cultivos bacteriológicos, sembrados en cuadrantes, siguieron las pautas de la Organización Mundial de la Salud (OMS) vigentes en ese momento15.
El aislamiento e identificación de S. pneumoniae se realizó, respectivamente, en los laboratorios de bacteriología del Hospital Escuela del Litoral (Paysandú) y en el CHPR. En todos los estudios la confirmación de los neumococos y la serotipificación se llevó a cabo en el Departamento de Laboratorios de Salud Pública (DLSP). En la serotipificación se empleó la técnica de “quellung”, con una colección de pools y antisueros específicos (Statens Serum Institut, Dinamarca) proporcionada por la Oficina Panamericana de la Salud (OPS). En algunos neumococos no se pudo reconocer el subtipo o el serotipo contenido en un pool por no disponer de antisueros para identificar serotipos poco frecuentes.
Los resultados de la serotipificación fueron respaldados por controles de calidad periódicos de los centros de referencia de Brasil (Instituto Adolfo Lutz) y de Canadá (Centro Nacional de Streptococcus), en el marco del Sistema Regional de Vacunas iniciado en 1993, actualmente denominado SIREVA II16.
Los tres estudios contaron con la aprobación ética, respectivamente, de las autoridades locales y de la comisión de la Facultad de Medicina.
El análisis estadístico se realizó en base a medidas de resumen y distribución de frecuencias.
Resultados
Se procesaron en total 831 muestras, con una proporción de recuperación de neumococos de 54,8% (n = 456); 223 de ellos fueron tipificados.
En el estudio I se obtuvieron 356 muestras, de las cuales se recuperaron 177 neumococos (49,7%), tipificándose 109 cepas en las que se identificaron 28 serotipos diferentes con 54,1% de serotipos vacunales. En el estudio II se obtuvieron 101 muestras en las que se aislaron 35 neumococos (34,6%) de los cuales 21 fueron tipificados, presentando 14 serotipos diferentes, con 23% de serotipos vacunales. En el estudio III, de 374 muestras, se identificaron 244 S. pneumoniae (65,2%), con 93 cepas tipificadas, 32 serotipos distintos y 6,4% de serotipos vacunales.
En la (Tabla 1) se listan los serotipos identificados en los diferentes grupos de niños incluidos en los tres estudios.
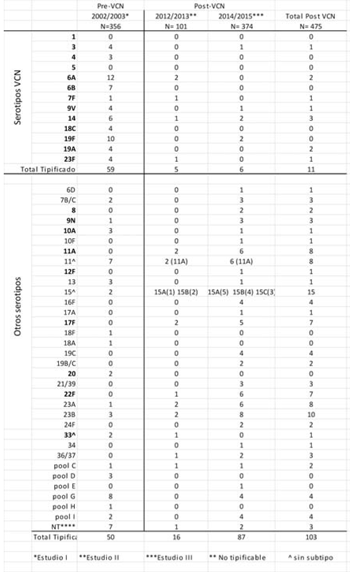
Tabla 1: Colonización nasofaríngea en niños pre-VCN y pos-VCN: serotipos identificados en cada período.
A pesar de las limitaciones metodológicas que interfieren con la comparación entre los estudios, la observación de los serotipos presentes en cada investigación proporciona diferentes evidencias. Datos prevacunación (estudio I) mostraron portación de serotipos invasores incluidos en las fórmulas de las VCN, con predominio de 6A, 6B, 14, 19F, pero en ninguno de los estudios se detectó portación del serotipo 5 ni del serotipo 1, ambos de reconocida capacidad invasora. Los resultados de los dos estudios posteriores a la vacunación muestran diferencias en las frecuencias de los serotipos vacunales. En el estudio II hay disminución de la frecuencia de esos serotipos, en tanto que en el estudio III se aprecia una casi desaparición de serotipos previamente predominantes, todos integrantes de la fórmula de la VCN 13. Los datos del estudio III confirman (6/93) que únicamente persisten los neumococos vacunales de los serotipos 14 (2), 19F (2), 3 (1) y 9V1.
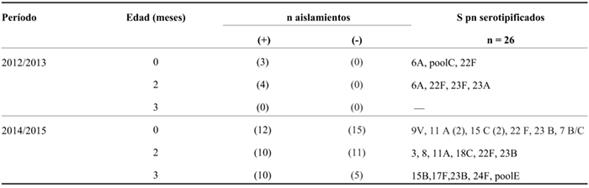
En la (Tabla 2) se muestran los neumococos que colonizan precozmente a lactantes, desde recién nacidos a 3 meses de edad, en ocasión de los dos estudios posvacunación. En el conjunto de ambos estudios se identificaron cinco cepas vacunales en un total de 26 neumococos tipificados.
Discusión
Los estudios de colonización nasofaríngea en niños permiten evaluar otro de los efectos preventivos de la vacunación con VCN, que controla los neumococos invasores en el reservorio nasofaríngeo, evitando su diseminación en la comunidad. Esos estudios informan además sobre cambios en la frecuencia de serotipos vacunales y la posible aparición o predominio de otros serotipos poco habituales. Proporcionan también información complementaria de los estudios etiológicos, que se caracterizan por su tradicional baja sensibilidad.
A pesar de la abundante bibliografía internacional referente al tema, no se localizaron publicaciones nacionales recientes, lo que valoriza la información que se presenta. Son resultados que corresponden a tres estudios independientes que permiten documentar la portación de serotipos en la nasofaringe de niños antes y luego de la aplicación de la VCN.
En el estudio I, previo a la introducción de la VCN (2002/2003), se comprobó en la nasofaringe de los niños un importante predominio de serotipos vacunales, como habían sido identificados en investigaciones de los años 1986/1987 y 1993/199517,18. También fue posible observar cambios en la presencia de las cepas vacunales (2012/2013 y 2014/2015), luego de la incorporación de las VCN al certificado esquema de vacunación. Existió una relativa persistencia de serotipos vacunales en el estudio II, lo que es explicable por una baja cobertura de la VCN debida a la edad de los niños o a su situación serológica que contraindica temporalmente la vacunación. En el estudio III el impacto atribuible a la VCN 13 lo evidenciaría la casi desaparición de los serotipos vacunales (6/93) previamente dominantes. En consecuencia, una menor circulación de los serotipos más patógenos prevendrá neumococcias severas como reiteradamente lo demostraron publicaciones nacionales sobre el impacto de la VCN19-22. Corresponde señalar, además, que la vacunación, con el tiempo, al reducir la circulación de los serotipos más invasores va creando en la población no vacunada una protección indirecta o inmunidad de rebaño23. No obstante, paulatinamente nuevos serotipos fueron ocupando el nicho ecológico abandonado por los serotipos vacunales, tal como se aprecia en el estudio III (2014/2015), pues casi la mitad de esos serotipos colonizaban la nasofaringe de los niños. Si bien son serotipos poco habituales en niños portadores, muchos de sus polisacáridos capsulares están representados en la vacuna 23-valente. Esta observación sustentaría la recomendación de vacunar con la VCN, complementada luego por la polisacarídica 23-valente a escolares y adolescentes con factores de riesgo24. De todos modos, la presencia de los serotipos 11A y 23B, poco habituales en las poblaciones infantiles, debe tenerse en cuenta y justifica la importancia de una estrecha vigilancia y seguimiento de su comportamiento futuro.
Se analizó también la colonización precoz de la nasofaringe de lactantes pequeños. Los primeros estudios realizados en países desarrollados demostraron que la colonización nasofaríngea ocurría luego de los 6 meses de edad, pero una investigación en niños de Nueva Guinea mostró colonización en los primeros días de vida25. En Uruguay reiteradamente se comprobó colonización temprana, presumiblemente por neumococos albergados por las madres18. La prevención de la colonización precoz, mediante inmunización materna con vacunas conjugadas y polisacarídicas, podría reducir o prevenir en los lactantes tiernos el riesgo que conlleva la portación de cepas invasoras y beneficiarse, además, de la transmisión de anticuerpos específicos en la leche materna26-28. No obstante, la Tabla 2 indica que los lactantes estudiados son también colonizados por serotipos no incluidos en ninguna de las vacunas disponibles.
Aun admitiendo las limitaciones metodológicas, la presentación de los resultados de los tres estudios proporciona información sobre aspectos epidemiológicos de una realidad inédita en el país. El registro de datos procedentes de períodos previos y posteriores a la introducción de las VCN en Uruguay permite destacar la efectividad de la vacuna para controlar la colonización nasofaríngea de niños en tiempos y grupos poblacionales diferentes.
Los resultados descritos proporcionaron datos sobre la presencia y cambios en la distribución de los serotipos en la nasofaringe de niños en distintas oportunidades. También documentaron la repercusión de la vacunación sobre el reservorio de S. pneumoniae durante los primeros años de su aplicación. La identificación de niños portadores de serotipos poco habituales es un llamado de atención que plantea el imperativo de instrumentar una vigilancia que monitorice la dinámica de la colonización en los niños a medida que pasan los años y aumentan las generaciones infantiles vacunadas con la VCN. En consecuencia, cabe señalar que esta información retrospectiva con resultados inéditos de tres períodos distintos, a pesar de las limitaciones metodológicas, confirma el impacto de la VCN y el reemplazo en el nicho ecológico nasofaríngeo por otros serotipos.