Introducción
La enfermedad injerto contra huésped (EICH) es una enfermedad multisistémica que aparece como complicación de un trasplante de progenitores hematopoyéticos (TPH) alogénico1. Representa la causa más importante de morbilidad y mortalidad tras la recidiva de la neoplasia hematológica que motivó el TPH2. La EICH se clasifica en dos tipos: aguda (EICHa) y crónica (EICHc), en función de sus distintos mecanismos fisiopatológicos y de su presentación clínica. La EICHc se presenta en 30%-70% de los pacientes3. La fisiopatología aún no es del todo conocida. Involucraría a linfocitos T del donante alorreactivos y linfocitos B con producción de anticuerpos4. En general, la EICHc se presenta tras los primeros 100 días post-TPH, con una media entre los 4 y 6 meses5. Son factores de riesgo para el desarrollo de EICHc: EICHa previa, pacientes o donantes de edad avanzada, mujer donante en receptor masculino, donante no emparentado o con incompatibilidad HLA, sangre periférica como fuente de progenitores hematopoyéticos, diagnóstico de leucemia mieloide crónica e infusión de linfocitos del donante6. Puede repercutir en cualquier órgano, siendo los más frecuen temente afectados la piel y la mucosa oral, siguiéndoles en frecuencia decreciente hígado y ojo3,7.
El diagnóstico se realiza en base a los criterios del National Institute of Health, actualizados en 2014 (Tabla 1). Esta clasificación establece criterios diagnósticos, distintivos y otros. En cuanto a la piel, los criterios diagnósticos no requieren realización de más estudios e incluyen: poiquilodermia, lesiones tipo liquen plano, esclerodérmicas, morfeiformes y tipo liquen escleroso. Las distintivas requieren estudio anatomopatológico y son: Lesiones vitiligoides y papuloescamosas. Otros hallazgos que se asocian, aunque no son lo suficientemente específicos, y apoyan el diagnóstico son la hipohidrosis, ictiosis, queratosis pilar, hipo e hiperpigmentación8. Clásicamente, en dermatología se han distinguido dos formas clínicas de EICHc cutánea: esclerodermiforme, con predominio de lesiones escleróticas, tipo liquen ecleroso y morfeiformes; y no esclerodemiforme, en la que las principales características clínicas son las lesiones liquenoides y poiquilodermia.
Tabla 1 Criterios diagnósticos del consenso del National Institute of Health, año 2014, en EICHc cutánea.
| Diagnósticos | Distintivos | Otros |
|---|---|---|
| Poiquilodermia Lesiones liquenoides Lesiones esclerodermiformes Lesiones morfeiformes Lesiones tipo liquen escleroso | Lesiones acrómicas Lesiones pápuloescamosas | Hipohidrosis Ictiosis Hipopigmentación Hiperpigmentación |
El tratamiento de la EICHc cutánea incluye medidas higiénico dietéticas, tratamientos tópicos en caso de enfermedad localizada, y sistémicos en caso de falla de los tratamientos tópicos, compromiso de múltiples órganos y compromiso generalizado de la piel. En cuanto a las medidas higiénico dietéticas se encuentran la fotoprotección y evitar agentes fotosensibilizantes. Los tratamientos tópicos incluyen emolientes, corticoides tópicos e inhibidores de la calcineurina9. El tratamiento sistémico de primera línea es la prednisona vía oral10. Ante el fracaso de esta, no existe un tratamiento de rescate estándar. En estos casos, se han utilizado terapias de segunda línea como sirolimus, mofetil micofenolato, rituximab, imatinib, metotrexato, fotoféresis extracorpórea, entre otros1. También se ha utilizado la fototerapia en distintas modalidades como psoralenos vía oral y luz ultravioleta A (PUVA), UVA-1, UVB y UVB banda estrecha (UVBbe)11. Reportamos el caso de una paciente con EICHc cutánea que respondió satisfactoriamente al tratamiento con fototerapia UVBbe.
Observación clínica
Paciente de 11 años de sexo femenino, con diagnóstico de leucemia linfocítica aguda el año 2008, a quien se le realizó en 2009 un TPH de sangre de cordón umbilical no emparentado. En el año 2013, presenta recaída igual al debut, realizándose un segundo TPH haploidéntico en marzo de 2014. A los seis meses, comienza con lesiones de piel en dorso, las que posteriormente se diseminan. En tratamiento con prednisona 20 mg al día vía oral.
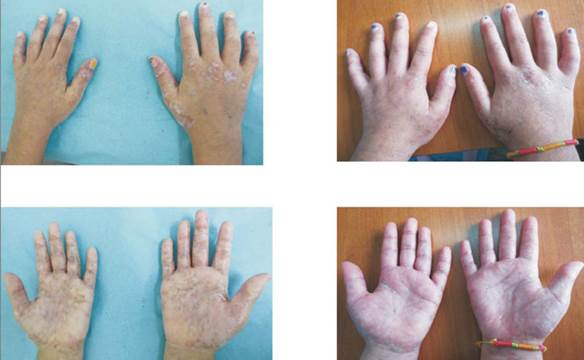
Es evaluada por la unidad de dermatología pediátrica en marzo del 2016. Al examen físico presenta compromiso de piel, faneras y mucosa oral. A nivel de piel, presenta un compromiso generalizado, con predominio en tronco y miembros superiores, dado por induración cutánea generalizada, placas esclerodermiformes vitiligoides. En codos y dorso de manos presenta pápulas y placas eritematosas con escama gruesa adherente, en dedos afinamiento digital y a nivel de palmas eritema y cambios dispigmentarios. En faneras, presenta en cuero cabelludo alopecia difusa, con escama blanquecina adherente y en uñas traquinoquia. Respecto a mucosas, presenta queilitis angular y a nivel de mucosa oral lesiones liquenoides y úlceras con dolor leve que no dificulta la alimentación. Prurito moderado. No presenta compromiso del tracto gastrointestinal, hepático ni refiere síntomas musculoesqueléticos. Resto del examen físico normal. Con estos hallazgos y contexto clínico diagnosticamos EICHc cutánea moderada e indicamos emoliencia con crema reparadora de barrera cutánea y clobetasol al 0,05% tópico una vez por día en palmas. Iniciamos fototerapia UVB banda estrecha tres veces por semana con dosis de 130 mJ/cm2, incrementándose dosis según tolerancia. A los tres meses de tratamiento, observamos una importante mejoría, en particular de la induración cutánea, lesiones eritematoescamosas y lesiones de manos. Figura 1 y Figura 2.
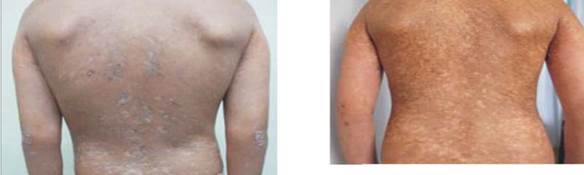
Figura 1 Cuadro clínico pretratamiento (a izquierda) y 2 meses postratamiento (derecha). Obsérvese disminución de lesiones esclerodermiformes a nivel de dorso medio y bajo; y de lesiones pápuloescamosas a nivel de codos
Discusión
La EICHc cutánea esclerodermiforme es una forma poco frecuente de EICHc, con una prevalencia estimada de un 3% a 11% de los pacientes que son sometidos a un TPH halogénico12. Su tratamiento continúa siendo un desafío, puesto que una opción terapéutica efectiva y segura, aún no se ha establecido. Los corticoides sistémicos son utilizados como tratamiento de primera línea, con o sin otros inmunosupresores asociados13,14. Si bien en muchos pacientes estos tratamientos logran cierta mejoría, los efectos adversos como el aumento del riesgo de infecciones y neoplasias, este último ya aumentado en los pacientes con EICHc, limitan su uso a largo plazo15,16. Es por esto, que continuamente se evalúan otras alternativas terapéuticas más seguras.
En el tratamiento de la EICHc cutánea, aunque se han utilizado una variedad de modalidades de fototerapia, la literatura actual se limita a reportes y series de casos. El uso de la fototerapia en estos pacientes se basa en el hecho de que ejerce efectos antiproliferativos y apoptóticos celulares (por ejemplo linfocitos T), inmunomodulación mediante la activación celular, presentación de antígenos, liberación de citoquinas y activación de colagenasas17-19.
A mayor longitud de onda, la luz se absorbe más profundamente en la piel, es así como la UVB se absorbe principalmente en la epidermis, mientras que la UVA penetra más profundamente en la dermis20. Por esta razón, se cree que las lesiones esclerodermiformes son mejor tratadas con fototerapia a base de UVA y las lesiones liquenoides con fototerapia a base de UVB11.
Los reportes han descrito tratamientos exitosos de formas esclerodermiformes y liquenoides con PUVA oral, baños con PUVA y UVA-121-23. En cuanto al tratamiento con UVB la literatura es escasa. Brazelli y colaboradores24 describieron una serie de 10 pacientes pediátricos con EICHc cutánea no esclerodermiforme tratados con UVBbe, en la cual, al año de tratamiento el 75% obtuvo una respuesta completa y el 25% una respuesta parcial. Enk y colaboradores25 reportaron una serie de tres pacientes con compromiso cutáneo tratados con UVB, de los cuales uno, con EICHc liquenoide, presentó respuesta completa, mientras que los dos restantes, con EICHc esclerodermiforme, presentaron mejoría del prurito y xerosis, sin embargo, no de las lesiones cutáneas. Recientemente, Sorenson y colaboradores26 reportaron un único caso de EICHc cutánea esclerodermiforme tratada con UVBbe, que mostró un mejoría significativa de las lesiones a los 2 meses de tratamiento. Respecto a la duración del tratamiento, aunque las series de casos reportan una duración de tratamiento de entre 2 y 6 meses, no existen pautas establecidas, por lo que se debe evaluar caso a caso.
Si bien la fototerapia con UVBbe en general no se considera en el tratamiento de las lesiones esclerodermiformes, esta produce efectos inmunomoduladores en la dermis, que es el sitio principal de la fibrosis en las lesiones esclerodermiformes27. Aún más, la UVBbe ha demostrado una reducción significativa en la severidad de la esclerodermia localizada autoinmune28.
Respecto a los efectos adversos, la fototerapia con UVB tiene importantes ventajas en comparación a PUVA en el tratamiento de la EICH. No requiere la administración de un psoraleno oral, el cual puede producir náuseas en algunos pacientes, llevando a una disminución en la adherencia al tratamiento. En raros casos el psolareno oral puede ser hepatotóxico. También se ha reportado un menor riesgo de cáncer de piel con UVBbe que con PUVA oral29.
Dados los buenos resultados en estudios preliminares y su perfil de seguridad, la fototerapia UBVbe es una opción terapéutica prometedora en el tratamiento de la EICHc cutánea. Sin embargo, se requieren estudios comparativos adicionales a gran escala para determinar su rol definitivo como terapia adyuvante o incluso de primera línea; el perfil de pacientes que más se beneficiará con su uso y los esquemas terapéuticos y dosis más efectivas.