Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Archivos de Pediatría del Uruguay
versión impresa ISSN 0004-0584versión On-line ISSN 1688-1249
Arch. Pediatr. Urug. vol.87 no.4 Montevideo dic. 2016
Uso de óxido nítrico inhalado en el tratamiento de la dificultad respiratoria temprana en el recién nacido pretérmino inmaduro y pretérmino tardío. Reporte de dos casos clínicos
Inhaled nitric oxide in the treatment of early respiratory failure in the late preterm and early term newborn. Report of two cases
Antonio Lustemberg1, Fernanda Blasina2, Fernando Silvera3, Lucía Vaamonde4
1. Pediatra Neonatólogo. Ex Asistente Neonatología. Hospital de Clinicas. UDELAR.2. Prof. Agda. Depto. Neonatología. Hospital de Clínicas. Facultad de Medicina. UDELAR.
3. Prof. Agdo. Depto. Neonatología. CHPR. Facultad de Medicina. UDELAR.
4. Prof Adj. Depto. Neonatología. Área básica. Hospital de Clínicas. Facultad de Medicina. UDELAR.
Depto. Neonatología. Hospital de Clínicas. Facultad de Medicina. UDELAR.
Trabajo inédito.
Declaramos no tener conflictos de intereses.
Fecha recibido: 17 de noviembre de 2015.
Fecha aprobado: 11 de mayo de 2016.
Resumen
La falla en la transición de la circulación fetal a la neonatal puede ser causada por la persistencia de resistencias vasculares elevadas, lo que induce al síndrome de hipertensión pulmonar (HPPN) que ocurre en aproximadamente 2 de cada 1.000 recién nacidos. La HPPN severa se asocia con recién nacidos de término o cercanos al término, si bien puede verse en recién nacidos prematuros. El tratamiento estándar de oro es el óxido nítrico inhalado (ONi) en neonatos con falla respiratoria hipóxica e HPPN. En el Departamento de Neonatología del Hospital de Clínicas de Montevideo se utilizó un generador in situ de óxido nítrico-NO- (TAS+plus®) portátil, capaz de producir continuamente el gas para ser entregado al recién nacido. Su bajo costo y accesibilidad han ampliado sus indicaciones en pacientes con asistencia ventilatoria mecánica (AVM), presión positiva continua en la vía aérea a través de cánula nasal (CPAP nasal) o bajo carpa cefálica.
Presentamos dos pacientes con dificultad respiratoria, en los que una vez descartada cardiopatía congénita estructural y con evidencia ecocardiográfica de HPPN se administró ONi, concomitante al soporte respiratorio con CPAP nasal, con el objetivo de evitar la progresión de la enfermedad respiratoria y AVM. Dichos pacientes de 32 y 37 semanas, presentaron buena evolución de su dificultad respiratoria.
La mejoría de la falla respiratoria hipóxica mediante la administración de ONi, sin necesidad de ventilación invasiva, fue posible, de bajo costo y fácil de aplicar a los pacientes, incorporando la utilización de un novel generador de ONi en la práctica clínica.
Palabras clave:
ÓXIDO NÍTRICO
SÍNDROME DE DIFICULTAD RESPIRATORIA
HIPERTENSIÓN PULMONAR
RECIÉN NACIDO
Summary
Failure in transition from fetal to neonatal circulation can be caused by the persistence of elevated vascular resistance, which can lead to pulmonary hypertension syndrome (HPPN), occuring in approximately 2 out of 1,000 live newborns. Severe HPPN is associated with term or near term newborns, although it may be seen in preterms. The gold standard treatment is inhaled nitric oxide (NOi) in neonates with hypoxic respiratory failure and HPPN. In the Department of Neonatology of the University Hospital in Montevideo, a portable, in situ generator of nitric oxide-NO- (TAS+plus®) was used, which is capable to continuously produce the gas to be delivered to the newborn. Its low cost and accessibility have expanded its indications to patients with mechanical ventilation (MVA), continuous positive airway pressure through nasal cannula (nasal CPAP) or cephalic carp.
We present two patients with respiratory distress, in whom, once the structural congenital heart disease and echocardiographic evidence of HPPN were discarted, NOi was administered, concomitant with nasal CPAP, in order to avoid the progression of respiratory disease and AVM. These patients of 32 and 37 weeks presented good evolution of their respiratory difficulty.
The improvement of hypoxic respiratory failure through the administration of NOi, without the need for invasive ventilation, was possible, low cost and easy to apply to patients, incorporating the use of a novel ONi generator in clinical practice.
Key words:
NITRIC OXIDE
RESPIRATORY DISTRESS SYNDROME
PULMONARY HYPERTENSION
NEWBORN
Introducción
La transición satisfactoria de la circulación fetal a la neonatal y el cese de la dependencia placentaria, requiere que se establezca un volumen pulmonar adecuado, concomitante con el descenso de la resistencia vascular pulmonar y el aumento del flujo sanguíneo pulmonar. Estos cambios fisiológicos se dan a partir de los primeros minutos de vida vinculados, por lo general, a la primera insuflación gaseosa de los pulmones y al aumento del contenido de O2 en sangre. Cuando esto no ocurre, la resistencia vascular arterial pulmonar permanece elevada. Esto deriva sangre a través del foramen oval y del ductus arterioso permeable desde las cavidades cardíacas derechas, al territorio sistémico configurando la entidad conocida como persistencia de la circulación fetal o hipertensión pulmonar persistente neonatal (HPPN).
El síndrome clínico de HPPN puede verse en aproximadamente 2 de cada 1.000 recién nacidos vivos, ocurre en asociación con varias enfermedades neonatales, incluyendo síndrome de aspiración de líquido amniótico meconial, sepsis por Streptococcus grupo B, hernia diafragmática congénita, enfermedad de membrana hialina (EMH), así como por causas indeterminadas (idiopáticas). Comúnmente la HPPN severa se asocia con neonatos de término o cercanos al término, si bien puede verse en recién nacidos prematuros con EMH o displasia broncopulmonar(1,2).
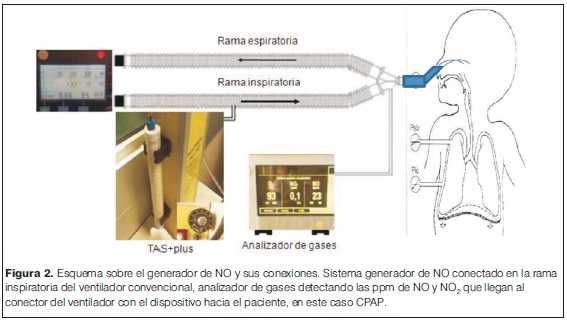
La terapia con óxido nítrico inhalado (ONi) disminuye el riesgo de oxigenación por membrana extracorpórea y la mortalidad en neonatos con falla respiratoria hipóxica e HPPN a las 34 semanas de edad gestacional, sin embargo el momento óptimo de severidad de la enfermedad para iniciar esta terapia con respecto a otras medidas de soporte no es claro(3-8). Su elevado costo y el tamaño de los dispositivos para su administración disminuyen sus aplicaciones terapéuticas. En el área básica del Departamento de Neonatología del Hospital de Clínicas de Montevideo, se diseñó un generador in situ de óxido nítrico-NO- (TAS+plus®) (figura 1), portátil, capaz de producir continuamente el gas para ser entregado al recién nacido. Su accesibilidad ha ampliado sus indicaciones pudiendo ser adaptado al circuito ventilatorio de pacientes en asistencia ventilatoria mecánica (AVM), con presión positiva continua en la vía aérea a través de cánula nasal (CPAP nasal) o bajo carpa cefálica (figura 2).
En los últimos años se han producido cambios conceptuales en la asistencia respiratoria inicial tanto en la sala de partos, como en la unidad de cuidados intensivos. Si bien el tipo de apoyo respiratorio dependerá de la severidad y la causa de la dificultad respiratoria, la tendencia actual es a utilizar métodos menos invasivos de soporte ventilatorio, como CPAP nasal, ventilación nasal, cánula nasal de alto flujo(9), basados en que la ventilación mecánica invasiva se asocia fuertemente con lesión pulmonar, infección y enfermedad respiratoria crónica(10). También se ha demostrado que el uso de surfactante temprano y la terapia con ONi mejora la evolución de recién nacidos de término o pretérmino tardío con falla respiratoria hipóxica moderada(11).
En este contexto presentamos dos pacientes con dificultad respiratoria temprana, en los que una vez descartada cardiopatía congénita estructural y con evidencia ecocardiográfica de HPPN se administró ONi, concomitante al soporte respiratorio con CPAP nasal con el objetivo de evitar la progresión de la enfermedad respiratoria hipóxica.
Criterios de inclusión:
- Dificultad respiratoria temprana.
- Necesidad de fracción inspirada de oxígeno (FiO2) entre 0,4 y 0,5.
- Inestabilidad clínica.
- Ecocardiograma con evidencia de HPPN sin falla en el ventrículo izquierdo.
Criterios de exclusión: presencia de cardiopatía congénita.
Intervención terapéutica:
- Administración de ONi a través de CPAP nasal, dosis inicial de 10 ppm y aumentando hasta 20 ppm.
- Duración del tratamiento: 72 horas.
Casos clínicos
Caso clínico 1
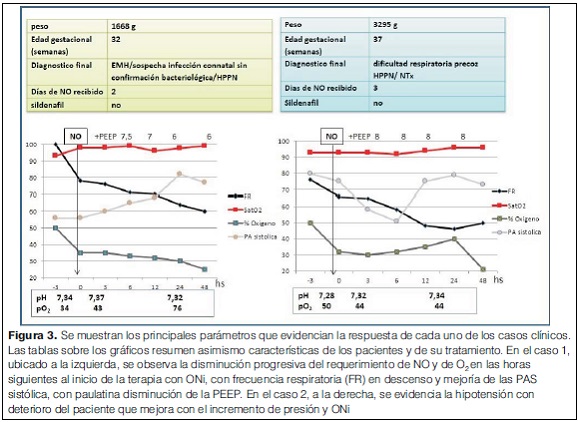
Madre de 23 años, portadora de útero bicorne, grupo sanguíneo A Rh +, serología para virus de inmunodeficiencia humana negativo, prueba serológica de sífilis VDRL negativo, serología para toxoplasmosis negativa. Segundo embarazo, fecha última menstruación no confiable, captación tardía, embarazo mal controlado, ingresó cursando 31 semanas de edad gestacional (por ecografía temprana) constatándose inicio de trabajo de parto, recibió 6 mg de dexametasona intramuscular. Cesárea de urgencia, 32 semanas de edad gestacional, recién nacido sexo masculino, Apgar 7/9, peso al nacer 1.668 g, longitud 43 cm, perímetro craneano 31 cm, gasometría de cordón normal. Fue ingresado a unidad de cuidados intensivos por presentar dificultad respiratoria temprana, se inició apoyo respiratorio con CPAP, a las 2 h de vida inestabilidad respiratoria y aumento de requerimientos de O2, radiografía de tórax compatible con EMH, por lo que se realizó intubación orotraqueal. Se administró una dosis de surfactante manteniéndose en AVM por 6 h, pasando nuevamente a CPAP nasal. Ecocardiograma primeras 24 h de vida normal, reiterado a los 4 días de vida, evidenció HPPN y se inició ONi. En lo infeccioso se administró ampicilina y gentamicina por sospecha de infección connatal no confirmada. En la evolución mejoría de la situación clínica que se detalla en figura 3.
Caso clínico 2
Madre de 22 años, fumadora, cuarto embarazo, bien controlado sin complicaciones, grupo sanguíneo A, Rh +, serología para virus de inmunodeficiencia humana negativo, prueba serológica de sífilis VDRL negativo, antígeno hepatitis B superficie negativo. Cesárea por dolor en segmento, sin trabajo de parto y membranas íntegras, 37 semanas de edad gestacional, recién nacido de sexo masculino, Apgar 8/8, peso al nacer 3.295 g, longitud 48 cm, perímetro craneano 37 cm. Instaló dificultad respiratoria temprana dado por trabajo respiratorio y quejido por lo que se inició aporte de O2 bajo carpa cefálica y se realizó hidratación parenteral.
Dada la persistencia de dificultad respiratoria se realizó traslado especializado en incubadora bajo carpa cefálica e ingresó a cuidados intensivos neonatales de la maternidad del Hospital de Clínicas. Examen físico a su ingreso: 5 h de vida, reactivo, palidez cutánea, aleteo, retracción costal, quejido intermitente, saturación de oxígeno 99%; a nivel cardiovascular ritmo regular de 140 cpm, ruidos bien golpeados, no soplos, presión arterial media 48 mmHg, pulsos femorales presentes. El paciente se traslada bajo carpa cefálica con O2 y llega a la unidad con saturación preductal 100% y posductal 98%. Se decide iniciar CPAP nasal, presión positiva al final de la espiración (PEEP) 6,5 cm H2O, FiO2 0,35.
Gasometría arterial a las 7 h de vida: pH 7,33, presión parcial de O2 (pO2) 64,7 mmHg, presión parcial de CO2 (pCO2) 43,2 mmHg, exceso de bases (BE) -3,3, HCO3 21,9 mmol/l, lactato 1,8 mmol/l, PaO2/FiO2= 184. Hemoglobina 12,3 g/dl, Hematocrito 37,9%.
A las 36 h de vida presentó deterioro clínico, con saturación de O2 preductal 92% y postductal 84%. Gasometría arterial pH 7,34, pO2 34,7 mmHg, pCO2 41,2 mmHg, saturación de O2 71,6%, BE -2,9 mmol/l, HCO3 22 mmol/l, glucosa 99 mg/dl, lactato 1,4 mmol/l, Hemoglobina 12,1 g/dl, Hto 37,4%, metahemoglobina 0,7%, K 3,5 meq/l, Na 141 meq/l. FiO2 0,5. PaO2/FiO2 =69,4.
Ecocardiograma: moderada HPPN con presión máxima en ventrículo derecho de 48 mmHg y fracción de eyección del ventrículo izquierdo normal. Se inició ONi a través de CPAP nasal, PEEP 6, FiO2 0,5, saturaciones estables pre y posductales de 98% y ONi a 15,6 ppm. Evolución favorable que se detalla en figura 3.
Discusión
Este reporte muestra el manejo de la falla respiratoria hipóxica mediante la administración de ONi sin necesidad de ventilación invasiva. Introduce además la utilización de un novel generador de ONi en la práctica clínica.
El NO es un vasodilatador selectivo a nivel pulmonar, que ha demostrado su eficacia en el tratamiento de la falla respiratoria hipoxémica severa asociada a la HPPN en los recién nacidos de término o pretérmino tardío desde 1992 (12, 13). En 1999 fue aprobado por la FDA para su uso en este grupo de pacientes con HPPN con el dispositivo Inomax ® y por la Agencia Europea de Evaluación Médica y la Comisión Europea en el año 2001(14).
Múltiples estudios demostraron que la administración de ONi en pacientes con hipoxemia mejora la oxigenación, evaluado por el índice de oxigenación (IO=FiO2 x presón media de la vía aérea x 100/PaO2) y disminuye la incidencia de muerte o necesidad de oxigenación por membrana extracorpórea (acrónimo en inglés: Extra Corporeal Membrane Oxygenation) en pacientes con HPPN (riesgo relativo (RR) 0,68 [95% intervalo de confianza (IC) 0,59–0,79]). De la misma manera la administración de ONi en los recién nacidos de término o pretérminos tardíos hipoxémicos redujo la necesidad de ECMO (RR 0,63, IC95% 0,54-0,75; diferencia de riesgo típica -0,19, IC95% -0,26 a-0,12. NNT= 5,3 IC95% 3,8-8,3), sin efecto sobre la incidencia aislada de muerte.
ECMO provee mediante un cortocircuito funcional soporte respiratorio y circulatorio, por un período de tiempo prolongado en el que la patología causal es tratada(15). En los países que disponen de ECMO neonatal se ha observado una disminución de su uso en los últimos años, esto se debe a mejoría en los cuidados perinatales y a la disponibilidad de terapias para la falla respiratoria hipóxica incluyendo: ventilación de alta frecuencia, surfactante y ONi. Los criterios generalmente aceptados para iniciar ECMO son la hipoxemia persistente con un IO >40 o un gradiente alveolar-arterial >600 a pesar de un agresivo tratamiento (en el que se incluye ventilación mecánica y ONi). En Uruguay no contamos con ECMO para el tratamiento de la HPPN grave y la falla respiratoria hipóxica grave del recién nacido por lo que la optimización del soporte respiratorio y la administración de ONi son las máximas terapias disponibles.
El IO baja a una media de 15,8 en unos 30 a 60 minutos luego de iniciar la terapia y la pO2 se incrementa a una media de 53 mmHg(16,17). Que los niños tengan una clara evidencia de HPPN en la ecocardiografía o no, no impresiona afectar la evolución. La incidencia de discapacidad, sordera y la valoración de los índices de desarrollo son similares entre los sobrevivientes que recibieron ONi o no.
Con respecto a la severidad de la enfermedad al momento del inicio de la terapia con ONi, iniciando éste a un grado menor de severidad, la revisión sistemática Cochrane de Finer y Barringnton demostró que previene la progresión de las formas menos severas a la más graves (grupo de ONi 61% progresaron a las formas más severas vs 81% en el grupo control), si bien no mostró reducir el riesgo de muerte o de requerimiento de ECMO, no encontrándose otras diferencias en cuanto a duración de ventilación mecánica, días de hospitalización, duración de oxigenoterapia, o incidencia de enfermedad pulmonar crónica(18). Por su parte el estudio de Golombek y colaboradores(7) (n=524) demostró que la administración de ONi a 20 ppm a recién nacidos de término y pretérminos tardíos con falla respiratoria hipóxica, fue efectivo en mejorar la oxigenación de manera aguda y en reducir los días de ventilación mecánica para todos los grados de severidad de la enfermedad estudiados (desde IO ³ 15 hasta IO ³ 40)(19).
El uso de ONi en recién nacidos prematuros ha llevado a la realización de una amplia variedad de estudios. En 1993 Abman y colaboradores reportaron una marcada mejoría en la oxigenación en recién nacidos prematuros tratados con ONi, que presentaban HPPN severa y resolución de la derivación extrapulmonar derecha-izquierda(20).
Hallazgos similares fueron reportados en recién nacidos pretérminos con falla respiratoria severa(21,22). Clark y colaboradores (2010), reportan un aumento de seis veces en el uso de ONi en recién nacidos pretérminos menores a 34 semanas de edad gestacional (de 0,3% a 1,8%) entre los años 2000 al 2008; el mayor incremento ocurrió entre los recién nacidos entre las 23 a 26 semanas de gestación (0,8% a 6,6%)(23).
Si observamos su uso para prevenir la broncodisplasia pulmonar, Schreiber y colaboradores reportaron un descenso en la incidencia de la misma en el grupo de los recién nacidos pretérminos que requirieron soporte ventilatorio y fueron tratados con ONi(24), este resultado no se reprodujo en los trabajos publicados por Kinsella y colaboradores ni por Mercier y colaboradores(25,26). Ballard y colaboradores realizaron un estudio caracterizado por tratamiento tardío (7-21 días de edad), duración más prolongada de exposición a ONi (25 días) y dosis acumulada más alta, evidenciando un beneficio modesto pero estadísticamente significativo (44% ONi vs 37% placebo; p=0,042)(27).
Se ha estudiado y descartado la utilidad del ONi como preventivo de la broncodisplasia pulmonar, pero aún resta evaluar la utilidad del mismo en los pacientes con broncodisplasia severa que muestran signos clínicos o ecocardiográficos de hipertensión pulmonar o en aquellos pacientes que presentan episodios de exacerbación en donde puede ponerse de manifiesto hipoxemia severa con mala respuesta a las terapias habituales. Cabe entonces preguntarse qué rol puede cumplir el ONi en estos pacientes ya sea para atenuar la hipertensión pulmonar subyacente o para revertir episodios de exacerbación de broncodisplasia pulmonar, para lo cual parece indispensable contar con dispositivos que proporcionen ONi sin límites y a bajo costo. Y de acuerdo a la línea de este trabajo la administración de ONi no invasivo para evitar intubación y AVM. En este sentido Kinsella y col (2016) recomiendan el uso de ONi en pretérminos sobre otros vasodilatadores pulmonares basados en la seguridad que ha mostrado esta terapia en numerosos estudios realizados.
La intubación endotraqueal y la ventilación mecánica están asociadas con daño pulmonar lo cual incrementa el riesgo y la severidad de la broncodisplasia pulmonar en los recién nacidos pretérminos. El inicio temprano del apoyo ventilatorio mediante el uso de CPAP podría disminuir la necesidad de intubación y el uso de la ventilación mecánica disminuyendo de este modo el riesgo de daño pulmonar inducido por la ventilación y broncodisplasia pulmonar, si bien la evidencia al respecto es controvertida(28).
Kinsella y colaboradores plantearon la hipótesis de si el uso temprano y prolongado de ONi con CPAP o cánula nasal podría reducir la necesidad de intubación endotraqueal, ventilación mecánica y el riesgo de broncodisplasia pulmonar en recién nacidos pretérminos, concluyendo que dicho tratamiento era seguro pero no disminuía la variable combinada de muerte/broncodisplasia pulmonar en los recién nacidos pretérminos con pesos de 500-1.250 g tratados dentro de las primeras 72 h luego del nacimiento, no hubo diferencia en la severidad de broncodisplasia pulmonar, la necesidad del uso de ventilación mecánica, la duración de la ventilación mecánica o el riesgo de hemorragia intracraneal severa(29).
Si consideramos su efecto en el desarrollo del sistema nervioso central, Mestan y colaboradores reportan una evolución más favorable del neurodesarrollo a un año de edad entre los recién nacidos pretérminos que recibieron ONi, pero no constata diferencias en la frecuencia de parálisis cerebral(30). La Academia Americana de Pediatría, basada en la evidencia actual, no apoya el tratamiento de recién nacidos pretérminos con ONi con el propósito de prevenir o disminuir la broncodisplasia pulmonar, la hemorragia intraventricular severa u otras morbilidades neonatales(31). Sin embargo, un estudio multicéntrico, randomizado, controlado, sugiere que el tratamiento con dosis de NO de 20 ppm, iniciado en la segunda semana posnatal, puede proveer una pequeña reducción en la frecuencia de broncodisplasia pulmonar(21). En análisis más recientes, la incidencia de parálisis cerebral, la afectación del neurodesarrollo o cognitiva, tanto en los recién nacidos pretérminos tratados con ONi como en el grupo control fue similar(24). En abril de 2015, Ellsworth y colaboradores(6) publicaron un estudio sobre el uso de ONi fuera de su indicación establecida por la Academia Americana de Pediatría en recién nacidos pretérminos <34 semanas en Unidades de Cuidado Intensivo Neonatal de los Estados Unidos. Concluyen que las tasas de uso fuera de su indicación continúan aumentando pese a la evidencia clínica y la opinión de expertos que sugieren la ausencia de beneficios claros en recién nacidos pretérminos. En este sentido los dos casos que se presentan aquí están enmarcados en indicaciones no clásicas, sustentado su uso con el objetivo de evitar la progresión de la dificultad respiratoria, su agravamiento y necesidad de intubación orotraqueal y AVM.
La administración de ONi sin necesidad de intubación orotraqueal es una estrategia que ha comenzado a estudiarse desde el año 2002 en el que Ambalavan y colaboradores(32) mostraron la aplicabilidad y la eficacia hemodinámica de la administración de ONi en carpa cefálica en cerdos con HPPN; en 2002 el mismo grupo de investigadores realizó un estudio piloto con solo 6 pacientes con edad gestacional > 34 semanas, con una diferencial alvéolo arterial de O2 entre 400 y 600 mmHg como criterio de inclusión, mostrando similares resultados, sin evidencia de contaminación ambiental o de efectos adversos o ambos a corto plazo(33). Lindwall y colaboradores estudiaron el impacto sobre el ambiente laboral de la administración de ONi mediante CPAP nasal, no encontrando alteraciones significativas en los valores de NO ni de NO2 ambientales(34). Posteriormente un estudio piloto en recién nacidos pretérminos con síndrome de dificultad respiratoria (edad gestacional promedio 32 semanas, n=15) mostró la mejoría significativa de la oxigenación sin efectos hemodinámicos adversos y en recién nacidos pretérminos expuestos a rotura prolongada de membranas e hipoplasia pulmonar (edad gestacional promedio 30 semanas, n= 7) la reducción de la persistencia de circulación pulmonar fetal(35, 36).
Con respecto a los costos, se estima una media de U$S 5.753 por día de terapia con ONi, considerando que fue usado en un total de 3.409 días paciente, durante el año 2013 en el Pediatrix Medical Group en las Unidades de Cuidado Intensivo Neonatal, esta prescripción fuera de lo indicado generó un costo de U$S 19,6 millones, si bien la exactitud de estas estimaciones no es clara(6). El equipo TAS+Plus® es capaz de entregar NO durante todo el tiempo que se requiera y a las dosis que se indiquen, no variando el costo según estos últimos parámetros. Se trata de un prototipo que fue desarrollado con la empresa fabricante Injectmatic de Suiza, trabajando en conjunto con el área básica del Depto. de Neonatología del Hospital de Clínicas. En este sentido, si bien la idea de generar NO al lado de la cama del paciente ha sido patentada (US5396882A), el uso del prototipo en Uruguay es innovador y su bajo costo (únicamente el inicial), genera la enorme ventaja de no limitar las indicaciones por motivos económicos. Se trata de un equipo productor de gas enriquecido en NO que se genera en forma pulsada que se entrega al paciente en un circuito que posea un flujo de O2/Aire o su mezcla continuo.
En nuestro caso, que la limitante de costos no se encuentra presente dado que se trata de un generador de NO con producción ilimitada del gas, el hecho clave de poder prevenir la progresión de la enfermedad a mayor severidad, son razones de peso para intentar la utilización con indicaciones más flexibles comparadas con las clásicas de IO de 15 o mayores. Es por eso que consideramos de enorme valor la experiencia aquí presentada con los casos referidos, dado que en ambos se observó la mejoría de la dificultad respiratoria y estabilización de los pacientes, sin necesidad de intubación orotraqueal para administración de ONi.
En países como el Uruguay, en el que la terapia máxima para el tratamiento de la HPPN es ONi y modos ventilatorios alternativos, esta posibilidad de intentar el tratamiento con ONi en casos de moderada severidad, con el objetivo de evitar la ventilación mecánica convencional y limitar la iatrogenia derivada de la misma, está plenamente justificada.
Conclusiones
En este reporte se muestran dos pacientes en quienes se administra ONi con suceso favorable utilizando un dispositivo generador de este gas al lado de la cama del paciente, mediante ventilación no invasiva en pacientes con HPPN. Muestra la efectividad de la terapia en controlar la HPPN evitando la ventilación mecánica invasiva.
Referencias bibliográficas
1. Kinsella JP. Nitric Oxide Therapy in Neonatology. En: Buonocore G, Bracci R, Weindling M, eds. Neonatology: a practical approach to neonatal disease. Milan: Springer-Verlag, 2012: 529-36.
2. Nair J, Lakshminrusimha S. Update on PPHN: mechanisms and treatment. Semin Perinatol 2014; 38(2):78-91.
3. Neonatal Inhaled Nitric Oxide Study Group. Inhaled nitric oxide in full-term and nearly full-term infants with hypoxic respiratory failure. N Engl J Med 1997; 336(9):597-604.
4. Roberts J Jr, Fineman J, Morin F, Shaul P, Rimar S, Schreiber MD, et al. Inhaled nitric oxide and persistent pulmonary hypertension of the newborn. N Engl J Med 1997; 336(9): 605-10.
5. Clark R, Kueser T, Walker MW, Southgate W, Huckaby JL, Perez J, et al; Clinical Inhaled Nitric Oxide Research Group. Low-dose nitric oxide therapy for persistent pulmonary hypertension of the newborn. N Engl J Med 2000; 342(7): 469-74.
6. Ellsworth MA, Harris MN, Carey W, Spitzer A, Clark R. Off-label use of inhaled nitric oxide after release of NIH consensus statement. Pediatrics 2015; 135(4):643-8.
7. Golombek S, Suttner D, Ehrlich R, Potenziano J. Target versus actual oxygenation index at initiation of inhaled nitric oxide in neonates with hypoxic respiratory failure: survey results from 128 patient cases. J Perinat Med 2014; 42(6):685-92.
8. Wessel D, Adatia I, Van Marter L, Thompson J, Kane J, Stark A, et al. Improved oxygenation in a randomized trial of inhaled nitric oxide for persistent pulmonary hypertension of the newborn. Pediatrics 1997; 100(5):E7.
9. Soll R, Edwards E, Badger G, Kenny MJ, Morrow K, Buzas J, et al. Obstetric and neonatal care practices for infants 501 to 1500 g from 2000 to 2009. Pediatrics 2013; 132(2):222-8.
10. Hutchison A, Bignall S. Non-invasive positive pressure ventilation in the preterm neonate: reducing endotrauma and the incidence of bronchopulmonary dysplasia. Arch Dis Child Fetal Neonatal Ed 2008; 93(1):F64-8.
11. Konduri G, Sokol G, Van K, Singer J, Ambalavanan N, Lee T, et al. Impact of early surfactant and inhaled nitric oxide therapies on outcomes in term/late preterm neonates with moderate hypoxic respiratory failure. J Perinatol 2013; 33(12):944-9.
12. Kinsella JP, Neish S, Shaffer E, Abman S. Low-dose inhalation nitric oxide in persistent pulmonary hypertension of the newborn. Lancet 1992; 340(8823):819-20.
13. Roberts J, Polaner D, Lang P, Zapol W. Inhaled nitric oxide in persistent pulmonary hypertension of the newborn. Lancet 1992; 340(8823):818-9.
14. INO Therapeutics. INOmax (Nitric Oxide): application No. 20-845. En: European Medicine Agency. Informe Público Europeo de evaluación (EPAR) 12/23/1999. Disponible en: http://www.emea.eu. (Consulta: 12 de octubre de 2015).
15. Lakshminrusimha S, Keszler M. Persistent Pulmonary Hypertension of the Newborn. Neoreviews 2015; 16(12): e680-92.
16. Mercier JC, Lacaze T, Storme L, Rozé JC, Dinh-Xuan A, Dehan M; French Paediatric Study Group of Inhaled NO. Disease-related response to inhaled nitric oxide in newborns with severe hypoxaemic respiratory failure. Eur J Pediatr 1998; 157(9):747-52.
17. Christou H, Van L, Wessel D, Allred E, Kane J, Thompson J, et al. Inhaled nitric oxide reduces the need for extracorporeal membrane oxygenation in infants with persistent pulmonary hypertension of the newborn. Crit Care Med 2000; 28(11): 3722-7.
18. Finer N, Barrington K. Nitric oxide for respiratory failure in infants born at or near term. Cochrane Database Syst Rev 2006; 18(4):CD000399.
19. Golombek S, Young J. Efficacy of inhaled nitric oxide for hypoxic respiratory failure in term and late preterm infants by baseline severity of illness: a pooled analysis of three clinical trials. Clin Ther 2010; 32(5):939-48.
20. Abman S, Kinsella JP, Schaffer MS, Wilkening R. Inhaled nitric oxide in the management of a premature newborn with severe respiratory distress and pulmonary hypertension. Pediatrics 1993; 92(4):606-9.
21. Peliowski A, Finer N, Etches P, Tierney A, Ryan C. Inhaled nitric oxide for premature infants after prolonged rupture of the membranes. J Pediatr 1995; 126(3):450-3.
22. Van K, Rhine W, Asselin JM, Durand D; Preemie NO Collaborative Group. Response of premature infants with severe respiratory failure to inhaled nitric oxide.. Pediatr Pulmonol 1997; 24(5):319-23.
23. Clark R, Ursprung R, Walker MW, Ellsbury D, Spitzer A. The changing pattern of inhaled nitric oxide use in the neonatal intensive care unit. J Perinatol 2010; 30(12):800-4.
24. Schreiber MD, Gin-Mestan K, Marks JD, Huo D, Lee G, Srisuparp P. Inhaled nitric oxide in premature infants with the respiratory distress syndrome. N Engl J Med 2003; 349(22):2099-107.
25. Kinsella JP, Cutter G, Walsh W, Gerstmann D, Bose C, Hart C, et al. Early inhaled nitric oxide therapy in premature newborns with respiratory failure. N Engl J Med 2006; 355(4): 354-64.
26. Mercier JC, Hummler H, Durrmeyer X, Sanchez-Luna M, Carnielli V, Field D, et al. Inhaled nitric oxide for prevention of bronchopulmonary dysplasia in premature babies (EUNO): a randomised controlled trial. Lancet 2010; 376(9738):346-54.
27. Ballard R, Truog W, Cnaan A, Martin R, Ballard P, Merrill JD, et al. Inhaled nitric oxide in preterm infants undergoing mechanical ventilation. N Engl J Med 2006; 355(4):343-53.
28. Committee on Fetus and Newborn, American Academy of Pediatrics. Respiratory support in preterm infants at birth. Pediatrics 2014; 133(1):171-4.
29. Kinsella JP, Cutter G, Steinhorn R, Nelin L, Walsh W, Finer N, et al. Noninvasive inhaled nitric oxide does not prevent bronchopulmonary dysplasia in premature newborns. J Pediatr 2014; 165(6):1104-8.e1.
30. Mestan K, Marks JD, Hecox K, Huo D, Schreiber MD. Neurodevelopmental outcomes of premature infants treated with inhaled nitric oxide. N Engl J Med 2005; 353(1):23-32.
31. Kumar P; Committee on Fetus and Newborn; American Academy of Pediatrics. Use of inhaled nitric oxide in preterm infants. Pediatrics 2014; 133(1):164-70.
32. Ambalavanan N, St John E, Carlo W, Bulger A, Philips J. Feasibility of nitric oxide administration by oxygen hood in neonatal pulmonary hypertension. J Perinatol 2002; 22(1):50-6.
33. Ambalavanan N, El-Ferzli G, Roane C, Johnson R, Carlo W. Nitric oxide administration using an oxygen hood: a pilot trial. PLoS One 2009; 4(2):e4312.
34. Lindwall R, Svensson ME, Frostell C, Eksborg S, Gustafsson L. Workplace NO and NO2 during combined treatment of infants with nasal CPAP and NO. Intensive Care Med 2006; 32(12):2034-41.
35. Lindwall R, Blennow M, Svensson M, Jonsson B, Berggren-Bostrom E, Flanby M, et al. A pilot study of inhaled nitric oxide in preterm infants treated with nasal continuous positive airway pressure for respiratory distress syndrome. Intensive Care Med 2005; 31(7):959-64.
36. Welzing L, Bagci S, Abramian A, Bartmann P, Berg C, Mueller A. CPAP combined with inhaled nitric oxide for treatment of lung hypoplasia and persistent foetal circulation due to prolonged PPROM. Early Hum Dev 2011; 87(1):17-20.
Correspondencia: Dr. Antonio Lustemberg.
Correo electrónico: alustemberg@hotmail.com