Services on Demand
Journal
Article
Related links
Share
Archivos de Pediatría del Uruguay
Print version ISSN 0004-0584On-line version ISSN 1688-1249
Arch. Pediatr. Urug. vol.87 no.2 Montevideo June 2016
Dengue: revisión y experiencia en pediatría
Dengue fever: a review article and experience in Pediatrics
Viviana Pavlicich1
1. Jefe Depto. Emergencia.
Hospital General Pediátrico Niños de Acosta Ñu
Declaro no tener conflicto de intereses.
Actualización del trabajo de revisión “Infección por Dengue en pediatría” realizado en el 2012 para el curso de educación virtual ECRI- SAP (No publicado en revistas indexadas y no indexadas).
Resumen
El fracaso en controlar la expansión del Aedes aegypti en el mundo y de evitar la diseminación de enfermedades transmitidas por mosquitos, entre ellas el dengue, otorga relevancia al abordaje detallado de este tema. El dengue, una patología de inicio agudo y sintomatología sumamente variada pero con un patrón de fases bien definido, ha sido protocolizado para su manejo. La clasificación actual en dengue y dengue grave, la identificación de los signos clínicos que anticipan el agravamiento: signos de alarma, y la identificación de las condiciones o factores de riesgo para el desarrollo de una enfermedad severa, otorgan herramientas esenciales para el manejo clínico de los casos. El desafío consiste en reconocerlo inicialmente entre las patologías comunes de la infancia, a pesar de presentar signos clínicos inespecíficos y tomar la decisión oportuna cuando existe riesgo de severidad. El diagnóstico de la enfermedad puede ser establecido dentro de los cinco primeros días por la detección directa de componentes virales en el suero. El tratamiento es de soporte, con un estrecho monitoreo de la evolución, dado que no existe una terapéutica especifica. La vacuna podría ser el elemento clave para disminuir la carga de la enfermedad.
Palabras clave:
DENGUE
DENGUE GRAVE
REVISIÓN
Summary
Failure to control the expansion of Aedes Aegypti in the world and to avoid the dissemination of diseases transmitted by mosquitoes, being dengue fever among these conditions, results in a relevant detailed approach to this topic. A protocol has been written to handle dengue fever, a pathology that initiates in an acute manner and whose symptoms are extremely varied, although it follows a well-defined pattern of stages. The current classification of dengue fever, dengue fever /SIC/ and severe dengue fever, identification of clinical signs that anticipate worsening of the disease: alarm signs and identification of risk conditions or factors for the development of a severe disease, provide essential tools for the clinical handling of cases. The constant challenge lies in being able to recognize it in initial stages, among other conditions that are frequent during childhood, in spite of its presenting non-specific clinical signs, and making a timely decision when there is a risk of it being severe. The disease may be diagnosed in the first five days by directly identifying viral components in the serum. Treatment consists of support, with a close monitoring of evolution, since there is no specific therapy. Vaccinations may be a key element to reduce the burden of the disease.
Key words:
DENGUE
SEVERE DENGUE
REVIEW
Introducción
El dengue es una infección viral sistémica trasmitida por mosquitos. Su expansión global implica un problema de salud pública para dos tercios de la población mundial. Es una enfermedad emergente, está en aumento el número de casos en las regiones endémicas y su expansión a nuevas regiones, convirtiéndose en una amenaza para muchos países. La diseminación por América del Sur recién se inicia después del año 1981 y se han calculado 5 a 9 millones de casos en el año 2013. El dengue es una de las enfermedades con mayor aumento de las tasas de incidencia estandarizada por edad, lo que contrarresta la tendencia mundial de la disminución de las enfermedades transmisibles(1).
En los últimos 30 años el dengue en las Américas ha tenido una tendencia ascendente, con picos epidémicos que se repiten cada 3 a 5 años casi de manera estable. Cada pico epidémico ha sido regularmente mayor al que le precedió. La causa de este comportamiento podría estar relacionada con la acumulación en esos períodos de tiempo de susceptibles asociado a la combinación de los diferentes serotipos del virus, e incluso a fenómenos propios de las cepas circulantes en su virulencia y patogenicidad. Sin dejar de estar presentes factores medioambientales que hacen que se incremente la presencia del vector transmisor.
Los factores medioambientales y socioeconómicos que básicamente contribuyen a este incremento son un crecimiento poblacional sin precedentes, una urbanización no planificada, las migraciones, el aumento de la pobreza y el desconocimiento del riesgo. Los viajeros tienen una participación esencial en la epidemiología mundial de las infecciones por dengue, ya que aquellos con viremia pueden transportar los serotipos y cepas del dengue hacia áreas con mosquitos que pueden transmitir la infección(2).
En los primeros meses de este año se detectaron en Uruguay 26 casos de dengue autóctonos. Esta situación era previsible debido a la existencia del vector a lo largo de todo el territorio nacional y a la alta prevalencia de la infección en los países vecinos. La mayoría de los casos se han producido en tres departamentos: Montevideo (59%), Canelones (17%) y Salto (4%). Todos los casos confirmados dieron positivo para el virus del dengue mediante RCP-RT (reacción en cadena de la polimerasa con retrotranscriptasa). El serotipo circulante fue el DEN-1(3).
Se estima que en el mundo es endémico en al menos 100 países. La OMS comunicó que 50 a 100 millones de personas se enferman anualmente, 500.000 requieren hospitalización y 22000 mueren, siendo en una gran proporción niños(4).
En los países sin endemia o con una corta historia se reportan casos principalmente en adolescente o adultos. La distribución de la edad en un determinado país y año tendrá una tendencia a cumplir un patrón de cambio de afección hacia los más jóvenes en las sucesivas epidemias.
El virus y el huésped
El virus del dengue (DEN) es un virus pequeño ARN monocatenario, que comprende 4 tipos diferentes de serotipos, (DEN-1 a DEN-4). Estos serotipos están estrechamente relacionados y pertenecen al género Flavivirus de la familia Flaviviridae.
Cada serotipo confiere inmunidad permanente específica contra el mismo, así como también inmunidad de corto plazo cruzada contra los otros tres serotipos que puede durar algunos meses. El virus y el antígeno NS1 están presentes en la sangre durante la fase aguda y altos niveles de viremia y de NS1 antigenemia han sido asociados con presentaciones clínicas más graves. La detección del NS1 es también la base de pruebas diagnósticas(5,6).
Los diferentes serotipos del virus del dengue se transmiten a los humanos mediante picaduras de mosquitos Aedes infectados, principalmente el Aedes aegypti.
El Aedes aegypti es relativamente raro por arriba de los 1.000 metros sobre el nivel del mar debido a las bajas temperaturas. Las etapas inmaduras se encuentran en hábitats cubiertos de agua, principalmente en recipientes artificiales estrechamente asociados con viviendas humanas y, a menudo, bajo techo. Los estudios sugieren que la mayoría de las hembras de Aedes aegypti pasan su período de vida en las casas o alrededor de ellas donde emergen como adultos. Esto significa que las personas, y no los mosquitos, trasladan rápidamente el virus dentro de las comunidades y entre ellas. Los brotes de dengue también se han atribuido a Aedes albopictus, Aedes polynesiensis y varias especies del complejo Aedes scutellaris. Cada una de estas especies tiene ecología, conducta y distribución geográfica determinadas(7).
La transmisión de la enfermedad se produce cuando un mosquito no infectado pica a un hombre enfermo, se contamina con el virus y al picar a un hombre sano le trasmite la enfermedad. El virus del dengue que circula en la sangre de humanos con viremia es ingerido por los mosquitos hembra durante la alimentación, de este modo el virus infecta el intestino medio y se produce una propagación sistémica durante un período de 8 a 12 días. Después de este período de incubación extrínseco, el virus se puede transmitir a otros seres humanos.
También están descriptas la transmisión durante el embarazo y la vía transfusional.
Después de un período de incubación de 4 a 10 días, la infección causada por cualquiera de los cuatro serotipos del virus puede producir una gran variedad de alteraciones, aunque la mayoría de las infecciones son asintomáticas o subclínicas.
Los factores individuales de riesgo determinan la gravedad de la enfermedad e incluyen: infección secundaria(8-10), edad, raza y posibles enfermedades crónicas (asma bronquial, anemia de células falciformes y diabetes mellitus). Los niños pequeños, en particular, pueden tener menor capacidad que los adultos para compensar la extravasación de plasma capilar y, por consiguiente, están en mayor riesgo de shock por dengue. También han sido identificados como factores de riesgo el sexo femenino, el índice alto de masa corporal, la cepa viral y variantes del complejo humano mayor de histocompatibilidad tipo I(11,12).
Cuadro clínico
El dengue es una enfermedad de presentación clínica variable pero de manejo sencillo en la gran mayoría de las veces que ocasiona un enorme desafío a los sistemas de salud cuando se presenta en epidemias.
Es una enfermedad sistémica, dinámica y presenta un amplio espectro clínico que incluye manifestaciones clínicas graves y no graves(13). Puede, en ocasiones, presentarse como un cuadro febril indiferenciado(14).
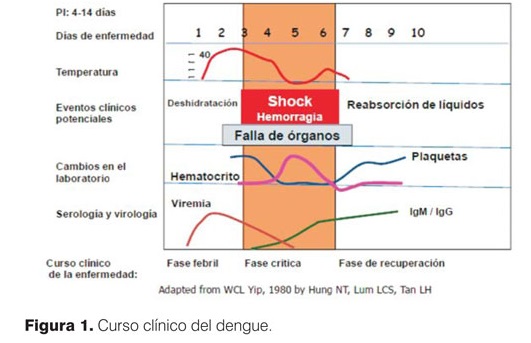
La evolución clínica es impredecible. Luego de un período de 3 a 7 días de incubación los síntomas comienzan súbitamente, pudiéndose diferenciar tres fases: febril, crítica y de recuperación.
Fase febril
Suele durar de 2 a 7 días. Se caracteriza por fiebre, acompañada por cefalea, vómitos, mialgias, dolor articular, a veces acompañada también por un rash macular. Los niños tienen fiebre alta, pero generalmente son menos sintomáticos que los adultos durante esta fase de la enfermedad. Pueden tener manifestaciones hemorrágicas leves como petequias y equimosis en los sitios de punción. Los hallazgos de laboratorio incluyen: leucopenia, leve trombocitopenia y aumento moderado de las transaminasas.
La fiebre es un marcador del inicio de la enfermedad. Su aparición es brusca, puede llegar a 40ºC, y remitir en meseta después del tercer día. En los primeros días hay escasa respuesta a antipiréticos. Los pacientes que ya han padecido la enfermedad tienden a tener un período febril más corto. La fiebre puede presentarse en forma bifásica. La cefalea es holocraneana e intensa, el dolor retro-ocular característico de esta enfermedad, puede empeorar con el movimiento de los ojos y se asocia a fotofobia.
Las artralgias son de pequeñas y grandes articulaciones, también suelen doler los huesos largos. Predominan las mialgias en la región lumbar y en los miembros inferiores.
El primer rash puede aparecer entre el tercer y cuarto día, siendo de característica maculopapular o escarlatitiforme generalizado, pudiendo a afectar la región palmoplantar.
Muchos pacientes se recuperan luego de esta fase sin complicaciones.
Fase crítica
Puede ocurrir en cualquier momento entre los 3 y 7 días de la enfermedad. En algunos pacientes se produce fuga capilar durante la defervescencia, evidenciado por hemoconcentración (aumento del hematocrito), hipoalbuminemia y por la presencia de derrame pleural, ascitis y edemas generalizados. Esta fuga capilar puede ocasionar el síndrome de shock por dengue (SSD).
Antes que se establezca el shock aparecen signos clínicos que fueron reconocidos como signos de alarma, estos signos preceden al deterioro clínico. Identificarlos permite iniciar precozmente los líquidos endovenosos y prevenir el shock. Es importante informar a los pacientes, a su familia y al equipo de salud para que los reconozca. Signos de alarma:
- Dolor abdominal continuo e intenso
- Vómitos persistentes.
- Derrames serosos en peritoneo, pleura y/o pericardio, detectados clínicamente y/o por imágenes.
- Sangrados de mucosas.
- Somnolencia o irritabilidad.
- Hepatomegalia mayor de 2 cm.
- Incremento brusco del hematocrito asociado a un rápido descenso en el recuento de plaquetas.
Las manifestaciones hemorrágicas generalmente ocurren durante la fase crítica, son menos frecuentes en los niños, usualmente asociadas con shock profundo y prolongado. Sin embargo en adultos puede presentarse severas hemorragias con signos menores de fuga capilar(15). Un aumento del tiempo de tromboplastina parcial activada y una disminución de los niveles de fibrinógeno están frecuentemente presentes(16,17).
Manifestaciones graves incluyen falla hepática, miocarditis y encefalopatía, estos cuadros se caracterizan por acompañarse con mínima fuga plasmática.
Aunque las publicaciones citan que el shock es el desencadenante de la muerte por dengue en niños, y que las otras complicaciones son en realidad consecuencia del shock prolongado y recurrente, en Paraguay existe la experiencia aun no publicada de encefalitis por dengue sin shock como causa de muerte en niños(21).
Fase de recuperación
Dura 2 o 3 días, terminada la fase crítica. Existe una rápida recuperación de la plaquetopenia durante esta fase. La alteración de la permeabilidad es corta, dura aproximadamente 48 a 72 horas y es simultáneo a la rápida mejoría clínica del paciente. Un segundo rash de características maculopapular y pruriginosas suele aparecer en esta fase (figura 1).
Fisiopatología del dengue grave
En el dengue existe una disfunción endotelial, pero no hay evidencias que el virus infecte directamente las células endoteliales y solo se han detectado cambios menores en la microvasculatura(22). Sin embargo han sido identificados eventos inmunopatogénicos con efecto definitivo sobre la permeabilidad microvascular (figura 2).
Datos preliminares sugieren que se produce una alteración transitoria en la función del glicocálix endotelial(23,24). Se sabe que tanto el propio virus, como el NS1 (proteína no estructural 1), se adhieren al heparán sulfato del glicocálix(25,26). Esta capa funciona como un tamiz molecular, restringiendo selectivamente las moléculas dentro del plasma de acuerdo a su forma, tamaño y carga. Debido a esto, son encontradas hipoalbuminemia y proteinuria en la infección por dengue, las proteínas más pequeñas y hasta del tamaño de la albumina son filtradas a través del glicocálix.
Un desequilibrio transitorio y reversible de mediadores inflamatorios como citoquinas y quimiocinas, se produce durante el dengue grave, probablemente debido a una alta carga viral, esto conduce a la disfunción de las células endoteliales vasculares y a un trastorno del sistema de coagulación resultante en pérdida de plasma, shock y hemorragias(27).
Los mecanismos que conducen a una enfermedad severa no están bien definidos, pero la respuesta inmune, las características genéticas del huésped y las variaciones del virus son los elementos que podrían estar implicados en el desarrollo de enfermedad grave
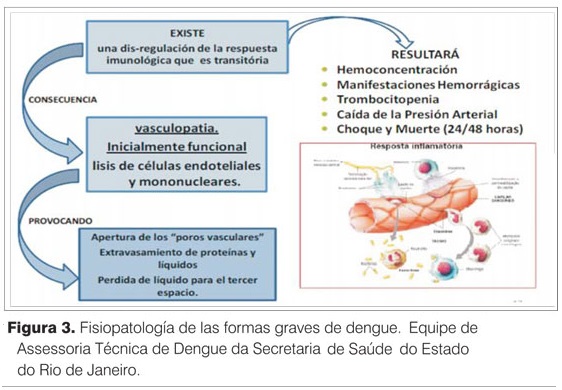
La pérdida de proteínas esenciales de la coagulación probablemente juega un papel importante en el desarrollo de la típica coagulopatía, que generalmente se manifiesta como un aumento en el tiempo parcial de tromboplastina acompañado de una disminución de los niveles de fibrinógeno, pero con poca evidencia de activación procoagulante. El heparán sulfato puede funcionar también como anticoagulante y contribuir a la coagulopatía (figura 3) (28,29).
Se ha postulado La hipótesis de la persistencia de anticuerpos maternos IgG subneutralizantes para el virus del dengue provenientes de madres previamente sensibilizadas en la patogénesis de enfermedad severa en niños pequeños por el efecto ADE (antibody-dependent enhancement)(30,31).
Clasificación: dengue y dengue grave
El Programa de Adiestramiento e Investigación en Enfermedades Transmisibles de la Organización Mundial de la Salud (TDR/OMS) auspició un estudio internacional, llamado DENCO (Dengue Control), uno de cuyos componentes era de clínica y su objetivo principal fue obtener información de un número elevado de enfermos con dengue confirmado, y encontrar una forma adecuada de clasificarlos, así como identificar signos de alarma que fueran útiles para mejorar el protocolo de manejo de casos de dengue.
Se obtuvo información clínica de casi 2.000 enfermos con dengue confirmado, procedentes de siete países de dos continentes.
El estudio DENCO también permitió identificar algunos signos y síntomas que estaban presentes en los enfermos un día antes de agravarse. Estos signos de alarma permiten identificar tempranamente el enfermo de dengue que va a evolucionar a Dengue severo y, sobre todo permite al médico iniciar de manera precoz el tratamiento con reposición de líquidos por vía intravenosa, mejorando así el pronóstico del enfermo.
El dolor abdominal a la palpación, o referido por el enfermo fue identificado como un factor de riesgo significativo para adultos y niños.
El estudio DENCO fue capaz de distinguir entre dengue grave y no grave con una sensibilidad y especificidad mayor del 95%. Identificó signos que estaban presentes antes de agravarse y la importancia de la comorbilidad(22).
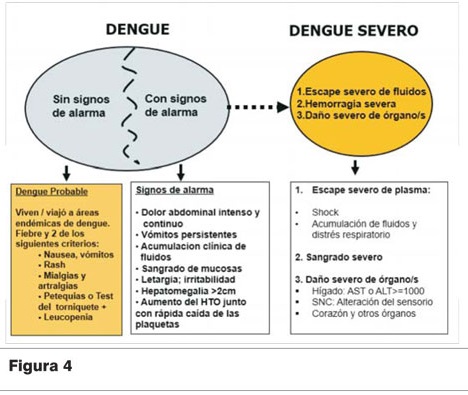
Un estudio multicéntrico llevado a cabo en 18 países, evaluó la utilidad de la clasificación revisada de dengue y concluyó que tiene un alto potencial para facilitar el manejo de los casos y mejorar la sobrevida(32).
Definición de caso sospechoso
La definición consta de un aspecto clínico y un aspecto epidemiológico: “Enfermedad febril aguda con un máximo de siete días de evolución que presenta dos o más de los siguientes síntomas: dolor de cabeza, dolor retroorbitario, mialgias, artralgias, postración o erupción cutánea. Con o sin la presencia de sangrado, leucopenia, y cualquier signo de alarma en un paciente que estuvo en los últimos 15 días en una región con presencia de Aedes aegypti y transmisión del virus del dengue.”
Manejo de casos
El diagnóstico clínico del dengue en niños es difícil porque los signos y síntomas tempranos de la enfermedad son inespecíficos e indiferenciado de otras enfermedades febriles agudas. Por otro lado, la presentación clínica cambia durante el curso de la enfermedad y varía según la gravedad de la misma. El conocimiento de las manifestaciones y del laboratorio en cada fase de la enfermedad es importante para resolverla.
Para una enfermedad que tiene manifestaciones complejas, el manejo es relativamente simple, barato y muy efectivo para salvar vidas, siempre y cuando las intervenciones sean correctas y oportunas. La clave es el reconocimiento temprano y la comprensión de los problemas clínicos durante las diferentes fases de la enfermedad. En otras palabras, evaluar la secuencia de las manifestaciones clínicas y de laboratorio para detectar en qué momento el paciente con dengue puede evolucionar a formas graves.
El futuro de los casos graves de dengue se deciden por lo general no en la Unidad de Cuidados Intensivos sino mucho antes, en la Unidad de Atención Primaria, el Departamento de Urgencias Médicas o la sala del hospital(33).
Para cumplir con el objetivo principal que es evitar la muerte por dengue es necesario: reconocer precozmente la dolencia, conocer su clasificación, comprender las alteraciones clínicas en las diferentes fases y adoptar una la conducta ajustada a la clasificación y a cada paciente en el tiempo apropiado.
Se considera población de riesgo:
- Menores de 2 años de edad*
- Mayores de 65 años de edad
- Embarazadas
- Adultos y niños con hipertensión, obesidad, diabetes o enfermedades crónicas.
- Incapaz de autocuidado que viva solo o no tenga cuidador.
- Falta de acceso a servicios de salud.
* Hemos estudiado esta población encontrando que el verdadero grupo de riesgo pareciera encontrarse en los menores de 1 año, especialmente los menores de 6 meses.
En las Américas la incidencia de dengue grave tiene un comportamiento bimodal, afectando a niños menores de 1 año de edad, escolares entre 5 a 9 años y adultos jóvenes. El grupo etario entre 1-4 años al parecer sería el menos susceptible de evolucionar a formas severas de la enfermedad.
1. ¿Tiene dengue? (Cumple criterios de definición de caso sospechosos).
2. ¿En qué fase se encuentra? (febril, critica o recuperación).
3. ¿Tiene signos de alarma?
4. ¿Tiene shock?
5. ¿Tiene comorbilidad?
6. ¿Pertenece a algún grupo especial?
7. ¿Tiene riesgo social?
Respondiendo estas cuestiones, el paciente puede clasificarse en las categorías de riesgo que se presentan en la tabla 1.
Es aquel paciente que cumple con la definición de sospecha de caso sin ningún otro factor que implique riesgo (edad, situación social, signos de shock, signos de alarma ni enfermedades crónicas).
Deben ser evaluados diariamente luego de tres días de iniciada la enfermedad para determinar progresión de la enfermedad y la aparición de signos de alarma hasta que estén fuera del periodo crítico. Se les debe animar a tomar por vía oral solución de rehidratación y jugos de fruta para reponer las pérdidas de la fiebre y vómitos, y reducir el riesgo de hospitalización.
El paracetamol es el antipirético de elección con un mínimo intervalo de dosificación de 6 horas. No se deben indicar esteroides ni antiinflamatorios no esteroideos ya que pueden agravar la gastritis y/o sangrado.
Los cuidadores deben ser informados de que el paciente debe ser trasladado al hospital de inmediato si se presenta alguna de las siguientes situaciones:
- No hay mejoría clínica.
- Deterioro en el momento de desaparición de la fiebre.
- Dolor abdominal intenso.
- Vómitos persistentes.
- Extremidades frías y húmedas.
- Letargo o irritabilidad / agitación.
- Sangrados (por ejemplo, heces negras o vómitos).
- No orina por más de 4-6 horas.
Grupo B
Deben ser ingresados en el hospital. Este grupo incluye aquellos pacientes con condiciones comórbidas o sociales, situaciones en que la atención domiciliaria no es adecuada por lo que los líquidos por vía oral pueden no ser suficientes y deben ser vigilados estrechamente (B1) y a aquellos pacientes con signos de alarma (B2). Esta subdivisión del grupo B se debe a que todos estos pacientes deben ser hospitalizados pero cada subgrupo merece una conducta terapéutica diferente (OPS 2011).
El paciente B1 básicamente se hospitaliza para realizar una monitorización cercana e intervención oportuna.
- Iniciar la administración de cristaloides a 10 ml/Kg en una hora.
- Reevaluar y si persisten los signos de alarma y la diuresis es < 1 ml/kg/h repetir carga 1 o 2 veces más.
- Reevaluar si hay mejoría clínica y la diuresis es ³ 1 ml/kg/h reducir el goteo a 5-7 ml/kg/h, por 2 a 4 h.
- Continuar la reducción a 3-5 ml/kg/h por 2-4 h.
- Continuar según necesidades del paciente.
Grupo C
Corresponde a los pacientes con fuga plasmática severa, hemorragias, o falla de órganos y deben ser manejados en hospitales con posibilidades de cuidados intensivos.
Los niños del grupo C requieren una urgente resucitación con cristaloides o coloides intravenosos con la finalidad de mantener una perfusión y diuresis adecuada y mejoría de la taquicardia.
En los pacientes con shock compensado (normotensos) los líquidos son iniciados a 10 ml/kg/h y luego ajustados basándose en la respuesta clínica y en mediciones seriadas del hematocrito. La mejoría está establecida cuando se recupera la perfusión, el flujo urinario y desciende el hematocrito.
En los pacientes con shock hipotensivo, se utilizan bolos de 20 ml/kg en 10 a 15 minutos. Luego los líquidos son ajustados según respuesta.
La falta de mejoría se evidencia por la persistencia del shock, disminución de la presión del pulso, empeoramiento de la acidosis metabólica y aumento del hematocrito.
Una caída del hematocrito durante un shock persistente puede indicar hemorragia y debe ser tratado con transfusión de plasma y glóbulos rojos.
Los pacientes de los grupos B y C requieren durante la hospitalización:
- Monitorización del estado hemodinámico, de la ingesta y balance de ingresos y egresos.
- Utilizar fluidos isotónicos (suero salino o Ringer lactato) si se requiere restaurar el volumen plasmático.
- Controlar la presencia de sangrados.
Realizamos un análisis para predecir en la emergencia, que niños del grupo B (Dengue con signos de alarma) progresarán al Grupo C (Dengue Grave), arrojó que la hemoconcentración con descenso de plaquetas aumentó 3,3 veces la posibilidad de tener Dengue Grave cuando está presente, pero su ausencia no implicó que no lo desarrollarían. Ninguna de las variables permitió predecir con suficiente solvencia la evolución a dengue grave en el momento del ingreso hospitalario(32).
En nuestros pacientes se produjo con más frecuencia shock precoz en niños escolares. Sin embargo el shock fue más frecuentemente refractario en lactantes(34).
Líquidos intravenosos
En el dengue existen algunas recomendaciones específicas respecto al manejo de las infusiones EV. Es importante infundir tipos de fluidos intravenosos (FIV) que tengan más probabilidades de permanecer en la vasculatura y no administrar líquidos más allá de lo necesario para evitar el acumulo extravascular. Por lo tanto se recomienda:
- Limitar los FIV en la fase febril a los pacientes que están deshidratados y no ingieren suficiente líquido por la boca.
- No usar soluciones cristaloides hipotónicas para la hidratación de mantenimiento ni aun entre los bolos.
- Dar la cantidad justa de FIV para mantener una buena perfusión y la producción de orina de al menos 0,5 ml/kg/h durante la fase crítica. Si el paciente tiene exceso de peso, el volumen se basa en el peso corporal ideal (PCI).
- Controlar el volumen de FIV con los HTO y los signos vitales. Vigilar la ingesta de líquidos y los egresos.
- Reducir los FIV en la medida que disminuye la tasa de fugas de plasma, esto ocurre cerca del final de la fase crítica y se evidencia mediante el aumento de la producción de orina, la ingesta adecuada de líquidos por vía oral y la disminución del valor HTO por debajo del nivel basal en un paciente estable.
Por otro lado en el shock refractario pueden utilizarse coloides luego del curso de cristaloides isotónicos. Los coloides permanecen en el intravascular a diferencia de los cristaloides, y han sido asociados con un ligero aumento de reacciones adversas.
En el lactante que no se alimenta se debe añadir una solución con dextrosa.
Los niños del grupo C requieren una urgente resucitación con cristaloides o coloides intravenosos con la finalidad de mantener una perfusión y diuresis adecuada y mejoría de la taquicardia.
En los pacientes con shock compensado (normotensos) los líquidos son iniciados a 10 ml/kg/h y luego ajustados basándose en la respuesta clínica y en mediciones seriadas del hematocrito. La mejoría está establecida cuando se recupera la perfusión, el flujo urinario y desciende el hematocrito.
Si el niño se encuentra en shock hipotensivo o descompensado se realiza la reanimación hídrica vigorosa con bolos de 20 ml/kg de cristaloide, seguido de coloide (nosotros utilizamos albumina al 0,5%), e inicio de inotrópicos y/o vasopresores según corresponda. La falta de mejoría se evidencia por la persistencia del shock, disminución de la presión del pulso, empeoramiento de la acidosis metabólica y aumento del hematocrito(35-37).
En niños hospitalizados por dengue con signos de alarma, el descenso de plaquetas al 5to día de enfermedad y el requerimiento de expansiones por dolor abdominal y/o signos tempranos de shock permiten identificar a pacientes que evolucionaran a grave en las próximas horas(38).
Una caída del hematocrito durante un shock persistente puede indicar hemorragia y debe ser tratado con transfusión de plasma y glóbulos rojos.
De esta forma el control seriado del HTO es orientador de los cambios fisiopatológicos y de las conductas terapéuticas en el paciente crítico.
Monitorización de los signos de sangrados
Hemos visto con cierta frecuencia sangrados vaginales en adolescentes, y hemorragias digestivas en algunos pacientes. Se debe tener especial cuidado en aquellos pacientes con ulcera péptica preexistente, anticoagulados, que utilizan AINEs o que han sufrido alguna forma de trauma.
Los factores de riesgo para las hemorragias importantes son el shock prolongado con hipotensión, acidosis metabólica y falla hepática y/o renal.
Las hemorragias de mucosas pueden presentarse en cualquier caso de dengue con independencia de su gravedad, pero generalmente mejoran rápidamente en la fase de recuperación.
Comparación del síndrome de shock dengue (SSD) con el shock séptico (SS)
Los pacientes con SSD fueron menos propensos a tener un síndrome de respuesta inflamatoria sistémica, sin embargo presentaron más frecuentemente estrechamiento de la presión del pulso, sangrados y un estado del sensorio preservado en relación a los pacientes con shock séptico. Estos resultados probablemente se deban al estado predominantemente vasodilatador en el shock séptico en comparación con el estado vasoconstrictor de la respuesta inicial en el DSS(39).
El SSD presenta algunas peculiaridades fisiopatológicas, especialmente relacionadas con el aumento significativo y precoz de la permeabilidad vascular y los relacionados con la coagulabilidad sanguínea.
Son características particulares del SSD(40):
- El sensorio frecuentemente inalterado, (no concordante con la alteración hemodinámica observada). En general no dura más de 24 a 48 horas y se producen recurrencias durante este periodo.
- La ausencia de fiebre (establecer un monitoreo cercano cuando el paciente se torna afebril).
- El aumento del hematocrito.
- La disminución de la albúmina.
- Puede acompañarse de bradicardia sinusal.
- Es precedido por una rápida caída de plaquetas
El shock séptico usualmente tiene una evolución más prolongada, mayor requerimiento de ventilación mecánica y de drogas vasoactivas.
Transfusión de plaquetas
Los pacientes con dengue y trombocitopenia profunda no son infrecuentes. Estos pacientes necesitan un estricto reposo en cama y deben ser protegidos de daño para reducir el riesgo de sangrado. No dar inyecciones intramusculares para evitar hematomas. No es necesario la transfusión de plaquetas profilácticas para la trombocitopenia grave en pacientes hemodinámicamente estables que no tienen hemorragia clínicamente significativa(41).
La práctica de la transfusión de plaquetas profiláctica NO se recomienda por las siguientes razones:
- Los estudios sugieren que el riesgo de sangrado no se correlaciona con el recuento de plaquetas. Más bien, shock prolongado puede aumentar el riesgo de hemorragia de un paciente.
- Las transfusiones de plaquetas no acortan el período de la trombocitopenia en pacientes con dengue, probablemente debido a la destrucción de las plaquetas.
- La transfusión de plaquetas puede provocar sobrecarga de fluidos y extensión de la hospitalización.
La transfusión está indicada en pacientes con trombocitopenia y sangrados activos que ponen en riesgo la vida. Petequias y equimosis, presentes con frecuencia en el dengue, no son considerados sangrados activos que requieran transfusión plaquetaria.
El diagnóstico de dengue puede ser establecido directamente por la detección de componentes virales en el suero o indirectamente por análisis serológicos.
La sensibilidad de cada una de estas pruebas está determinada por los días de evolución de la enfermedad que lleva el paciente(42).
Al ordenar pruebas diagnósticas de un caso sospechoso de dengue, el médico debe tener en cuenta cuando el virus está presente en la sangre y cuando se producen los anticuerpos.
En la fase aguda, cuando el paciente está febril, aproximadamente en los primeros 5 días después de la aparición de los síntomas se puede detectar el ácido nucleico viral en suero por medio de la reverse-transcriptase–polymerase-chain reaction (RT-PCR), o por la detección de la proteína 1 no estructural (NS1) por medio de ELISA (enzyme-linked immunosorbent assay) o del test rápido.
En las personas que no han sido infectadas previamente la sensibilidad diagnóstica de la detección de NS1 en el periodo febril es mayor del 90%, disminuyendo a un 60 a 80% en la infección secundaria(43,44).
Existe diferencia en la sensibilidad y especificidad de diferentes marcas comerciales para la detección de NS1(45-48).
El Centro para el Control y Prevención de Enfermedades (CDC) ha desarrollado el test CDC DENV-1-4 Real Time RT PCR Assay, puede ser realizado con el mismo equipo que muchos laboratorios de Salud Publica utilizan para diagnosticar influenza y puede identificar los 4 tipos de virus(47,48).
En la fase de convalecencia se debe solicitar el anticuerpo Inmunoglobulina M anti dengue (IgM anti-DENV ELISA). Se encuentra detectable una vez que desaparece la fiebre, generalmente entre los días 4 y 7 de evolución y se mantiene por aproximadamente 3 meses. Se considera diagnostico cuando se produce seroconversión entre dos muestras pareadas obtenidas en las fases aguda y de convalecencia respectivamente.
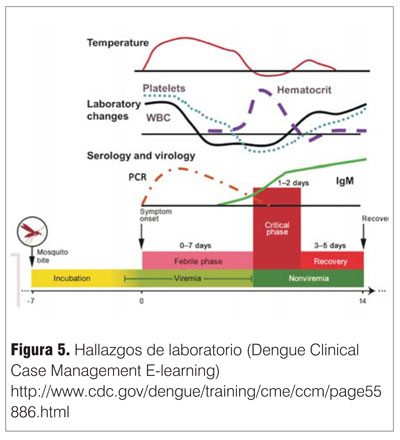
La detección de IgG en suero no es útil como test diagnóstico de dengue, se vuelve positiva generalmente recién luego del noveno día de enfermedad en la infección primaria, estando detectable desde el primer día en una infección secundaria. Puede dar reacción cruzada con otros flavivirus y en pacientes vacunados por fiebre amarilla (figura 5).
Valor de los exámenes complementarios en dengue
Hematocrito: guía la terapéutica hídrica, un aumento del 20% por encima del basal se considera hemoconcentración y cuando se asocia a disminución brusca de plaquetas es un signo de alarma que predice el desarrollo de dengue grave. En la mayoría de las guías se le ha dado un asignado valor a la determinación seriada para estimar la fuga capilar, actualmente esta evaluación está siendo reemplazada por otros métodos(49).
Recuento de plaquetas: suelen disminuir sin necesariamente implicar un aumento del riesgo de sangrado.
Leucopenia: muy frecuente, aunque su ausencia no excluye la enfermedad.
En nuestra experiencia, los lactantes presentan leucopenia más tardía que otras edades, esto puede dificultar el diagnostico al inicio de la enfermedad y denota la necesidad de pruebas de antigenemia para el diagnóstico(50).
Hipoalbuminemia: denota la existencia de fuga capilar, está presente durante la fase crítica en el dengue grave.
Hiponatremia: está presente con relativa frecuencia en pacientes con dengue.
Transaminasas: habitualmente aumentan 2 a 4 veces del valor normal. El aumento superior a 1.000 UI es propio de hepatitis por dengue y es un cuadro grave.
Enzimas cardiacas y troponina I cuantitativa ultrasensible: útiles para evaluar una posible miocarditis dentro de un contexto clínico sugerente.
Ecocardiografía: monitoreo de la función ventricular en el paciente grave, detección de derrame.
Acidosis metabólica: presente en el shock, debe corregirse con volumen oportunamente.
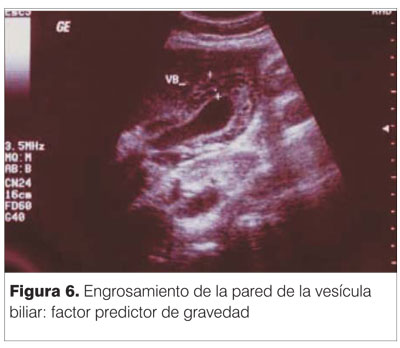
Radiografía de tórax y ecografía: útiles para detectar y cuantificar los derrames serosos durante la fase crítica cuando existe fuga capilar. La colecistitis alitiásica debe buscarse en todos los enfermos con dolor abdominal, se puede ver en estos casos una vesícula distendida con paredes engrosadas sin cálculos en su interior (figura 6). Este hallazgo ha sido descripto en numerosos estudios como predictor de dengue grave.
Diagnóstico diferencial
El diagnóstico clínico fuera de epidemias puede ser difícil porque los signos y síntomas iniciales son inespecíficos y porque la presentación clínica puede diferir según la fase de la enfermedad en la que se encuentre (véase ejemplos en la tabla 2).

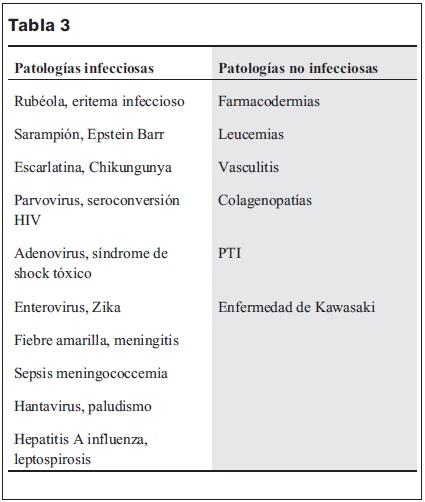
Dependiendo de la presentación clínica y de la historia de exposición se pueden valorar distintos diagnósticos diferenciales (tabla 3).
Complicaciones y causas de muerte.
Las causas de muerte incluyen las siguientes:
- No reconocer la enfermedad.
- No reconocer el shock o que el mismo sea prolongado.
- No diagnosticar hemorragias ocultas.
- Hipervolemia y edema pulmonar por exceso de fluidos EV.
- Infecciones nosocomiales.
- Falla hepática.
Los estudios han demostrado que el mayor factor de riesgo para el desarrollo de dengue grave es una infección secundaria con un serotipo de dengue diferente del virus infectante original.
Los niños con dengue severo pueden tener disfunción miocárdica, evidenciándose clínicamente con hepatomegalia y taquicardia que no responde a la infusión de líquidos. Estos pacientes pueden responder al uso cuidadoso de agentes inotrópicos y vasodilatadores, después de una adecuada reanimación con líquidos. La disfunción miocárdica en el dengue es transitoria y la función cardíaca regresa a la normalidad(51).
Los pacientes que desarrollan distrés respiratorio debido al shock o a la fuga capilar pueden beneficiarse con presión positiva nasal continua en la vía aérea. Si esta modalidad fracasa, deben ser ventilados tempranamente(52).
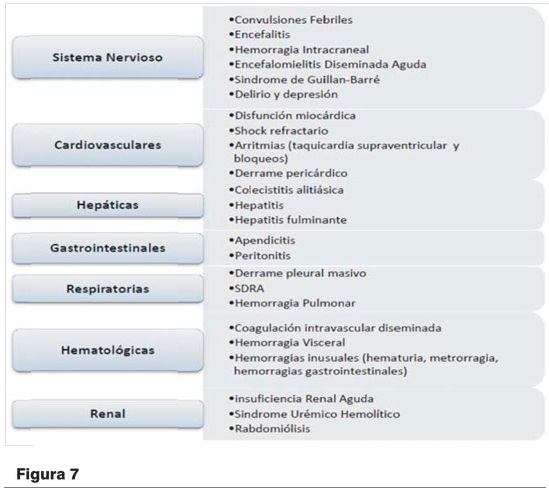
Las complicaciones observadas en la infección por dengue se observan en la figura 7, siendo infrecuentes algunas de ellas(53).
Prevención
Las estrategias de prevención en lo que respecta al combate del vector y las medidas a adoptar por viajeros en zonas endémicas no serán desarrolladas en esta revisión.
Respecto a la vacuna, CYD-TDV es la primera vacuna contra el dengue que ha completado la Fase 3 en ensayos de eficacia. Los ensayos multicéntricos en Asia y América Latina han mostrado una eficacia desigual en diversos factores: la seropositividad basal, el serotipo, y la edad
- La eficacia fue consistentemente mayor en los mayores de los 9 años de edad en todas las variables estudiadas: eficacia contra el dengue confirmados virológicamente de cualquier gravedad y serotipo.
- La comprensión de las razones de la relación riesgo / beneficio transitoria en el tercer año después de la vacunación en niños muy pequeños es crítica para el desarrollo de futuras vacunas contra el dengue(54,55).
Conclusiones
El diagnóstico de dengue en niños, especialmente en lactantes, es un verdadero desafío debido a la presentación clínica inespecífica. Los datos epidemiológicos son de gran utilidad para establecer la sospecha. Aunque la enfermedad es leve en la mayoría de los casos, algunos evolucionan a formas graves y solamente el monitoreo cuidadoso posibilita una intervención oportuna. Reconocer los signos de alarma es importante para identificar posibles evoluciones a dengue grave. Aunque diferentes aspectos de la fisiopatología siguen siendo investigados, es claro que la fuga capilar en pacientes con y sin shock es un evento frecuente en el dengue.
Las epidemias suponen una enorme presión asistencial en los servicios de salud y requieren de la planificación e implementación de estrategias específicas. La extensión de la enfermedad en América Latina hace necesario que los médicos de la región estén familiarizados con las manifestaciones clínicas, los métodos diagnósticos y las recomendaciones para el manejo. Una vacuna contra el dengue segura y eficaz será la piedra angular de cualquier programa de control de éxito. Hasta que esté universalmente disponible, deben continuar los esfuerzos para mejorar el tratamiento a través de la aplicación de las mejores prácticas existentes, un triaje eficiente y el manejo apropiado de los líquidos.
1. Stanaway J, Shepard D, Undurraga E, Halasa Y, Coffeng L, Brady O, et al. The global burden of dengue: an analysis from the Global Burden of Disease Study 2013. Lancet Infect Dis 2016; pii: S1473-3099(16)00026-8. [Epub ahead of print].
2. Wilder-Smith A, Wilson ME. Sentinel surveillance for dengue: international travelers. [Unpublished report].
3. Uruguay. Ministerio de Salud Pública. Dengue. Montevideo: MSP, 2016. Disponible en: http://www.msp.gub.uy/publicaci%C3%B3n/dengue. [Consulta: 15 de mayo de 2016].
4. World Health Organization. Dengue and severe dengue: Fact sheet N°117 Updated 2016. Geneva: WHO, 2016. Disponible en: http://www.who.int/entity/mediacentre/factsheets/fs117/en. [Consulta: enero de 2012].
5. Libraty D, Young P, Pickering D, Endy T, Kalayanarooj S, Green S, et al. High circulating levels of the dengue virus nonstructural protein NS1 early in dengue illness correlate with the development of dengue hemorrhagic fever. J Infect Dis 2002; 186(8):1165-8.
6. Vaughn D, Green S, Kalayanarooj S, Innis B, Nimmannitya S, Suntayakorn S, et al. Dengue viremia titer, antibody response pattern, and virus serotype correlate with disease severity. J Infect Dis 2000; 181(1):2-9.
7. Reiter P. Aedes albopictus and the world trade in used tires, 1988-1995: the shape of things to come? J Am Mosq Control Assoc 1998; 14(1):83-94.
8. Sangkawibha N, Rojanasuphot S, Ahandrik S, Viriyapongse S, Jatanasen S, Salitul V, et al. Risk factors in dengue shock syndrome: a prospective epidemiologic study in Rayong, Thailand. I. The 1980 outbreak. Am J Epidemiol 1984; 120(5):653-69.
9. Burke D, Nisalak A, Johnson D, Scott R. A prospective study of dengue infections in Bangkok. Am J Trop Med Hyg 1988; 38(1):172-80.
10. Kouri G, Guzmán MG, Bravo JR, Triana C. Dengue haemorrhagic fever/dengue shock syndrome: lessons from the Cuban epidemic, 1981. Bull World Health Organ 1989; 67(4):375-80.
11. Anders K, Nguyet N, Chau N, Hung N, Thuy T, Lien B, et al. Epidemiological factors associated with dengue shock syndrome and mortality in hospitalized dengue patients in Ho Chi Minh City, Vietnam. Am J Trop Med Hyg 2011; 84(1):127-34.
12. Rico-Hesse R, Harrison L, Salas R, Tovar D, Nisalak A, Ramos C, Boshell J, et al. Origins of dengue type 2 viruses associated with increased pathogenicity in the Americas. Virology 1997; 230(2):244-51.
13. Jessie K, Fong MY, Devi S, Lam S, Wong K. Localization of dengue virus in naturally infected human tissues, by immunohistochemistry and in situ hybridization. J Infect Dis 2004; 189(8):1411-8.
14. Rigau-Pérez J, Clark G, Gubler D, Reiter P, Sanders E, Vorndam A. Dengue and dengue haemorrhagic fever. Lancet 1998; 352(9132):971-7.
15. Phuong H, de Vries P, Nga T, Giao P, Hung Q, Binh T, et al. Dengue as a cause of acute undifferentiated fever in Vietnam. BMC Infect Dis 2006; 6:123.
16. Wichmann O, Hongsiriwon S, Bowonwatanuwong C, Chotivanich K, Sukthana Y, Pukrittayakamee S. Risk factors and clinical features associated with severe dengue infection in adults and children during the 2001 epidemic in Chonburi, Thailand. Trop Med Int Health 2004; 9(9):1022-9.
17. Wills B, Oragui E, Stephens A, Daramola O, Dung N, Loan H, et al. Coagulation abnormalities in dengue hemorrhagic Fever: serial investigations in 167 Vietnamese children with Dengue shock syndrome. Clin Infect Dis 2002; 35(3):277-85.
18. Wills B, Tran V, Nguyen T, Truong T, Tran T, Nguyen MD, et al. Hemostatic changes in Vietnamese children with mild dengue correlate with the severity of vascular leakage rather than bleeding. Am J Trop Med Hyg 2009; 81(4):638-44.
19. Giraldo D, Sant’Anna C, Périssé A, March F, Souza A, Mendes A, et al. Characteristics of children hospitalized with dengue fever in an outbreak in Rio de Janeiro, Brazil. Trans R Soc Trop Med Hyg 2011; 105(10):601-3.
20. Marón G, Escobar G, Hidalgo E, Clara A, Minniear T, Martinez E, et al. Characterization of dengue shock syndrome in pediatric patients in El Salvador. Pediatr Infect Dis J 2011; 30(5):449-50.
21. Martínez T, Polanco A, Pleites E. ¿Por qué y cómo mueren los niños con dengue? Rev Cuba Med Trop 2008; 60(1):40-7.
22. Alexander N, Balmaseda A, Coelho I, Dimaano E, Hien T, Hung N, et al; European Union, World Health Organization (WHO-TDR) supported DENCO Study Group. Multicentre prospective study on dengue classification in four South-east Asian and three Latin American countries. Trop Med Int Health 2011; 16(8):936-48.
23. Leong A, Wong K, Leong T, Tan P, Wannakrairot P. The pathology of dengue hemorrhagic fever. Semin Diagn Pathol 2007; 24(4):227-36.
24. Michel C, Curry F. Microvascular permeability. Physiol Rev 1999; 79(3):703-61.
25. Levick JR, Michel C. Microvascular fluid exchange and the revised Starling principle. Cardiovasc Res 2010; 87(2):198-210.
26. Wills B, Oragui E, Dung N, Loan H, Chau N, Farrar JJ, et al. Size and charge characteristics of the protein leak in dengue shock syndrome. J Infect Dis 2004; 190(4):810-8.
27. Avirutnan P, Zhang L, Punyadee N, Manuyakorn A, Puttikhunt C, Kasinrerk W, et al. Secreted NS1 of dengue virus attaches to the surface of cells via interactions with heparan sulfate and chondroitin sulfate E. PLoS Pathog 2007; 3(11):e183.
28. Simmons C, Farrar JJ, Nguyen V, Wills B. Dengue. N Engl J Med 2012; 366(15):1423-32.
29. World Health Organization. Dengue, guidelines for diagnosis, treatment, prevention and control. 9 ed. Geneva: WHO, 2009.
30. Chau T, Hieu N, Anders K, Wolbers M, Lien B, Hieu L, et al. Dengue virus infections and maternal antibody decay in a prospective birth cohort study of Vietnamese infants. J Infect Dis 2009; 200(12):1893-900.
32. Lugo S, Morilla L, Bejarano O, Basualdo W, Pavlicich V. En dengue con signos de alarma: ¿podemos predecir evolución a grave desde la emergencia? Pediatr (Asunción) 2013; 40(3):209-16.
33. Figueiró A, Hartz Z, Brito C, Samico I, Siqueira F, Cazarin G, et al. Óbito por dengue como evento sentinela para avaliação da qualidade da assistência: estudo de caso em dois municípios da Região Nordeste, Brasil, 2008. Cad Saúde Pública 2011; 27(12):2373-85.
34. Arce M, Lugo S, Pavlicich V. Estudio comparativo de características clínicas, laboratoriales y terapéuticas en lactantes y escolares hospitalizados por fiebre dengue. Pediatr (Asunción) 2014; 41(1):17-23.
35. Dung N, Day N, Tam D, Loan H, Chau H, Minh L, et al. Fluid replacement in dengue shock syndrome: a randomized, double-blind comparison of four intravenous-fluid regimens. Clin Infect Dis 1999; 29(4):787-94.
36. Ngo N, Cao X, Kneen R, Wills B, Nguyen V, Nguyen T, et al. Acute management of dengue shock syndrome: a randomized double-blind comparison of 4 intravenous fluid regimens in the first hour. Clin Infect Dis 2001; 32(2):204-13.
37. Wills B, Nguyen MD, Ha T, Dong T, Tran T, Le T, et al. Comparison of three fluid solutions for resuscitation in dengue shock syndrome. N Engl J Med 2005; 353(9):877-89.
38. Lugo S, Pavlicich V. Indicadores tempranos de dengue grave en pacientes hospitalizados. Pediatr (Asunción) 2014; 41(2):113-20.
39. Ranjit S, Kissoon N, Gandhi D, Dayal A, Rajeshwari N, Kamath S. Early differentiation between dengue and septic shock by comparison of admission hemodynamic, clinical, and laboratory variables: a pilot study. Pediatr Emerg Care 2007; 23(6):368-75.
40. Marón G, Escobar G, Hidalgo E, Clara A, Minniear T, Martinez E, et al. Characterization of dengue shock syndrome in pediatric patients in El Salvador. Pediatr Infect Dis J 2011; 30(5):449-50.
41. Trung D, Thao le T, Dung N, Ngoc T, Hien T, Chau N, et al. Clinical features of dengue in a large Vietnamese cohort: intrinsically lower platelet counts and greater risk for bleeding in adults than children. PLoS Negl Trop Dis 2012; 6(6):e1679.
42. Peeling R, Artsob H, Pelegrino JL, Buchy P, Cardosa MJ, Devi S, et al. Evaluation of diagnostic tests: dengue. Nat Rev Microbiol 2010; 8(12 Suppl):S30-8.
43. Tricou V, Minh N, Farrar J, Tran H, Simmons C. Kinetics of viremia and NS1 antigenemia are shaped by immune status and virus serotype in adults with dengue. PLoS Negl Trop Dis 2011; 5(9):e1309.
44. Chaterji S, Allen JC, Chow A, Leo Y, Ooi E. Evaluation of the NS1 rapid test and the WHO dengue classification schemes for use as bedside diagnosis of acute dengue fever in adults. Am J Trop Med Hyg 2011; 84(2):224-8.
45. Centers for Disease Control and Prevention. Dengue Homepage: laboratory guidance and diagnostic testing. Atlanta, GA: CDC, 2010. Disponible en: http://www.cdc.gov/dengue/clinicalLab/laboratory.html. [Consulta: 7 junio 2012].
46. Chakravarti A, Kumar A, Malik S. Detection of dengue infection by combining the use of an NS1 antigen based assay with antibody detection. Southeast Asian J Trop Med Public Health 2011; 42(2):297-302.
47. Centers for Disease Control and Prevention. New CDC test for dengue approved June 20, 2012. Atlanta, GA: CDC, 2012 Disponible en: http://www.cdc.gov/media/releases/2012/p0620_dengue_test.html. [Consulta: 15 mayo 2016].
48. Guzman MG, Jaenisch T, Gaczkowski R, Ty V, Sekaran S, Kroeger A, et al. Multi-country evaluation of the sensitivity and specificity of two commercially-available NS1 ELISA assays for dengue diagnosis. PLoS Negl Trop Dis 2010; 4(8):e811.
49. Rosenberger K, Lum L, Alexander N, Junghanss T, Wills B, Jaenisch T; DENCO Clinical Study Group. Vascular leakage in dengue - clinical spectrum and influence of parenteral fluid therapy. Trop Med Int Health 2016; 21(3):445-53.
50. Lugo S, Arce M, Mesquita M, Pavlicich V. Incidencia del dengue grave en lactantes. Pediatr (Asunción) 2015; 42(1):22-30.
51. Khongphatthanayothin A, Lertsapcharoen P, Supachokchaiwattana P, La-Orkhun V, Khumtonvong A, Boonlarptaveechoke C, et al. Myocardial depression in dengue hemorrhagic fever: prevalence and clinical description. Pediatr Crit Care Med 2007; 8(6):524-9.
52. Cam B, Tuan D, Fonsmark L, Poulsen A, Tien N, Tuan H, et al. Randomized comparison of oxygen mask treatment vs. nasal continuous positive airway pressure in dengue shock syndrome with acute respiratory failure. J Trop Pediatr 2002; 48(6):335-9.
53. Balasubramanian S, Ramachandran B, Amperayani S. Dengue viral infection in children: a perspective. Arch Dis Child 2012; 97(10):907-12.
54. Wilder-Smith A, Massad E. Age specific differences in efficacy and safety for the CYD-tetravalent dengue vaccine. Expert Rev Vaccines 2016; 15(4):437-41.
55. Basuki P, Budiyanto, Puspitasari D, Husada D, Darmowandowo W, Ismoedijanto I, et al. Application of revised dengue classification criteria as a severity marker of dengue viral infection in Indonesia. Southeast Asian J Trop Med Public Health 2010; 41(5):1088-94.
Correspondencia: Dra. Viviana Pavlicich.
Correo electrónico: p_viviana@hotmail.com