Services on Demand
Journal
Article
Related links
Share
Archivos de Pediatría del Uruguay
On-line version ISSN 1688-1249
Arch. Pediatr. Urug. vol.85 no.2 Montevideo June 2014
CASO CLÍNICO
Arch Pediatr Urug 2014; 85(2)
Intoxicación por imidazólicos en pediatría
Experiencia del Centro de Información y Asesoramiento Toxicológico en niños y adolescentes
Fernando Bazzino1, Florencia Del Cioppo2, Antonio Pascale3, Patricia Dall´Orso4
1. Pediatra. Servicio de Emergencia Hospital Británico.
2. Residente de Toxicología. Depto. de Toxicología Hospital de Clínicas. Facultad de Medicina. UDELAR.
3. Médico Toxicólogo. Prof. Adj. del Depto. de Toxicología. Hospital de Clínicas. Facultad de Medicina. UDELAR.
4. Prof. Agda de Emergencia Pediátrica. Depto. de Emergencia Pediátrica, CHPR. Facultad de Medicina. UDELAR. Pediatra Referente del Depto. de Emergencia Pediátrica Hospital Británico.
Centro de Información y Asesoramiento Toxicológico. Montevideo, Uruguay. Hospital Británico. Montevideo, Uruguay.
Fecha recibido: 22 de abril de 2014.
Fecha aprobado: 12 de agosto de 2014.
Resumen
Introducción: los derivados imidazólicos del tipo de la nafazolina son utilizados como vasoconstrictores locales, descongestivos nasales y oftálmicos. Su utilización en niños puede ocasionar una intoxicación aguda potencialmente grave. Conocer la epidemiología de esta enfermedad, los aspectos toxicológicos y la forma de presentación clínica puede contribuir a disminuir su incidencia.
Objetivos: comunicar la experiencia del Centro de Información y Asesoramiento Toxicológico (CIAT) en menores de 15 años expuestos a imidazólicos y presentar tres casos clínicos de intoxicación por nafazolina asistidos en el Servicio de Emergencia Pediátrica del Hospital Británico (HB).
Material y métodos: estudio retrospectivo de las consultas telefónicas por exposición a derivados imidazólicos realizadas al CIAT desde el 1° de enero del 2010 al 31 de diciembre del 2012. Revisión de historias clínicas de tres niños intoxicados por nafazolina asistidos en el 2013 en el HB.
Resultados: el CIAT registró 27 casos, edad promedio 2 años y 10 meses. El agente más frecuente fue nafazolina (n=23). La vía intranasal administrado por un familiar, sin indicación médica, y la vía oral por ingesta accidental fueron las circunstancias de exposición más frecuentes. Los tres niños asistidos en el HB se presentaron como pacientes graves. Depresión neuropsíquica, hipotermia, bradicardia, frialdad periférica e hipertensión arterial transitoria o hipotensión, fueron los síntomas predominantes.
Conclusiones: el uso de imidazólicos genera riesgo de intoxicación aguda, los niños pequeños son los más afectados, a pesar de la forma típica de presentación clínica puede confundirse con otras patologías. El pediatra es fundamental en la prevención, desaconsejando formalmente su uso.
Palabras clave: NAFAZOLINA; ENVENENAMIENTO; NIÑO
Summary
Introduction: naphazoline type imidazole derivatives are used as local vasoconstrictors, nasal and ophthalmic decongestants. Potentially severe acute poisoning in children use is described. Know about the disease epidemiology, toxicological aspects and clinical presentation can contribute to reduce their incidence.
Objectives: communicate the experience of the
Material and methods: retrospective study of phone consultations by exposure to imidazole derivatives at
Results:
Conclusions: use of imidazolic derivatives generates great risk of acute intoxication. Young children are the most affected despite the typical form of clinical presentation can be confused with other severe diseases. The pediatrician has a critical role in preventing formally and discouraging its use.
Key words: NAPHAZOLINE; POISONING; CHILD
Introducción
Las intoxicaciones agudas son motivo de consulta habitual en los servicios de urgencia y emergencia pediátrica. En nuestro medio, las intoxicaciones en menores de 15 años presentan mayoritariamente un mecanismo accidental, y los medicamentos ocupan la primera causa(1,2).
Los derivados de la imidazolina o imidazólicos son un grupo de compuestos químicos que por sus acciones simpaticomiméticas son utilizados como vasoconstrictores locales, descongestivos nasales y oftálmicos(3). Son rápidamente absorbidos a través de la mucosa nasal, conjuntival o gastrointestinal con un inicio rápido de acción(3).
Su efecto descongestivo vasoconstrictor resulta de la estimulación de los receptores alfa 2 adrenérgicos de los vasos sanguíneos. Además presentan una gran afinidad por receptores imidazólicos localizados en la médula ventrolateral y algunos tejidos periféricos. Estos dos mecanismos explican las manifestaciones típicas de esta intoxicación: depresión neuropsíquica, hipertensión arterial transitoria, palidez, hipotermia, frialdad periférica, sudoración, bradicardia e hipotensión(4).
En nuestro país existen preparados comerciales utilizados como descongestivos nasales que contienen nafazolina, oximetazolina o xilometazolina. Se presentan en frasco gotero a concentraciones que varían entre 0,5 a 1 mg por ml de solución, solos o en asociaciones con antibióticos, antisépticos o corticoides. También están disponibles descongestivos oftálmicos que contienen clorhidrato de nafazolina a razón de 0,1 a 0,5 mg/ml de solución, solos o asociados con antibióticos, antisépticos, antialérgicos o corticoides (tabla 1).
La División Química y Medicamentos del Ministerio de Salud Pública, en la Resolución 881/989, establece que: “Los laboratorios nacionales productores de especialidades farmacéuticas que contengan nafazolina deben destacar claramente en sus envases, prospectos o etiquetas: los riesgos, advertencias, contraindicaciones, vía de administración, grupo etario a quienes se destina el producto y posología de la misma, así mismo la mayor exactitud en el método de administración relacionado con los envases y goteros correspondientes. Disponer que las farmacias den cumplimiento al decreto 252/87 en el que se determina la venta bajo receta médica de los medicamentos que contengan nafazolina”(5).
Estos fármacos frecuentemente utilizados por los adultos, presentan riesgo potencial en la población pediátrica, pudiendo ocasionar intoxicaciones agudas potencialmente graves.
Sin bien los niños intoxicados con nafazolina tienen generalmente una buena evolución, la asistencia inicial de estos pacientes suele generar dudas diagnósticas y confundirse con otras enfermedades graves de la infancia.
Conocer los datos epidemiológicos de esta intoxicación en Uruguay y su forma de presentación clínica puede contribuir a disminuir su incidencia, facilitando el diagnóstico oportuno y un abordaje adecuado.
Objetivos
1. Comunicar la experiencia del Centro de Información y Asesoramiento Toxicológico (CIAT) en menores de 15 años expuestos a imidazólicos durante el período 2010-2012.
2. Presentar tres casos clínicos de niños intoxicados por nafazolina asistidos en el año 2013 en el Servicio de Emergencia Pediátrica del Hospital Británico.
Material y métodos
Se realizó un estudio retrospectivo observacional de las consultas por exposición a derivados imidazólicos realizadas al CIAT por vía telefónica entre el 1 de enero del 2010 y el 31 de diciembre del 2012. Se incluyeron todos aquellos pacientes menores de 15 años en los cuales hubo una exposición, voluntaria o accidental, por parte del paciente y/o por sus familiares. Los casos fueron seleccionados del Sistema IPCS/INTOX, base de datos utilizada por el CIAT para el registro de casos e incidentes. Toda la información se obtuvo de la historia clínica generada en la sala de respuesta telefónica de urgencia del CIAT, analizándose las siguientes variables: edad, sexo, procedencia, agente involucrado, uso del mismo, vía y circunstancia de exposición, dosis, latencia entre la exposición y la consulta, presentación clínica, tratamiento instituido y evolución.
En base a la revisión de las historias clínicas de los pacientes que consultan en la Emergencia Pediátrica del Hospital Británico, se presentan 3 casos clínicos de niños intoxicados por nafazolina asistidos en el año 2013.
Resultados
El CIAT registró 27 casos en el período del estudio, con edades comprendidas entre 28 días y 14 años. El promedio de edad fue de 2 años y 10 meses. De los casos analizados, 17 correspondían al sexo femenino. Con respecto a la procedencia, 20 consultas eran de Montevideo y las restantes del interior del país. El agente más frecuentemente involucrado fue nafazolina (n=23), seguido por oximetazolina (n=3) y xilometazolina (n=1).
En 24 casos se presentaba como gotas nasales y en 3 casos para uso ocular.
En la tabla 2 se muestran la vía y circunstancia de exposición: la vía intranasal administrada por un familiar, sin indicación médica, y la vía oral por ingesta accidental fueron las más frecuentemente reportadas. El caso de autoadministración correspondió a un niño de 10 años.
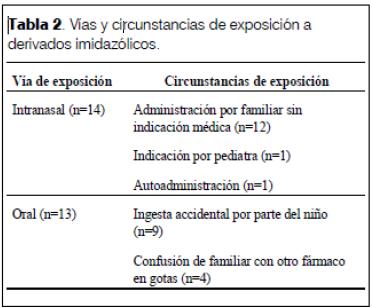
La exposición fue única en 23 casos. En las cuatro consultas donde la exposición fue repetida, se reportó que un familiar le aplicó gotas nasales.
El período de latencia entre la exposición y la consulta fue menor o igual a 2 horas en 17 casos (tabla 3).

Las dosis fueron consignadas en 17 casos y oscilaban entre 1 a 3 gotas en cada narina para la aplicación nasal, y de 11 gotas a 10 ml para los casos de ingesta. En 16 pacientes se evidenciaron elementos clínicos compatibles con intoxicación aguda por imidazólicos, 15 eran menores de 3 años. En 12 de estos, la vía de exposición fue nasal y en 4 casos oral. Depresión neuropsíquica, hipotermia y bradicardia fueron las manifestaciones prevalentes (tabla 4). En la mayoría de los casos (n=10) fueron reportadas en las primeras 12 horas de la exposición.
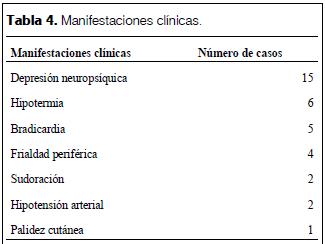
En tres pacientes en los cuales hubo ingesta, la clínica apareció entre las 12 a 24 horas de la exposición, y las dosis máximas estimadas oscilaron entre 7 a 10 ml de la solución.
En el primer semestre del año 2013 se asistieron en la Emergencia del Hospital Británico tres pacientes con diagnóstico final de intoxicación aguda por nafazolina.
A continuación se exponen los tres casos clínicos.
Caso clínico 1
Fecha de consulta: 22/01/2013.
Varón, 8 años, sano. Certificado esquema de vacunación (CEV) vigente. En tratamiento con amoxicilina por infección respiratoria alta (IRA).
Motivo de consulta: somnolencia y palidez.
Horas previas a la consulta, instala malestar general con tendencia al sueño, palidez intensa, sudoración profusa y frialdad periférica. No se registró la temperatura.
Sin otros síntomas acompañantes. Niega traumatismos, ingesta de fármacos y contacto con tóxicos o medicamentos.
Examen físico: Glasgow 15. Palidez intensa con sudoración fría con relleno capilar menor a 2 segundos. Temperatura axilar 35ºC. Frecuencia respiratoria 18 rpm. Frecuencia cardíaca 48 lpm. PA 100/74 mmHg. Oximetría de pulso 99% VEA. Pupilas intermedias, simétricas. Reflejo foto motora y consensual conservada. No rigidez nuca. Resto normal.
Se realiza monitorización cardiorrespiratoria. La valoración infecciosa y metabólica fue normal. Radiografía de tórax sin alteraciones. Electrocardiograma con ritmo sinusal y bradicardia de 48 latidos/minuto. Ecocardiograma normal. Ingresa a sala de cuidados críticos.
Buena evolución posterior.
Reinterrogando en la evolución se detecta el antecedente de la administración en el hogar de gotas nasales conteniendo nafazolina. El intervalo fue difícil de establecer.
Caso clínico 2
Fecha de consulta: 15/03/2013.
Varón, 2 años y 8 meses, sano. CEV vigente. IRA alta en curso.
Motivo de consulta: somnolencia y sudoración profusa.
En las 12 h previas al ingreso, decaimiento, somnolencia y sudoración profusa. No registro de temperatura. Sin otros síntomas acompañantes. No contacto con tóxicos.
Examen físico: Glasgow 13. Palidez cutánea, bien hidratado y perfundido. Temperatura axilar 35ºC. Frecuencia respiratoria 20 rpm. Frecuencia cardíaca 70 lpm. PA 94/54 mmHg.
Oximetría de pulso 98% VEA. Pupilas intermedias, simétricas. Reflejo foto motora y consensual conservada. No signos focales. Resto normal.
Se realiza monitorización cardiorrespiratoria, la valoración infecciosa y metabólica fue normal. Drogas en orina negativas. Punción lumbar sin alteraciones. ECG con ritmo sinusal de 60 lpm. QT normal. Ecocardiograma normal. Ingresa a sala de cuidados críticos.
Buena evolución, sin complicaciones.
En la evolución un familiar del niño refiere el antecedente de la administración en el hogar de nafazolina intranasal. El intervalo entre la administración de las gotas y la aparición de los síntomas no pudo establecerse.
Caso clínico 3
Fecha de consulta: 13/06/2013
Varón, 2 años y 11 meses, sano. CEV vigente. En tratamiento con amoxicilina por otitis media aguda.
Motivo de consulta: somnolencia.
El día de la consulta, lo notan pálido, sudoroso, con tendencia al sueño. No registro de temperatura. No orina en últimas 12 h. Sin otros síntomas acompañantes. Niega traumatismos, ingesta de fármacos o contacto con tóxicos.
Examen físico: Glasgow 13, palidez cutánea, sudoración profusa y frialdad periférica con relleno capilar menor a 2 segundos. Temperatura axilar 35,6ºC. Frecuencia respiratoria 18 rpm. Frecuencia cardíaca 60lpm. PA 115/56mmHg. Oximetría de pulso 98% VEA. Pupilas intermedias, simétricas. Reflejo foto motora y consensual conservada. No rigidez nuca.
Se realiza monitorización cardiorrespiratoria, aporte de suero fisiológico 20 ml/kg en 30 minutos. La valoración infecciosa y metabólica fue normal. Ingresa a sala de cuidados críticos. Buena evolución posterior. El lapso entre la aplicación de las gotas y los síntomas no puedo determinarse.
En la evolución surge el antecedente de la administración en el hogar de nafazolina intranasal.
Todos los pacientes presentaron una buena evolución, encontrándose asintomáticos a las 24 horas de la exposición. En todos los casos la conducta terapéutica consistió en el sostén de funciones vitales, basado principalmente en el aporte de fluidos por vía intravenosa (suero fisiológico en bolo), conservación de la temperatura, oxigenoterapia, observación y monitoreo clínico de las funciones vitales (control de temperatura, control de frecuencia cardíaca y presión arterial, estado de conciencia, frecuencia respiratoria y saturación de oxígeno), todas ellas medidas tendientes a evitar complicaciones.
Comentarios
Los derivados imidazólicos han sido ampliamente utilizados como descongestivos nasales y oculares desde la década del 40. En los últimos 40 años surgen reportes de casos y estudios epidemiológicos retrospectivos, con resultados similares a los hallados en este estudio, advirtiendo sobre los riesgos de utilizar estos compuestos en niños pequeños.
En esta serie la intoxicación aguda por derivados imidazólicos predominó en niños menores de 3 años, coincidiendo con series de casos en la literatura internacional, donde la media de edad se sitúa entre 1 y 3 años(6,7). Existe una especial vulnerabilidad en niños pequeños, en los cuales la aplicación nasal de 1 o 2 gotas de una solución al 0,05% puede resultar en intoxicación aguda(8). Por lo tanto todos estos derivados implican un alto riesgo de toxicidad en niños a las dosis que usualmente se utilizan en la población adulta. Las recomendaciones pueden variar de acuerdo a la normativa vigente en cada país, pero existe un consenso general de no indicar el uso de descongestivos nasales y oculares que contengan imidazólicos en niños menores de 6 años(8). La Administración de Alimentos y Medicamentos de Estados Unidos (Food and Drug Administration, FDA), considerando el riesgo de intoxicación por ingesta accidental de imidazólicos, extiende la recomendación hasta los 12 años de edad(9). Los derivados imidazólicos poseen un estrecho rango terapéutico, lo que incrementa el riesgo de intoxicación aun a dosis terapéuticas(6,10). Algunos autores plantean que la vulnerabilidad relacionada con la edad se relaciona con un menor peso corporal y una mayor capacidad de absorción en niños(11).
En esta serie la nafazolina fue el compuesto más frecuentemente involucrado como agente etiológico. En relación a su efecto sedante sobre el sistema nervioso central (SNC) y a su acción sobre la frecuencia cardíaca y presión arterial por efecto alfa-adrenérgico, la nafazolina posee una elevada potencia en relación a otros imidazólicos(12-14).
Su potencia guarda relación con su toxicidad aguda. Existe también una mayor disponibilidad de nafazolina como descongestivo en los productos farmacéuticos que contienen imidazólicos en nuestro país (tabla 1). Probablemente esta observación explique el mayor número de consultas por nafazolina en nuestro medio.
La vía intranasal, administrada por un familiar sin indicación médica, y la vía oral por ingesta accidental fueron las más frecuentemente reportadas. Este hallazgo coincide con Mahieu, quien describe en una serie de casos de niños expuestos a imidazólicos que la aplicación nasal, a dosis única o repetida y la ingesta en forma accidental son las circunstancias más frecuentes(6,7).
En nuestra serie la exposición repetida se consignó solamente en cuatro casos. Si bien la intoxicación aguda puede ocurrir con la aplicación única por vía nasal, esta forma de aplicación agrava el curso de la intoxicación. Esta modalidad debe ser considerada en aquellos casos en los cuales no existe una clara correlación temporal entre la exposición y el inicio y persistencia de los síntomas. Este dato suele ser difícil de obtener en la práctica clínica al interrogar al familiar en la urgencia(15).
El tiempo transcurrido entre la exposición y la consulta al CIAT fue de menos de 2 horas en 17 casos (63% de la serie). Esto es debido a la rápida absorción de los derivados imidazólicos y su rápido inicio de acción, la mayoría en los primeros 20 minutos, con una duración de su efecto de 4 a 8 horas, a excepción de oximetazolina de mayor duración(5,16). Sus vidas medias de eliminación oscilan entre 2 a 4 horas. De acuerdo a otros estudios de casos, en general el cuadro clínico se resuelve en 24 h (6,10,15,17,18), tal como se observó en nuestra serie.
Las dosis reportadas fueron mayores en los casos de ingesta, como se describe en otras publicaciones de casos (7,11). Las manifestaciones clínicas descritas (tabla 3) son similares a otras series de casos internacionales y traducen clínicamente el mecanismo fisiopatológico de esta intoxicación. Los derivados imidazólicos estimulan receptores alfa2-adrenérgicos periféricos lo cual puede explicar la frialdad periférica, taquicardia e hipertensión arterial, habitualmente transitoria. Sin embargo estos compuestos también estimulan receptores alfa-adrenérgicos centrales (denominados imidazólicos) tendiendo a inhibir el centro vasomotor simpático y disminuyendo el tono vascular periférico(4,5,16). El efecto simpaticolítico se manifiesta por depresión neuropsíquica (particularmente en el niño), hipotermia, sudoración profusa, bradicardia e hipotensión arterial. En casos graves puede haber coma alternando con hiperactividad o agitación, convulsiones y apnea(8,19). Si bien se han descrito complicaciones graves asociadas (edema pulmonar severo, hemorragia intracraneana)(20,21), no se han descrito muertes por ingestión y aplicación nasal u ocular.
El diagnóstico es clínico. En casos graves se recomienda la realización de electrocardiograma y gasometría arterial por el riesgo de arritmias y acidosis respectivamente. En aquellos pacientes con depresión profunda del SNC se sugiere la realización de estudios imagenológicos y del líquido cefalorraquídeo para descartar diagnósticos diferenciales(8).
El tratamiento de la intoxicación aguda por derivados imidazólicos consiste en el sostén de funciones vitales y manejo de las complicaciones(4,7,10,15-18). En nuestra serie de casos todos los pacientes evolucionaron favorablemente con medidas de sostén sin necesidad de tratamiento farmacológico. No existe un antídoto específico(22). Algunos autores han utilizado naloxona, antagonista opioide, dado que los derivados imidazólicos comparten las propiedades farmacológicas de la clonidina, sin resultados concluyentes (8,23,24). La hipertensión arterial transitoria habitualmente no requiere tratamiento farmacológico (4,8). En caso de hipertensión arterial severa puede plantearse el uso de fentolamina, no disponible en nuestro medio (11). La hipotermia responde a medidas de calentamiento físico. No se recomienda el uso de atropina a menos de que se presente bradicardia con repercusión hemodinámica(16,18). En pacientes con hipotensión arterial se recomienda inicialmente la administración de fluidos intravenosos y de no responder a los mismos, inotrópicos tales como adrenalina o noradrenalina (8,19). En general el tratamiento farmacológico se reserva para aquellos casos graves, refractarios a las primeras medidas de sostén.
En nuestra serie no se realizaron medidas de decontaminación digestiva. El vaciamiento gástrico y administración de carbón activado no están indicados en los casos de ingesta accidental en niños y adolescentes dado que son formulaciones líquidas que se absorben rápidamente, perdiendo su eficacia (25). Por otra parte, su rápido inicio de acción determina una depresión neuropsíquica temprana, particularmente en los niños, por lo que el riesgo de aspiración de la vía aérea supera claramente el potencial beneficio de dichas medidas(4,8,19).
En relación a los tres casos clínicos reportados, todos se presentaron en el departamento de emergencia como pacientes graves, con formas clínicas típicas de intoxicación por nafazolina. El compromiso de conciencia, la hipotermia, bradicardia, frialdad periférica e hipotensión, fueron los síntomas predominantes, presentes en los tres casos, solo un caso tuvo HTA leve sistólica.
Sin embargo, la ausencia de contacto inicial planteó dudas diagnósticas que justificaron la realización de exámenes complementarios pensando en otras etiologías.
Dos de los tres casos eran niños pequeños, coincidiendo con la casuística nacional e internacional(6,7). Un dato importante a considerar es que todos estaban cursando una infección respiratoria al momento de la consulta. La desobstrucción nasal constituye una recomendación frecuente del pediatra en el curso de infecciones respiratorias, por lo cual este dato debe alertar al pediatra emergencista sobre la posibilidad de contacto nasal con imidazólicos en determinado momento epidemiológico.
En los tres casos fue difícil definir el tiempo, la dosis y las circunstancias de exposición.
Luego de corregir la falla hemodinámica y realizar una estricta monitorización cardiaca, los tres presentaron una buena evolución. Como es habitual no fue necesaria la utilización de fármacos para el control de los síntomas típicos de intoxicación.
A pesar de la reglamentación vigente las familias acceden a estos fármacos en forma libre, lo que constituye una práctica riesgosa.
La implementación de programas de prevención promovidos por las autoridades sanitarias, en conjunto con las sociedades científicas y académicas, contribuirán a evitar esta intoxicación.
Conclusiones
El uso de derivados imidazólicos administrados por vía nasal, ocular u oral en la población pediátrica genera riesgo de intoxicación aguda.
Conocer la forma de presentación clínica, los fármacos disponibles en nuestro medio e insistir con identificar estos productos en el hogar, facilitarán un diagnóstico oportuno evitando exámenes innecesarios. El pediatra constituye un recurso fundamental en la prevención de esta enfermedad desaconsejando formalmente su uso. Seguramente el cumplimiento de la reglamentación vigente contribuirá a disminuir su frecuencia.
Referencias bibliográficas
1. Juanena C, Battocletti A, Carballal L, Taran Peña L. Intoxicaciones en menores de quince años. En: Centro de Información y Asesoramiento Toxicológico. Intoxicaciones: casuísticas del Centro de Información y Asesoramiento Toxicológico. Montevideo: UDELAR, Unidad de Comunicación, Departamento de publicaciones, 2011: 15-26.
2. Bernadá M, Assandri E, Cuadro MN, Perdomo V, García L, Chamorro F, et al. Accidentes en la infancia: prevalencia, características y morbilidad determinada por los accidentes en una población de Uruguay. Rev Méd Urug 2010; 26(4): 224-37.
3. Thomas CW, David PW. Agonistas y antagonistas adrenérgicos. En: Brunton LL, Lazo JS, Parker K, eds. Goodman & Gilman: las bases farmacológicas de la terapéutica. 11 ed. México, DF: Mc Graw-Hill-Interamericana, 2006:237-97.
4. Tomassoni AJ, Weisman RS. Antihistamines and decongestants. En: Nelson L, Lewin N, Howland MA, Hoffman R, Goldfrank L, Flomenbaum N. Goldfrank´s toxicologic emergencies. 9 ed. New York: Mc Graw-Hill, 2011: 748-58.
5. Uruguay. Ministerio de Salud Pública. División Química y Medicamentos. Resolución 811/989: venta bajo receta médica de los medicamentos que contengan nafazolina.
6. Mahieu LM, Rooman RP, Goossens E. Imidazoline intoxication in children. Eur J Pediatr 1993; 152(11):944-6.
7. Bucaretchi F, Dragosavac S, Vieira RJ. Exposiçao aguda a derivados imidazolinicos em crianças. J Pediatr (
8. Klasco RK, ed. POISINDEX® System.
9.
10. Stamer UM, Buderus S, Wetegrove S, Lentze MJ, Stüber F. Prolonged awakening and pulmonary edema after general anesthesia and naphazoline application in an infant. Anesth Analg 2001; 93(5):1162-4.
11. Wenzel S, Sagowski C, Laux G, Kehrl W, Metternich FU. Course and therapy of intoxication with imidazoline derivate naphazoline. Int J Pediatr Otorhinolaryngol 2004; 68(7): 979-83.
12. Delbarre B, Schmitt H. Sedative effects of alpha-sympathomimetic drugs and their antagonism by adrenergic and cholinergic blocking drugs. Eur J Pharmacol 1971; 13(3):356-63.
13. Autret AM, Schmitt H, Fenard S, Pétillot N. Comparison of haemodynamic effects of alpha-sympathomimetic drugs. Eur J Pharmacol 1971; 13(2):208-17.
14. Timmermans PB, Fluitman PH, Mackaay JC, van Zwieten PA. Hypotensive and bradycardic effects of classical alpha-sympathomimetic drugs upon intravenous administration to pentobarbitone-anaesthetized rats. Arch Int Pharmacodyn Ther 1978; 231(1):98-103.
15. Dunn C, Gauthier M, Gaudreault P. Coma in a neonate following single intranasal dose of xylometazoline. Eur J Pediatr 1993; 152(6):541.
16. Tomassoni AJ, Wallace KL. Imidazoline, guanidine and oxazoline: antihypertensives and decongestants. En: Brent J, Wallace KL, Burkhart KK, Phillips SD, Donovan JW. Critical care toxicology: diagnosis and management of the critically poisoned patient. Philadelphia: Elsevier-Mosby, 2005:441-7.
17. Claudet I, Fries F. Danger des vasoconstricteurs nasaux chez le nourrisson: a propos d’une observation. Arch Pédiatr 1997; 4:538-41.
18. Paksu Mª, Paksu ª, Akkuº T, Baysal K. One drop can be beneficial, one swig can be deadly: tetrahydrozoline intoxication. Turk J Pediatr 2012; 54(6):658-60.
19.
20. Zavala JA, Pereira ER, Zétola VH, Teive HA, Nóvak EM, Werneck LC. Hemorrhagic stroke after naphazoline exposition: case report. Arq Neuropsiquiatr 2004; 62(3B):889-91.
21. Fukushima H, Norimoto K, Seki T, Nishiguchi T, Nakamura T, Konobu T, et al. Acute pulmonary edema associated with naphazoline ingestion. Clin Toxicol (Phila) 2008; 46(3):254-6.
22. Ricart Campos S, Fernández Santervas Y, Vallina Jordana E, Luaces i Cubells C. Intoxicación accidental por descongestionante tópico nasal. An Pediatr (Barc) 2006; 64(1):100-8.
23. Holmes JF, Berman DA. Use of naloxone to reverse symptomatic tetrahydrozoline overdose in a child. Pediatr Emerg Care 1999; 15(3):193-4
24. Katar S, Taskesen M, Okur N. Naloxone use in a newborn with apnea due to tetrahydrozoline intoxication. Pediatr Int 2010; 52(3):488-9.
25. Alvarez-Pitti J, Rodríguez-Varela A, Morales-Carpi C, Lurbe E, Estañ L. Naphazoline intoxication in children. Eur J Pediatr 2006; 165(11):815-6.
Correspondencia: Dr. Fernando Bazzino Rubio. Correo electrónico: fbazzino@gmail.com














