Services on Demand
Journal
Article
Related links
Share
Archivos de Pediatría del Uruguay
On-line version ISSN 1688-1249
Arch. Pediatr. Urug. vol.85 no.1 Montevideo Mar. 2014
ARTÍCULO ORIGINAL
Arch Pediatr Urug 2014; 85(1)
Características epidemiológicas y clínicas de niños hospitalizados con tos convulsa durante el 2012 en el Hospital Pediátrico del Centro Hospitalario Pereira Rossell
Mónica Sosa1, Marcela Castro2, Sergio Salomón3, Gustavo Giachetto4
1. Asistente Clínica Pediátrica “C”. Facultad de Medicina, UDELAR.
2. Posgrado de Pediatría Clínica Pediátrica “C”. Facultad de Medicina, UDELAR.
3. Residentes de Pediatría Clínica Pediátrica “C”. Facultad de Medicina, UDELAR.
4. Prof. Clínica Pediátrica “C” Facultad de Medicina, UDELAR.
CHPR, UDELAR.
Fecha recibido: 27 de noviembre de 2013.
Fecha aprobado: 3 de junio de 2014.
Resumen
Introducción: en Uruguay desde la incorporación de la vacuna antipertussis en 1963 disminuyó significativamente las notificaciones de tos convulsa. En el año 2011 se registra un aumento del número de casos con formas graves especialmente en niños menores de 4 meses. En febrero del 2012 se incorporó la vacuna antipertussis acelular a los 12 años.
Objetivos: describir las características epidemiológicas y clínicas de los niños hospitalizados con diagnóstico de tos convulsa confirmado en el HP-CHPR.
Material y métodos: estudio descriptivo, retrospectivo. Incluye los niños hospitalizados con diagnóstico de tos convulsa confirmado entre el 1 de enero y el 31 de diciembre de 2012. Variables: edad, sexo, criterios de hospitalización, complicaciones, inmunizaciones, estadía hospitalaria, ingreso a CTI, muertes.
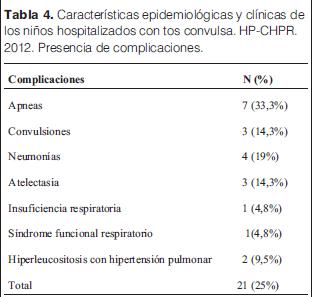
Resultados: ingresaron 84 niños con diagnóstico confirmado de tos convulsa, 18 a UCI (21,4%); 42 menores de 4 meses (50%) niños; 58 niños presentaron certificado esquema de vacunación vigente (69%); la media de la estadía hospitalaria fue 7 días (rango 1–25 días); presentaron complicaciones 21 niños: apneas siete (33,3%), atelectasias tres (14,3%), neumonía cuatro (19%), convulsiones tres (14,3%), insuficiencia respiratoria uno (4,8%), hipertensión pulmonar-hiperleucocitosis dos (9,5%), uno con síndrome funcional respiratorio (4,8%). Los casos más graves ingresaron a UCI, los que desarrollaron hipertensión pulmonar y recibieron exsanguinotransfusión. Se encontró una asociación estadísticamente significativa entre ingreso a CTI y recuento leucocitario elevado (30.000–60.000 elementos/mm3), menor edad, apneas reiteradas e HTP. Falleció un niño en UCI.
Discusión y conclusión: la tos convulsa afecta principalmente a menores de 12 meses, la gravedad se asocia con la edad, la presencia de apneas reiteradas, hiperleucocitosis e hipertensión pulmonar. Se debe mantener la vigilancia y fortalecer las estrategias de vacunación.
Palabras clave:
TOS FERINA
NIÑO HOSPITALIZADO
Summary
Introduction: notifications of whooping cough was significantly reduced by in Uruguay since the introduction of the vaccine antipertussis in 1963. In the year 2011 is recorded an increase in the number of cases with severe forms specially in children younger than 4 months. In February 2012 was incorporated acellular pertussis vaccine at age 12.
Objectives: to describe the clinical and epidemiological characteristics of children hospitalized with a diagnosis of cough whooping confirmed in HP-CHPR.
Material and methods: retrospective descriptive study. It includes children hospitalized with whooping cough diagnostic confirmed from 1/1 to 31/12/12. Variables: age, sex, criteria for hospitalization, complications, immunizations, hospital stay, admission to CTI, deaths.
Results: entered 84 children with whooping cough confirmed, to UCI 18 (21,4%); less than 4 months 42 (50%) children; presented certified 58 existing immunization schedule (69%) children; the average hospital stay was 7 days (range 1-25 days); 21 children presented complications: apneas 7 (33,3%), atelectasis 3 (14,3%), pneumonia 4 (19%), seizures 3 (14,3%), 1 respiratory failure (4,8%), pulmonary hypertension - hiperleucocitosis 2 (9,5%), functional respiratory syndrome 1 (4,8%). The most serious cases admitted to ICU, which developed HTP and received exchange transfusion, found a statistically significant association between high WBC count (30.000-60.000 elements/mm3), younger age, repeated apneas and admission to ICU. Died 1 child in ICU.
Discussion and conclusion: the whooping cough affects mainly children under 12 months; gravity is associated with age, the presence of repeated apneas, hiperleucocitosis and pulmonary hypertension. Must be vigilance and strengthen vaccination strategies.
Key words:
WHOOPING COUGH
CHILD, HOSPITALIZED
Introducción
La tos convulsa es una enfermedad infecciosa respiratoria aguda, producida por Bordetella pertussis y en menor medida por Bordetella parapertussis. Constituye una causa importante de morbimortalidad infantil. Se estima que esta enfermedad es responsable de 50 millones de casos y 300.000 defunciones anuales a nivel mundial. La tasa de letalidad en países en desarrollo alcanza cifras de hasta 4% en menores de 12 meses. En la región de las Américas, durante el año 2011 y a comienzos del 2012 se registraron brotes en Argentina, Colombia, Chile, Canadá y EEUU que afectaron predominantemente adolescentes y recién nacidos*. Estos brotes se caracterizaron por elevada letalidad especialmente en menores de 6 meses(1).
* Boletín Integrado de Vigilancia. Secretaria de Promoción y Programas Sanitarios. No 109. SE 8. Enero 2012. Boletín Epidemiológico del Instituto Nacional de Salud. Informes periódicos, coqueluche. Departamento de Epidemiologia. Ministerio de Salud de Chile.
Centros para el Control y la Prevención de Enfermedades. Pertussis Outbreaks. Disponible en: http://www.cdc.gov/pertussis/outbreaks.html
Se trata de una enfermedad controlable pero no totalmente prevenible por vacuna. La eficacia luego de la tercera dosis varía entre 87 y 93%, en fase epidémica y endémica respectivamente. La protección de la vacuna antipertussis declina 50% luego de un periodo de 6 a 12 años(2,3).
En Uruguay desde la incorporación de la vacuna antipertussis al Programa Ampliado de Inmunizaciones en 1963 disminuyeron significativamente las notificaciones, observándose un comportamiento endémico con brotes epidémicos cada 3 a 4 años(4,5). Históricamente la cobertura de la 3ª dosis de vacuna pentavalente se ha mantenido en promedio en 97%. En el año 2011 se registró un brote con un total de 630 casos notificados(4,5).
Las formas graves de tos convulsa pueden adoptar diversas presentaciones. Una de ellas es con leucocitosis importante que recuerdan reacciones leucemoides y que se acompañan de hipertensión pulmonar e hipoxemia. Los factores de riesgo de enfermedad grave son: edad menor a 4 meses, hiperleucocitosis mayor a 100.000 elementos/mm3, foco de consolidación en la radiografía de tórax e hipertensión pulmonar(1,4-7).
El objetivo de este estudio es describir las características epidemiológicas y clínicas de los niños hospitalizados con diagnóstico de tos convulsa confirmada en el Hospital Pediátrico del Centro Hospitalario Pereira Rossell (HP-CHPR) en el año 2012.
Material y métodos
Se realizó un estudio descriptivo, retrospectivo entre el 1 de enero y el 31 de diciembre de 2012 en el que se incluyeron todos los niños hospitalizados en el HP-CHPR con diagnóstico confirmado de tos convulsa.
Se consideraron las siguientes definiciones operativas:
- Caso sospechoso de tos convulsa. Tos persistente de al menos 14 días de duración o tos de cualquier duración que se presenta en forma paroxística o acompañada de uno o más de los siguientes síntomas o signos: estridor o reprise inspiratorio, vómito luego de la tos, apnea, cianosis, convulsiones, antecedente de contacto con caso sospechoso; sin otra causa que lo explique(4).
- Caso confirmado de tos convulsa. Caso sospechoso que presente reacción en cadena de polimerasa (RCP) positiva para Bordetella pertussis o Bordetella parapertussis(4).
La confirmación diagnóstica se realizó en el Laboratorio Central del CHPR mediante técnica de RCP para Bordetella pertussis y Bordetella parapertussis. Esta técnica utiliza doble hibridación lo cual permite discriminar entre fragmentos amplificados específicos y no específicos. La sensibilidad del test es 97% y la especificidad 100%*.
* SPO 11: Ensayo oligocromatográfico para la detección y diferenciación cualitativa de Bordetella pertussis y Bordetella parapertussis en muestras clínicas. Vircell microbiologists. SPEED-OLIGO®BORDETELLA.
Se excluyeron aquellos niños con antígenos virales positivos y RCP negativa para B. pertussis o B. parapertussis en muestras de aspirado nasofaríngeo.
Los pacientes se identificaron a partir del sistema informático del HP-CHPR.
Se analizaron las siguientes variables: edad al ingreso; sexo; número de dosis de vacuna recibidas; criterios de hospitalización (menores de 12 meses cuando presentan paroxismos con cianosis, casos graves o con complicaciones)(7,8), recuento leucocitario (normal entre 5.000 y 15.000 elementos/mm3, leucopenia < 5.000 elementos/mm3, leucocitosis > 15.000 elementos/mm3); hallazgos en la radiografía de tórax (normal, infiltrados bilaterales y difusos, atelectasia, neumotórax, imágenes de consolidación homogénea o inhomogénea), tratamiento antibiótico administrado; complicaciones pulmonares (infecciosas y/o mecánicas), hipertensión pulmonar, compromiso hemodinámico, falla renal, necesidad de cuidado intensivo (UCI), estadía hospitalaria en días, fallecimientos y causas, indicación de tratamiento y quimioprofilaxis*, registro de la denuncia a la División Epidemiologia del Ministerio de Salud Pública (MSP).
* Centers for Disease Control and Prevention. Recommended antimicrobial agents for the treatment and post exposure prophylaxis of pertussis: 2005 CDC guidelines.MMWR 2005; 54 (N° RR-14): [1-13].
Se consideró caso grave cuando presentaba alguno de los siguientes criterios: apnea en menor de 3 meses, insuficiencia respiratoria aguda, convulsiones hipóxicas reiteradas o prolongadas, leucocitosis > 20.000 elementos/mm3 con aumento mayor a 1.000–1.500 elementos/mm3 por hora(7,8).
La fuente de datos fueron las historias clínicas. Los datos se registraron en un formulario elaborado para este estudio y fueron recabados por los propios investigadores.
El protocolo de estudio fue aprobado por la Dirección y el Comité de Ética del HP-CHPR.
Análisis estadístico
Las variables cualitativas se expresaron en frecuencias absolutas y relativas, las variables cuantitativas en media y rango.
Para la comparación de proporciones se aplicó c² de Pearson y test de Fisher.
Se consideró estadísticamente significativo p<0,05. Para el procesamiento de datos se utilizó el Programa Epi info versión 3.2.2 (2004).
Resultados
En el periodo estudiado fueron hospitalizados 10.799 niños**; por probable tos convulsa 164 (1,5%).
** Fuente: informe SINADI y partes diarios de ingresos y egresos de pacientes. Departamento de Registro y Consulta Pediátrico. Centro Hospitalario Pereira Rossell. 2012.
Fueron notificadas a la División de Epidemiologia del MSP 146 de los 164 casos sospechosos (89%) (9).
En 14 niños (8,5%) no fue posible conocer el resultado de la RCP, en 66 (40,2%) la RCP fue negativa. El diagnóstico se confirmó por RCP en 84 niños (51,2%): Bordetella pertussis 81 (96,4%) y Bordetella parapertussis tres (3,6%).
La tasa de hospitalización por tos convulsa confirmada en el 2012 en el HP-CHPR fue 7,8/1.000 (IC95% 6,1–9,4).
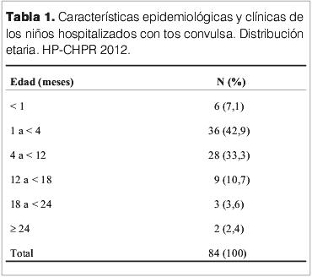
La distribución por grupo etario de los casos confirmados se muestra en la tabla 1. El 50% (n=42) fueron menores de 4 meses. El promedio de edad fue 5,5 meses (mínimo 4 días–máximo 24 meses). La razón sexo masculino/sexo femenino fue 1,1 (44 niños y 40 niñas).
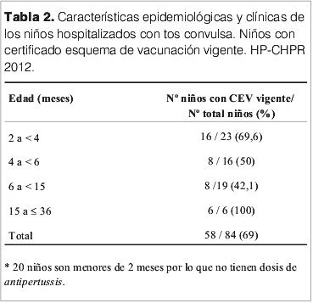
En la tabla 2 se muestra el número de niños con certificado esquema de vacunación (CEV) vigente. El 69% de los casos confirmados (n=58) presentaron CEV vigente para la edad. Presentaron inmunización primaria completa antipertussis (tres dosis de vacuna pentavalente) ocho de los 19 niños (42,1%) que debían haberla recibido.
El 46,4% (n=39) ingresaron por ser menores de 12 meses y presentar paroxismos con cianosis; 11,9% (n=10) por complicaciones; 41,7% (n=35) por cumplir con criterios de gravedad.
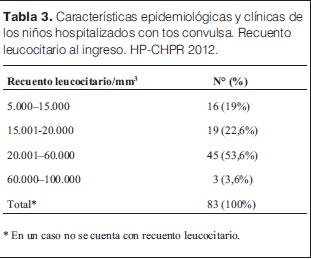
El recuento leucocitario al ingreso se muestra en la tabla 3. En uno de los 84 niños no se pudo obtener el dato. Tuvieron recuento normal 16 niños (19%) y aumentado 67 (79,8%): entre 15.001 y 20.000 leucocitos/mm3 19 (22,6%), entre 20.001 y 60.000 leucocitos/mm3 45 (53,6%) y mayor a 60.000 elementos/mm3 tres niños (3,6%). No se observó ningún caso con recuento mayor de 100.000 leucocitos/mm3.
El 97,6% (n=82) recibió tratamiento acorde a las recomendaciones; con azitromicina 76,2% (n= 64) o claritromicina 21,4% (n=18). Dos niños con diagnóstico de tos convulsa no recibieron tratamiento.
El promedio de la estadía hospitalaria fue 7 días (rango 1 a 25 días). Permanecieron hospitalizados menos de 3 días 14 (3,6%), 4 a 6 días 40 (47,6%), 7 a 12 días 17 (20,2%); 13 a 20 días ocho (9,5%) y 21 a 31 días cinco (5,9%). Fueron derivados a Unidad de Cuidado Intensivo (UCI) 18 (21,4%) niños.
En la tabla 5 se comparan las características clínicas y evolución de los niños hospitalizados en la UCI versus aquellos que no requirieron hospitalización en dicha unidad.
Se observó relación significativa entre hospitalización en la UCI y menor edad, recuento leucocitario mayor a 60.000 elementos/mm3, apneas reiteradas e hipertensión pulmonar. El único fallecimiento ocurrió en este grupo de pacientes.
Falleció un varón de 2 meses, procedente de Montevideo, hijo de una madre de 20 años que presentaba tos desde hace 20 días. No había recibido aún las vacunas de los 2 meses. Su enfermedad se había iniciado 3 días antes del ingreso con tos coqueluchoide. Agrega dificultad respiratoria. Al ingreso presentaba 68.500 leucocitos/mm3 (51% linfocitos), frecuencia cardíaca 212 cpm, insuficiencia respiratoria tipo II. El ecodoppler cardiovascular no evidenció signos de hipertensión pulmonar. Se inicia asistencia ventilatoria mecánica. A las 12 horas 84.800 leucocitos/mm3 (linfocitos 39,7%). Acidemia extrema persistente. Se reitera ecocardiograma que muestra hipertensión pulmonar (45-55 mmHg). Fallo hemodinámico refractario, insuficiencia renal que no responde a diálisis peritoneal. Se realizó exanguinotransfusión en dos oportunidades. Fallece a las 24 horas. Este caso fue notificado al MSP.
Discusión
En el año 2011 en Uruguay se registró un brote epidémico con un total de 630 casos notificados con un pico máximo en la semana epidemiológica 44. Esta cifra de notificación es la más alta registrada desde 1987. Un hecho destacable es la elevada letalidad que afectó a lactantes pequeños(9). Esto determinó reuniones de expertos, elaboración de comunicados dirigidos al equipo de salud reforzando el reconocimiento de casos, la importancia de la notificación, los criterios de diagnóstico, tratamiento y prevención. Se realizó una campaña gratuita de vacunación con triple bacteriana con componente antipertussis acelular (dpaT) dirigida a personal de salud y cuidadores de menores de 6 meses embarazadas en el tercer trimestre, madres y padres de menores de 6 meses. Además, se actualizaron las recomendaciones de diagnóstico y tratamiento de casos graves y se incluyó esta vacuna en el CEV a los 12 años en forma universal, gratuita y obligatoria. La campaña de vacunación realizada entre noviembre 2011 y febrero de 2012 tuvo baja adherencia, se administraron 39 552 dosis (4,7,9).
En el año 2012, la tasa de notificación de tos convulsa en Uruguay fue 12,63/100.000 habitantes. Comparado con el año 2011, a pesar de un mayor número de notificaciones, se constata una tendencia descendente con oscilaciones, con menor número de casos respecto a los notificados durante el brote de 2011(9-16). Es importante señalar que del HP-CHPR se recibieron 292 notificaciones: 132 del Departamento de Emergencia y 146 del área de internación.
Si bien la mayoría de los casos analizados en esta serie fueron denunciados al MSP se comprobó subnotificación.
Una de las recomendaciones del Grupo Técnico Asesor (GTA) sobre Enfermedades Prevenibles por Vacunación es desarrollar estrategias para fortalecer la vigilancia a fin de monitorizar la carga de la enfermedad y evaluar el impacto de la vacunación. Si bien el comportamiento actual parece indicar que Uruguay atraviesa una etapa de defervescencia del brote epidémico, es difícil establecer claramente el nivel de endemia por la subnotificación (9).
Según datos de la División Epidemiologia y el Programa de Auditoría de Muertes de niños menores de 15 años del MSP, entre abril de 2011 y noviembre de 2012 fallecieron 18 menores de 1 año por tos convulsa. Estas muertes coincidieron con el brote de la enfermedad. En el año 2012 ocurrieron ocho de las 18 muertes. Una de estas muertes ocurrió en la UCI del HP-CHPR, dos correspondieron a muertes inesperadas en domicilio y las cinco restantes ocurrieron en otras UCI del sistema de salud. Al igual que lo observado en este caso, la mayoría fueron lactantes pequeños (media y moda 2 meses), cumplían con la definición de caso ampliada, presentaron hiperleucocitosis y anomalías radiológicas compatibles con consolidación y/o atelectasia, desarrollaron rápidamente polipnea e hipertensión pulmonar(10).
La tasa de hospitalización estimada en este estudio (7,8/1.000) es similar a la comunicada en otras series nacionales e internacionales(1,4-7). Se debe considerar que al problema de la subnotificación se agrega el sesgo de inclusión, ya que en este trabajo, si bien analiza un centro de referencia nacional para los usuarios del subsector público, conocer la realidad epidemiológica implica el análisis multicéntrico.
Se destaca que la incidencia fue mayor en niños menores de 4 meses. Estos resultados reafirman el concepto que ha cambiado la edad en que enferman los niños por tos convulsa. Mientras que en la era prevacunación la incidencia era mayor luego del año de vida, actualmente la enfermedad afecta predominantemente a niños menores de un año, especialmente menores de 6 meses(1,4-7).
La enfermedad natural así como la inmunidad natural desencadenan inmunidad tanto humoral como celular. Esta inmunidad disminuye con la edad. Esto explica por qué se afectan los adultos jóvenes, aunque sin riesgo de presentar formas graves, y por qué los lactantes pequeños son susceptibles y tienen mayor riego de presentar formas graves con mayor número de complicaciones(1-7). En esta serie la mayoría de los ingresos estuvieron motivados por la forma de presentación grave y/o con complicaciones.
Aunque el cultivo continúa siendo el “gold standard” para confirmar el diagnóstico, la RCP ha comenzado a reemplazarlo. Se trata de un método rápido, específico cuya sensibilidad garantiza la positividad aun en fases tardías del curso de la enfermedad. La RCP permanece positiva luego de 7 días de tratamiento antibiótico. Esta técnica ha pasado a ser el método de elección en muchos laboratorios clínicos(11,12). En este estudio la RCP realizada en el laboratorio del HP-CHPR confirmó el diagnóstico de tos convulsa.
Aunque la vacuna no evita la enfermedad es conocido el impacto que tiene en su control luego de la tercera dosis. Un hallazgo preocupante es la baja cobertura de la tercera dosis en esta población, inferior a la comunicada en la población general(13-18). Este hecho sumado a la vulnerabilidad social aumenta el riesgo de diseminación, enfermar y padecer formas graves(15-17).
Al igual que lo citado en la literatura, la mayoría de los niños presentó radiografías normales. Los hallazgos patológicos corresponden a las alteraciones habitualmente descritas compatibles con las complicaciones más frecuentes de la tos convulsa (infiltrados difusos, atelectasia, neumonía, cisuritis)(6,8,11,19-21).
Las características de los niños que requirieron UCI contemplan los criterios definidos en las recomendaciones nacionales(7).
La leucocitosis con linfocitosis absoluta es un hallazgo frecuente en esta enfermedad y se correlaciona con formas graves especialmente en lactantes(7,22). Los casos más graves que ingresaron a UCI, desarrollaron HTP y recibieron exanguinotransfusión, se encontró una asociación estadísticamente significativa entre recuento leucocitario elevado (30.000–60.000 elementos/mm3) e ingreso a UCI. Es necesario profundizar en el análisis de otros factores de riesgo de gravedad(7).
La prescripción de macrólidos constituye una de las medidas recomendadas para el control de la tos convulsa. Esto contribuye a disminuir la transmisibilidad aunque no modifica la severidad de la enfermedad(13,14). Si bien la indicación fue elevada (98%) no se cumplió en la totalidad de los casos.
La infección con B. pertussis puede ser controlada por vacunas. Las vacunas disponibles muestran una eficacia de 80% a 85% después de la inmunización primaria completa. Se han propuesto diversas estrategias para intentar controlar este problema de salud pública. Sin embargo, hasta la fecha existen controversias en relación a la eficacia de las diferentes estrategias. En julio de 2013, el Grupo Técnico Asesor de Enfermedades prevenibles por vacunación (GAT), realizó las siguientes recomendaciones:
- Los países que tienen esquemas de vacunación con vacuna a células completas, como Uruguay, deben continuar con sus esquemas actuales. No se han demostrado beneficios al cambiar a vacunas acelulares.
- Realizar los máximos esfuerzos en mantener niveles de cobertura ³95% y en forma oportuna.
- Fortalecer la vigilancia epidemiológica para mejorar el monitoreo de la enfermedad.
- En caso de confirmar brotes comenzar la edad de vacunación a las 6 semanas de vida y vacunar las mujeres embrazadas solamente en las áreas afectadas por el brote. En la actualidad no hay suficiente evidencia para recomendar la vacunación rutinaria a todas las embarazadas(23).
Conclusiones
La tos convulsa es una enfermedad endémica con brotes epidémicos; afecta principalmente a menores de 12 meses, la gravedad se asocia con la edad, la presencia de apneas reiteradas, hiperleucocitosis e hipertensión pulmonar. Se debe mantener la vigilancia y fortalecer las estrategias de vacunación.
Referencias bibliográficas
1. Organización Panamericana de la Salud. Alerta Epidemiológica: tos ferina (Coqueluchoide). Washington, DC: OPS/OMS, 2012. Disponible en: http://www.paho.org/hq/index.php?option=com_docman&task=doc_view&gid=17052&Itemid . [Consulta: 11 setiembre 2013].
2. Ramsay ME, Farrington CP, Miller E. Age-specific efficacy of pertussis vaccine during epidemic and non-epidemic periods. Epidemiol Infect 1993; 111(1):41-8.
3. Jenkinson D. Duration of effectiveness of pertussis vaccine: evidence from a 10 year community study. Br Med J (Clin Res Ed) 1988; 296(6622):612-4.
4. Uruguay. Ministerio de Salud Pública. Dirección General de la Salud. División Epidemiología. Situación epidemiológica de la infección por Bordetella pertussis (Tos convulsa) y recomendaciones para su manejo: comunicado al equipo de salud 28/10/2011. Disponible en: http://www2.msp. gub.uy/uc_5777_1.html. [Consulta:29 agosto 2013]
5. Uruguay. Ministerio de Salud Pública. Dirección General de la Salud. División Epidemiológica. Unidad de Información Nacional en Salud. Programa de Salud de la Niñez. Mortalidad infantil: Uruguay 2011. Disponible en: http://www2.msp.gub.uy/andocasociado.aspx?6487,26081. [Consulta 27 agosto 2013].
6. Quian J. Tos ferina: vieja enfermedad, nuevos desafíos. Biomedicina 2012; 7(3): 22-7. Disponible en: http://www. um.edu.uy/docs/tos_ferina.pdf. [Consulta:29 agosto 2013].
7. Machín C, Serra A, Olagüe C, Menchaca A. Protocolo de tratamiento de la tos convulsa grave en la Unidad de Cuidados Intensivos de Niños (UCIN) del Centro Hospitalario Pereira Rossell. Arch Pediatr Urug 2011; 82(3):174-6.
8. Uruguay. Universidad de la República. Facultad de Medicina. Clínica Pediátrica A. Atención Pediátrica: pautas de diagnóstico, tratamiento y prevención. 7 ed. Montevideo: Oficina del Libro-AEM, 2008.
9. Uruguay. Ministerio de Salud Pública. Dirección General de la Salud. División Epidemiológica. Informe de actualización: situación de os convulsa a la semana epidemiológica 37 de 2012. Disponible en: http://www.msp.gub.uy/sites/default/files/archivos_adjuntos/Informe_tos_convulsa_SETIEMBRE_2012%20%284%29.pdf. [Consulta: 2 setiembre 2013].
10. Uruguay. Ministerio de Salud Pública. Dirección General de la Salud. División Epidemiología. Unidad de Información Nacional en Salud. Programa de Salud de la Niñez. Mortalidad Infantil en Uruguay 2012. Montevideo: MSP, 2013. Disponible en: http:// www2.msp.gub.uy/andocasociado.aspx?6487,2608. [Consulta: 2 setiembre 2013].
11. Quian J, Cerisola A, Russomano F, Fernández A, Cappeta M, Uriarte R, et al. Infecciones por Bordetella pertussis en niños menores de un año hospitalizados y sus contactos del hogar. Arch Pediatr Urug 2006; 77(3): 229-36. Disponible en: http://www.scielo.edu.uy/scielo.php?script=sci_arttext &pid=S0004-05842006000300004&lng=es. [Consulta:29 agosto 2013].
12. Murphy T, Bisgard K, Sanden G. Diagnosis and laboratory methods. En: Centers of Disease Control and Prevention. Guidelines for the control of pertussis outbreak. Atlanta, GA: CDC, 2000:7-8.
13. Centers for Disease Control and Prevention. Manual for the surveillance of vaccine-preventable diseases. Atlanta, GA: CDC, 2008.
14. Faulkner A, Skoff T, Martin S, Cassiday P, Tondella ML, Liang J, et al. Chapter 10: pertussis. En: Centers for Disease Control and Prevention. Manual for the surveillance of vaccine preventable diseases. 5.ed. Atlanta, GA: CDC, 2012. Disponible en: http://www.cdc.gov/vaccines/pubs/surv-manual/chpt10-pertussis.pdf. [Consulta:30 agosto 2013].
15. Organización Panamericana de la Salud. Unidad de inmunización. Área de Salud Familiar y Comunitaria. Coberturas de vacunación, 1999-2013. Washington, DC: OPS, 2013. Disponible en: http://www.paho.org/spanish/dd/ ais/cp_858.htm. [Consulta: 27 agosto 2013].
16. World Health Organization. Inmunization, Vaccines and Biologicals. Pertussis. Geneva: WHO, 2011. Disponible en: http://www.who.int/immunization/topics/pertussis/en/#. [Consulta: 27 agosto 2013].
17. Centros para el Control y la Prevención de Enfermedades. Proteja a los bebés contra la tos ferina (pertussis). Atlanta, GA: CDC, 2013. Disponible en: http://www.cdc.gov/spanish/especialesCDC/tosferina/. [Consulta: 27 agosto 2013].
18. Uruguay. Ministerio de Salud Pública. Comunicado a equipos de salud. Medidas para prevenir las infecciones respiratorias en invierno: responsabilidad de todos. Montevideo: MSP, 2012. Disponible en: http://www2.msp.gub.uy/ucepidemiologia_6325_1.html. [Consulta: 28 agosto 2013].
19. Sociedad Latinoamericana de Infectología Pediátrica. Manual de vacunas de Latinoamérica. 3 ed. Madrid: SLIPE, 200:75-96. Disponible en: http://www.infectologiapediatrica.com/attachments/manual_vacunas.pdf. [Consulta: 5 setiembre 2013].
20. Organización Panamericana de la Salud. Informe final de la XIX Reunión del Grupo Técnico Asesor sobre Enfermedades Prevenibles por Vacunación: vacuna a tu familia, protege a tu comunidad. Buenos Aires: OPS, 2011. Disponible en: http://new.paho.org/hq/index.php?option=com_content&task=view&id=1862&Itemid=1674. [Consulta: 2 setiembre 2013].
21. Santoro A, Ferreira E, Ferrari AM. Infecciones respiratorias agudas bajas en niños menores de tres años: referencia a unidades de cuidado intensivo. Arch Pediatr Urug 2002; 73(4):196-202.
22. Snyder J, Fisher D. Pertussis in childhood. Pediatr Rev 2012; 33(9):412-20.
23. Organización Panamericana de la Salud. Informe final de la XIX Reunión del Grupo Técnico Asesor sobre Enfermedades Prevenibles por Vacunación: vacunación una responsabilidad compartida. Quito: OPS, 2013. Disponible en: http://new.paho.org/hq/index.php?option=com_content& task=view&id=1862&Itemid=1674. [Consulta: 2 setiembre 2013].
Correspondencia: Dra. Mónica Sosa.
Correo electrónico: moniq@adinet.com.uy