Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Archivos de Pediatría del Uruguay
versión On-line ISSN 1688-1249
Arch. Pediatr. Urug. vol.84 no.2 Montevideo 2013
Abscesos profundos por Staphylococcus aureus meticilino resistente adquirido en la comunidad
Reporte de cuatro casos clínicos
Patricia Dall´Orso 1, Lucía Maurente 2, Rodrigo Suarez 3, Bernardo Berazategui 4, Catalina Pirez 5
Resumen
El Staphylococcus aureus meticilino resistente adquirido en la comunidad (SAMR-AC) emergió en Uruguay en el año 2001 y desde ese momento se ha establecido como agente de múltiples enfermedades infecciosas de la infancia.
Algunas formas clínicas de presentación más frecuentes, como las infecciones superficiales, no ofrecen habitualmente dificultades diagnósticas. Otras menos frecuentes, como los abscesos de localización profunda, son formas menos conocidas donde el diagnóstico no es sencillo y existe riesgo de tratamiento tardío lo cual contribuye a una mayor carga de morbimortalidad por este agente.
En este trabajo se comunican cuatro casos clínicos de abscesos profundos por SAMR-AC, en pacientes hospitalizados en los años 2009- 2011 en el Hospital Pediátrico del Centro Hospitalario Pereira Rossell.
Se presentan tres casos de abscesos musculares, dos de ellos retroperitoneales, y un caso de abscesos hepáticos, forma de presentación infrecuente pero típica de este agente.
Se destacan en esta serie las dificultades para el diagnóstico temprano por lo inespecífico de la presentación clínica, el apoyo fundamental de la imagenología en la confirmación diagnóstica, la necesidad de tratamiento antimicrobiano prolongado y del drenaje adecuado del material colectado importante en la identificación microbiológica del agente implicado.
Palabras clave:
STAPHYLOCOCCUS AUREUS
RESISTENTE A METICILINA
INFECCIONES COMUNITARIAS
ADQUIRIDAS
ABSCESO
Summary
The community-acquired methicillin-resistant Staphylococcus aureus (CA-MRSA) emerged in Uruguay in 2001, and since then it has established as an agent of many infectious diseases of childhood.
Some more frequent clinic forms of presentation such as superficial infections do not habitually offer diagnostic difficulties. Others less frequent as the deep-seated abscesses are less known forms where the diagnosis is not easy and there is a risk of delayed treatment which contributes to increase morbidity and mortality caused by this agent.
In this work, four clinic cases of CA-MRSA abscesses deep are communicated in patients hospitalized in the years 2009 to 2011 at the Pediatric Hospital-Pereira Rossell Hospital Center (HP-PRHC).
As an unfrequent but usual presentation of this agent three cases of muscular abscesses are presented, two of them retroperitoneals and a case of hepatic abscesses.
The difficulties for early diagnosis according to the nonspecific of clinical presentation, the fundamental support of imaginology in the diagnostic confirmation, the need for prolonged antimicrobial therapy and adequate drainage of the collected material which is important to identify the involved microbial agent are emphasized in these series.
Keywords:
METHICILLIN-RESISTANT
STAPHYLOCOCCUS AUREUS
COMMUNITY-ACQUIRED INFECTIONS
ABSCESS
Introducción
Las infecciones por Staphylococcus aureus meticilino resistente han aumentado su frecuencia globalmente desde los años noventa, surgiendo posteriormente el Staphylococcus aureus meticilino resistente adquirido en la comunidad (SAMR-AC) con un perfil de resistencia característico.
Emergió en nuestro país en el año 2001 ocasionando entre los años 2003-2004 una importante alarma sanitaria, desde ese momento se ha establecido como patógeno emergente de denuncia obligatoria, a pesar de lo cual existen pocos datos sobre su prevalencia actual en la infancia (1).
La cepa predominante en nuestro país llamada “Clona Uruguay” UR 6, difiere genéticamente de las cepas de Estados Unidos y Europa (MW2) (2-4). La identificación de un cassette cromosómico característico denominado SSCmec tipo IVc, que expresa la proteína de unión a la penicilina 2a (PBP2a), la de unión al colágeno (cna) y la Leucocidina de Panton Valentine (PVL) han permitido conocer los mecanismos de virulencia relacionados con las infecciones por este agente (2-4).
Afecta fundamentalmente a niños y jóvenes, siendo la forma clínica más frecuente de presentación la infección de piel y partes blandas.
En un porcentaje menor pero con mayor morbimortalidad se presenta como infecciones profundas e invasivas, tales como abscesos viscerales, miositis, infecciones osteoarticulares y neumonías complicadas con empiema y necrosis (3,5-7).
Los abscesos son acumulaciones de pus en los tejidos encontrándose como infecciones superficiales o profundas en cualquier órgano interno (8).
En la práctica clínica identificar abscesos superficiales no genera habitualmente dificultades diagnósticas. Por el contrario, los abscesos profundos son menos conocidos, quizás por su menor frecuencia, y se presentan con clínica inespecífica lo cual contribuye al diagnóstico tardío, aumentando la probabilidad de complicaciones locales y sistémicas.
El objetivo de este trabajo es comunicar cuatro casos clínicos de abscesos profundos por SAMR-AC, en pacientes hospitalizados en los años 2009, 2010 y 2011 en el Hospital Pediátrico del Centro Hospitalario Pereira Rossell (HP-CHPR).
Se presentan tres casos de abscesos musculares, dos de ellos retroperitoneales, el cuarto caso corresponde a abscesos hepáticos.
Casos clínicos
Caso 1
Adolescente de 13 años, sexo femenino, raza blanca, sana, procedente de Montevideo, medio socioeconómico (MSEC) deficitario.
Quince días antes del ingreso consulta por disuria y tumoración lumbar izquierda en apirexia, con diagnóstico de probable infección urinaria, se indica tratamiento antibiótico que recibe en forma irregular. En la evolución aumento de tamaño de la tumoración y fiebre de 40ºC, por lo que consulta en enero del 2009 en el Departamento de Emergencia Pediátrica del Centro Hospitalario Pereira Rossell (DEP–CHPR).
De los exámenes realizados en la primer consulta se destaca: examen de orina normal, proteína C reactiva (PCR): 36,7 mg/l y leucocitosis: 11.800 elementos/mm3.
Ecografía que informa probable absceso de músculo psoas izquierdo.
Ingresa con cefuroxime y gentamicina i/v y diagnóstico de absceso intramuscular perirrenal. Frente al hallazgo de fluctuación a nivel de la tumoración lumbar se solicita segunda ecografía, que ubica el absceso en el plano de los músculos paravertebrales con un volumen aproximado de 20 ml (figuras 1 y 2).
Se rota plan antibiótico a clindamicina y gentamicina i/v, que recibe por 6 días.
Persiste febril hasta el drenaje quirúrgico que se realiza a las 48 horas del ingreso, del que se obtienen 60 ml de pus que desarrolla SAMR-AC sensible a gentamicina, trimetroprim-sulfametoxazol (TMP-SMX) y clindamicina. Hemocultivo sin desarrollo.
Se valora con resonancia nuclear magnética (RNM), descartándose la afectación ósea vertebral y medular.
Hospitalizada durante 10 días presenta una buena evolución, completándose 21 días de tratamiento con clindamicina vía oral.
Caso 2
Adolescente de 13 años, sexo femenino, raza blanca, sana, procedente de Young, MSEC aceptable.
Tres meses previos impétigo en miembros inferiores tratado con antibioticoterapia oral. Veinte días antes de la consulta politraumatismos moderados en accidente de tránsito. Consulta en setiembre de 2009 en el hospital de Young por dolor en flanco y fosa lumbar izquierda, fiebre de 39°C y anorexia.
En la ecografía se constata imagen redondeada y heterogénea, en seno renal izquierdo.
Leucocitosis: 16.300 elementos/mm3, velocidad de eritrosedimentación (VES): 130, urocultivo sin desarrollo. Se comienza ampicilina-sulbactam i/v y se traslada al DEP-CHPR.
Al ingreso se constata masa palpable de 8 cm en flanco y fosa lumbar izquierda dolorosa, leucocitosis de 22.000 elementos/mm3, neutrófilos: 78%, PCR: 242 mg/l. Proteinuria: 1, 19 g/l, sedimento en orina: escasos hematíes.
Ecografía: en riñón izquierdo se objetiva imagen heterogénea con sectores hipodensos de 30 mm en tercio medio de la valva posterior, con aspecto de absceso renal. Psoas homolateral con absceso de 9 cm de diámetro que desplaza el riñón en sentido anterior.
Tomografía computada (TC) realizada en HP-CHPR, que muestra absceso renal y de psoas izquierdo, con derrame pleural ipsilateral (figura 3).
Con diagnóstico de absceso renal y de psoas, se realiza drenaje percutáneo guiado por ecografía, obteniéndose 60 ml de líquido hematopurulento.
Urocultivo y hemocultivo sin desarrollo.
Cultivo del pus extraído del psoas: SAMR-AC con resistencia inducible a la clindamicina. Sensible a gentamicina, vancomicina y trimetropim-sulfametoxazol.
Evolución: en apirexia desde las 24 horas posdrenaje, disminución de leucocitosis y VES.
Recibe 6 días de ampicilina-sulbactam más clindamicina i/v, con el antibiograma se rota a vancomicina que recibe por 15 días i/v hasta el alta hospitalaria.
Ecografía de control que constata franca disminución de los abscesos.
Se otorga el alta con tratamiento ambulatorio con TMP-SMX por vía oral por 15 días.
Caso 3
Adolescente de 11 años, sexo femenino, procedente de San José, MSEC aceptable.
Intervenida a los 4 y a los 11 meses por cirugía reparadora de paladar.
Veinticuatro horas previas a la consulta dolor en miembro inferior derecho permanente, de moderada a gran intensidad, localizado en región anterolateral de muslo, migrando a la región inguinal con irradiación a fosa ilíaca derecha y flanco derecho. No fiebre. Niega antecedente traumático.
Consulta en el DEP-CHPR en octubre del 2011, destacándose en el examen físico al ingreso: buen aspecto general, hemodinamia estable, abdomen: blando, depresible, dolor a la palpación profunda en fosa ilíaca derecha y a la extensión del miembro inferior derecho, no se constata dolor con la flexión y la abducción. No se palpan tumoraciones abdominales.
Evaluada por traumatólogo y cirujano, se descarta patología osteoarticular y cuadro quirúrgico abdominal.
Ecografía abdominal que informa a nivel del psoas ilíaco derecho tumoración sólida de 50 mm de longitud x 30 mm anteroposterior.
Hemograma: glóbulos blancos 14.100 elementos/mm3, neutrófilos 77,7%, hemoglobina 10,7 mg/dl, PCR: 55 mg/dl. Con diagnóstico de absceso de psoas derecho ingresa a sala.
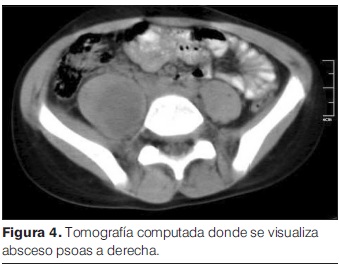
Se inicia tratamiento con clindamicina i/v que recibe por 12 días, solicitando a las 24 horas del ingreso TC de abdomen y pelvis (figura 4) que informa a nivel de psoas derecho extensa colección de 12 cm en sentido céfalo-caudal x 4cm x 3cm en sus ejes transversos.
Evoluciona con mejoría franca del dolor pero persiste febril, por lo que se reitera ecografía abdominal que muestra tumoración de 105 mm x 40 mm x 32 mm.
Se realiza drenaje percutáneo guiado por ecografía obteniéndose 120 ml de líquido purulento y hematopurulento.
Cultivo de pus del absceso que desarrolla SAMR- AC sensible a clindamicina, gentamicina, vancomicina y TMP-SMX.
Hemocultivo sin desarrollo. Buena evolución a los 13 días de internación se otorga el alta con clindamicina vía oral hasta completar 30 días.
Caso 4
Niña de 2 años, raza blanca, sana, procedente de área rural de Fray Bentos.
Quince días previos al ingreso dolor abdominal, fiebre intermitente, vómitos y diarrea. Se constata deshidratación, nitritos en orina, leucocitosis, VES elevada y funcional y enzimograma hepático normal. Con diagnóstico de infección urinaria ingresa al hospital de Fray Bentos y recibe cefuroxime intravenoso.
En la evolución reinstala fiebre por lo que se envía en enero del 2010 al DEP-CHPR donde se destaca dolor abdominal a predominio de hipocondrio derecho con defensa.
Ecografía y TC de abdomen que muestran dos abscesos hepáticos, uno subcapsular pequeño y otro mayor en lóbulo derecho, elementos de peritonitis y un derrame pleural homolateral.
Valorada por cirujano se realiza laparotomía que encuentra peritonitis con exudado purulento, plastrón subhepático y compromiso del epiplón.
En el postoperatorio agravación del estado general, elementos de falla hemodinámica, requiere cargas de volumen y permanece 72 horas en cuidados intensivos pediátricos.
Recibe 5 días de ceftazidime, gentamicina y metronidazol, se agrega vancomicina ante la noción epidemiológica de impétigo en la familia.
En el cultivo de los abscesos y del exudado peritoneal desarrolla SAMR-AC sensible a gentamicina, vancomicina y trimetroprim-sulfametoxazol, resistente a ciprofloxacina y cefuroxime. Hemocultivo negativo.
En sala se completa tratamiento con clindamicina i/v por 4 semanas. Buena evolución clínica, constatándose disminución del tamaño de los abscesos en el control ecográfico.
A los 35 días de internación se otorga el alta con TMP-SMX vía oral que recibe durante 11 días en domicilio.
Comentarios
Se presentaron cuatro casos clínicos de infecciones profundas e invasivas por SAMR-AC, poco habituales pero típicas de este agente. En todos los casos existieron dificultades diagnósticas y la estadía hospitalaria fue prolongada en relación a la media del CHPR.
Este tipo de infecciones requiere un nivel elevado de sospecha, ya que su presentación clínica es poco específica y se confunde con otras patologías más frecuentes de la infancia.
Los tres primeros casos corresponden a miositis piogénicas en la cual existe una acumulación de pus a nivel muscular con la formación de un absceso a ese nivel. Las infecciones bacterianas del músculo esquelético es una patología rara en climas templados pero endémica en los trópicos, más frecuente en escolares y adolescentes de sexo masculino (9,10). En esta serie los tres casos son adolescentes de sexo femenino.
El agente etiológico de las miositis piogénicas en más del 90% es el Staphylococcus aureus, seguido en frecuencia por el Streptococcus pyogenes (10-12).
La primera comunicación internacional de piomiositis a SAMR-AC es del año 1996. En estudios nacionales previos referidos a infecciones invasivas por SAMR-AC en un total de 78 niños se constató un caso de miositis piogénica (1).
Según la literatura cualquier músculo puede verse afectado, pero los miembros inferiores y la pelvis son las regiones más frecuentemente involucradas, la piomiositis de cuádriceps representa 26,3% de los casos, mientras que se desconoce la prevalencia exacta de la afectación del psoas-ilíaco. La localización paravertebral es rara, con una frecuencia cercana a 4% (2,11,13,14).
En esta serie, al igual que se describe en la bibliografía, la clínica es inespecífica e insidiosa con elementos de repercusión general y locales inflamatorios dependientes de la región afectada y el tiempo de evolución de la enfermedad. Las complicaciones locoregionales también son dependientes de la localización, la posibilidad de que se produzca una infección generalizada sistémica existe, aunque es poco frecuente.
La localización paravertebral puede desencadenar invasión del canal raquídeo, con efectos por compresión de raíces como parestesias y dolor. También pueden aparecer artritis y/u osteomielitis vertebrales secundarias.
El absceso del psoas se relaciona con frecuencia con trombosis venosas profundas y tromboembolismo pulmonar como complicaciones evolutivas (9,15-19).
En estos tres casos de abscesos musculares profundos no se registraron complicaciones sistémicas.
Es destacable que dos de estos tres casos comparten el antecedente de traumatismos previos, factor predisponente que se encuentra con frecuencia en la literatura.
En ambos casos, la secuencia patogénica teórica se corresponde entonces con una lesión muscular, que frente a una bacteriemia genera una colonización en el área, desarrollándose finalmente una colección supurada. Esa lesión muscular localizada es provocada por un traumatismo que puede ser leve y tan lejano como de hasta un mes previo al diagnóstico (16,19-21).
En el primer caso claramente el traumatismo es en la región del absceso, mientras que en el segundo la paciente sufre politraumatismos que seguramente causaron lesiones musculares menores.
En cuanto al absceso del psoas, no siempre es clara la etiopatogenia, pudiendo ser primario, producto de una bacteriemia, o secundario a focos contiguos, renales, óseos o intestinales (enfermedad de Crohn, apendicitis).
En esta paciente se planteó un absceso de psoas primario (10,21,22).
En estos tres casos las imágenes ecográficas y tomográficas ocuparon un lugar importante en el diagnóstico.
La ecografía, la TC y RNM, aisladas o combinadas, aportan elementos específicos al diagnóstico, siendo en ocasiones complementarias (6,13,23).
La RNM ofrece una sensibilidad del 100% y una especificidad de hasta 88%, es la técnica más usada y rentable, siendo considerada el gold standard para valorar las lesiones espinales.
El contraste con gadolinio es útil en los casos de afectación espinal o paraespinal, como en el primero de esta serie (2,4,9,11,14,15,24,25).
En el primer caso, la RNM permitió descartar la afectación vértebro-medular, siendo de utilidad para localizar el absceso previo al drenaje quirúrgico (26).
En el segundo y tercer caso, la ecografía y tomografía realizadas por técnicos avezados en niños, fueron suficientes y complementarias para establecer el diagnóstico y la localización del absceso.
El tratamiento instaurado consideró el perfil de resistencia en Uruguay y las recomendaciones internacionales, requiriéndose antibioticoterapia parenteral prolongada asociada a drenaje quirúrgico en los 3 casos (9,15,27).
En el caso de piomiositis en etapas iniciales, o cuando es difícil o peligroso el abordaje quirúrgico de la colección supurada, puede considerarse la posibilidad de tratamiento antibiótico exclusivo. Si ésta es la decisión, la antibioticoterapia debe ser prolongada y acompañarse de un adecuado control clínico e imagenológico, que permita asegurar la desaparición de los abscesos (9,15,27).
La duración del tratamiento es de una a seis semanas. En el caso de absceso del psoas no existe consenso sobre la duración. En estos casos se realizó antibioticoterapia prolongada con antibióticos efectivos de acuerdo al germen planteado.
El drenaje quirúrgico, indispensable para la mejoría clínica de estos pacientes, permitió la confirmación bacteriológica del agente en todos los casos (9,16,27-30).
La cuarta paciente tuvo una forma clínica de presentación inespecífica, lo que determinó dificultades en el diagnóstico inicial, lo cual contribuyó a un diagnóstico evolucionado con repercusión sistémica.
Los abscesos hepáticos tienen una incidencia global variable, con un comportamiento endémico en regiones del tercer mundo. El 80% de los mismos es de causa bacteriana y, como ocurrió en este caso, el agente más frecuentemente involucrado es el Staphylococcus aureus, seguido por otros gram positivos, gram negativos y anaerobios.
En esta paciente se comprobó la existencia de dos abscesos en lóbulo derecho, siendo ésta la localización más frecuente.
La presentación clínica inicial estuvo centrada en el dolor abdominal y la fiebre, elementos semiológicos inespecíficos que se describen en la bibliografía como presentes en el 50% de los casos. La tríada clínica clásica de: fiebre, dolor en el hipocondrio derecho, e ictericia se presenta sólo en el 10%.
La ecografía y la TC facilitaron el diagnóstico previo a la exploración quirúrgica, siendo la primera la técnica más usada en estos casos, a pesar de que tiene menor sensibilidad (97% versus 100%) que la TC con contraste. Esta última, se prefiere evitar ya que es más cara, irradia y puede asociarse a complicaciones por la administración del contraste.
El tratamiento antibiótico prolongado se recomienda también en el caso de los abscesos hepáticos. Para lesiones solitarias con drenaje completo se sugiere un tratamiento de 4 a 6 semanas, y de 12 semanas para abscesos múltiples. En este caso se realizaron 6 semanas de tratamiento antibiótico.
En cuanto al tipo de drenaje, el más aceptado actualmente en el mundo es el percutáneo continuo por catéter durante 2 o 3 semanas, que es más efectivo, y evita los riesgos de la anestesia general, ya que se coloca en el lecho del absceso por vía transcutánea. En este caso, dado el compromiso peritoneal, se decide abordaje por laparotomía y lavado peritoneal.
En todos los casos se objetivó una elevación de los reactantes de fase aguda como se observa habitualmente en las infecciones de origen bacteriano. Los abscesos hepáticos se relacionan además, según la literatura, con anemia, elevación de las transaminasas y de la fosfatasa alcalina, elementos últimos que no se evidenciaron en esta paciente.
A pesar del comportamiento invasivo, en los cuatro casos los hemocultivos no tuvieron desarrollo, aislándose el agente en el cultivo del material del drenaje. Esto concuerda con la literatura que describe un bajo rendimiento de los hemocultivos, aislando el agente en sólo un tercio de los casos (9,10,12,20,27,30).
Las cepas de SAMR-AC aisladas en estos casos son sensibles a gentamicina, vancomicina y trimetroprim-sulfametoxazol, resistentes a ciprofloxacina y a todos los betalactámicos, teniendo en un caso resistencia inducible a la clindamicina, lo que marca el perfil de la clona UR6.
El tratamiento empírico inicial con clindamicina y/o vancomicina asociado eventualmente a gentamicina, es adecuado ante la sospecha de este agente.
En esta serie se evidenció la utilidad que tienen los estudios por imágenes en el diagnóstico de esta enfermedad permitiendo definir la topografía, la extensión del proceso y guiar el drenaje necesario para la confirmación microbiológica y la remoción terapéutica del material colectado.
Esta forma de presentación clínica de enfermedad por SAMR-AC es poco frecuente y requiere un alto grado de sospecha para garantizar un diagnóstico temprano y un tratamiento oportuno.
Referencias bibliográficas
1. Amorín MB, Castro M, Sandín D, Chamorrro F, Romero C, Giachetto G, et al. Infecciones invasivas por Staphylococccus aureus meticilino resistente adquirido en la comunidad. Presentación clínica y evolutiva observada en dos centros universitarios. Uruguay 2003-2007. Rev Med Urug 2008; 24(4):230-7.
2. Organización Panamericana de la Salud. Staphylococcus aureus meticilino resistente: informe. Ateneo general sobre Staphylococcus aureus meticilino resistente, 2004. Montevideo: OPS, 2004.
3. Galiana Villar A. Infección por Staphylococcus aureus meticilino-resistente adquirido en la comunidad. Arch Pediatr Urug 2003; 74(1):26-9.
4. Benoit SR, Estivariz C, Mogdasy C, Pedreira W, Galiana A, Galiana A, et al. Community Strains of Methicillin- Resistant Staphylococcus aureus as Potential Cause of Healthcare-associated Infections, Uruguay, 2002–2004. Emerg Infect Dis 2008; 14(8):1216-23.
5. Kaplan S, Hulten KG, Gonzalez BE, Hammerman WA, Lamberth L, Versalovic J, et al. Three–year surveillance of community –acquired Staphylococcus aureus infections in children. Clin Infect Dis 2005; 40(12):1785-91.
6. Saïd-Salim B, Mathema B, Kreiswirth B. Community-Acquired Methicillin-Resistant Staphylococcus aureus: An Emerging Pathogen. Infect Control Hosp Epidemiol. 2003; 24(6):451-5.
7. National Nosocomial Infections Surveillance System. National Nosocomial Infections Surveillance (NNIS) System Report, data summary from January 1992 through June 2004, issued October 2004. Am J Infect Control 2004; 32(8):470-85.
8. Health Protection Agency. BSOP 14: investigation of abscesses and deep-seated wound infections. London: HPA, 2009.
9. Pannaraj PS, Hulten KG, Gonzalez BE, Mason EO, Kaplan SL. Infective pyomyositis and myositis in children in the era of community-acquired, methicillin-resistant Staphylococcus aureus infection. Clin Infect Dis 2006; 43(8):953–60.
10. Gómez O, Arroyo A, Kaplan J, Dardanelli E, Goldberg A, Moguillansky S. Absceso de psoas en pediatría: cuadro clínico, diagnóstico por imágenes y tratamiento. Rev Arg Radiol 2004; 68(1):89-93.
11. Feigin RD, Cherry JD, Demmler GJ, Kaplan SL, eds. Textbook of pediatric infectious diseases. 5 ed. Philadelphia: Saunders, 2004:737–41.
12. García-Mata S, Hidalgo A, Esparza J. Piomiositis primaria del músculo psoas en clima templado: revisión a propósito de dos casos en niños seguidos a largo plazo. An Sist Sanit Navar 2006; 29(3):419-31.
13. Elliott DJ, Zaoutis T, Troxel A, Loh A, Keren R. Empiric antimicrobial therapy for pediatric skin and soft-tissue infections in the era of methicillin-resistant Staphylococcus aureus. Pediatrics 2009; 123(6):e959-66.
14. Duong M, Markwell S, Peter J, Barenkamp S. Randomized, controlled trial of antibiotics in the management of community-acquired skin abscesses in the pediatric patient. Ann Emerg Med 2010; 55(5):401-7.
15. Lo BM, Fickenscher BA. Primary pyomyositis caused by ca-MRSA. Int J Emerg Med 2008; 1(4):331-2.
16. Méndez Echevarría F, Baquero Artigao F, Velázquez Fragua R, García Ascaso MT, Merino Muñoz R, del Castillo Martín F. Piomiositis paravertebral resuelta con tratamiento antibiótico exclusivo. An Pediatr (Barc) 2004; 60(6):591-603.
17. Tauro LF, Kamath A, George C, Hegde BR, Nazareth E. Primary Pyomyositis of Paraspinal Muscles: A rare location. J Clin Diag Res 2008; 2(3):867-870.
18. Caillaud A, Lipsich J, Sierre S, Hernández C, Navia M, Gonzalez F; Hospital de Pediatría “Prof. Dr. J.P Garrahan”. Absceso de psoas. Buenos Aires: SAP, 2008.
19. Muñoz D, Gohurdett C. Absceso del psoas en la edad pediátrica. Caso clínico y revisión de la literatura. Revista ANACEM 2009; 3(1):34-5.
20. Taksande A, Vilhekar K, Gupta S. Primary pyomyositis in a child. Int J Infect Dis 2009; 13(4):e149-51.
21. Nikolopoulos DD, Apostolopoulos A, Polyzois I, Liarokapis S, Michos I. Obturator internus pyomyositis in a young adult: a case report and review of the literature. Cases J 2009; 2:8588.
22. Diefenbach K, Moss L. Intra-abdominal visceral and retroperitoneal abscesses. En: Long S, Pickering L, Prober C. Principles and Practice of Pediatric Infectious Disease. 3 ed. Churchill Livingston: Elsevier, 2008:429-33.
23. Ma XX, Galiana A, Pedreira W, Mowszowicz M, Christophersen I, Machiavello Set al. Community acquired Methicillin-resistant Staphylococcus aureus, Uruguay. Emerg Infect Dis 2005; 11(6):973-6.
24. Pedreira W, Anzalone L, Galiana A, Blanco JC, Seijas V, Andújar M. Infecciones de piel y partes blandas. Biomedicina 2006; 2(3):240-5.
25. Bonino A, Gnesetti A, Pujadas M, Broggi A. Infecciones por Staphylococcus aureus meticilino resistente adquirido en la comunidad: análisis de la población pediátrica asistida en el Hospital Policial de Uruguay, 2004. Arch Pediatr Urug 2007; 78(1):41-7.
26. Chambers HF. The changing epidemiology of Staphylococcus aureus. Emerg Infect Dis 2001; 7(2):178-82.
27. Olson D, Soares S, Kanade S. Community-Acquired MRSA Pyomyositis: Case Report and Review of the Literature. J Trop Med 2011; 2011:970848.
28. Hassan FO, Shannak A. Primary pyomyositis of the paraspinal muscles: a case report and literature review. Eur Spine J 2008; 17(2):S239-42.
29. Block AA, Marshall C, Ratcliffe A, Athan E. Staphylococcal pyomyositis in a temperate region: epidemiology and modern management. Med J Aust 2008; 189(6): 323-5.
30. Villamil-Cajoto I, Maceiras-Pan F, Villacián-Vicedo MJ. Piomiositis: presentación de 17 casos en niños y adultos. Rev Méd Chile 2006; 134(1):31-38.
Correspondencia: Dra. Patricia Dall´Orso.
Correo electrónico: padal@netgate.com.uy