Servicios Personalizados
Revista
Articulo
Links relacionados
Compartir
Archivos de Pediatría del Uruguay
versión impresa ISSN 0004-0584versión On-line ISSN 1688-1249
Arch. Pediatr. Urug. vol.82 no.3 Montevideo 2011
ARTÍCULO ORIGINAL
Arch Pediatr Urug 2011; 82(3)
Hipotermia en recién nacidos con asfixia perinatal
Fernando Silvera 1
1. Prof. Agdo. Neonatología del Hospital de Clínicas. Facultad de Medicina. Ex-Asistente Área Básica del departamento de Neonatología del Hospital de Clínicas. Facultad de Medicina.
Asociación Española Primera de Socorros Mutuos (AESPM).
Departamento de Neonatología del Hospital de Clínicas.
Fecha recibido: 12 de julio de 2011.
Fecha aprobado: 15 de noviembre de 2011.
Resumen
Se ha demostrado que la hipotermia controlada puede reducir la muerte o discapacidad grave, la mortalidad y los trastornos del neurodesarrollo en recién nacidos que han sufrido asfixia perinatal.
Con el objetivo de implementar la realización de hipotermia se analizó su aplicación en 10 recién nacidos de término que cumplieron con criterios de inclusión en dos centros neonatales de Montevideo en un período de dos años. Se alcanzó la temperatura objetivo (33,5°C) en las primeras 6 horas de vida de los pacientes y se mantuvo en ese rango durante 72 horas en 7/10 pacientes. En 8/10 pacientes se utilizó un gorro con agua fría circulante y en 2/10 placas de gel congelado para el enfriamiento encefálico directo y de todo el cuerpo en forma indirecta. Tres pacientes se retiraron del protocolo luego de 48 horas de hipotermia por alteraciones de la coagulación, bradicardia mantenida y paro cardiorrespiratorio, respectivamente. El recalentamiento se logró en todos los casos en seis horas sin alteraciones. El 60% de los pacientes presentaron convulsiones durante su internación y el 100% recibieron fenobarbital. En el grupo analizado se produjeron dos muertes, uno de ellos próximo a la supresión de la terapia y otro en la evolución alejada.
De manera complementaria se presentó la caracterización del impacto de la hipoxia severa y de la inducción de hipotermia sobre las variables más relevantes en un modelo de cerdo recién nacido.
Se concluye que el desarrollo de hipotermia controlada es una estrategia terapéutica posible y segura, que brinda una oportunidad a los pacientes que han sufrido asfixia perinatal.
Palabras clave:
ASFIXIA NEONATAL
HIPOTERMIA INDUCIDA
HIPOXIA-ISQUEMIA ENCEFÁLICA
RECIÉN NACIDO
Summary
Controlled hypothermia has been shown to reduce death or severe disability, mortality and neurodevelopment disorders in infants who have suffered perinatal asphyxia.
In order to implement the achievement of hypothermia the application was analyzed in 10 infants that met inclusion criteria in two medical centers in Montevideo. Target temperature (33,5°C) was reached within 6 hours of life of patients and was kept in that range for 72 hours in 7 / 10 patients. In 8/10 patients a cap with circulating cold water and 2/10 frozen gel plates were used for direct brain cooling and whole body. Three patients withdrew from the protocol after 48 hours of hypothermia due to clotting problems, severe bradycardia and cardiorespiratory arrest respectively. The warming was achieved in all cases within six hours. 60% of patients had seizures during hospitalization and 100% received phenobarbital. In the study group two patients died.
In addition a newborn pig model shows the impact of severe hypoxia and induction of hypothermia on the most relevant variables.
We conclude that the development of controlled hypothermia is a feasible and safe therapeutic strategy that provides an opportunity for patients who have suffered perinatal asphyxia.
Key words:
ASPHYXIA NEONATORUM
HYPOTHERMIA, INDUCED
HYPOXIA-ISCHEMIA, BRAIN
INFANT, NEWBORN
Introducción
La encefalopatía hipóxico-isquémica (EHI) causada por un aporte insuficiente de oxígeno y/o sangre, se presenta con una incidencia que varía según los centros, pudiendo alcanzar 2 a 4 cada 1.000 nacidos vivos mayores de 37 semanas de edad gestacional. Contribuye de manera significativa a la mortalidad (20% a 50% de los recién nacidos con EHI mueren en el primer mes de vida) y morbilidad neonatal, incluyendo alteraciones del neurodesarrollo a largo plazo por encima del 25% a 60% (1,2).
Esta incidencia puede ser aún mayor en los países con menores recursos asistenciales. En Uruguay se detectó una prevalencia de 2,12% en el Centro Hospitalario Pereira Rossell en el año 2005 (3). En el año 2009 fue el determinante de 19% de todas las muertes en el período neonatal en este servicio de neonatología.
El tratamiento del recién nacido con asfixia perinatal se ha limitado a los cuidados intensivos de sostén hemodinámico, respiratorio y metabólico así como al tratamiento de convulsiones, monitorizando la disfunción multiorgánica ocurrida. Esta estrategia terapéutica no actúa eficazmente en la injuria hipóxico-isquémica cerebral dado que no se contrapone a la secuencia fisiopatológica de la enfermedad (4).
La hipotermia controlada ha sido propuesta como una intervención terapéutica para reducir la injuria neuronal secundaria. Estudios experimentales en animales recién nacidos han mostrado que la reducción en la temperatura central entre 2 y 5ºC puede disminuir la evidencia histológica de lesión cerebral y la falla energética secundaria, estudios pilotos en humanos sugieren que la hipotermia moderada (33 a 34ºC) puede reducir las secuelas neurológicas de la hipoxia isquemia sin efectos adversos mayores (5,6). Estudios multicéntricos controlados (7-10) realizados en la última década, y revisiones sistemáticas independientes (11,12) han mostrado que en niños con encefalopatía moderada a severa, la hipotermia controlada determina una reducción significativa en la evolución combinada de muerte y alteración del neurodesarrollo mayor a los 18 meses de vida, además de una reducción de la mortalidad. En este contexto la recomendación de los expertos ha sido adherirse estrictamente a protocolos disponibles que se han desarrollado para llevar adelante estudios multicéntricos (13).
El objetivo de este estudio es demostrar que la hipotermia controlada es una metodología que aplicable a nivel nacional en recién nacidos afectados de asfixia perinatal y aportar observaciones en un modelo animal de hipoxia severa que muestran la seguridad de la terapia en el período de inducción.
Material y método
Hipotermia controlada en pacientes
El protocolo se realizó tomando como base estudios controlados realizados a nivel internacional (7,14). Luego de obtenido el consentimiento de los familiares se incluyó de manera prospectiva a los recién nacidos con edad gestacional ³ a las 35 semanas, que cumplieron con más de uno de los siguientes criterios: score de Apgar £ a 5 al 5º minuto de vida; necesidad de reanimación incluyendo intubación endotraqueal o ventilación con máscara a los 10 minutos de vida; pH de arteria de cordón umbilical < 7.00 o pH de arteria periférica o capilar < 7.00 en los primeros 60 minutos de vida; y que además presentaron signos neurológicos (encefalopatía hipóxico-isquémica), tales como alteraciones del estado de conciencia (letargia, estupor o coma) y al menos uno de los signos siguientes: hipotonía, reflejos anormales incluyendo oculomotores y pupilares, succión ausente o pobre, convulsiones clínicas.
No se incluyeron aquellos pacientes con anormalidades congénitas mayores detectables en las primeras 6 horas de vida.
Una vez arribado a la unidad se procedió a la estabilización cardiorrespiratoria y hemodinámica del paciente. Se inició tempranamente la monitorización completa a través del registro continuo de presión arterial invasiva (PAI), electrocardiograma (ECG), saturometría de pulso, así como de las variables metabólicas: gasometría arterial, ionograma y glicemia.
Desde el ingreso del paciente se retiró la fuente de calor como medida preventiva para evitar hipertermia, una vez confirmado que cumplía los criterios de inclusión se colocó termómetro a nivel del tercio distal del esófago, cuya posición se confirmó mediante radiografía de tórax. Iniciándose desde ya el registro controlado de la temperatura.
Se colocaron, además, dos termómetros accesorios a nivel rectal, a 3 cm de la margen anal, y termómetro cutáneo en zona libre de piel a los efectos de caracterizar y confirmar la temperatura en forma completa en cada paciente.
El equipo de enfriamiento utilizado en 8 de los 10 pacientes fue Blanketroll ® (Cincinati SubZero) que permitió a la vez el control manual de la temperatura del agua y de la temperatura del paciente para mantenerla en el rango deseado ya que el termómetro esofágico despliega los datos en el mismo. En estos pacientes se colocó en la cabeza una gorra confeccionada de tubos siliconados por la cual circuló agua (figura 1 A), inicialmente a 10ºC, una vez lograda la temperatura objetivo de 33,5ºC, se ajustó para mantenerla en un rango de 1ºC (33 a 34ºC) por 72 horas.
En dos de 10 pacientes se utilizó como método de enfriamiento la colocación, previa protección del cuero cabelludo, de placas de gel congelado en la proximidad de las regiones témporo-parietales del paciente (figura 1B), al no contarse con equipo Blanketroll. También el objetivo fue alcanzar 33,5ºC y mantenerse en un rango de variabilidad no mayor a 0,5ºC por 72 horas, para esto se aproximó o retiró frío durante este periodo.
El protocolo no incluyó la administración de inotrópicos, sedantes o anticomiciales de manera obligatoria y los mismos se realizaron de acuerdo a las necesidades de los pacientes.
Una vez completadas las 72 horas se procedió al recalentamiento de los pacientes siendo el objetivo el aumento de 0,5ºC por hora hasta alcanzar la temperatura normal.
La discontinuación de la terapia se realizó sólo si a criterio del equipo médico la continuidad del enfriamiento significó un riesgo mayor para el paciente de acuerdo con las complicaciones que se presentaron.
Dentro de la valoración inicial se incluyó en todos los pacientes valoración infecciosa y fueron tratados con antibióticos hasta el resultado de los cultivos.
En las primeras 24 horas de vida se solicitó ecografía transfontanelar (ETF) para descartar hemorragia intraventricular o malformaciones cerebrales.
Se solicitó en todos los casos EEG en las primeras 48 horas de vida.
Hipotermia en modelo de cerdo recién nacido
Con el objetivo de reproducir las consecuencias de la hipoxia isquemia y su evolución durante la inducción de hipotermia controlada se desarrolló en el laboratorio del Área Básica de Neonatología del Hospital de Clínicas un modelo experimental animal a tales efectos.
En cerdo recién nacido, anestesiado y traqueotomizado, en asistencia ventilatoria mecánica, se cateterizó arteria femoral, pulmonar y vena yugular. Basados en estudios experimentales de hipoxia isquemia en cerdos recién nacidos (15) que demostraron lesión cerebral anatomopatológica se llevó a cabo el siguiente protocolo. Una vez estabilizado se descendió la fracción inspirada de O2 (FiO2) de manera controlada hasta alcanzar 8%, manteniéndose en esta situación hasta que el registro concomitante de la amplitud integrada (aEEG) por monitoreo de función cerebral (MFC) (Olympic CFM ® 6000) mostró un descenso por debajo de 5 µv durante al menos 10 minutos. Se realizaron maniobras de reanimación que constaron básicamente en la reoxigenación con FiO2 1 y masaje cardíaco, cuando la presión arterial sistémica cayó por debajo de 30 mmHg.
Posteriormente, y luego de la estabilización del modelo, se inició el descenso progresivo de la temperatura, mediante la aproximación de placas de gel congelado en la región parietal y frontal de la cabeza cuya piel se protegió para evitar lesiones por contacto. Concomitantemente se suprimió el aporte de calor al resto del cuerpo. La temperatura central se controló a nivel esofágico. Al cabo de 30 minutos se alcanzó una diferencia de –4°C con la temperatura considerada basal para cerdos recién nacidos (38,5 a 39°C). De esta manera se logró inducir hipotermia de la cabeza y corporal total que ha mostrado ser efectiva como estrategia de neuroprotección (16). Se controlaron variables hemodinámicas (frecuencia cardíaca, presión arterial sistémica y pulmonar), saturometría de pulso (SpO2) y MFC.
Resultados
En un período de dos años 10 pacientes cumplieron con los criterios de inclusión en una institución de asistencia médica colectiva de Montevideo y en la maternidad del Hospital de Clínicas, cuyas características se muestran en la tabla 1. Se incluyen eventos prenatales centinelas, la vía de parto en la que se destaca la cesárea de urgencia como vía de parto más común. Los pacientes nacieron al término de la gestación (edad gestacional promedio fue de 39 semanas (± 1,6) semanas) y fueron adecuados a la edad gestacional ya que solo uno de los pacientes presentó un peso por encima de los 2 DS para su edad gestacional.
Todos los pacientes requirieron reanimación con intubación orotraqueal y ventilación manual con aporte de O2 al 100%, necesitando la continuidad de la asistencia ventilatoria mecánica. El examen clínico inicial en todos se mostró alterado con signos neurológicos de encefalopatía hipóxico-isquémica dentro de los que se destacan necesidad de asistencia ventilatoria mecánica al ingreso, pérdida de reflejos de succión, hipotonía marcada y coma.
El procedimiento se inició en todos los casos dentro de las primeras 6 horas de vida.
La temperatura central se mantuvo dentro del rango de temperatura deseado, aunque la evolución muestra una mayor variabilidad en las primeras 2 a 3 horas, entre las 27 y 34 horas y entre las 69 y 72 horas del inicio del enfriamiento (figura 2A). El 80% de los registros de temperatura central de los pacientes estudiados se encontró en el rango de ± 0,5°C de a temperatura objetivo de 33,5°C (figura 2B).
El procedimiento completó 72 horas en 7 de los 10 pacientes. Uno de ellos se retiró a las 6 horas del inicio por trastorno de la crasis sanguínea con sangrado pulmonar e hipertensión pulmonar mantenida, el segundo paciente se retiró a las 48 horas de iniciado el enfriamiento por bradicardia sinusal mantenida y en otro paciente se suspendió a las 55 horas por paro cardiorrespiratorio (PCR) de causa no aclarada retirándose hipotermia inmediatamente luego de la reanimación completa.El recalentamiento se llevó a cabo en 6 horas de manera progresiva y lenta, aun cuando el enfriamiento no completó las 72 horas programadas. No se detectaron incidentes en ninguno de los casos (figura 3).
De los controles hemodinámicos realizados se destaca la estabilidad de la frecuencia cardiaca (FC) en un rango de normalidad para los valores promedio. La presión arterial sistémica media (PAM) muestra el menor valor promedio hacia las 19 horas de iniciado el proceso (PAM 41 mmHg ± 14) (figura 3). Durante el recalentamiento la FC aumentó de manera significativa hacia el final del mismo (FC inicio de calentamiento 124 ± 19 vs FC final de calentamiento 154 ± 20; p=0,04), la PAM se mantuvo próximo a los valores previos al inicio (figura 4).
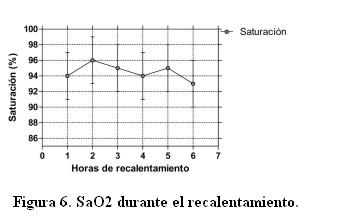
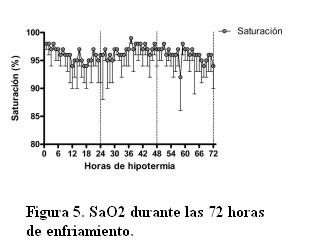
El tiempo de asistencia ventilatoria mecánica (AVM) fue muy variable, pacientes que sólo requirieron 12 horas y pacientes que requirieron durante toda su estadía no pudiéndose retirar el soporte dada la gravedad de la afección (> 72 h de AVM). La saturación promedio se mantuvo por encima de 90% durante todo el periodo de enfriamiento y recalentamiento (figuras 5 y 6).
 En 6/10 de los pacientes incluidos en este estudio se diagnosticaron convulsiones clínicas, de éstos cuatro presentaron diagnóstico electroencefalográfico de crisis convulsivas durante la internación y un quinto paciente presentó crisis convulsivas con diagnóstico de epilepsia de difícil tratamiento luego de otorgada el alta del servicio (cuyos EEG iníciales fueron normales).
En 6/10 de los pacientes incluidos en este estudio se diagnosticaron convulsiones clínicas, de éstos cuatro presentaron diagnóstico electroencefalográfico de crisis convulsivas durante la internación y un quinto paciente presentó crisis convulsivas con diagnóstico de epilepsia de difícil tratamiento luego de otorgada el alta del servicio (cuyos EEG iníciales fueron normales). Al 100% de los pacientes se administró fenobarbital en algún momento de su internación, 60% como tratamiento de crisis convulsivas y 40% en la primera hora de vida como coadyuvante del tratamiento de sostén (dosis única de 40 mg/kg administrada en una hora).
No se observaron otros efectos adversos que los descriptos como causales de supresión de la terapia. Se utilizó soporte inotrópico en la totalidad de los pacientes que recibieron hipotermia.
Se realizaron estudios imagenológicos como valoración de la repercusión encefálica, en todos se realizaron ecografías transfontanelares seriadas que invariablemente mostraron signos indirectos de edema cerebral; en cinco pacientes se realizó tomografía axial computada previo al egreso, en todos los casos elementos de atrofia cerebral difusa; en un paciente se realizó resonancia magnética siendo el resultado normal.
De esta serie de pacientes, a la fecha fallecieron tres de ellos, uno inmediatamente luego de suspendido el enfriamiento y dos en la evolución alejada (19 y 24 meses) por causas vinculadas a su asfixia perinatal.
Modelo animal
La amplitud se mantuvo en rango normal (límite superior del trazado > 10µv y límite inferior del trazado < 5µV) en los primeros minutos de hipoxia, luego descendió bruscamente, mostrando afectación severa con supresión marcada (límite superior e inferior del trazado < 5µv) que coincidió con la repercusión hemodinámica de la hipoxia traduciendo la claudicación de los mecanismos compensatorios. Esta supresión de la amplitud se mantuvo durante la reanimación y luego durante todo el período de hipotermia observado (figura 7).
Durante la inducción de la hipotermia controlada en el modelo animal se observaron cambios que no alteraron la situación hemodinámica global tales como el descenso de la frecuencia cardíaca (169 lpm a 145 lpm), y el aumento transitorio de la presión arterial sistémica sistólica para volver a valores iniciales (83 mmHg a 76 mmHg) , sin que se constataran cambios significativos en la saturación o en los valores de presión arterial pulmonar sistólica (42 mmHg a 46 mmHg) al alcanzar la temperatura central objetivo de 34 a 35°c (-4°C por debajo de la temperatura basal) (figura 8).
Discusión
La asfixia perinatal es uno de los procesos patológicos más devastadores en esta etapa de la vida y sigue siendo una importante causa de muerte y de secuelas permanentes. Son muy pocas las intervenciones terapéuticas que tienen impacto sobre la evolución de la encefalopatía hipóxico-isquémica y el daño multiorgánico, en general limitado a medidas de sostén.
Este trabajo es el primero en mostrar que la hipotermia controlada durante 72 horas en recién nacido de término es una estrategia terapéutica realizable en nuestro medio.
Los criterios de inclusión fueron modificados de acuerdo a las condiciones de los pacientes admitidos con diagnóstico de encefalopatía hipóxico-isquémica en nuestro medio, en el protocolo original se requería un score de apgar menor de 5 al 10º minuto lo cual fue cambiado por un score menor de 5 al 5º minuto con el objetivo de aumentar el número de pacientes a tratar. Por otra parte en el estudio TOBY se incluía la necesidad de la realización de un EEG de amplitud integrada (EEGa) o monitoreo de la función cerebral lo cual no fue posible realizar al no contar con el equipo en el momento de la inclusión de pacientes.
El desarrollo de la terapia así como los controles clínicos y paraclínicos se apegaron de manera estricta al mismo como mecanismo de control en su realización.
La temperatura central al ingreso a la unidad de cuidados intensivos en la mayoría de los casos se situó por debajo de 36,5°C, la supresión de fuentes de calor coloca al paciente en hipotermia pasiva lo cual favorece el inicio temprano de la terapia y la eficacia de la misma. Esta conducta requiere del control temprano de la temperatura central puesto que en estudios realizados se ha constatado sobreenfriamiento (temperaturas < 33°C) en pacientes en hipotermia pasiva (17).
Se eligió como método de inducción y mantenimiento de la hipotermia el enfriamiento selectivo de la cabeza con enfriamiento moderado de todo el cuerpo en forma pasiva(7), tanto para los que se enfriaron mediante gorro de agua circulante como en los que se aplicó placas de hielo.
La temperatura objetivo de 33,5ºC se alcanzó sin problemas en el plazo de las primeras 6 horas de vida y pudo mantenerse de manera estable en el rango de seguridad, 80% de todos los registros de temperatura central en el rango de ± 0,5°C y 92% en el rango de ± 1°C de la temperatura objetivo de 33,5°C así lo demuestran. Sin necesidad de suspender el enfriamiento por este motivo. Este es un hecho muy importante puesto que de esta estabilidad depende el éxito de la terapia, requiere de personal de enfermería que controle de manera estricta la evolución de la temperatura, evitando cambios bruscos y mayores a (±) 0,5ºC por hora.
Los resultados muestran la estabilidad cardiorrespiratoria durante el procedimiento. Los requerimientos de AVM fueron variables no quedando vinculadas de manera directa al periodo de hipotermia sino a la situación clínica del paciente. En algún caso fue posible la extubación a las 12 horas de vida lo cual muestra la buena tolerancia y que la hipotermia no requiere de AVM como requisito para su realización. Éste es un dato importante para evitar complicaciones secundarias a AVM entre las que se destaca el riesgo de hiperventilación e hipocapnia luego de la estabilización ventilatoria de los pacientes.
La hipertensión pulmonar secundaria es una complicación frecuente de la asfixia perinatal, en estudios experimentales se ha demostrado un aumento de las resistencias vasculares pulmonares en presencia de hipotermia moderada o profunda (18). En ningún caso de los aquí estudiados se presentaron complicaciones con la oxigenación durante el enfriamiento o el recalentamiento, recomendándose el control del índice de oxigenación o del incremento de los requerimientos de FiO2 en forma periódica, en caso de ser necesario puede utilizarse oxido nítrico inhalado (ONi) como terapia vasodilatadora pulmonar mientras se completa el período de enfriamiento sin necesidad de interrupción del mismo y se debe ser cauteloso en el inicio del enfriamiento si los requerimientos de O2 son mayores al 0,50 de FiO2 (19).
El descenso de la temperatura corporal se asocia a cambios cardiocirculatorios, dentro de los que se destacan la disminución del gasto cardíaco global lo cual puede verse exacerbado por disfunción miocárdica hipoxia luego del agravio hipóxico-isquémico (20). En este estudio por indicación médica, y no por la inclusión en el protocolo de hipotermia todos los pacientes recibieron soporte inotrópico, en este contexto se pudo observar la estabilidad hemodinámica de la mayoría de ellos. Hipotermia controlada como procedimiento no requiere de la administración de inotrópicos o del aporte extra de volumen, pero se ha observado una retirada mucho más lenta de los mismos una vez iniciados en los pacientes que han padecidos asfixia (21).
En estudios previos se ha mostrado el descenso de la frecuencia cardíaca durante el enfriamiento (19) con recuperación de la misma luego del calentamiento lo cual también se ha confirmado en este grupo de pacientes.
Sin embargo, uno de los pacientes se retiró del protocolo por bradicardia sinusal mantenida, no se encontró ninguna causa determinante de dicha situación y el equipo tratante optó por suspender el enfriamiento con lo cual la situación se revirtió. Una de las causas citadas como causales es la prolongación del intervalo QT, que en este paciente no se confirmó, de todas formas debe tenerse en cuenta la realización de ECG para descartarla siempre que la frecuencia cardíaca sea menor de 70 lpm (22).
Uno de los pacientes en el transcurso del enfriamiento presentó PCR de causa no aclarada, descartándose hipotermia profunda como etiología del mismo, el equipo asistencial optó por la suspensión de la terapia de neuroprotección luego de la recuperación, lográndose la estabilidad con buena evolución posterior.
Uno de los argumentos para el recalentamiento lento es que la restauración de la temperatura corporal se acompaña de vasodilatación sistémica la cual si se da de manera repentina puede determinar hipotensión lo cual no se observó en este grupo de pacientes (19). Es de destacar que aun en los casos en que se decidió la suspensión de la terapia antes de las 72 horas, el recalentamiento se realizó de manera progresiva.
En este grupo de pacientes no se reportaron complicaciones metabólicas aunque se deben controlar de manera seriada, siendo muy importante la estabilidad de la glicemia así como del sodio, el potasio, el calcio, el magnesio frecuentemente alterados como complicación secundaria de la repercusión multiorgánica de la asfixia perinatal y exacerbada o alterada por el enfriamiento llevado a cabo.
Numerosos trabajos muestran que la hipotermia controlada no aumenta la incidencia de hemorragia durante el procedimiento aunque es bien conocido los efectos sobre el sistema de coagulación (10,23-25). En este estudio uno de los pacientes presentó sangrado clínico significativo que se inició durante el período de enfriamiento con alteraciones de la crasis sanguínea que obligaron a la utilización de plasma fresco y vitamina K como tratamiento. El agravamiento del sangrado clínico obligó a la suspensión progresiva de la terapia, persistiendo luego de lograda la temperatura corporal normal. Todo esto remarca la importancia del control periódico del estado de coagulación.
Las convulsiones son un marcador tardío y fidedigno de la gravedad de la encefalopatía hipóxico-isquémica, también queda en evidencia en los pacientes estudiados ya que el 60% las presentaron. En este caso el diagnóstico clínico se corroboró con el EEG en la mayoría de ellos.
El fenobarbital es el anticomicial de primera elección en el tratamiento de las convulsiones neonatales. Su indicación como neuroprotector con reducción de la incidencia de muerte o alteraciones del neurodesarrollo sólo se demostró en un estudio randomizado pequeño (26), actualmente no se recomienda su uso de manera sistemática en recién nacidos con asfixia perinatal ante la falta de estudios con calidad metodológica y tamaño adecuados (27), tomando en cuenta, además, que es una droga no exenta de efectos secundarios en el desarrollo del sistema nervioso central. De todas maneras aún queda por establecer el posible efecto benéfico cuando se agrega durante la hipotermia controlada como se ha observado en estudios animales recientes (28).
El correcto desarrollo del protocolo depende del personal de enfermería, en su apego al mismo así como en la habilidad para mantener y controlar la temperatura central del paciente. Es indispensable una unidad de enfermería “al lado” del paciente, lo cual queda de manifiesto en el número de controles por paciente, que alcanza un mínimo 400 durante las 72 horas y las 6 de recalentamiento que lleva el procedimiento en su totalidad. Esto puede considerarse un efecto benéfico colateral ya que determina una mayor rigurosidad en el control de los pacientes que son sometidos a esta terapia de neuroprotección.
Para alcanzar el efecto protector deseado es importante la profundidad, la estabilidad y la duración del enfriamiento, en este grupo los dos primeros objetivos se lograron sin inconvenientes en todos los casos, pero no completaron las 72 horas 3/10 pacientes. Si bien los motivos y las circunstancias de suspensión del tratamiento deben ser objeto de análisis por el equipo tratante, dos pacientes alcanzaron las 48 horas de hipotermia lo cual no es despreciable puesto que hay estudios que han mostrado reducción de la mortalidad y de alteraciones motoras con este período de enfriamiento (9).
Actualmente se cuenta con la posibilidad de monitorizar la función cerebral (MFC) de manera continua al lado de la cama del paciente mediante EEGa. Básicamente este equipo registra un EEG de canal único desde electrodos parietales o frontales, siendo la señal obtenida filtrada, rectificada, suavizada con integración de la amplitud. La interpretación de los resultados se basa en el reconocimiento de una franja o registro de fondo de amplitud patrón (4). La alteración moderada o severa del EEGa se ha utilizado en varios estudios como uno de los criterios de inclusión para el inicio de hipotermia. En las primeras 6 horas de vida ha mostrado ser el mejor predictor individual de la evolución neurológica en pacientes normotérmicos con encefalopatía hipóxico-isquémica (29), también se ha postulado para valoración y diagnóstico de convulsiones clínicas y subclínicas mostrando ser sensible pero dependiente del técnico que interprete los resultados, por lo que se recomienda la complementación con EEG convencional (30). El modelo animal permitió observar el comportamiento de la actividad eléctrica cerebral a través del registro de EEGa desde el inicio del evento hipóxico hasta su resolución pasando por el periodo de reanimación y establecimiento de la hipotermia controlada (figura 7). La inducción de la hipotermia en este modelo de injuria hipóxica grave no generó inestabilidad hemodinámica ni respiratoria siendo bien tolerada, así como tampoco modificó el patrón de amplitud de afectación severa previamente establecido.
De manera complementaria en la figura 9 se muestran registros de MFC en momentos evolutivos diferentes, en pacientes con asfixia perinatal no incluidos en el estudio presentado. En el paciente 1 de un registro de depresión severa de la amplitud evolucionando a un registro de afectación moderada a las 48 horas de vida permaneciendo con características muy similares a la semana de vida. En el paciente 2 se observa depresión severa de la amplitud con convulsiones en el primer minuto de vida, evolucionando a un registro de afectación moderada a las 48 horas y un patrón típicamente normal a los 10 días de vida. En el paciente 3 se observa un registro de “dientes de sierra” que traduce convulsiones mantenidas sin depresión de la amplitud, a las 48 horas evoluciona a un registro de afectación moderada con convulsiones aisladas y a los 15 días de vida el registro tiene un patrón de amplitud en límites normales.
ConclusionesEn el grupo de pacientes estudiados se realizó hipotermia controlada con temperatura objetivo en 33,5ºC que se logró mantener estable por el periodo establecido de 72 horas en el 70% de los casos. Se realizó hipotermia cefálica moderada con enfriamiento corporal pasivo siendo los eventos secundarios más destacables los trastornos de la crasis sanguínea y hemodinámicas, aunque no es posible atribuirlos exclusivamente a la terapia realizada.
Es posible concluir que la neuroprotección activa mediante hipotermia sumado a las medidas de sostén, apegándose a un protocolo previamente avalado, es una opción terapéutica en los pacientes que han sufrido asfixia perinatal y encefalopatía hipóxico-isquémica.
Agradecimientos
Al Prof. Dr. Miguel Martell quien impulsó el desarrollo e implementación de la hipotermia en este país participando en la asistencia de estos pacientes.
A la Prof. Adj. Dra. Fernanda Blasina por su colaboración en la corrección de este trabajo.
A los Dres. M. Costa, M. Hermida, A. Mele, M. Viña, E. Mayans, R. Kesishian, E. Di Lucci y al Prof. Dr. G. Giambruno por su participación en la asistencia y colaboración en los registros de los pacientes estudiados.
A los Dres. S. Tellechea, P. Bolioli, M. Moraes, R. Ruffo y M. Soma; a la Bioq. L. Vaamonde y al Aux. José Barreto del Área Básica del Departamento de Neonatología del Hospital de Clínicas por su participación en el modelo animal.
Al equipo de enfermería de la unidad neonatal de AESPM y del Departamento de Neonatología del Hospital de Clínicas.
Referencias bibliográficas
1. Vannucci SJ, Hagberg H. Hypoxia-ischemia in the immature brain. J Exp Biol. 2004; 207(Pt 18): 3149-54.
2. Robertson CM, Finer NN, Grace MG. School performance of survivors of neonatal encephalopathy associated with birth asphyxia at term. J Pediatr 1989; 114(5): 753-60.
3. Nozar F, Fiol V, Briozzo L. Análisis de la prevalencia de sufrimiento fetal agudo y síndrome hipoóxico-isquémico en la maternidad del Centro Hospitalario Pereira Rossell. Arch Gin Obstet 2005; 43(1): 45-9.
4. Sankaran S. Neonatal Encephalopathy: Treatment with hypothermia. NeoReviews 2010; 11: e85-e92.
5. Thoresen M, Penrice J, Lorek A, Cady EB, Wylezinska M, Kirkbride V, et al. Mild hypothermia after severe transient hypoxia-ischemia ameliorates delayed cerebral energy failure in the newborn piglet. Pediatr Res 1995; 37(5): 667-70.
6. Gunn AJ, Gunn TR, de Haan HH, Williams CE, Gluckman PD. Dramatic neuronal rescue with prolonged selective head cooling after ischemia in fetal lambs. J Clin Invest 1997; 99(2): 248-56.
7. Gluckman PD, Wyatt JS, Azzopardi D, Ballard R, Edwards AD, Ferriero DM, et al. Selective head cooling with mild systemic hypothermia after neonatal encephalopathy: multicentre randomised trial. Lancet 2005; 365(9460): 663-70.
8. Shankaran S, Laptook AR, Ehrenkranz RA, Tyson JE, McDonald SA, Donovan EF, et al. Whole-body hypothermia for neonates with hypoxic-ischemic encephalopathy. N Engl J Med 2005; 353(15): 1574-84.
9. Eicher DJ, Wagner CL, Katikaneni LP, Hulsey TC, Bass WT, Kaufman DA, et al. Moderate hypothermia in neonatal encephalopathy: safety outcomes. Pediatr Neurol 2005; 32(1): 18-24.
10. Azzopardi DV, Strohm B, Edwards AD, Dyet L, Halliday HL, Juszczak E, et al. Moderate hypothermia to treat perinatal asphyxial encephalopathy. N Engl J Med 2009; 361(14): 1349-58.
11. Schulzke SM, Rao S, Patole SK. A systematic review of cooling for neuroprotection in neonates with hypoxic ischemic encephalopathy - are we there yet? BMC Pediatr 2007; 7: 30.
12. Jacobs S, Hunt R, Tarnow-Mordi W, Inder T, Davis P. Cooling for newborns with hypoxic ischaemic encephalopathy. Cochrane Database Syst Rev 2007, issue 4. Disponible en: http://cochrane.bvsalud.org [consulta: 20 ene. 2011].
13. Azzopardi D, Edwards AD. Hypothermia.Semin Fetal Neonatal Med 2007; 12(4): 303-10.
14. Azzopardi D, Brocklehurst P, Edwards D, Halliday H, Levene M, Thorensen M, et al. The TOBY Study. Whole body hypothermia for the treatment of perinatal asphyxial encephalopathy: a randomized controlled trial. BMC Pediatr 2008; 8: 17.
15. Björkman ST, Foster KA, O’driscoll SM, Healy GN, Lingwood BE, Burke C, et al. Hypoxic/Ischemic models in newborn piglet: comparison of constant FiO2 versus variable FiO2 delivery. Brain Res 2006; 1100(1): 110-7.
16. Tooley JR, Satas S, Porter H, Silver IA, Thoresen M. Head cooling with mild systemic hypothermia in anesthetized piglets is neuroprotective. Ann Neurol 2003; 53(1): 65-72.
17. Robertson N, Kendall GS, Thayyil S. Techniques for therapeutic hypothermia during transport and in hospital for perinatal asphyxial encephaloptahy. Semin Fetal Neonatal Med 2010; 15: 276-86.
18. Benumof JL, Wahrenbrock EA. Dependency of hypoxic pulmonary vasoconstriction on temperature. J Appl Physiol 1977; 42: 56–8.
19. Thoresen M, Whitelaw A. Cardiovascular changes during mild therapeutic hypothermia and rewarming in infants with hypoxic-ischemic encephalopathy. Pediatrics 2000; 106(1 Pt 1): 92-9.
20. Gebauer CM, Knuepfer M, Robel-Tillig E, Pulzer F, Vogtmann C. Hemodynamics among neonates with hypoxic-ischemic encephalopathy during whole-body hypothermia and passive rewarming. Pediatrics. 2006; 117(3): 843-50.
21. Battin MR, Thoresen M, Robinson E, Polin RA, Edwards AD, Gunn AJ, et al. Does head cooling with mild systemic hypothermia affect requirement for blood pressure support? Pediatrics 2009; 123(3): 1031-6.
22. Battin MR, Penrice J, Gunn TR, Gunn AJ. Treatment of term infants with head cooling and mild systemic hypothermia (35.0°C and 34.5°C) after perinatal asphyxia. Pediatrics 2003; 111: 244-251.
23. Thorensen M. Supportive Care During Neuroprotective Hypothermia in the term Newborn: Adverse effects and Their Prevention. Clin Perinatol 2008; 35: 749-63.
24. Glass HC, Ferriero DM. Curr Treat Options Neurol 2007; 9(6): 414-23.
25. Gunn AJ, Gluckman PD. Hypothermia: an evolving treatment for neonatal hypoxic ischemic encephalopathy. Pediatrics 2008; 121: 648-9.
26. Hall RT, Hall FK, Daily DK. High-dose phenobarbital therapy in term newborn infants with severe perinatal asphyxia: a randomized, prospective study with three-year follow-up. J Pediatr 1998; 132(2): 345-8.
27. Evans DJ, Levene M, Tsakmakis M. Anticonvulsants for preventing mortality and morbidity in full term newborns with perinatal asphyxia. Cochrane Database Syst Rev 2007; issue 3. Obtenido de: http://cochrane.bvsalud.org [consulta: 20 ene.2011].
28. Barks JD, Liu YQ, Shangguan Y, Silverstein FS. Phenobarbital augments hypothermic neuroprotection. Pediatr Res. 2010 May;67(5):532-7.
29. Hellstrom-Westas L, Rosen I, Svenningsen NW. Predictive value of early continuous amplitude-integrated EEG recordings on outcome after severe birth asphyxia in full-term infants. Arch Dis Child Fetal Neonatal Ed 1995; 72: F34-8.
30. Frenkel N, Friget M, Meledin I, Berger I, Marks K, Bassan H, et al. Neonatal seizure recognition - Comparative study of continuous-amplitude integrated EEG versus short conventional EEG recordings. Clin Neurophysiol 2011; 122(6):1091-7.
Correspondencia: Dr. Fernando Silvera.
Dirección: Avenida Rivera 2810 Apto. 501. Montevideo, Uruguay
Correo electrónico: silverafernando5@gmail.com