Services on Demand
Journal
Article
Related links
Share
Archivos de Pediatría del Uruguay
On-line version ISSN 1688-1249
Arch. Pediatr. Urug. vol.79 no.3 Montevideo Sept. 2008
CASO CLÍNICO
Arch Pediatr Urug 2008; 79(3)
Síndrome de Stevens Johnson:
una enfermedad habitualmente producida por medicamentos
Dres. Héctor Telechea 1, Noelia Speranza 1, Gustavo Giachetto 2, María Catalina Pírez 3
1. Residente de Pediatría, Asistente Departamento de Farmacología y Terapéutica.
2. Prof. Agregado Clínica Pediátrica, Prof. Agregado Departamento de Farmacología y Terapéutica.
3. Prof. Clínica Pediátrica, Directora Clínica Pediátrica “A”.
Clínica Pediátrica “A”, Departamento de Pediatría, Facultad de Medicina, Universidad de la República.
Fecha recibido: 23 de mayo de 2008.
Fecha aprobado: 29 de octubre de 2008.
Resumen
El síndrome de Stevens Johnson, forma menor de la necrosis epidérmica tóxica, es una enfermedad grave, típicamente secundaria a medicamentos. Se describe el caso de un niño de 4 años que presentó un síndrome de Stevens Johnson con un compromiso cutáneo de 15%, probablemente secundario a carbamacepina. Establecer la relación causal entre un medicamento y un evento adverso exige un alto índice de sospecha y conocer la importancia de la patología inducida por medicamentos en la práctica clínica. La notificación de las sospechas de reacciones adversas a medicamentos es la herramienta fundamental para detectar señales de alerta sobre la seguridad de los mismos. Esta comunicación tiene como objetivos sensibilizar a los pediatras sobre la importancia y potencial gravedad de la patología inducida por medicamentos y revisar la conducta terapéutica frente al SSJ, una de las reacciones adversas graves más frecuentes.
Palabras clave:
SÍNDROME DE STEVENS-JOHNSON
PREPARACIONES FARMACÉUTICAS-efectos adversos
VIGILANCIA DE PRODUCTOS COMERCIALIZADOS
Summary
Stevens Johnson Syndrome is a manifestation of toxic epidermal necrosis. It is a rare disease usually secondary to drugs. The case of a four-year old child who had 15% of cutaneous compromise, secondary to carbamacepine is presented. Drug induced diseases the establishment of a relationship between a drug and a side effect requires a high level of suspicion. Any case of probable drug induced side effect should be notified in order to establish the drug's safety. The objective of this paper is to highlight the importance of the topic and also to revise the treatment of Stevens Johnson Syndrome which is a severe and frequent adverse reaction.
Key words:
STEVENS-JOHNSON SYNDROME
PHARMACEUTICAL PREPARATIONS-adverse effects
PRODUCT SURVEILLANCE, POSTMARKETING
Introducción
En los últimos años se ha reconocido que las reacciones adversas a medicamentos (RAMs) causan importante morbimortalidad. Su importancia ha sido determinada en diferentes trabajos. En el año 1994 se estimó que las RAMs constituyeron el 4,7% de los ingresos hospitalarios y se encontraban entre las seis primeras causas de muerte en EE.UU. (1).
La magnitud de este problema en niños es poco conocida. En un metaanálisis se observó que la incidencia de RAMs en niños hospitalizados fue 9,5% y representaron el 2% de las admisiones hospitalarias (2).
Estos datos muestran la necesidad de incluir la detección, evaluación y prevención de los riesgos asociados a los medicamentos (fármacovigilancia) a la práctica clínica (3). La notificación espontánea es la principal herramienta de trabajo (3).
Las reacciones adversas cutáneas son las más frecuentes y en la mayoría de los casos son leves (4). Sin embargo, en algunos pacientes ocurren reacciones dermatológicas graves, de elevada letalidad como el síndrome de Stevens Johnson (SSJ) y la necrosis epidérmica tóxica (NET).
El SSJ y la NET constituyen un espectro de la misma enfermedad dermatológica y comparten aspectos etiológicos, histológicos y terapéuticos. Ambas entidades se caracterizan por presentar compromiso simultáneo de piel y de dos o más mucosas. Se diferencian en el porcentaje de superficie corporal comprometida, siendo mayor a 30% en la NET y menor a 10% en el SSJ.
Se han descrito casos de SSJ en todas las edades, razas y en ambos sexos. Se describe que su incidencia varía entre 1,5 y 2 casos por millón de personas-año (4,5). Su mortalidad es del 5% (5,6).
Se trata de una enfermedad producida casi exclusivamente por medicamentos, para la cual no se dispone de un tratamiento específico.
Se describe el caso de un niño de 4 años que presentó un SSJ grave probablemente secundario a carbamacepina (CZP). Esta comunicación tiene como objetivos sensibilizar a los pediatras sobre la importancia y potencial gravedad de la patología inducida por medicamentos y revisar la conducta terapéutica frente al SSJ, una de las reacciones adversas graves más frecuente.
Observación clínica
NG, sexo masculino, 4 años, raza negra, procedente de Montevideo, sin antecedentes familiares a destacar. Producto de tercer embarazo, cesárea de urgencia a las 39 semanas por sufrimiento fetal agudo, peso al nacer 2.900 g, sin patología perinatal. Buen crecimiento y desarrollo. Certificado esquema de vacunación vigente. Portador de asma intermitente y epilepsia primaria tipo gran mal, en tratamiento con CZP 300 mg/día, que inicia 15 días antes del ingreso.
Ingresa el 18 de setiembre de 2007 al Servicio de Pediatría del Hospital Central de las Fuerzas Armadas.
Comienza 48 horas antes con fiebre de 38,0º C axilar, odinofagia y lesiones tipo aftas dolorosas en mucosa yugal y lengua. Múltiples consultas a servicios de emergencia móvil. En la evolución rechazo total del alimento, no ingiere líquidos. Al examen físico se destaca buen estado general, temperatura axilar 37,7ºC, eupneico. Piel y mucosas normocoloreadas, lesiones tipo aftas en mucosa yugal, lengua y paladar. Escasas lesiones similares en labios. Lesiones máculopapulosas en tronco que desaparecen a la digitopresión. Bien hidratado y prefundido; resto del examen físico normal. El hemograma muestra leucocitosis 17.400 elementos/mm3; polimorfonucleares: 82%, hemoglobina: 12,6 g/dl; hematocrito: 36,2%; plaquetas 150.000 elementos /mm3; velocidad de eritrosedimentación: 29 mm/h; glicemia 67 mg/dl; Na+ 138 meq/l, K+ 3,9 meq/l. La dosificación plasmática de CZP, predosis matinal, fue 5,9 m g/ml. Se administra dipirona por vía intravenosa y se mantiene hidratación parenteral.
A las 24 horas persiste febril, con deterioro del estado general, irritabilidad y tendencia al sueño. Extensión de las lesiones cutáneomucosas. Edema de labios. Al examen: mal estado general, puntaje de Glasgow 11, frecuencia respiratoria: 36 respiraciones/min, sin tirajes. Saturación de oxígeno al aire 87%. Lesiones máculopapulosas eritematosas y vesículas a contenido claro en cuello y dorso. Flictenas de contenido claro en palmas y plantas. Vesículas y lesiones ulceradas en mucosa yugal y en paladar que sangran al mínimo contacto. Labios edematizados y agrietados. Congestión conjuntival bilateral con supuración. A nivel cardiovascular: punta en quinto espacio intercostal izquierdo, línea de referencia; frecuencia cardíaca: 126 ciclos/min; pulsos normales. Presión arterial: 60/30 mmHg. Tiempo de recoloración: 3 segundos.
Ingresa a cuidados intensivos el 19 de setiembre de 2007. Se inicia asistencia ventilatoria mecánica (AVM), cargas de volumen con suero fisiológico, apoyo inotrópico, gammaglobilina por vía intravenosa (i/v) 1 g/kg/día durante dos días; hidrocortisona 10 mg/kg/dosis cada 6 horas i/v; clorfeniramina 4 mg i/v; vancomicina, ceftriaxona y aciclovir i/v. Se suspende CZP. Curación de las lesiones. Los planteos diagnósticos fueron sepsis bacteriana, viral (posiblemente herpética), RAM cutánea grave, SSJ.
En ese momento el hemograma muestra leucocitos 2.600 elementos/mm3, hemoglobina 9,1 g/dl, plaquetas 111.000 elementos/mm3; velocidad de eritrosedimentación 27 mm/h; Na+ 145 meq/l, K+ 3,5 meq/l; glicemia 60 mg/dl. La azoemia es 0,15 mg/dl y la creatininemia 0,28 mg/dl. El funcional hepático muestra bilirrubina total 0,25, TGO 21, TGP 9, fosfatasa alcalina 258 u/ml. En la crasis KPTT 38”, tasa de protrombina 22%, fibrinógeno 414 mg/dl. Se realiza estudio citoquímico del líquido cefalorraquídeo (LCR): proteínas 10 mg/dl, glucosa 68 mg/dl, Pandy negativo, glóbulos rojos 50 elementos/mm3, leucocitos 1 elemento/mm3. El hemocultivo y cultivo de LCR fueron estériles. La investigación de herpes virus en el LCR fue negativa.
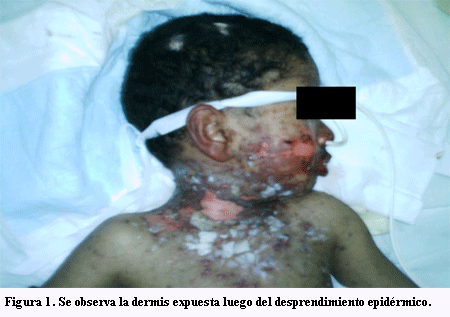
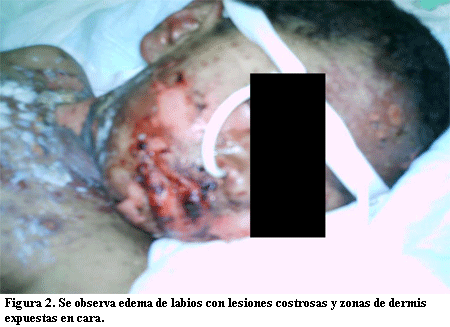
En la evolución agrega nuevas flictenas en cara, tronco, palmas y plantas con desprendimiento epidérmico que compromete aproximadamente el 15% de la superficie corporal. Flictenas en mucosa anal y glande. Peoría de lesiones bucofaríngeas, intenso edema de labios con fisuras sangrantes. Persiste supuración ocular y agrega edema en párpados (figuras 1 y 2).
Se mantiene en AVM con bajos parámetros ventilatorios durante 4 días. Al segundo día de internación en CTI se inicia alimentación por gastroclicis continua. Teniendo en cuenta la presentación clínica, la evolución y los hallazgos paraclinicos, se aleja el planteo de enfermedad infecciosa y se suspende la terapia antimicrobiana a los 10 días.
Se realizan lavados con suero fisiológico y curaciones con propóleo en palmas y plantas y sulfadiazina argéntica más clorelase en tronco.
Se otorga alta del CTI el 1 de octubre de 2007 sin secuelas oculares ni digestivas. Persiste con lesiones en mucosa yugal que dificultan alimentación. Reepitelización de la mayoría de las lesiones cutáneas.
Se notifica el caso a la Unidad de Fármacovigilancia (FV) del Ministerio de Salud Pública (MSP).
Discusión
La primera descripción de esta enfermedad fue realizada en el año 1922 por Stevens y Johnson en dos niños de 7 y 8 años que se presentaron con fiebre, conjuntivitis, estomatitis y exantema generalizado.
El SSJ presenta un período prodrómico de uno a tres días caracterizado por fiebre, astenia, cefaleas, mialgias, artralgias, odinofagia y tos (7,8). Posteriormente se agrega afectación de la piel y de dos o más superficies mucosas. Las mucosas afectadas con mayor frecuencia son la mucosa yugal y las conjuntivas. Se estima que el 100% de los casos de SSJ presentan estomatitis y el 90% conjuntivitis (7-10). En esta etapa inicial es frecuente atribuir los síntomas a procesos infecciosos virales como gingivoestomatitis herpética o faringitis, tal como sucedió en este caso.
La erupción característica comienza con lesiones eritematosas, máculopapulosas en cara y tronco que rápidamente se extienden hacia miembros superiores e inferiores. En la evolución presentan coloración púrpura en el centro y formación de flictenas que reflejan la necrosis de la epidermis que se separa de la dermis (signo de Nikolsky) (4,11). Esta fue la evolución que presentaron las lesiones en este paciente, que alcanzaron a comprometer el 10 a15% de la superficie corporal.
Se plantea que el SSJ es una forma de NET de menor severidad. Estas entidades se diferenciarían únicamente en el porcentaje de superficie corporal que presenta despegamiento epidérmico. En la NET el compromiso es mayor al 30% y en el SSJ menor al 10%. El porcentaje de superficie corporal comprometida es el principal factor pronóstico en esta enfermedad (11).
La mayoría de los casos de SSJ son provocados por medicamentos. La etiología infecciosa es menos frecuente. Mycoplasma pneumoniae y herpes virus son los agentes infecciosos más implicados (9,10).
Se han identificado más de 100 medicamentos como agentes de SSJ y de NET. Los medicamentos más frecuentemente implicados son los antibióticos (sulfonamidas, aminopenicilinas, cefalosporinas, quinolonas), anticonvulsivantes, antiinflamatorios no esteroideos de tipo oxicam, alopurinol y antifúngicos de tipo imidazol (12).
En el grupo de los anticonvulsivantes, los más frecuentemente asociados son fenobarbital, difenilhidantoína, carbamacepina, lamotrigina y ácido valproico (12-14).
En este caso clínico los síntomas comenzaron luego de iniciado el tratamiento con CZP planteándose este medicamento como posible agente etiológico.
Para determinar la relación de causalidad entre un medicamento y un evento adverso se utilizan algoritmos como el de Karch y Lasagna, que incluyen la evaluación sistemática de los siguientes aspectos (15):
1. Existencia de secuencia temporal adecuada entre la exposición al medicamento y el evento.
2. Plausibilidad biológica. Existencia de un mecanismo posible para dicho evento.
3. Descartar otras etiologías.
4. Mejoría con el retiro del fármaco.
5. Reexposición.
El riesgo de presentar SSJ y NET por anticonvulsivantes es mayor al inicio del tratamiento, principalmente en los primeros dos meses. En una serie de 41 pacientes con SSJ asociado a CZP, 39 comenzaron con las manifestaciones típicas en los primeros 60 días del tratamiento. Otros anticonvulsivantes como lamotrigina, fenobarbital y difenilhidantoína presentan un comportamiento similar (13). En este paciente el período de latencia fue 15 días.
Se plantea un mecanismo plausible para el SSJ secundario a medicamentos. En este síndrome se produce apoptosis de los queratinocitos determinando separación de la unión dermo-epidérmica. Este proceso cursa con escasa respuesta inflamatoria. Se postula que los fármacos se unen a las proteínas de membrana de los queratinocitos transformándolos en diana para el ataque celular. En los queratinocitos se expresa el antígeno Fas (CD95), un receptor transmembrana que al unirse al ligando Fas (LFas) desencadena la apoptosis. Si bien este LFas es una proteína de membrana, también se encuentra en forma soluble en el plasma (11,16).
Habitualmente los queratinocitos expresan cantidades bajas de LFas. En los pacientes con SSJ y NET se observa un aumento en la cantidad de LFas a nivel de los queratinocitos. Este proceso de apoptosis es inhibido in vitro por inmunoglobulinas que tienen la capacidad de bloquear el receptor Fas. Ésta es la base para el uso de gammaglobulina en el manejo de estas patologías (11,16).
Independientemente del mecanismo implicado en la reacción, el SSJ inducido por CZP corresponde a una reacción adversa tipo B. Las reacciones adversas tipo B no están relacionadas con el mecanismo de acción del fármaco ni con la dosis. Se consideran idiosincrásicas (15).
No se han identificado factores de riesgo para el desarrollo de esta reacción adversa. Se desconoce si la titulación progresiva de la dosis disminuye la frecuencia de esta complicación. Por lo tanto, hasta el momento, el SSJ por medicamentos no es prevenible.
Este SSJ ocurrió en un niño asmático y epiléptico, sin antecedentes ambientales a destacar, que al momento del inicio de la enfermedad se encontraba en aparente buen estado de salud. No existen explicaciones alternativas evidentes. El factor desencadenante más probable es la CZP.
Por otra parte, se observó mejoría de la enfermedad al suspender el fármaco.
Como sucede en la mayoría de las sospechas de reacciones adversas a medicamentos, la reexposición al posible agente causal está contraindicada debido a la gravedad del evento.
En función de este análisis, y siguiendo los pasos antes mencionados, este caso de SSJ se clasifica como una reacción adversa probable a la CZP.
El tratamiento del SSJ es de sostén. Se plantea que el retiro temprano del agente desencadenante es la única medida que mejora la evolución. En un estudio retrospectivo con 113 pacientes (74 SSJ y 39 NET) el probable medicamento causal se retiró en forma temprana en 64 y en forma tardía en 49. Fallecieron 7 pacientes en el primer grupo y 13 en el segundo. El beneficio fue más marcado cuando el medicamento implicado tenía corta vida media de eliminación (17).
Se destaca entonces la importancia del diagnóstico temprano. Para ello es necesario un alto índice de sospecha, debiendo incorporar la patología inducida por medicamentos dentro de los diagnósticos diferenciales en pacientes que cursan enfermedades con erupción, especialmente si existe compromiso simultáneo cutáneo y mucoso.
Los glucocorticoides (GC) habitualmente son utilizados en el tratamiento, pero no se han demostrado beneficios en la evolución de la enfermedad. El SSJ se caracteriza por cursar con escasa inflamación, predominado la necrosis por apoptosis, por lo que no sería necesario el uso de antiinflamatorios. Se plantea además que podrían empeorar el pronóstico. En un estudio de casos y controles el uso reciente de GC se asoció con un riesgo 12 veces mayor de NET- SSJ. Es decir, los GC podrían ser un agente etiológico (11,12).
En los últimos años se ha recomendado el uso de gammaglobulina para el tratamiento de estos pacientes. La gammaglobulina inhibe la apoptosis in vitro y se plantea que podría mejorar la evolución de los pacientes con SSJ y NET. Hasta el momento no se dispone de ensayos clínicos controlados que evalúen los efectos del tratamiento con gammaglobulina. Las evidencias para su uso sistemático son escasas. En un estudio prospectivo, no controlado, 34 pacientes adultos y adolescentes con SSJ y NET recibieron inmunoglobulina G 1 g/kg/día i/v en dos dosis. No se permitió el uso de GC ni otros inmunosupresores. Fallecieron 11 pacientes, la mayoría mayores de 70 años, siendo la causa más frecuente el shock séptico. En este estudio descriptivo no se observaron efectos beneficiosos del uso de inmunoglobulina G i/v sobre la evolución de las lesiones ni la tasa de mortalidad (18). Una revisión sistemática concluye que no existen evidencias suficientes para recomendar el uso sistemático de inmunoglobulina tanto en el SSJ como en la NET (19).
Resulta necesario sensibilizar a los profesionales de la salud en relación a la importancia de la “patología inducida por medicamentos” y promover su capacitación en el diagnóstico. Para ello es imprescindible desarrollar una nueva cultura sobre los medicamentos, reconociendo sus dos propiedades inseparables: el beneficio y el riesgo.
En Uruguay, desde el año 2006 el Ministerio de Salud Pública impulsa el desarrollo de un Sistema Nacional de Fármacovigilancia. Para su fortalecimiento deberá promoverse la notificación espontánea de todas las sospechas de RAMs. Sólo de esta forma se podrá conocer la epidemiología local, identificar posibles factores de riesgo y adoptar medidas de prevención.
Referencias bibliográficas
1. Lazarou J, Pomeranz BH, Corey PN. Incidence of adverse drug reactions in hospitalized patients.JAMA 1998; 279: 1200-5.
2. Impicciatore P, Choonara I, Clarkson A, Provasi D, Pandolfini C, Bonati M. Incidence of adverse drug reactions in paediatric in/out-patients:a systematic review and meta-analysis of prospective studies. Br J Clin Pharmacol 2001; 52: 77-83.
3. The Uppsala Monitoring Centre. Vigilancia de los medicamentos. Guía para la instalación y puesta en funcionamiento de un Centro de Farmacovigilancia [en línea]. Uppsala: UMC, 2008 < http://www.who-umc.org > [consulta: 10 mar 2008].
4. Cutaneous drug reaction case reports: from the world literature. Am J Clin Dermatol 2003; 4: 511–21.
5. Roujeau JC, Stern RS. Severe adverse cutaneous reactions to drugs. N Engl J Med 1994; 331:1272-1285.
6. Wolkenstein P, Revuz J. Drug-induced severe skin reactions. Incidence, management and prevention. Drug Saf 1995; 13(1): 56-68.
7. Leaute-Labreze C, Lamireau T, Chwki D, Maleville J, Taieb A. Diagnosis, classification, and management of erythema multiforme and Stevens-Johnson syndrome. Arch Dis Child 2000; 83: 347-52.
8. Lam N-S, Yang Y-H, Wang L-C, Lin Y-T, Chiang B-L. Clinical characteristics of childhood erythema multiforme, Stevens-Johnson syndrome and toxic epidermal necrolysis in Taiwanese children. J Microbiol Inmunol Infect 2004; 37:366-370.
9. Auquier-Dunant A, Mockenhaupt M, Naldi L, Correira O, Schroder W, Roujeau J-C, et al. Correlations Between Clinical Patterns and Causes of Erythema Multiforme Majus, Stevens-Johnson Syndrome, and Toxic Epidermal Necrolysis. Results of an International Prospective Study. Arch Dermatol 2002; 138: 1019-24.
10. Forman R, Koren G, Shear N. Erythema Multiforme, Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis in Children. Drug Safety 2002; 25 (13): 965-72.
11. García Doval I, Roujeau J-C, Cruces Prado M. Necrólisis epidérmica tóxica y síndrome de Stevens-Johnson: clasificación y actualidad terapéutica. Actas Dermosifiliogr 2000; 91: 541-51.
12. Roujeau J-C, Nelly J, Naldi L, Rzany B, Stern R, Anderson T, et al. Medication use and the risk os Stevens Johnson Syndrome or Toxic Epidermal Necrolysis. N Engl J Med 1995; 333: 1600-7.
13. Mockenhaupt M, Messenheimer J, Tennis P, Schlingmann J. Risk of Stevens syndrome and toxic epidermal necrolysis in new users of antiepileptics. Neurology 2005; 64: 1134-8.
14. Devi K, George S, Criton S, Suja V, Srivedi PK. Carbamazepine-The commonest cause of toxic epidermal necrolysis and Stevens-Johnson syndrome: A study of 7 years. Indian J Dermatol Venereol Leprol 2005; 71(5):325-328.
15. Laporte J, Capellà D. Mecanismo de producción y diagnóstico clínico de los efectos indeseables producidos por medicamentos. En: Laporte J, Tognoni G. Principios de epidemiología del medicamento. 2 ed. Barcelona: Masson, 1993: 95-109.
16. Abe R, Shimizu T, Shibaki A, Nakamura H, Watanabe H, Shimizu H. Toxic Epidermal Necrolysis and Stevens-Johnson Syndrome Are Induced by Soluble Fas Ligand. Am J Pathol 2003; 162: 1515-20.
17. García-Doval I, LeCleach L, Bocquet H, Otero X-L, Roujeau J-C. Toxic Epidermal Necrolysis and Stevens-Johnson Syndrome. Does early Withdrawal of Causative Drugs Decrease the Risk of Death?. Arch Dermatol 2000; 136: 323-7.
18. Bachot N, Revuz J, Roujeau J-C. Intravenous Inmunoglobulin Treatment for Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis. A Prospective Noncomparative Study Showing No Benefit on Mortality or Progression. Arch Dermatol 2003; 139: 33-6.
19. Mittmann N, Chan B, Knowles S, Cosentino L, Shear N. Intravenous Immunoglobulin Use in Patients with Toxic Epidermal Necrolysis and Stevens-Johnson Syndrome. Am J Clin Dermatol 2006; 7(6): 359-68.
Correspondencia: Dr. Héctor Telechea
Correo electrónico: hmteleor@hotmail.com