Services on Demand
Journal
Article
Related links
Share
Archivos de Pediatría del Uruguay
On-line version ISSN 1688-1249
Arch. Pediatr. Urug. vol.74 no.1 Montevideo Mar. 2003
Errores congénitos del metabolismo
DRA. AíDA LEMES1
1. Instituto de Genética Médica. Hospital Italiano, Montevideo.
¿Qué son los errores congénitos
del metabolismo (ECM)?
Los ECM son un grupo de enfermedades genéticas determinadas por el bloqueo de un paso metabólico. La causa del bloqueo es la mutación de genes responsables del funcionamiento de dicho paso metabólico, ya sea porque el producto génico, que puede ser una enzima o una coenzima, esté cuali o cuantitativamente afectado. El mecanismo de herencia es, en la gran mayoría de los casos, autosómico y recesivo y en contadas situaciones ligado al cromosoma X.
¿Son enfermedades frecuentes?
Los ECM son afecciones genéticas individualmente raras pero colectivamente numerosas. Más de 300 enfermedades humanas debidas a ECM han sido reconocidas hasta el momento actual. Este número está aumentando constantemente en la medida en que se dispone de nuevos conceptos y técnicas para la identificación de fenotipos bioquímicos. En cuanto a la incidencia, si bien cada vez hay mayor número de casos reportados, se considera que hay una subestimación de la misma dado que serían frecuentes los casos confundidos con otras afecciones más frecuentes o no detectados.
¿Es posible el diagnóstico clínico
de los ECM?
Su diagnóstico depende primariamente de un alto índice de sospecha por parte del médico. Con este objetivo, se hace necesario la aplicación de un método de evaluación clínica sencillo y de un protocolo de recolección de muestras. El primero permitirá plantear grupos de ECM para cada cuadro clínico y las muestras biológicas, adecuadamente recolectadas y almacenadas, permitirán establecer un diagnóstico preciso.
¿Cuáles serían los elementos clínicos que deberían hacer sospechar un ECM?
Son numerosas las circunstancias clínicas en las que el pediatra puede verse enfrentado a una posible enfermedad metabólica, considerando que son múltiples los signos y síntomas de las mismas.
De acuerdo a la orientación clínica del Dr. JM Saudubray (Hospital Necker Enfants Malades de Paris), habría cuatro grupos básicos de circunstancias en que el pediatra debería plantearse la posibilidad de estar ante un ECM:
1) Síntomas agudos en el período neonatal.
2) Síntomas agudos e intermitentes de inicio más tardío.
3) Síntomas neurológicos progresivos.
4) Síntomas específicos
Grupo 1: síntomas agudos en el período neonatal. Un muy sugestivo cuadro clínico es aquel de un recién nacido sin antecedentes durante el embarazo ni el parto que luego de un período libre de síntomas (horas o días), instala un cuadro de deterioro clínico sin causa aparente y sin respuesta al tratamiento sintomático. De acuerdo al elemento clínico más destacado: deterioro neurológico, convulsiones, hipotonía, compromiso cardíaco, compromiso hepático, combinados con el resultado de la paraclínica de rutina (tabla 1), es posible hacer una aproximación a uno de los cinco tipos de presentación aguda neonatal, a partir de la cual se iniciarán estudios específicos. Por ejemplo, si presenta deterioro neurológico, alcalosis respiratoria e hiperamoniemia, muy probablemente se trate de un defecto del ciclo de la urea; deterioro neurológico con acidosis metabólica y anión restante aumentado, con o sin aumento de amoníaco, posiblemente sea una acidosis orgánica; convulsiones de difícil control e hipotonía importante, con patrón de descarga-supresión en el EEG, podría tratarse de hiperglicinemia no cetósica; hepatomegalia y coletasis en un recién nacido alimentado a pecho con movilización de transaminasa, incluyendo o no un leve aumento de ácido láctico, debería sugerir una posible galactosemia o tirosinosis tipo I. Se subraya la importancia, en este grupo 1, de incorporar a la paraclínica de rutina, dosificación de ácido láctico y de amoníaco. Es importante la recolección de todas las muestras biológicas en el mismo momento y el adecuado almacenamiento de las mismas (tabla 1). La interpretación de los resultados de los estudios paraclínicos deberá efectuarse cuidadosamente, considerando siempre el momento de recolección y el tratamiento que el paciente recibía entonces. Los ECM que más frecuentemente se presentan en el neonato son: defectos del ciclo de la urea, acidurias orgánicas, leucinosis e hiperglicinemia no cetósica.
Grupo 2: síntomas agudos e intermitentes de inicio más tardío. La presentación más frecuente es bajo la forma de: vómitos recurrentes y letargia, ataxia, coma. Algunos autores insisten en que todo tipo de coma puede tratarse de un ECM, incluyendo casos con signos neurológicos focales. Coma con hiperglicemia, glucosuria y cetoacidosis puede ser el debut de una acidosis orgánica o un defecto de la cetolisis y puede confundirse con coma diabético. Formas de inicio tardío de defectos en el ciclo de la urea como la deficiencia de ornitinatranscarbamilasa (OTC) pueden presentarse en mujeres como cuadro agudo psiquiátrico con alucinaciones, delirio, ansiedad y agresividad. A modo de ejemplo, otras formas de presentación de este grupo 2 son: acidosis metabólica (acidosis orgánicas), cetosis (defectos de la cetolisis), acidosis láctica (defecto energético mitocondrial), hipoglicemia (defectos en la glucogenólisis o gluconeogénesis), muerte súbita (defectos en la beta oxidación de los ácidos grasos -BOAG-), intolerancia al ejercicio con mioglobinuria recurrentes (defectos en BOAG), dolor abdominal recurrente (malabsorción de lactosa), cardiomiopatía y/o trastornos del ritmo cardíaco (defectos en la BOAG). Este grupo de ECM y el anterior son los que se presentan en forma aguda y en los que la recolección de las muestras biológicas es de fundamental importancia a fin de establecer el diagnóstico mediante estudios paraclínicos específicos. Es importante recolectar las mismas en etapa sintomática, momento en que podrán detectarse metabolitos anormales. El episodio agudo puede evolucionar a un rápido restablecimiento una vez iniciado el tratamiento sintomático, situación en la que difícilmente puedan detectarse metabolitos diagnósticos.
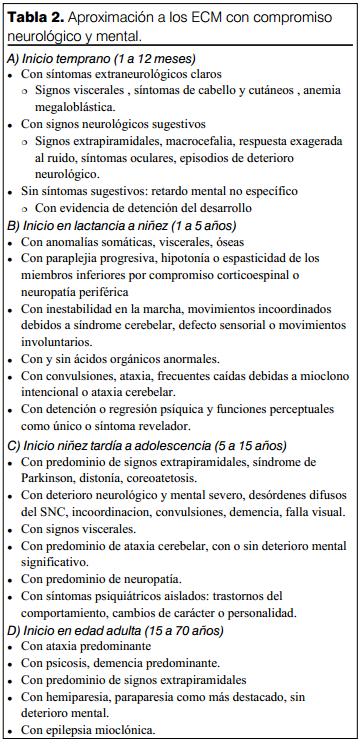
Grupo 3: síntomas neurológicos y mentales progresivos. El abanico de posibles ECM es muy amplio para este grupo. Un número importante de enfermedades metabólicas puede presentar síntomas neurológicos, retraso del desarrollo, trastornos psiquiátricos o deterioro mental. Las afecciones a plantear dependen esquemáticamente de la edad al comienzo de los síntomas, así como de los signos neurológicos y de posibles signos extraneurológicos asociados. Cuando estos últimos están presentes (cutáneos, óseos, viscerales, oculares, etcétera), generalmente constituyen la clave para el diagnóstico. La tabla 2 muestra la clasificación de ECM en este grupo de acuerdo a la edad al inicio de los síntomas.
Grupo 4: síntomas específicos. Varios ECM tienen como primera manifestación clínica signos específicos, por ejemplo dislocación de cristalino y accidentes tromboembólicos en la homocistinuria, deterioro neurológico progresivo y mancha rojo cereza en la enfermedad de Tay-Sachs, etcétera. Estos síntomas específicos han sido clasificados en oculares, hematológicos, de la piel, viscerales y endocrinos.
- Oculares: cataratas (síndrome de Lowe), opacidad de córnea (alfa manosidosis), mancha rojo cereza (gangliosidosis GM1), retinitis pigmentosa (lipofuscinosis ceroidea).
- Hematológicos: anemia macrocítica no regenerativa (aciduria orótica congénita, síndrome de Pearson), pancitopenia, neutropenia, trombocitopenia (enfermedad de Gaucher tipo I, acidosis orgánicas).
- Piel: ictiosis (defecto congénito de la glicosilación), hiperqueratosis (síndrome de Conradi-Hunermann), lesiones vesiculosas (deficiencia de biotinidasa), distribución particular de la grasa subcutánea (defecto congénito de la glucosilación), nódulos subcutáneos (enfermedad de Farber), angioqueratomas (enfermedad de Fabry), alopecia (enfermedad de Menkes).
- Viscerales: hepatomegalia (enfermedad por almacenamiento de glucógeno), esplenomegalia (enfermedad de Niemann-Pick), hepatoesplenomegalia (enfermedad de Wolman), cardiomiopatía (enfermedd de Pompe), infiltrado pulmonar intersticial (intolerancia proteica lisinúrica), tubulopatía renal (cistinosis).
- Endocrinológicas: diabetes, hipoparatiroidismo, insuficiencia adrenal primaria, deficiencia de hormona del crecimiento. Se describen casos con deficiencias endócrinas en desórdenes de la cadena respiratoria mitocondrial.
Se nombran entre paréntesis, a modo de ejemplo, solamente algunas de las afecciones que pueden presentar los diferentes elementos clínicos.
La presentación de los ECM por grupos o categorías es, como para otras enfermedades o situaciones en medicina, una forma de aproximarnos a los distintos diagnósticos desde la clínica, no es un esquema rígido sino que el solapamiento de grupos es habitual, lo mismo que pacientes con una enfermedad por ECM que no podemos categorizar.
El motivo de este breve artículo impide un extenso desarrollo de los cuatro grupos básicos. Remitimos a los lectores que deseen mayor información a las publicaciones que han sido nuestra referencia primaria.
¿Tienen tratamiento estas enfermedades?
Para algunas formas de presentación aguda (recién nacidos y formas agudas e intermitentes más tardías), el tratamiento de emergencia tiene por objeto disminuir la producción del metabolito tóxico proximal al punto de bloqueo estimulando el anabolismo mediante aporte energético elevado. Por otro lado, dependiendo de la gravedad del cuadro al momento del diagnóstico, pueden utilizarse medidas de depuración exógenas como: exanguíneo transfusión, diálisis peritoneal, hemodiálisis, hemofiltración y en algunos casos aumentar la eliminación del producto tóxico mediante la estimulación de vías alternativas específicas. Estas medidas son aplicables para acidurias orgánicas, defectos del ciclo de la urea y algunos defectos de la beta-oxidación de los ácidos grasos. El transplante hepático ha mostrado ser un procedimiento con riesgos, pero curativo para algunas afecciones del metabolismo intermediario como defectos del ciclo de la urea y algunas acidurias orgánicas. Para las afecciones progresivas, como las enfermedades de acúmulo lisosomal (EAL), se están desarrollando terapias específicas como la terapia de reemplazo enzimático (TRE), la cual consiste en la administración de la enzima específica deficiente. Hace ya unos años que este tipo de terapia se aplica para la enfermedad de Gaucher. En la Comunidad Económica Europea ha sido aprobado un producto farmacéutico para la TRE en la enfermedad de Fabry. Se encuentran en etapa avanzada los ensayos clínicos para TRE en algunos tipos de mucopolisacaridosis. El aporte enzimático permanente (la enzima deficiente) en las EAL puede también lograrse con el transplante de médula ósea, que tiene elevada morbimortalidad y para el que se requiere donante compatible. Una dieta que restrinja el producto que no puede metabolizarse es el tratamiento de elección para algunas afecciones como la fenilcetonuria y leucinosis (enfermedad con olor a caramelo quemado en la orina). Por último, hay un grupo de ECM que aún no tiene tratamiento específico.
¿Cuál es la importancia del diagnóstico para los ECM?
En todos los casos, por tratarse de enfermedades genéticas, el diagnóstico preciso del propósito o afectado es indispensable para un adecuado asesoramiento genético a la familia. Para los padres del paciente siempre hay un alto riesgo de recurrencia de la misma situación. Es importante también ante eventual diagnóstico prenatal. Para aquellos ECM con tratamiento específico, el diagnóstico preciso es fundamental además por este relevante aspecto.
Bibliografía
Fernandes J, Saudubray JM, Van Den Berghe G. Inborn Metabolic Diseases. Diagnosis and Treatment. 3ra ed. Berlin: Springer-Verlag, 2000.
Scriver CR, Beaudet AL, Sly WS, Valle D. The Metabolic and Molecular Bases of Inherited Diseases. 8ª ed. New York: Mc Graw-Hill, 2001.
Nyhan WL, Ozand PT. Atlas of Metabolic Diseses. London: Chapman & Hall Medical, 1998.
Lyon G, Adams RD, Kolodny EH. Neurology of Hereditary Metabolic Diseases of Children. 2ª ed. New York: Mc Graw-Hill, 1996.