Introducción
A nivel mundial, la prevalencia de cardiopatías congéntitas es muy variable, con cifras que estiman entre 0,5 y 9 casos cada 1.000 recién nacidos vivos. Considerando que nacen 135 millones de niños al año, se estima que 1,3 millones de ellos son portadores de cardiopatías congénitas 1. La coartación de aorta (CoAo) corresponde al 6-8% de dichas cardiopatías congénitas 2,3.
Se caracteriza por un estrechamiento de la aorta descendente distal al origen de la arteria subclavia izquierda, lo que determina una obstrucción al flujo sanguíneo. Hay un engrosamiento de la capa media aórtica e hiperplasia de la íntima distal al origen de dicha arteria, de longitud variable. Ante la sospecha clínica, la confirmación diagnóstica suele realizarse mediante el ecocardiagrama Doppler, que permite también definir la severidad. Se describen diferentes grados de necrosis quística en la capa media arterial, que se incrementa con la edad4.
De acuerdo con su relación espacial con el ductus arterioso, la CoAo se clasifica en preductal, ductal y posductal4.
Puede presentarse aislada o asociada a otras anomalías congénitas cardiovasculares o extracardiovasculares, entre ellas: anomalías de la válvula aórtica (15-85% válvula aórtica bicúspide), defectos septales interventriculares (30-55%), hipoplasia del arco aórtico distal, síndrome de Shone. Con menor frecuencia se asocia con comunicación interatrial (CIA), anomalías de la válvula mitral, defectos de la tabicación auriculoventricular, transposición de grandes arterias (TGA), origen anómalo de la arteria subclavia derecha, fibroelastosis endocárdica o truncus arterioso. En el 20% de los pacientes se presenta como lesión única.
Se puede asociar con aneurismas de arterias cerebrales. Como consecuencia de esta asociación lesional, el 13% de los pacientes presentan hemorragias intracraneales en la evolución. La CoAo puede estar presente en el síndrome de Turner (15-36%), síndrome de Down y síndrome de Williams4-6.
En la evolución de la CoAo se puede constatar hipertensión arterial (HTA), dilatación de la aorta ascendente, recoartación, arterioesclerosis primaria prematura, enfermedad coronaria temprana. Esto determina un aumento de la morbimortalidad y una menor expectativa de vida aún luego de su corrección7.
El diagnóstico de CoAo se sospecha por la clínica, variable según la edad del paciente. La precocidad y la severidad de las manifestaciones clínicas dependen principalmente del tipo anatómico 6,8.
Clásicamente se describen dos grupos de acuerdo con la edad de presentación4,6,8:
1. Clínicamente evidente en el recién nacido. Constituye en general una situación de gravedad. Al cerrarse el ductus, se produce una falla hemodinámica progresiva que puede evolucionar a la muerte4,6,8,10.
2. Clínicamente evidente en la etapa del niño escolar o en la adolescencia. La aparición y gravedad de la sintomatología están estrechamente relacionadas con el desarrollo de la circulación colateral dirigida a compensar el compromiso del flujo distal a la obstrucción. Los pacientes pueden presentarse en un abanico clínico amplio, con formas asintomáticas, desarrollo de HTA, síntomas y signos de mala tolerancia al ejercicio u otros síntomas cardiovasculares. El hallazgo de un gradiente de presión arterial sistólica de 20 mmHg o más entre miembros superiores e inferiores es una constante.
La confirmación del diagnóstico se realiza con base en la presencia de síntomas y signos clínicos orientadores y el ecocardiograma Doppler, que permite también evaluar la severidad de la CoAo. La tomografía computada con reconstrucción tridimensional y la resonancia nuclear magnética tienen indicaciones precisas.
Sujeta a su evolución natural, sin mediar tratamiento, la CoAo es una entidad de mal pronóstico, con una mortalidad de 25, 50, 75 y 92% a los 20, 30, 46 y 60 años, respectivamente 3. La media de sobrevida es de 34 años3. El 20% de los pacientes son asintomáticos en la vida adulta3. La hipoplasia segmentaria de la aorta y la presencia de otras anomalías congénitas son de peor pronóstico3,4,7,11.
La indicación del momento y tipo de tratamiento depende de la forma y la edad de presentación6. Los recién nacidos con CoAo crítica requieren tratamiento médico inmediato previo a la cirugía, con el fin de mantener la permeabilidad del ductus.
La decisión del tratamiento (cirugía o angioplastia) la determina el equipo tratante, según la morfología de la coartación y su experiencia. La mayoría de los centros en el mundo opta por la cirugía en todos los niños menores de 5 años. Los pacientes con CoAo y anatomía favorable (lesión circunscrita, centrada con buen sector aórtico proximal y distal, peso mayor o igual a 25 kg) pueden someterse a angioplastia con balón y/o colocación de stent13,15,16.
La recoartación es más frecuente en lactantes menores de 3 meses, con istmo aórtico menor a la mitad del tamaño de la aorta ascendente, diámetro del segmento coartado < 3,5 mm antes de dilatarlo y < 6 mm luego de la dilatación, con gradiente residual inmediato mayor de 20 mmHg.
A pesar de ser una cardiopatía congénita prevalente y los avances diagnósticos y terapéuticos sustanciales observados en las últimas décadas, en Uruguay no se han documentado series numerosas que permitan caracterizar la población local de pacientes con CoAo.
Objetivo
Describir las características clínicas y anatómicas, el tipo de tratamiento y la evolución de los niños menores de 15 años con diagnóstico de CoAo asistidos en un hospital pediátrico de referencia de Uruguay.
Material y método
Se realizó un estudio observacional descriptivo y retrospectivo. Se incluyeron niños y adolescentes de 0 a 15 años con CoAo asistidos en el Centro Hospitalario Pereira Rosell (CHPR), Montevideo (Uruguay), en el período comprendido entre 1/1/1999 y 31/3/2016.
Se consideraron las siguientes variables:
• Edad en meses y años.
• Sexo.
• Forma anatómica: preductal, ductal, posductal.
• Hipoplasia del istmo o del arco aórtico.
• Síntomas y signos clínicos que orientaron al diagnóstico: disminución o ausencia de pulsos femorales, mayor perfusión y saturación de oxígeno en miembros superiores comparado con los inferiores (diferencia de saturación > 3% en miembros superiores respecto a los miembros inferiores), HTA con presión arterial sistólica en miembros superiores > 20 mmHg por encima de la de los miembros inferiores, soplo sistólico eyectivo en borde esternal superior izquierdo y base con irradiación interescapular izquierda.
• Repercusión hemodinámica y signos de insuficiencia cardíaca: polipnea, fatiga, sudoración o signos de shock cardiogénico (hipoperfusión e hipotensión arterial).
• Tratamiento: quirúrgico o por angioplastia.
• Mortalidad.
• Recoartación.
Definición de caso
El diagnóstico de CoAo se realiza mediante la presencia de síntomas y signos clínicos orientadores: disminución o ausencia de pulsos femorales, mayor perfusión y saturación de oxígeno en miembros superiores comparado con los inferiores (diferencia de saturación > 3%), HTA (gradiente de presión arterial sistólica entre miembros superiores e inferiores > 20 mmHg), soplo sistólico eyectivo en borde esternal superior izquierdo y base con irradiación interescapular izquierda; confirmándose a través de ecocardiograma Doppler y/o angiografía4,6,8. Criterios ecocardiográficos: en el Doppler color se consideró la presencia de un flujo de alta velocidad a nivel de la estenosis aórtica, y con el Doppler continuo, que permite estimar los gradientes tensionales, se consideró que un gradiente medio mayor de 20 mmHg era compatible con el diagnóstico de CoAo, así como también un flujo anterógrado de alta velocidad que se continuaba en la diástole (“rampa diastólica”), lo que confirma el diagnóstico y define la severidad de la estenosis. El hallazgo más significativo con el modo pulsado era el hallazgo de un retraso de la onda de pulso y una prolongación del flujo anterógrado en diástole en la aorta abdominal17.
Se consideró que existía recoartación en presencia de obstrucción aórtica con un gradiente superior a 20 mmHg en el sitio de la reparación. Los signos ecocardiográficos de recoartación fueron: prolongación diastólica de la onda de flujo, estrechamiento de un sector del arco aórtico que generaba un gradiente pre y poscoartación, pulsatilidad de la aorta abdominal disminuida o ausente4,6,7,8.
Fuente de datos
Se utilizaron historias clínicas, exámenes paraclínicos, descripciones operatorias de los registros en la policlínica de Cardiología, en la historia clínica del CHPR y del Instituto de Cardiología Integral (ICI).
El análisis estadístico se estableció con base en distribución de frecuencias, medidas de resumen y pruebas de significancia estadística, considerando estadísticamente significativo un valor de p ≤ 0,05. Esta investigación fue aprobada por el Comité de Ética del CHPR.
Resultados
Se analizaron 40 casos: 57,5 % de sexo masculino (n = 23) y 42,5% de sexo femenino (n = 17). Seguimiento: media 88,6 meses, mediana 49 meses, moda 203 meses.
Los pacientes se dividieron en dos grupos etarios: menores de un año (grupo 1, n = 34) y mayores a un año al diagnóstico (grupo 2, n = 6). A su vez, los pacientes del grupo 1 se dividieron en un subgrupo 1 A, con diagnóstico en el primer mes de vida (n = 24) y un subgrupo 1 B, cuyo diagnóstico se confirmó entre el primer mes y el primer año de edad (n = 10, tabla 1).
El número de pacientes del subgrupo 1 A (24/40) corresponde al 60% de los pacientes, el subgrupo 1 B (10/40) corresponde a un 25% y el grupo 2 (6/40) corresponde al 15% del total de pacientes.
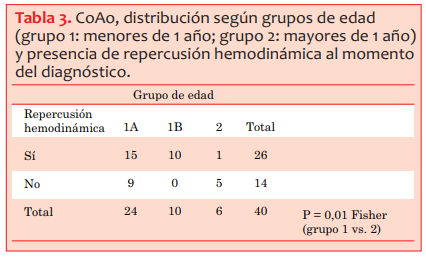
La forma preductal se observó en el 55% de los casos (n = 22), en el 62% de los del grupo 1 (n = 21) y en el 16,7% del grupo 2 (n = 1).
La forma ductal se observó en el 35% de los casos (n = 14), en el 32% de los del grupo 1 (n = 11) y en el 50% del grupo 2 (n = 3, tabla 2).
El 56% (n = 19) de los pacientes del grupo 1 y el 33% de los del grupo 2 (n = 2) presentaron hipoplasia del istmo y/o del arco aórtico.
La repercusión hemodinámica (insuficiencia cardíaca, shock) fue la manifestación predominante en el grupo 1 (74% vs. 33% en el grupo 2, p = 0,01, tabla 3), mientras que lo más frecuente en el grupo 2 fue la presencia de hallazgos al examen clínico, como soplo, ausencia de pulsos, diferencial de presión arterial > 20 mmHg, HTA (67% vs. 12% en el grupo 1).
El shock se presentó en el 15% del subgrupo 1 (n = 5), mientras que en el grupo 2 no hubo ningún caso.
En el análisis de subgrupos, tanto el subgrupo 1 A como el 1 B tuvieron la repercusión hemodinámica como presentación más frecuente (67% y 100%, respectivamente).
Otra forma de presentación fue el hallazgo de signos orientadores en el examen clínico sin repercusión hemodinámica (soplo o por valoración de rutina), en el subgrupo 1 A durante el control de síndrome de Down o malformaciones asociadas (17%) y en el subgrupo 1 B durante la internación de un lactante por estado de mal convulsivo.
La presencia de signos orientadores al diagnóstico (con o sin repercusión hemodinámica) se dio en el 50% (n = 17) del grupo 1 y en el 83% del grupo 2 (n = 5). En el análisis de subgrupos, el subgrupo 1 A presentó estos signos en 58% (n = 14), mientras que se presentaron en 30% del subgrupo 1 B (n = 3).
El tratamiento de elección fue cirugía en todos los casos.
La recoartación global se observó en el 17,5% (16,7% del subgrupo 1 A, n = 4) y 30% del subgrupo 1 B (n = 3), sin presentarse casos en el grupo 2. El 85,7% de las recoartaciones se trataron mediante angioplastia con balón (n = 6), mientras que un caso requirió cirugía.
Durante el seguimiento fallecieron 5 pacientes, todos ellos del grupo 1, lo que representa una mortalidad global de 13% (tabla 4).
Discusión
Los resultados de nuestro estudio son concordantes con los de la literatura internacional en cuanto al predominio en el sexo masculino (58%)3 y las edades de presentación, con un mayor porcentaje en el primer mes de vida4(tabla 1).
Se evidenció una tendencia (p = 0,057) de predominio de la forma anatómica preductal en el primer año de vida (62%), frente a la presentación de dicha patología luego de esta edad (17%), como está descrito en la literatura8. Pensamos que el tamaño de la muestra incide en los resultados (tabla 2).
Es de destacar que la repercusión hemodinámica fue la forma de presentación mayoritaria antes del primer año (74%) (tabla 3).
Cuando se analizó la presencia de signos orientadores al diagnóstico (con o sin repercusión hemodinámica), la mayoría de los pacientes mayores de 1 año (83%) y un 50% de los pacientes menores de 1 año presentaban dichos signos al momento del diagnóstico.
Cuando se discriminó la presencia de signos orientadores al momento del diagnóstico en los pacientes con repercusión hemodinámica, un 50% de los menores de 1 año lo tenían presente (y el único caso de 1 año con repercusión hemodinámica presentaba signos orientadores).
Por lo tanto, es razonable inferir que en cerca de la mitad de los casos en menores de 1 año se podría haber hecho el diagnóstico a través del examen clínico antes de desarrollar la repercusión hemodinámica, para anticiparse a la complicación. Este hecho es muy preocupante porque evidencia un claro déficit en el diagnóstico precoz de esta patología.
El tamaño de la muestra y la ausencia de mortalidad durante el seguimiento de los pacientes del grupo 2 pensamos que explica la ausencia de significación estadística en la mayor mortalidad en los pacientes menores de 1 año (p = 0,42), hecho que sería concordante con lo publicado en la literatura internacional8. La explicación de la mayor mortalidad que se ha reportado internacionalmente en este grupo está dada porque los pacientes en los que se diagnostica la CoAo antes del año de vida tienen una patología más severa confirmándose el diagnóstico en pacientes con mayor severidad clínica, generalmente con repercusión hemodinámica de grado variable.
Hay que destacar que el seguimiento promedio fue de 88,6 meses luego del tratamiento, sin disponer de un análisis de mortalidad a más largo plazo.
Si bien el porcentaje de recoartación fue mayor en el grupo 1 que en el grupo 2 (21% sin ningún caso registrado en el grupo 2), concordante con la literatura internacional3,4,8, estos resultados no alcanzaron significancia estadística (p = 0,57), lo que atribuimos al pequeño tamaño muestral. Por otro lado, la mayoría de los casos (86%) se corrigieron con angioplastia.
Tabla 1 CoAo, distribución según grupos de edad. Grupo 1: menores de 1 año. Grupo 2: mayores de 1 año.
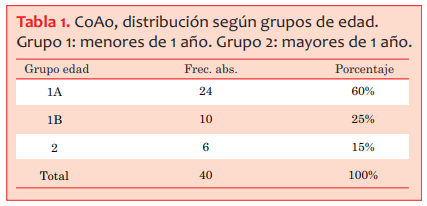
Tabla 2 CoAo, distribución según grupos de edad (grupo 1: menores de 1 año; grupo 2: mayores de 1 año) y tipo anatómico.
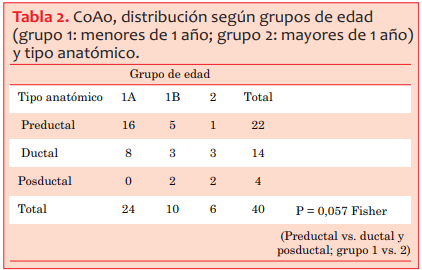
Tabla 3 CoAo, distribución según grupos de edad (grupo 1: menores de 1 año; grupo 2: mayores de 1 año) y presencia de repercusión hemodinámica al momento del diagnóstico.
Conclusiones
Las características anatomoclínicas de la población local estudiada son concordantes con lo descrito en la literatura internacional: predominio del sexo masculino, edad de presentación predominantemente en el primer mes de vida y forma anatómica preductal más frecuente en el primer año4.
Es de destacar la presencia de un déficit en el diagnóstico precoz de la CoAo y la morbimortalidad asociada a este hecho, un 50% de los niños del grupo 1 presentaban signos orientadores al diagnóstico, de haberlos constatado y tomado las medidas correspondientes, es posible que se hubiera podido evitar la evolución a una situación de extrema gravedad como es el shock.
Con base a nuestros resultados descriptivos podemos hacer las siguientes recomendaciones:
• Profundizar en la enseñanza de los signos clínicos que orientan sobre la presencia de una CoAo tanto a los neonatólogos como a los pediatras, médicos generales, médicos de familia y aquellos que trabajan en urgencia y emergencia.
• Sistematizar la realización del ecocardiograma prenatal para el diagnóstico de esta patología intraútero13.
• Realizar un registro nacional de los casos de esta patología en el Uruguay que posibilite el seguimiento a largo plazo y concreción de acciones de salud pertinentes y efectivas.