Sr. Editor:
Introducción
El shock cardiogénico es una complicación poco frecuente en el infarto agudo de miocardio que afecta al 10% de los pacientes. La revascularización precoz es la principal herramienta que ha demostrado disminuir la mortalidad en dicho contexto. El mantenimiento de un adecuado soporte hemodinámico mediante dispositivos de asistencia ventricular podría beneficiar a aquellos pacientes con bajo gasto cardíaco a pesar del apoyo de drogas vasoactivas, con el objetivo de mantener una adecuada oxigenación y perfusión tisular como puente a la recuperación de la función ventricular o como puente a trasplante cardíaco.
El propósito del presente artículo es analizar el caso clínico de una grave complicación de una patología tan prevalente como el infarto agudo de miocardio (IAM), haciendo hincapié en el soporte circulatorio llevado a cabo en un destacado hospital europeo.
Caso clínico
Paciente de sexo masculino, 54 años, tabaquista, sin antecedentes personales a destacar. Cuadro de 72 horas de evolución dado por episodios de angina de esfuerzo clase III CCS. Consulta a unidad de emergencia móvil por progresión del ángor que se hace de reposo, de 4 horas de duración y moderada intensidad que lo despierta en la madrugada, por lo que se traslada a puerta de emergencia. A su llegada el paciente está lúcido, taquicárdico, hipotenso (PA 90/60), mal perfundido. Electrocardiograma: RS 110, onda P y segmento PR normal, QRS 140 ms con imagen de bloqueo completo de rama izquierda, sin alteraciones secundarias de la repolarización, tras lo cual se activa código IAM. A las dos horas del ingreso presenta inestabilidad hemodinámica, shock cardiogénico (SC) con alto requerimiento de inotrópicos y vasopresores, así como varios episodios de taquicardia ventricular (TV) y fibrilación ventricular que revierten tras cardioversión eléctrica. Dado el estado crítico del paciente se decide por parte del heart team la colocación de un dispositivo de oxigenación por membrana extracorpórea (ECMO) de tipo venoarterial como puente a la revascularización coronaria. Para ello se realiza canulación venosa femoral derecha y arterial femoral derecha. Se programa la bomba centrífuga a 3000 rpm, se genera un flujo de 3 litros por minuto con franca mejoría hemodinámica y de la perfusión distal y se logra disminuir la noradrenalina a 0,1 mcg/kg/min y dobutamina a 5 mcg/kg/min.
Posterior a ello se realiza cineangiocoronariografía de urgencia, en la que se destaca lesión crítica 90% de tronco coronario izquierdo distal que compromete el origen de la arteria descendente anterior; arteria circunfleja con ateromatosis difusa y lesión severa 80% de segundo ramo marginal; arteria coronaria derecha sin lesiones y descendente posterior con lesión severa 80% distal. Se decide realizar angioplastia transluminal con colocación de stent farmacoactivo a nivel de tronco coronario izquierdo orientado hacia la arteria descendente anterior con buen resultado (flujo TIMI 3) sin complicaciones. Concomitantemente se coloca balón de contrapulsación intraaórtico (BCIA) por vía femoral izquierda 1:1. En el ecocardiograma transtorácico se observa disfunción biventricular severa, con ventrículo izquierdo (VI) no dilatado y aquinesia generalizada e hipoquinesia inferobasal con FEVI de 15%, sin valvulopatías significativas.
En la evolución el paciente presenta fiebre persistente y elevación de reactantes de fase aguda, con hemocultivos positivos a Enterobacter cloacae, por lo que se inicia antibioticoterapia empírica con amoxicilina clavulánica que luego se rota a meropenem y daptomicina.
Dada la buena evolución hemodinámica y la mejoría progresiva de la función ventricular (FEVI 25%) con adecuado índice cardíaco (2,8 L/min/m2) y mínimo apoyo del ECMO y drogas vasoactivas, se decide retirar la asistencia cardiopulmonar al noveno día, así como el BCIA a las 24 horas siguientes sin incidentes. Desde el punto de vista infeccioso, a las 72 horas reitera fiebre persistente a pesar de antibioticoterapia, con aumento de requerimiento de noradrenalina hasta 1 mcg/kg/min y oxigenoterapia. Se realizó Body TAC que muestra embolias sépticas pulmonares bilaterales de probable foco de cánula venosa de ECMO, donde se evidenciaba imagen móvil previo a su retirada. Se solicitó ecocardiograma transesofágico (ETE) que no muestra signos sugestivos de endocarditis en cavidades derechas. El paciente evoluciona de manera favorable con franca mejoría clínica, con TAC de control con persistencia de émbolos sépticos y edema intersticial. A nivel arrítmico presentó rachas de TVMS a 160 cpm con inestabilidad hemodinámica que requiere CVE. En la evolución, dado el requerimiento persistente de ARM, se realiza traqueostomía sin incidencias.
Como se trata de un paciente con un IAM con severo compromiso de la función biventricular, con una anatomía coronaria no favorable para revascularización, se decide colocar un dispositivo de asistencia ventricular izquierda de larga duración tipo Heartmate III a los 45 días del evento, como puente a trasplante cardíaco. Dicho procedimiento quirúrgico se realizó por abordaje mediante esternotomía media total y circulación extracorpórea. Se coloca dispositivo a nivel del ápex del VI, el cual mediante una bomba centrífuga envía la sangre hacia la aorta ascendente a través de la interposición de un tubo protésico de Dacron. El ETE pos-CEC comprueba el correcto posicionamiento de la cánula de asistencia ventricular en el VI, ventrículo derecho con disfunción sistólica e hipertensión pulmonar moderada. Se traslada a UCI hemodinámicamente estable con perfusión de noradrenalina, adrenalina, milrinona y dobutamina. Heartmate III a 4800 rpm, con un flujo continuo de 4,2 litros/minuto y un índice de pulsatilidad correcto de 3,1. El paciente presentó una buena evolución en UCI, mejoría hemodinámica con paulatino destete de drogas vasoactivas sin complicaciones significativas. En el momento de esta comunicación, continúa ingresado en cuidados moderados realizando rehabilitación cardiovascular.
Discusión
El shock cardiogénico se define como un estado de insuficiencia circulatoria sistémica generado por disfunción cardíaca severa. Clínicamente se caracteriza por hipotensión arterial (presión arterial sistólica < 90 mmHg o necesidad de vasopresores para mantener una PAS > 90 mmHg) y signos de afectación de perfusión tisular (alteraciones del estado de conciencia, oliguria o incrementos del lactato > 2 mmol/L). Recientemente se han agregado como criterios hemodinámicos adicionales un índice cardíaco < 2,2 L/min/m2 o un incremento en las presiones de llenado ventricular (presión capilar pulmonar > 15 mmHg). La incidencia del shock cardiogénico pos-síndrome coronario agudo es del 5 a 10% con una mortalidad a 30 días y al año de 40% y 50%, respectivamente. Según el estudio SHOCK, las principales causas se deben a disfunción ventricular izquierda (78,5%) como en el caso de nuestro paciente, seguido por insuficiencia mitral aguda severa (6,95%), rotura del septum interventricular (3,9%), disfunción ventricular derecha (2,8%) y taponamiento cardíaco (1,4%). La piedra angular del tratamiento del shock cardiogénico pos-IAM es la reperfusión coronaria precoz y el soporte hemodinámico. La enfermedad multivaso se encuentra presente en el 70% de los pacientes con shock cardiogénico. En cuanto a la estrategia de revascularización más adecuada (PCI vs. CABG), la evidencia proviene de estudios observacionales y se destaca una mortalidad similar entre ambos tratamientos. Sin embargo, actualmente la cirugía de revascularización miocárdica de emergencia se realiza solo en un bajo porcentaje (3,2%-8,85%) y se reserva para casos donde la anatomía coronaria no es factible para PCI.
A pesar de la revascularización temprana, la mortalidad del IAM con SC sigue siendo elevada. En vistas a mejorar la hipoperfusión tisular y la eventual disfunción multiorgánica existen dispositivos de asistencia ventricular temporal que comprenden el BCIA, Impella, TandemHeart y el ECMO venoarterial. Estos pueden utilizarse tanto como terapia puente a la recuperación cardíaca, al trasplante cardíaco o al implante de un dispositivo de larga duración como el Heartmate III, utilizado en este paciente1.
El ECMO venoarterial (figura 1) es un sistema simplificado de circulación extracorpórea que consiste en una bomba centrífuga que drena la sangre venosa desaturada hacia un oxigenador, luego la reintroduce en forma oxigenada en el sistema arterial; esto permite un soporte ventricular capaz de generar un flujo continuo hasta 7 L/min. Para ello, se debe anticoagular al paciente con heparina no fraccionada con un objetivo de tiempo de coagulación activada de entre 180 y 220 segundos o mediante bivalirudina o dabigatrán en casos de trombocitopenia inducida por heparina o de resistencia a la heparina. El ECMO venoarterial puede colocarse por vía central en pacientes poscardiotomía, donde se utilizan las mismas cánulas de circulación extracorpórea, en aquellas situaciones de inestabilidad hemodinámica con fracaso en el weaning, a pesar del apoyo de drogas vasoactivas; o por vía periférica en pacientes con shock cardiogénico y parada cardíaca. En dicho caso el abordaje venoso puede ser femoral y/o yugular interno y el arterial femoral o subclavio1.
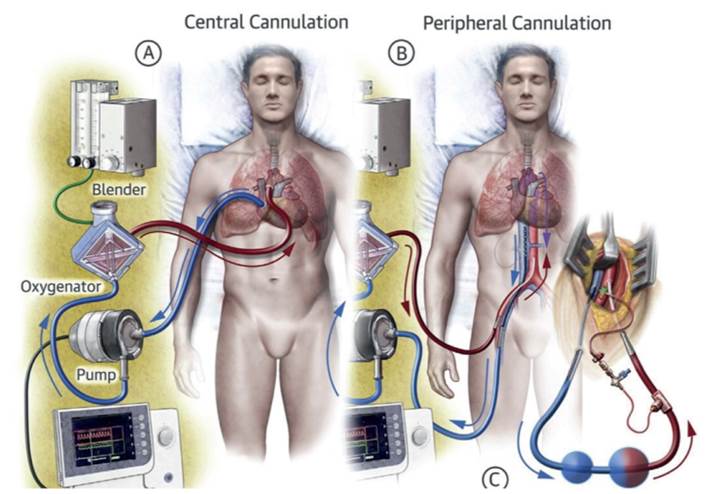
Figura 1: Canulación básica para ECMO veno-arterial. A) Canulación central. B) Canulación periférica. Tomado de 3.
Aunque no existe evidencia suficiente en cuanto a los objetivos específicos recomendados, se aconseja mantener un flujo entre 50-70 ml/kg/min con una presión arterial media > 60 mmHg, en vistas a mantener en forma satisfactoria la función respiratoria y hemodinámica (saturación arterial de O2 en miembro superior derecho > 90%, saturación venosa de O2 un 20%-25% por debajo de la saturación arterial y una adecuada perfusión tisular determinada por la presión arterial, saturación venosa y niveles de lactato sanguíneo)2.
Durante la asistencia de pacientes con ECMO venoarterial resulta fundamental una estrecha monitorización por parte del equipo (perfusionistas, cirujanos cardíacos y cardiólogos), los cuales deben estar debidamente capacitados dado el complejo manejo de dicho dispositivo y estar atentos ante potenciales complicaciones que podrían desarrollarse. Uno de los principales inconvenientes es el incremento de la poscarga generado por el flujo retrógrado a través de la canulación arterial periférica femoral que puede provocar un vaciado incompleto del VI, aumento de las demandas metabólicas de oxígeno, isquemia subendocárdica, aumento de las presiones de llenado ventricular, edema pulmonar e insuficiencia respiratoria, lo cual podría comprometer el weaning del soporte circulatorio3.
El VI (severamente afectado) debe ser capaz de generar la suficiente presión para superar dicha poscarga y permitir la apertura de la válvula aórtica, ya que, de lo contrario, se podría producir estasis sanguínea dentro del VI, trombosis, stroke y embolia periférica. Existen varias estrategias para solucionar dicha situación, como la disminución del flujo del ECMO, aumento del soporte inotrópico, uso de vasodilatadores, BCIA (como se utilizó en nuestro paciente), septostomía atrial percutánea, Impella o venteo del VI por vía quirúrgica o percutánea. Otra de las posibles complicaciones asociadas es el denominado síndrome de Arlequín, que se produce en situaciones de ECMO periférico, como resultado de una mejoría de la función cardíaca y mala ventilación pulmonar. En este caso, si la mezcla de sangre arterial desoxigenada eyectada por el VI se mezcla con la sangre arterial oxigenada retrógrada proveniente del ECMO en un sector distal a la arteria subclavia, podría generarse un alto riesgo de hipoxia cerebral, cardíaca y de las extremidades superiores. En dicha situación debería mejorarse el soporte ventilatorio o pasar a una canulación arterial axilar o central. Otros problemas frecuentes son el sangrado, el cual ocurre en el 30%-50% de los individuos debido a alteraciones en la anticoagulación, así como complicaciones infecciosas, como ocurrió en este paciente, relacionadas al sitio de canulación3.
Una vez que se logra una estabilidad hemodinámica y una adecuada función pulmonar con escaso apoyo del ECMO se puede proceder al weaning y remover las cánulas. No existe evidencia robusta en cuanto al beneficio del ECMO venoarterial en pacientes con shock cardiogénico pos-IAM. Un reciente metaanálisis de 13 estudios observacionales que incluyen este tipo de pacientes demostró una diferencia significativa de la sobrevida a 30 días a favor del grupo de ECMO en comparación con el uso de BCIA (diferencia de riesgo absoluta 13%, IC 6%-20%)4.
Dada la falta de evidencia y la escasez de ensayos randomizados, las últimas guías europeas de revascularización miocárdica recomiendan el uso de dispositivos de asistencia circulatoria con un nivel de evidencia IIb-C. Es por esto que la evaluación para su uso debe considerar la edad del paciente, comorbilidades, función neurológica y sobrevida. En el caso de este paciente, pudo realizarse el destete del ECMO y la posterior colocación de un dispositivo de asistencia ventricular izquierda de larga duración como el Heartmate III (figura 2). Este consiste en una bomba centrífuga que permite mediante un levitador magnético generar un flujo axial continuo, drenando la sangre mediante una cánula de inflow colocada en el ápex del VI y eyectándola hacia un conducto de outflow a la aorta ascendente. El Heartmate III puede ser monitoreado y configurado mediante un módulo de control externo que permite modificar la velocidad de la bomba (revoluciones por minuto), así como valorar el flujo, el índice de pulsatilidad y la energía de la batería5. El registro ELEVATE se trata de un estudio observacional prospectivo multicéntrico que incluye 540 pacientes a los que se les implanta un dispositivo Heartmate III, en donde el 66% de los casos el motivo del implante fue como puente al trasplante y en un 26% como terapia destino. A los 2 años de seguimiento la sobrevida fue de un 83,4%; la mayoría se encuentra en clase funcional I-II de la NYHA y una mejoría persistente en la calidad de vida6.
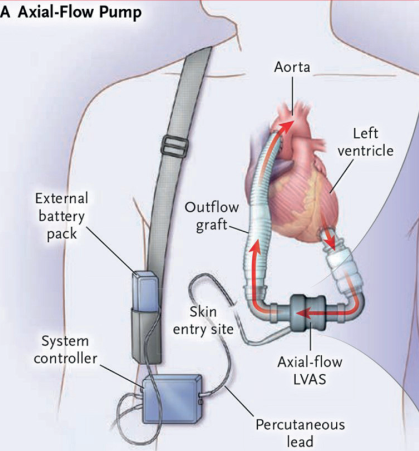
Figura 2: Dispositivo de asistencia ventricular izquierda de tipo Heartmate III. Tomado de Deshpande S. Efficacy and Safety of Left Ventricular Assist Devices with Centrifugal Flow Pumps. N Engl J Med, 2017.
En conclusión, si bien el shock cardiogénico pos-IAM es en la actualidad poco frecuente, presenta una elevada mortalidad, donde no solo resulta fundamental y mandatoria la revascularización precoz, sino también mantener un adecuado soporte circulatorio. El uso de ECMO venoarterial en este contexto parece mostrar una mejoría significativa en la sobrevida y es fundamental un correcto conocimiento y manejo de las potenciales complicaciones para lograr resultados satisfactorios. Dado que un gran porcentaje de estos pacientes quedan con una función ventricular izquierda severamente afectada a pesar de la revascularización, debemos tener en mente la existencia de dispositivos de asistencia ventricular de larga duración como puente a trasplante cardíaco, los cuales, si bien aún no se encuentran disponibles en nuestro medio, han mostrado buenos resultados a mediano plazo.















